刺五加水煎煮提取动力学模型的建立
韩林辛, 倪 键*, 玄 律, 窦津晶
(1.北京中医药大学中药学院,北京 100102;2.北京市海淀区北太平庄医院,北京 100088)
中药在提取过程中的质量参数、工艺参数、物料参数等是影响成品质量的关键因素,而有效成分的浸出量也因上述条件的不同而存在差异。本文研究了中药刺五加提取过程的一些关键因素对有效成分含量的影响,对其随提取时间、溶剂倍量和药材粒度的变化规律进行了研究,建立了刺五加提取动力学模型,并通过提取实验对该模型进行了检验。
1 中药提取动力学模型的推导
为提高中药提取效率,应对药材有效成分的提取过程进行定量研究和分析[1],可将数学模拟方法应用于提取过程进行研究[2]。中草药有效成分提取过程的实质是溶质从药材固体向溶剂中的传质过程[3]。一般地说来,植物性药材煎煮过程可由三个步骤组成[4]:第一步,溶剂向药材内部渗透;第二步,溶质溶解到固液界面上;第三步,溶质从固液界面向溶剂主体扩散。一般地,浸提时溶剂的渗透和溶质的溶解进行的较快[5]。按照动力学定律,在煎煮溶剂中,药材中的溶质溶解速率很大,使溶质转移到溶液中去也是很快的,而扩散作用的进行却慢得多。因此对煎煮速率具有决定性影响的是扩散作用,而不是溶解速率,即多数情况下第三步为煎煮过程的控制因素。
由Fick第一定律可得:
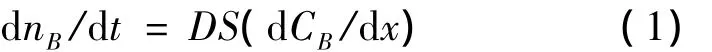
其中dnB/dt为溶质B的扩散速率,dCB/dx为溶质B的浓度梯度,S为固液界面积,nB为溶质B的物质的量,D为扩散系数。
根据希格比传质穿透模型理论,可近似认为以药材颗粒为一个传质单元,液相主体中小团液体m借助药材沸腾后的湍流涡旋运动由A点走向二相界面B点,并在界面上移动一段距离后到达C点,然后脱离界面达到D点。这样液团m在界面上停留ts秒中,固相中可溶性成分不断扩散溶解到液团m中,形成了一个不稳定的传质过程。也可以这样认为,当药材粉碎颗粒在液相中上浮时,一液团m可以先与气泡顶部某处界面接触。随着药材颗粒向上运动或其它维向运动,固液界面不断更新,药材颗粒中的可溶性成分不断溶入液相主体中直到平衡。见图1。
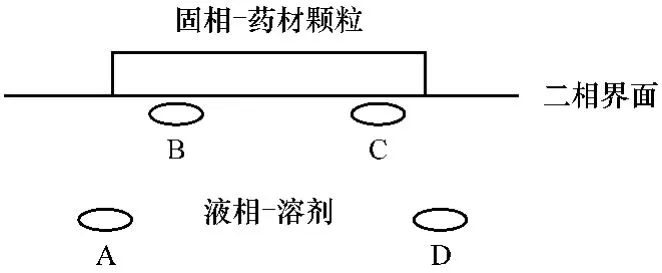
图1 传质过程图解
上述过程,可近似地用下面一维不稳定传质方程表示:
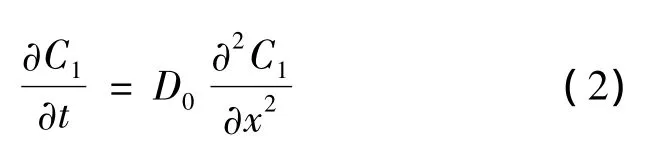
为求解上述方程,可取一新变量

代入(1)式,用η代替(1)式中t与x得
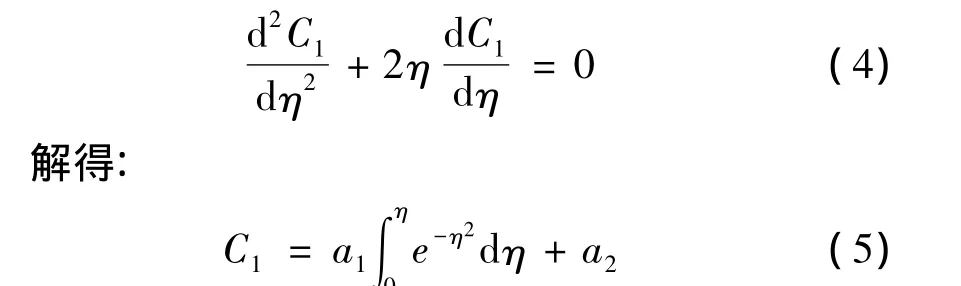
边界条件:
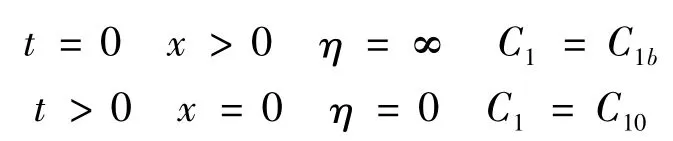
C10为药材的初始浓度即溶液沸腾时溶液中溶质的浓度,C1b为溶液主体浓度即沸腾是溶质药材的浓度。C1b-C10应当为药材的有效成分浓度。
得:
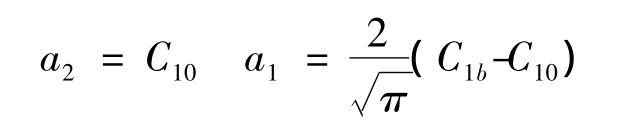
由此得:
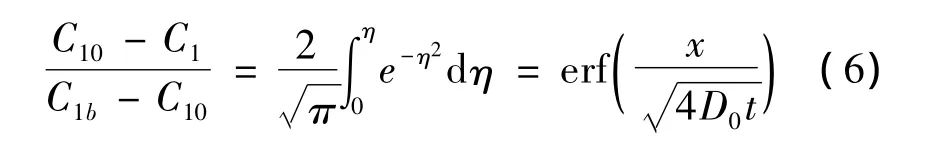
将(6)式微分得在x=0处,时间为t时
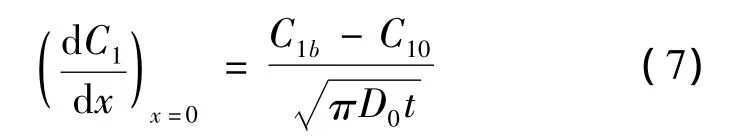
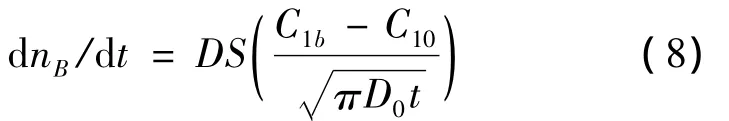
浓度对扩散系数的影响不大,而对浓溶液,扩散系数则是浓度的函数[6]。根据林亚平[7]等研究,认为扩散系数与溶液浓度的幂成正比,即
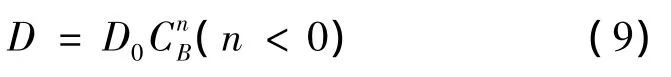
其中D0是一个仅与溶质性质和温度等有关的的常数,称之为溶质的固有扩散系数。
由nB=VCB,将(9)式代入到(8)中,得:
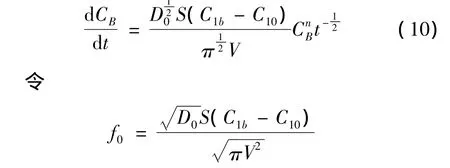
将(7)式代入(2)式中得:
则(10)变形为:
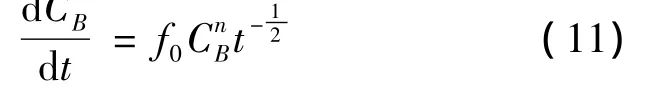
积分得:
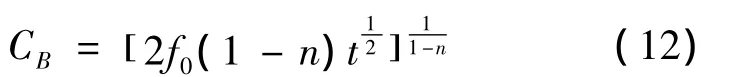
煎煮过程中,一般把药材粉碎成颗粒状,以提高有效成分的提取率,假定药材颗粒为小圆柱形,药材颗粒数为ω,颗粒粒度为σ1,高为σ2,药材总的干质量为G,密度为ρ,则有:
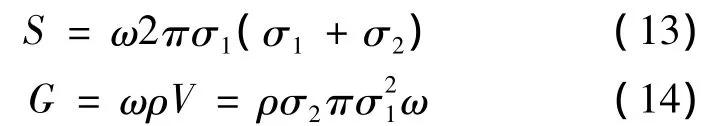
(13)与(14)式相比得:
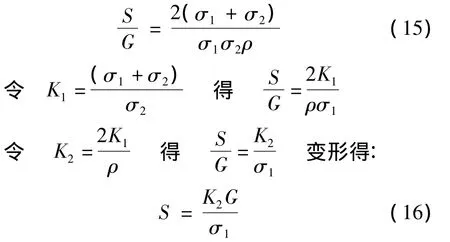
如果不计因蒸发而引起的溶剂蒸发。此时溶剂倍量可以用下式表示:

其中R为药材充分吸收吸湿所需水体积与干的药材质量之比
(16)与(17)联立得:
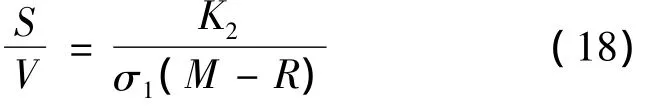
将(18)式代入(12)式得:
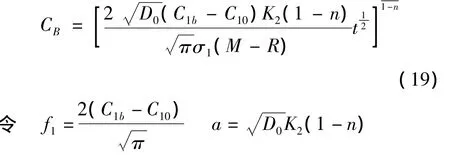
1
则(19)化简为:
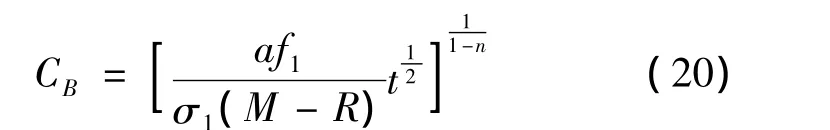
(20)式即为本次推导出得的中药煎煮过程的动力学模型,它表示了煎煮出的有效成分浓度与溶剂倍量、颗粒粒度及煎煮时间之间的函数关系。
(1)若只改变煎煮时间时,对(20)取对数可得:
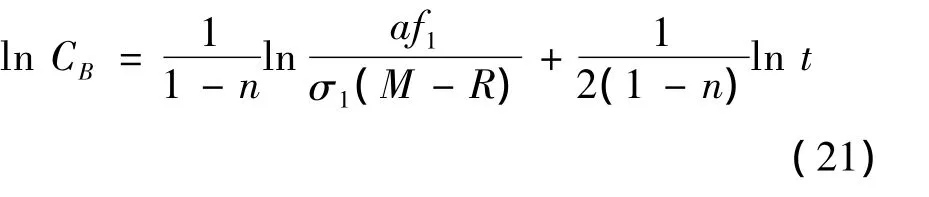
(2)若只改变颗粒粒度,对(20)取对数可得:
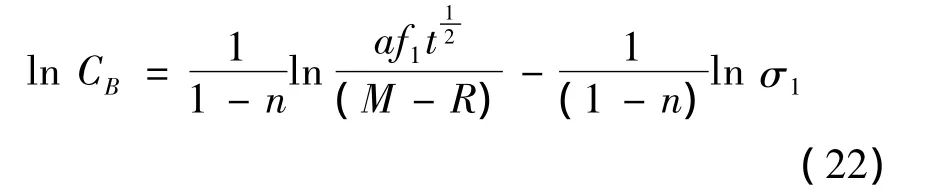
(3)若只改变溶剂倍量,对(20)取对数可得:
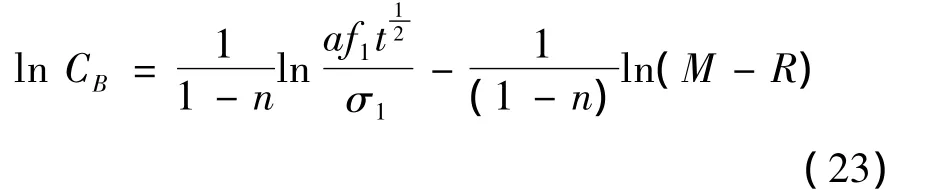
2 试验研究[9]
2.1 仪器与试药
刺五加药材(市售)(刘春生副教授鉴定 北京中医药大学生药系);刺五加苷B对照品(A0253)、刺五加苷E对照品(A0254)(购自北京嘉信众义科技有限公司);岛津LC-20AT高效液相色谱仪,四元泵,DAD检测器。甲醇、乙腈为色谱纯(生产于北京化工厂),水为高纯水,其余试剂均为分析纯。
2.2 刺五加苷有效成分含量测定方法
2.2.1 测定方法 刺五加根和根茎中的主要成分为酚苷类化合物,是主要的生物活性成分[10],其中刺五加苷B、E为主要有效成分[11],以刺五加药材中的刺五加苷B和刺五加苷E含量之和为指标,测定刺五加药材的有效成分含量。液相色谱条件为:色谱柱:Intersil ODS C18(5 μm 150 ×4.6 mm),流动相 A为乙腈,B为水,梯度洗脱:0~11 min:A(10%),B(90%);11.1 ~25 min:A(15%),B(85%);25.1~35 min:A(10%),B(90%)。检测波长:刺五加苷B为264 nm,刺五加苷E为206 nm。柱温:35℃。
2.2.2 标准曲线 分别将刺五加苷B对照品和刺五加苷E对照品溶于甲醇制成对照品溶液,用上述液相色谱条件绘制的标准曲线,得回归方程为:刺五加苷 B:Y=2 574 140X+14 075,r=0.999 2,刺五加苷B 在0.03 μg~0.23 μg范围内线性关系良好;刺五加苷 E:Y=5 020 944X+534,r=0.999 6,刺五加苷E在0.04 μg~0.26 μg范围内线性关系良好。式中x为进样量,单位为μg,y为峰面积。
2.2.3 精密度试验 精密吸取对照品溶液10 μL,重复进样6次,计算相对标准偏差。结果刺五加苷B和刺五加苷E的RSD分别为0.66%、0.52%。实验证明精密度良好。
2.2.4重复性试验 取同一批号样品,分别制备6份样品供试液,测得峰面积值并计算含量,结果刺五加苷B和刺五加苷E的RSD分别为2.72%、2.32%。实验证明重复性良好。
2.2.5 稳定性试验 精密吸取同一供试品溶液10 μL,分别于配制后 0、2、4、8、12、24、48 h 进样,测得峰面积值,结果刺五加苷B和刺五加苷E的RSD分别为0.86%、1.28%。实验证明稳定性良好。
2.2.6 回收率试验 精密称取含量已知的刺五加样品6份,每份约0.5g,分别精密加入适量刺五加苷B和刺五加苷E对照品,按样品溶液的制备项下操作,进行HPLC分析平均回收率。结果刺五加苷B和刺五加苷E的RSD分别为2.23%、2.47%。详见表1。
2.3 刺五加水煎煮提取实验
2.3.1 干药材吸溶剂率的测定 取不同质量的刺五加药材颗粒分别置与烧杯中,分别向其中缓缓加入水,直至药材充分吸湿,记录溶剂体积,结果见表2。
将四组数据所得结果求平均值得药材的吸溶剂率R=2.37 mL/g。
2.3.2f1的测定与计算
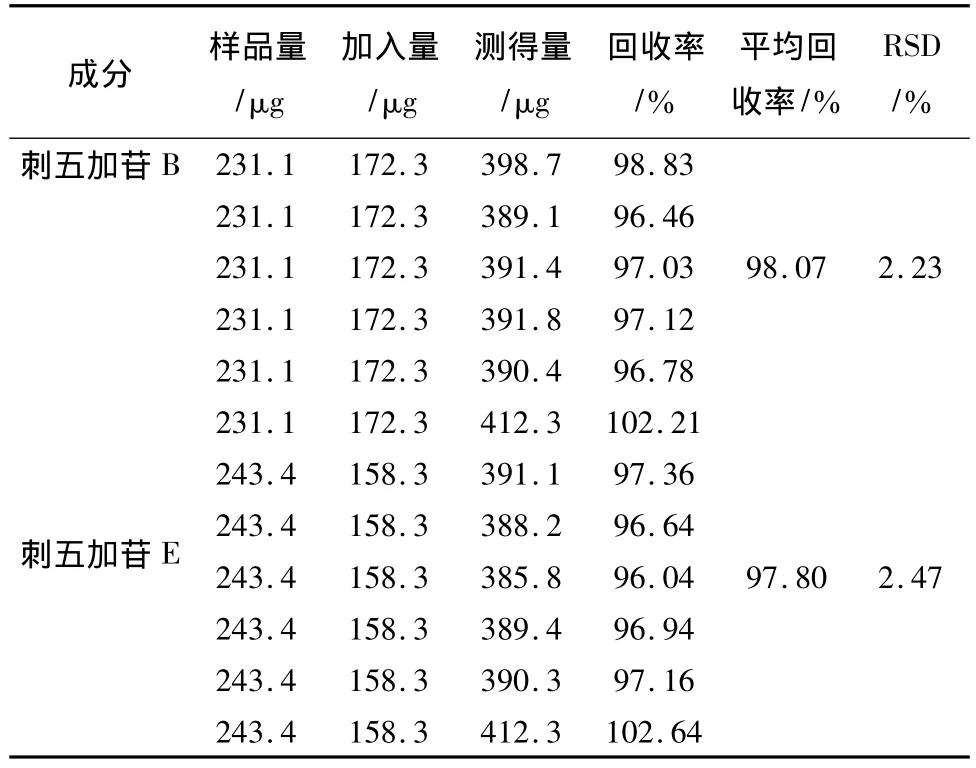
表1 回收率试验结果
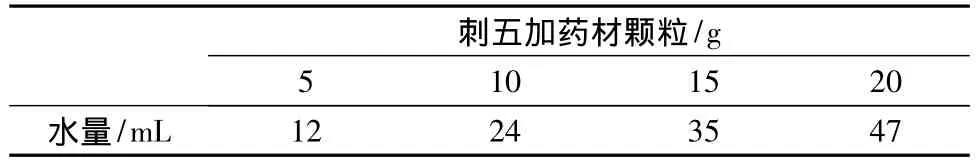
表2 药材充分吸湿所需要溶剂体积
2.3.3 刺五加水煎煮提取方法 采用三口圆底烧瓶,电热套加热进行水煎煮提取,为减少水分蒸发,安装冷凝回流装置。考虑到刺五加材质坚硬,将其粉碎过细不适于中试生产,故本实验固定粒度因素(σ1=296.25 μm),实验考察药材提取时间(以t表示),固液比(以M表示)两因素对有效成分含量的影响。
2.3.4 实验结果
2.3.4.1 提取时间对提取率的影响 升高温度能加快分子运动,提高分子扩散速率,从而可以提高提取速率,提高有效成分的提取率[12]。采用高效液相色谱法测定上述实验条件下有效成分的浓度,结果见表3。
通过实验数据做lnCB~lnt曲线,考察煎煮出的有效成分浓度是否遵守(21)式,结果见图2。
由图线性回归可得,当M=8 mL/g,σ=296.25 μm时,线性回归方程为y=0.054 9x-2.904 9,R2=0.994 7;当M=10 mL/g,σ =296.25 μm 时,线性回归方程为y=0.054 4x-2.933 1,R2=0.991 9;当M=14 mL/g,σ =296.25 μm 时,线性回归方程为y=0.054 4x- 2.942,R2=0.998 8;当M=16 mL/g,σ =296.25 μm 时,线性回归方程为y=0.054 4x- 2.962 3,R2=0.998 6。在上述理论推导中,若只改变煎煮时间,则理论方程可以转化为

表3 提取时间对提取率影响
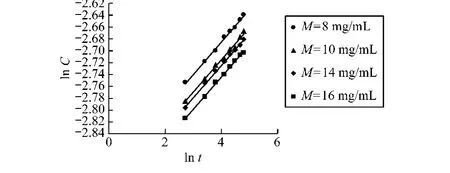
图2 提取时间对有效成分浓度影响
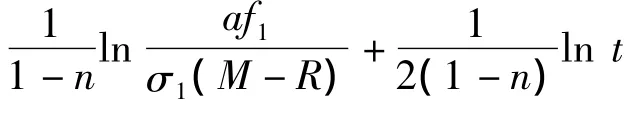
2.3.4.2 溶剂倍量M对提取的影响 采用高效液相色谱法测定各实验条件下刺五加苷B和E的浓度,结果见表4。

表4 溶剂倍量对提取影响
通过实验数据做lnC~ln(M-R)曲线,考察煎煮出的有效成分浓度是否遵守(23)式,结果见图3。
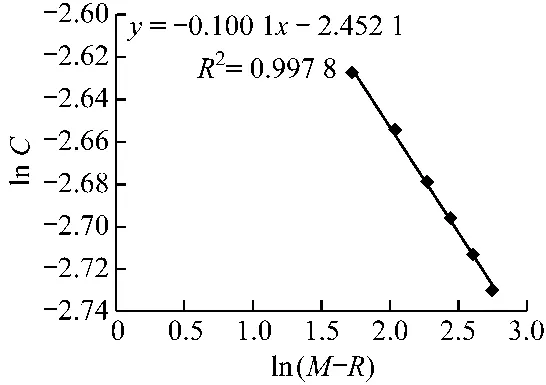
图3 溶剂倍量对提取影响
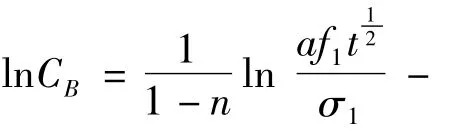
由图2,图3看出,lnCB~ lnt与lnCB~ln(M-R)均成较好的线性关系,因此可以认为,水煎煮提取刺五加中刺五加苷B和刺五加苷E的过程,基本与所建立的动力学理论模型相吻合。
2.3.4 方程的建立
各a和n值求均值得a=3.98×10-9,n=-8.580 1,将两者代入(20)式中,求得本次研究所建立的刺五加水煎煮提取过程动力学模型:
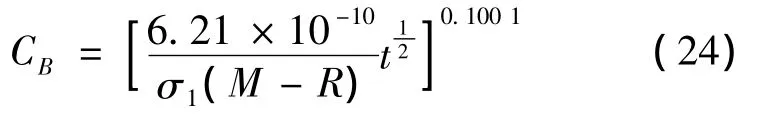
3 小结
本实验测定了在不同溶剂倍量和不同提取时间条件下,水煎煮提取刺五加中刺五加苷B和刺五加苷E的浓度变化情况,建立了动力学模型。根据实验结果,在单因素变化的情况下,lnC对lnt和ln(M-R)均成线性关系,符合本模型。
但应指出,本次建立的动力学模型是从工业生产实际操作出发,其他温度条件对刺五加苷动力学方程的影响有待进一步研究。
[1]周永传,戴洁婷.丹参酚酸B水提取动力学研究进展[J].南京工业大学学报,2007,29(2):106-110.
[2]李有润,郑 青.中草药提取过程的数学模拟与优化[J].中草药,1997,28(7):399-401.
[3]陈玉昆.中药提取生产工艺[M].沈阳:辽宁出版社,1999.
[4]单熙滨主编.制药工程[M].北京:中国医科大学,中国协和医科大学联合出版,1994.
[5]Robert E T.Mass-Transfer Operations[M].Second Edition New York:McGraw-Hill Book Company,1968.
[6]戴干策,任德呈,范自晖.传递现象导论[M].北京:化学工业出版社,1996.
[7]林亚平,卢维伦.非溶蚀型药物体系的释放动力学新模型-Fick第一定律的修正及其应用[J].药学学报,1997,32(11):869-873.
[8]储茂泉,古宏晨,刘国杰.中草药浸提过程的动力学模型[J].中草药,2000,31(7):504-506.
[9]玄 律.补肝明目颗粒的制备工艺及质量标准的研究[D].北京中医药大学,2009:7.
[10]张 晶,刘芳芳,陈彦池,等.刺五加化学成分及药理学研究进展[J].中国野生植物资源,2008,27(2):6-10.
[11]封士兰,胡芳弟,赵健雄,等.RP-HPLC法研究刺五加注射液中刺五加苷E、刺五加苷B在大鼠体内的药代动力学和组织分布特性[J].药物分析杂志,2006,26(6):741-744.
[12]周永传,余海杰,邓 修.第四届全国制药工程科技与教育研讨会论文集[C].上海:华东理工大学出版社,2005,26(1):457.

