胃乐新颗粒中多糖的含量测定
,,
(1.白求恩医科大学制药厂,吉林 长春 130021;2.吉林大学公共卫生学院,吉林 长春 130021)
胃乐新颗粒是采用长白山珍贵野生资源小刺猴头菌经深层发酵、培养、提取其有效成分制成的冲剂。猴头多糖是猴头菌中的主要活性成分,有保护胃黏膜,抗肿瘤作用,其含量在一定程度上反映了胃乐新颗粒的质量,特建立了测定胃乐新颗粒中多糖含量的方法[1-3]。
1 仪器与试药
1.1 仪器 紫外-可见分光光度计(UV-2450岛津公司),低速自动离心机(LDZ5-2北京医用离心机厂),电子分析天平(AB104-N梅特勒-托利多仪器上海有限公司)。
1.2 试药 D-无水葡萄糖对照品(中国药品生物制品检定所,批号:110833-200503);胃乐新颗粒(白求恩医科大学制药厂,批号:100326;100415;100538;100607);蒽酮溶液:取蒽酮0.2 g,加硫酸溶解并稀释至100 mL。此试剂应临用新制。其他试剂均为分析纯。
2 方法与结果
2.1 对照品溶液的制备 精密称取D-无水葡萄糖对照品10 mg,置100 mL量瓶中,加水溶解并稀释至刻度,摇匀,既得0.1 mg/mL对照品溶液。
2.2 标准曲线的制备 精密量取对照品溶液0.0、0.1、0.3、0.5、0.7、0.9 mL,各加水至2.0 mL,分别加入预先用冷水冷却的蒽酮溶液4 mL,混匀,置沸水浴中加热6 min,迅速冷却至室温,约20 min时,照分光光度法,在625 nm的波长处分别测定吸收度,以测得吸收度与其对应的浓度,计算回归方程。回归方程为:Y=8.245 21X-0.006 38。结果表明:葡萄糖溶液1.7~15.0 μg/mL与吸光度呈良好的线性关系。
2.3 供试品溶液的制备 精密称取供试品2.5 g,溶于10 mL水中,时时振摇浸渍30 min,滤过,作为储备液。精密量取储备液1 mL,置10 mL离心管中,分4次加入无水乙醇,每次1 mL并摇匀,静置5 min,4 000 r/min离心10 min,倾去上清液;沉淀加水0.2 mL振摇溶解,再分2次加入无水乙醇,每次1 mL,同法重复操作,离心,倾去上清液,沉淀加95%乙醇5 mL,振摇使成混悬液,离心,倾去上清液;沉淀再加无水乙醇5 mL,同法洗涤1次。取沉淀,用水溶解并稀释至50 mL为供试品溶液。
2.4 测定法 精密吸取供试品2.0 mL,照标准曲线制备项下自“加入预先用冷水冷却的蒽酮溶液4 mL起”依法操作,由回归方程计算多糖含量。
2.5 精密度试验 精密量取对照品溶液0.5 mL,加水至2.0 mL,加入预先用冷水冷却的蒽酮溶液4 mL,混匀,置沸水浴中加热6 min,迅速冷却至室温,约20 min时测定吸收度。平行6分,以纯化水2 mL加相应的试剂做空白,计算其RSD为1.89%,表明仪器的精密度良好。
2.6 稳定性试验 取样品(批号:100326)新制得的供试品溶液2.0 mL,加入预先用冰水冷却的蒽酮溶液4 mL,混匀,置沸水浴中加热6 min,迅速冷却至室温,以纯化水2 mL加相应的试剂做空白,在0、2、4、8、16、24 h时测定吸光度。计算其RSD为1.56%,表明供试品溶液在24 h内稳定。
2.7 重复性试验 取同一批号的样品(批号:100326)6分,每分各2.5 g,精密称定,按“2.3”项下方法制备溶液,测定。计算RSD为2.05%,表明重复性良好。
2.8 回收率试验 精密吸取1 mL已知含量的供试品溶液6分,每2分分别精密加入0.2、0.4、0.6 mL的葡萄糖对照品溶液(0.1 mg/mL),照“2.2”项下方法测定其吸收度,并计算含量,结果见表1。
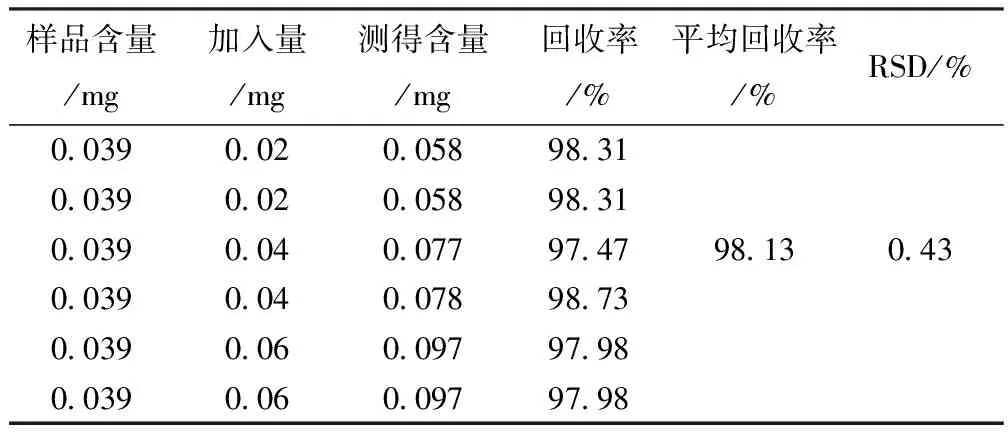
表1 加样回收率测定结果
2.9 样品测定 取4批样品,按上述供试品溶液的制备方法制备供试品溶液,测定吸收度,并计算其多糖含量,结果见表2。
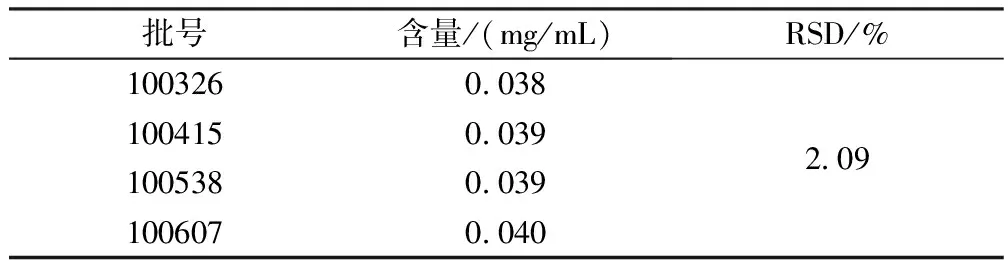
表2 硫酸-蒽酮法测定胃乐新颗粒多糖的含量结果
3 小结
3.1 制备供试品溶液的过程中,分4次加入无水乙醇,每次1 mL,比1次加入4 mL无水乙醇对供试品的溶解性要好[4]。
3.2 蒽酮溶液加得快慢不同,相当于在不同的温度显色,因此加入的速度应一致[5]。
3.3 因硫酸黏度高易产生气泡影响吸收度,建议加热显色后趁热充分振摇,一旦冰浴冷却后不要再摇。
[1]中华人民共和国卫生部药典委员会.药品标准中药成方制剂[S].第11册,WS3-B-2182-96.
[2]徐增香,师健友.天南星中多糖的测定[J].华西药学杂志,2010,25(2):208-209.
[3]钟方晓,任海华,李岩.多糖含量测定方法比较[J].时珍国医国药,2007(8):218-219.
[4]杨瑞瑞,李国华,樊宝娟.灵芝多糖的含量测定方法探讨及改进[J].陕西中医学院学报,2009,32(5):223-224.
[5]许乐文,周林彬.胃乐新片中多糖的含量测定[J].中南药学,2006,4(4):294-296.

