乙炔的制取及性质实验的创新设计
李新勇
(江苏省江阴长泾中学江苏江阴214411)
乙炔的制取及性质实验的创新设计
李新勇
(江苏省江阴长泾中学江苏江阴214411)
根据新课程化学实验教学的要求,研究人教版乙炔的制取及性质实验,发现其存在缺陷,作者通过多次的实验尝试,创新设计了一种实验方案可以很好的解决其存在的问题。
新课程;乙炔;化学实验;创新设计
一、新课程高中化学实验教学的要求
1.安全性
化学实验与其它实验的最大不同在于:实验者接触到的多是有毒、有腐蚀性、易燃易爆的化学药品和易裂、易碎的玻璃仪器,稍有不慎就会造成仪器破损,轻者影响实验顺利进行,重者会造成实验人员的人身伤害,故高中实验设计应充分考虑学生实验中的安全问题,使学生在实验过程中尽量避免使用那些毒害性大、腐蚀性强的药品和进行具有一定危险性的实验操作。
2.绿色环保
绿色化学实验是化学实验教学的目标,也是新课程反复强调的重要课题之一。《化学课程标准》在课程性质中明确指出要让学生懂得运用化学知识和方法去治理环境污染。
3.微型化
易于操作、现象明显、简单快捷、安全可靠,提高了课堂教学质量。减少药品用量,从而减少了浪费,提高药品使用效率,降低了实验成本,实现了原子经济性,培养学生的可持续发展意识。
4.简洁易操作
实验设计应尽可能简单易行,应采用简单的实验装置,用较少的实验步骤和实验药品,并能在较短的时间内完成。
二、问题的提出
现行人教版高中化学教科书(必修加选修)第二册中有关乙炔的制取和性质实验,在实际教学中发现存在一些不妥之处:
1.乙炔的实验室制法中,考虑到水与CaC2反应过于剧烈,产生气体过快,并会产生大量泡沫易堵塞导管,而改用饱和食盐水代替,但实际效果并不理想。
2.CaC2中混有CaS、Ca3P2等杂质,与水反应会产生H2S、PH3等还原性有毒气体,既影响后面乙炔性质实验的验证,又污染环境,对师生健康造成一定的伤害。
3.常规乙炔性质实验探究往往是将生成的乙炔气体先经过净化再分别通入溴水和酸性KMnO4溶液中,是分步、敞口的,实验药品用量较多,操作较为繁琐。
三、实验的改进
1.实验用品
大小培养皿各一个、小塑料盖、镊子、胶头滴管、棉花、滤纸。
电石、饱和硫酸铜溶液、溴水、酸性KMnO4溶液。
2.实验装置及操作步骤
(1)先将小培养皿放在滤纸上(滤纸的作用是便于观察到明显的实验现象),并在培养皿的中央放入一个塑料盖(塑料盖的作用是防止反应放热炸裂小培养皿)。(图1);
(2)取米粒大小的碳化钙固体一颗,用棉花包住后放入塑料盖中(图2);
(3)向培养皿中塑料盖旁的两边分别滴入1滴高锰酸钾溶液和1滴溴水(图3)。
(4)最后向塑料盖中滴入4~5滴硫酸铜溶液,并立即盖上大培养皿,注意观察实验现象(图4)。

图1
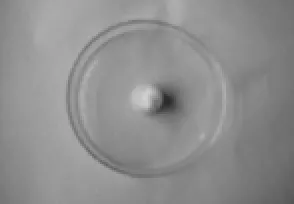
图2
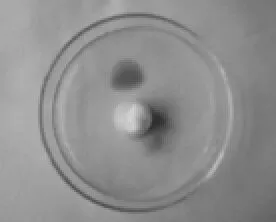
图3

图4
3.实验特点
(1)实验微型化,降低了实验成本。实验仪器简单常见,且不易造成损坏,而实验药品的用量极少,大大降低了实验成本。
(2)操作简单,节省实验时间。如果按照书本上的要求做,完成乙炔的制取和性质实验的全过程一般需要十分钟左右,而根据这个实验设计进行实验只需二三分钟。
(3)实验效果好。滴加硫酸铜溶液后,首先看到滴加位置的棉花变黑,那是电石和水反应生成乙炔气体,同时产生的H2S、PH3气体被硫酸铜溶液吸收生成黑色物质,随后很快可见溴水和酸性高锰酸钾溶液褪色。
(4)最大限度的实现实验的绿色化。主要体现在两个方面:一是产生的有毒气体被硫酸铜溶液吸收了,二是电石、溴水、酸性高锰酸钾溶液的用量极少,避免了实验废液造成污染。
[1]李旻.乙烯的制取和性质实验的微型化尧绿色化[J].中学化学,2009,(8):20
[2]齐琳.乙炔制备和性质实验的组合设计[J].中学化学,2009,(1):22
1008-0546(2011)03-0077-01
G633.8
B
10.3969/j.issn.1008-0546.2011.03.038
——以硫酸铜饱和溶液析出晶体的计算为例

