微波消融治疗骨肿瘤
范清宇,马保安,周 勇,张明华,杨彤涛,龙 华,李 钊
继续教育
微波消融治疗骨肿瘤
范清宇,马保安,周 勇,张明华,杨彤涛,龙 华,李 钊
骨肿瘤;微波
消融(ablation)在医学上是指通过物理、化学方法(微波、液氮、射线或不可逆电穿孔等)去除某部分生物组织或杀死肿瘤细胞。1975年,国际高温肿瘤学大会在华盛顿召开,自此,消融在全世界范围内被成功应用于肝癌、肺癌、肾癌和骨癌等肿瘤的治疗。本文就微波消融治疗骨肿瘤的相关基础与临床研究进行探讨,同时介绍了唐都医院在该领域的研究成果和成熟经验。
1 微波消融的原理
实体肿瘤区域内杂乱无章的血管构型导致局部微环境的变化(如缺氧、pH值增高等),使肿瘤细胞较正常细胞对高温敏感。肿瘤细胞耐受的温度上限为43℃,在此温度水平以上,肿瘤细胞可被选择性地杀灭或损伤,而正常组织则不受损害。
微波可激励肿瘤中的极性水分子产生超高速振动,水分子的振动、发热可使瘤段骨升温,肿瘤表面和中心温度快速提高,肿瘤细胞出现凝固性坏死。而在所有肿瘤细胞均被杀灭的同时,周围正常组织特别是血管神经由于采取局部隔热降温等保护性措施,可以免受高温损伤。可见,通过高温的局部热效应及热传导作用,微波消融技术既控制了肿瘤的发展,又完整地保留骨与关节结构的稳定结构性,最大限度地保存肢体和关节功能。
2 微波消融的相关基础研究
2.1 杀死活细胞的热剂量问题
确定微波杀死肿瘤活细胞的热剂量,掌握灭活骨组织所需的温度和时间,对微波消融治疗骨肿瘤的临床研究具有重要意义。唐都医院应用可精确控制时间和温度的MAS-II微波工作站持续发射微波,采用酶组织化学染色、ATP检测和流式细胞仪等方法确定细胞活性。结果(图1,2)表明,可靠杀死活性细胞的热量下限为“50℃×5 min”。
2.2 灭活骨的再生研究
灭活骨微波灭活后的病理转归过程与自体骨及异体骨移植后的病理变化有许多相似之处。我院对16只杂种成年犬灭活骨的远期归宿进行研究,墨汁灌注法(图3)证实灭活骨可逐渐进行再血管化,四环素标记和骨扫描结果(图4,5)则显示灭活骨具有良好的骨再生潜能。这一结论也得到了临床随访骨扫描结果的证实。
2.3 灭活骨力学性质的研究
微波消融技术治疗骨肿瘤尽管在临床上取得满意效果,但仍面临着术后病理性骨折的预防问题,因此研究微波消融对灭活骨力学性质的影响,有助于采取针对措施,减少甚至避免病理性骨折的发生。我们将灭活骨和对照骨试样置于Instron-1341仪上(图6),对其拉伸应力、压缩应力、骨折功和拉伸率等进行测量,结果发现,压缩应力明显增加,而牵张应力改变不明显;四点弯曲实验证实灭活骨的疲劳寿命呈指数性下降,说明微波高温降低了皮质骨的弯曲能力,骨组织脆性增加,易突发断裂。这一结果提示在临床上需改进治疗方法,实施钢板内固定以增加骨折功,降低病理性骨折的发生率。
3 微波消融的相关临床研究
3.1 骨盆肿瘤
有相当比例的原发性和继发性肿瘤发生于骨盆,常侵犯至髋臼周围。由于骨盆区域解剖复杂,肿瘤深在,因此确诊时往往已处于中晚期。该部位肿瘤手术创伤较大,并发症较高,以复发和感染为主。复习关于骨盆肿瘤治疗的文献,最常见的评价为:“巨大的挑战”、“出奇地困难”、“想要保证患者术后的行走功能,没有比髋臼区肿瘤手术再难的了”、“骨盆肿瘤治疗面临着越来越多的失败率”等等。总而言之,即使是对于一个非常富有经验的骨肿瘤医生而言,骨盆肿瘤的治疗依然是一个艰巨的任务。
Enneking将骨盆肿瘤分为4型,Ⅰ型:髂骨区;Ⅱ型:髋臼周围区;Ⅲ型:坐骨耻骨区;Ⅳ型:骶骨区。骨盆环由大块的扁平松质骨组成。恶性肿瘤在松质骨内的播散阻隔很小,侵犯范围往往大于影像学资料显示的范围,但髋臼顶、髋关节前后柱到分区分界线的距离很难确定,而这涉及到精确的截除线问题。内半骨盆切除术是治疗骨盆肿瘤的有效手段,但技术要求较高,不易达到手术的安全界限(有时甚至完全不可能),因而术后复发率甚高(图7);同时,内半骨盆切除术后缺损较大,需采取相应的重建措施以恢复脊柱和下肢之间的连续性,以及骨盆环的完整性和稳定性。
3.1.1 微波消融的手术过程
3.1.1.1 显露切口(图8)(1)骨盆内侧暴露:切开腹壁肌,腹膜外分离髂窝,显露并牵开髂外血管和股神经,暴露坐骨大孔,如瘤体较大尚需与盆内脏器分开;(2)骨盆外侧暴露:掀开臀大肌肌皮瓣,显露坐骨神经和坐骨大孔。一般来说,单纯的坐骨肿瘤仅需骨盆外侧显露,耻骨肿瘤仅需骨盆内侧暴露。其他情况则需要同时进行内外侧暴露(T型切口)。
3.1.1.2 灭活肿瘤 用长止血钳穿过坐骨大孔,拉出3~4块湿纱布以覆盖坐骨神经,此时需注意的是,如瘤体较大并充满坐骨大孔,则应格外小心,切勿捅破肿瘤污染手术野。分离完毕后即可进行灭活。灭活范围主要根据MRI显示的信号异常区,布置好天线后开始输入微波能。密切监测温度,确保肿瘤区的任一部位均达到至少60℃~80℃,加热时间通常为30 min。灭活过程中需不时向穿过坐骨神经的纱布滴水降温,以保护坐骨神经。如肿瘤十分接近髋臼软骨,则需要在关节内建立水循环降温系统,有时甚至需要将髋关节脱位,以确保头、臼软骨不被破坏。
3.1.1.3 肿瘤切除与骨盆重建 灭活后切除或刮除失活的松软肿瘤组织,恢复骨盆的骨性轮廓。有时需要采取简单的重建措施(图9),如植骨、水泥或钢板固定、假体置换等,使骨盆环的承重力线保持连续。
3.1.2 微波消融的临床效果 自1994年7月至2009年3月,我们对204例恶性或高度侵袭性骨盆肿瘤(包括71例高度恶性肿瘤、56例低度恶性肿瘤、52例侵袭性肿瘤和25例孤立性转移癌)患者实施微波消融手术,其中软骨肉瘤、成骨肉瘤、骨巨细胞瘤和转移癌是常见诊断。术后高度恶性肿瘤3年以上存活率为54.9%,低度恶性肿瘤为89%,所有侵袭性肿瘤(主要为骨巨细胞瘤)得到局部和全身控制,仅1例需做超半骨盆截除。25例孤立性转移癌患者中14例于术后6个月至3年内发生其他部位转移,主要因肺转移或脑转移而死亡,余11例无瘤存活至少3年以上。所有患者术前不能忍受的疼痛均得到极大减轻或完全消失。手术并发症较低,局部复发率7.8%,骨折率1.3%,感染率
1.2 %。结果证实,与截肢或其他治疗方法相比,微波消融治疗在肿瘤学效果上至少没有负面影响,但功能学效果远超于任何治疗手段。典型病例见图10~16。
3.2 肢体肿瘤
随着影像学技术、新辅助化疗以及手术技巧的进步,保肢手术成为肢体肿瘤治疗的主流。唐都医院采用微波消融保肢手术治疗肢体肿瘤,无论在肿瘤学结果还是功能学结果方面都具有明显的优点,结果令人鼓舞。
我们设计的新型微波消融保肢手术模式,是仅将荷瘤骨从周围的正常组织分离而无需将整块骨关节切除,然后通过微波天线阵列对肿瘤原位灭活,最后对灭活的荷瘤骨段进行加固(包括自体骨移植、异体骨移植、钢板螺钉内固定等)。该术式使骨肿瘤邻近的自然大关节结构得以保留,极大地促进了骨肿瘤患者近期和远期的肢体功能。我们自1992年7月至2009年3月为719例肢体肿瘤患者施行微波消融保肢手术(典型病例见图17~27)。其中高度恶性肿瘤629例(主要是成骨肉瘤,恶性纤维组织细胞瘤和伊文氏肉瘤分别居第2、3位),低度恶性肿瘤62例(主要有软骨肉瘤42例、造釉细胞瘤16例),孤立性转移癌28例。肿瘤类型分布,患者性别、年龄与文献报道无明显差别。术前均给予2~3个疗程的化疗。微波消融保肢术后高度恶性肿瘤3年生存率为59.1%,低度恶性肿瘤3年生存率为88.7%。尽管转移癌患者手术的主要目的是姑息性和减轻症状,但也有11例得到长期的局部和全身控制。并发症包括局部复发(8.5%),深部感染(1.8%),术后骨折(5%,多发生在研究早期)。绝大多数存活病例所保留的肢体无论从美容学上还是功能学上均满意,按世界保肢学会标准,平均功能得分在90%以上。一旦痊愈无远期松动之虞。
3.3 脊柱肿瘤
脊柱肿瘤的治疗仍是骨肿瘤医师必须面对的重大挑战,所谓的全椎体切除往往不能达到严格意义上的“无瘤操作”,瘤体破碎后污染手术野,成为术后复发的主要原因。微波对于单发的椎体肿瘤,可以较为方便地进行消融治疗(图28)。尽管仅适用于脊柱肿瘤中的少部分病例,但容易达到安全界限,控制率较高。目前我们应用此法处理数十例病例,近期效果满意,随访正在进行之中。
在脊柱肿瘤外科领域中,骶骨肿瘤的治疗是难点之一。以常见的脊索瘤为例,切除后复发率甚高。往往从影像学资料判断,截除平面似乎已达到安全界限,但仍有部分病例复发。我们有3例截除病例,本以为截断面是安全的,但镜下依然发现有肿瘤灶存在(图29)。因此,在截除骶骨之前,首先于预计的截骨线处插入微波天线,实行消融措施,然后再进行手术,复发率可获明显降低。对于高达S1平面的肿瘤,少数学者报道全骶骨切除治疗方式,但手术创伤大,失血多,术后神经功能缺失较为明显,脊柱和骨盆间的联系也不容易稳定,尽管有钉棒系统加植骨等重建方法,但往往不甚牢靠,易出现脊柱下沉。因此对于某些高位骶骨病变,可以采取微波消融后刮除的方法;而对于某些神经源起源的肿瘤,可直接摘除,控制率高,骨腔无需植骨,效果较好。我们对97例骶骨肿瘤进行微波消融治疗。其中33例为脊索瘤,施行骶骨部分切除手术,8例(24%)出现复发;11例为神经源肿瘤,均手术摘除,无一例复发。53例S1~S3平面的骶骨肿瘤中,33例行单纯刮除手术,18例先行微波消融然后刮除,结果全部得到控制。典型病例见图30,31。
4 存在问题
4.1 儿童病例的治疗选择
对于骨发育不成熟的儿童病例而言,发生在膝关节周围的恶性骨肿瘤如实行假体置换,则需要牺牲股骨远端和胫骨近端2个大骨骺,发育成熟后患儿肢体长度的不平衡将会达到不可接受的程度,且各种可延长假体的技术尚未成熟。微波消融保肢技术仅需牺牲1个大骨骺。我们对12岁以上的儿童实行保肢手术,肢体不平衡约3 cm左右,可通过矫形鞋等予以克服。
4.2 适应证问题
微波消融的最佳适应证是所有骨盆和长管骨的早中期恶性肿瘤。但诊断偏晚的患者往往瘤体较大,骨质破坏严重,残留的可资利用的骨质甚少,灭活后重建困难。在这种情况下,我们倾向于假体置换或异体骨移植。
4.3 精确加温问题
微波消融过程中一旦温度过低,哪怕只是微小的部位,也很容易造成局部复发;温度过高则没有必要,对骨再生也有负面影响。在临床上往往采取宁高勿低(better higher than lower)的原则。肿瘤是物理学上的非均质体,有些病例以溶骨为主,有些病例以成骨为主,其介电系数差异较大,因而对微波能量的吸收速率相差显著。在实行微波消融时,所需天线的数量以及分布方式等尚无精确的标准,多依赖于医生的经验。尽管我们采用有限元重建、计算机模拟等方法进行系统研究,但这些方法何时能指导临床尚未可知。与工程技术人员密切协作,设计出更为简单易行而又精确的加热方法,也是未来研究的一个方向。
(本文编辑 白朝晖)

图1 Calcein-AM&PI染色结果

图2 流式细胞仪检测杀死活细胞的热剂量结果 2A 50℃5 min 2B 60℃5 min 2C 70℃5 min 2D 80℃ 5 min 2E 95℃10 min 2F正常
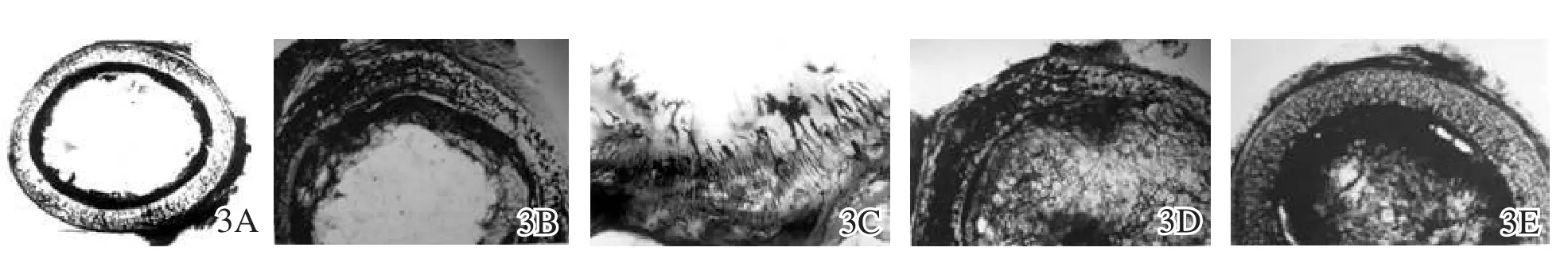
图3 墨汁灌注法显示犬灭活骨远期归宿结果 3A 12周 3B,3C 6个月 3D 1年 3E正常

图4 四环素标记法显示哈弗氏管周围有新骨生成(2周~11个月追踪结果)
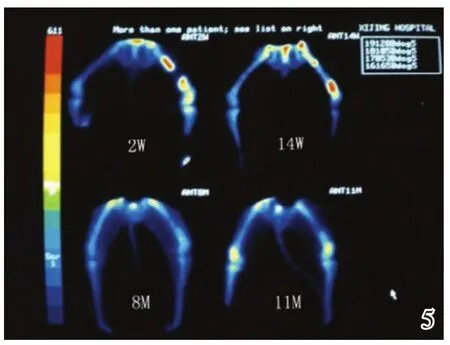
图5 骨扫描结果(2周~11个月追踪结果)

图6 Instron-1341仪和测试样本
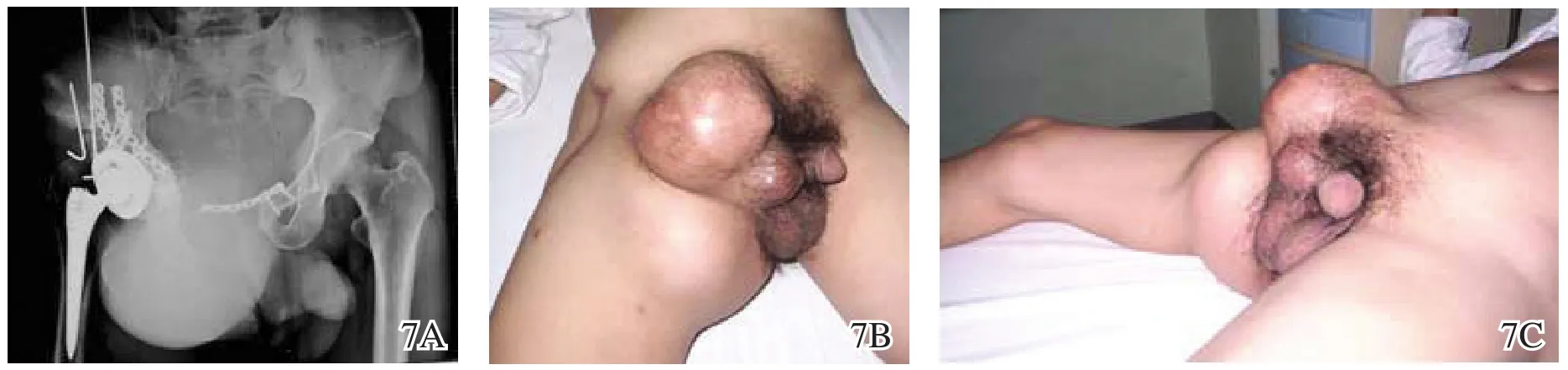
图7 耻骨上支软骨肉瘤切除加重建术后严重复发图片 7A术后X线片 7B,7C术后肿瘤复发
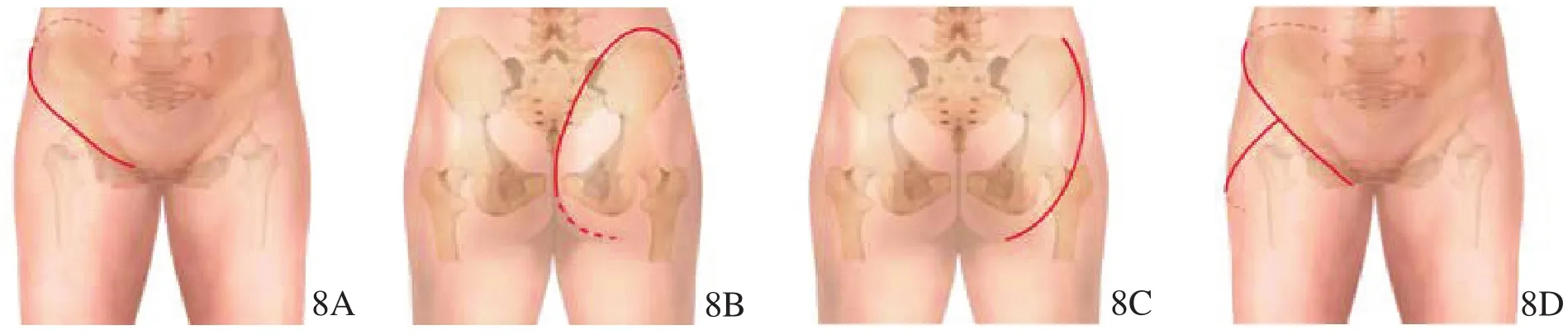
图8 骨盆肿瘤微波消融手术常用切口示意图(8A,8B臀大肌瓣向外翻 8C,8D臀大肌瓣向内翻)8A单纯前方 8B单纯后方 8C单纯后方 8D T形切口

图9 骨盆肿瘤手术常用重建方法示意图 9A旷置 9B髂股融合 9C坐股融合 9D金属假体置换 9E鞍状假体置换 9F异体骨盆移植或瘤骨体外灭活再植术
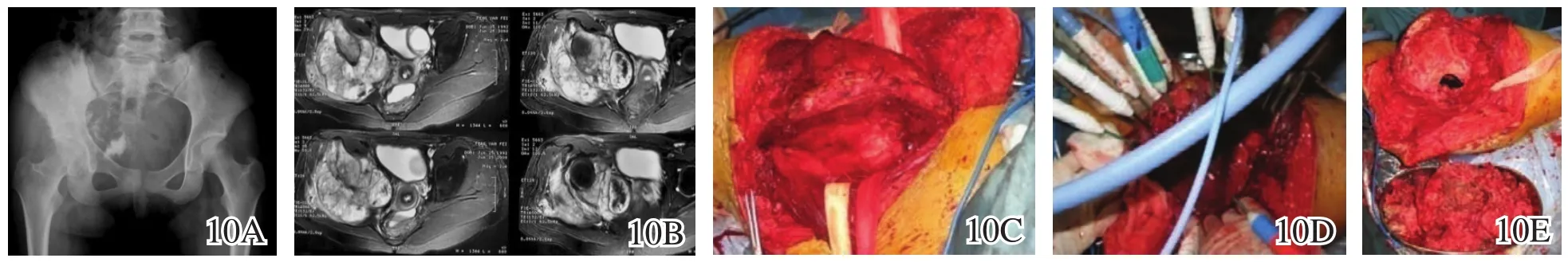
图10 骨盆巨大软骨肉瘤微波消融手术前后图片 10A X线片示骨盆软骨肉瘤伴不规则异位钙化 10B MRI示肿瘤突入并充满坐骨大孔10C盆腔内外暴露 10D微波灭活及温度监控 10E去除松软灭活肿瘤,恢复骨轮廓
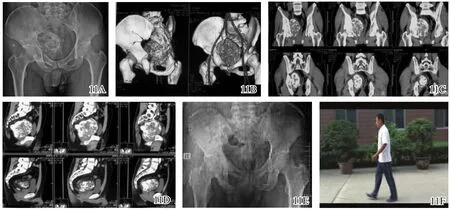
图11 骨盆巨大软骨肉瘤微波消融治疗前后图片 11A~11D术前影像学图片示侵及1、2、3区的骨盆巨大软骨内瘤 11E术后X线片11F术后功能完好,可跑跳

图12 耻骨上支软骨肉瘤微波消融围术期图片 12A,12B术前X线及CT扫描 12C~12G仅需内侧暴露,1根天线即可达到灭活目的,闭孔神经也得以保留 12H,12I术后影像学图片
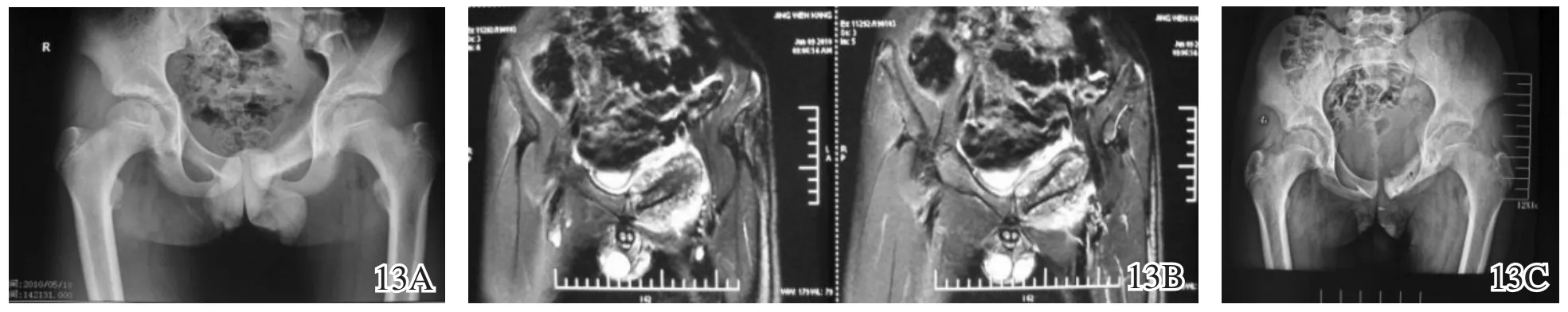
图13 耻骨上支成骨肉瘤微波消融手术前后图片 13A,13B术前影像学图片示骨轮廓外包块较大且侵及髋臼前柱 13C术后X线片

图14 典型II区恶性肿瘤微波消融手术前后图片 14A~14C术前影像学图片 14D微波灭活肿瘤 14E模式图显示髋关节降温措施14F,14G用骨粒和骨水泥混合物充填髋关节内柱和上方残腔,并以钢板固定 14H术后X线片

图15 坐骨恶性肿瘤微波消融治疗图片 15A~15C术前影像学图片 15D仅需骨盆外侧暴露,切断骶结节韧带和骶棘韧带,置一大纱布垫于肿瘤和盆内脏器之间,以保护坐骨直肠窝的内脏不受热损伤 15E微波灭活 15F,15G去除灭活后的松软肿瘤组织
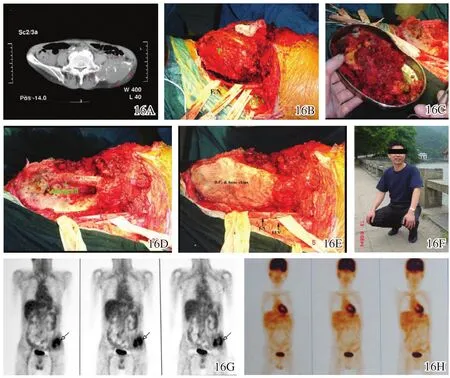
图16 孤立性肝癌转移骨盆巨大病灶微波消融手术前后图片 16A术前CT显示肿瘤侵犯骶髂关节 16B骨盆内外侧暴露,牵开并保护重要的血管神经 16C去除灭活后的松软肿瘤组织 16D自体骨移植 16E用骨粒和骨水泥混合物重塑骨盆壁 16F术后8年功能依然完好 16G,16H术前PET显示左侧骨盆高浓缩区,术后PET高浓缩区完全消失

图17 保肢手术前后图片 17A术前X线片 17B 术后X线片,佩戴免负重支架3~6个月 17C术后11年,肢体功能完好
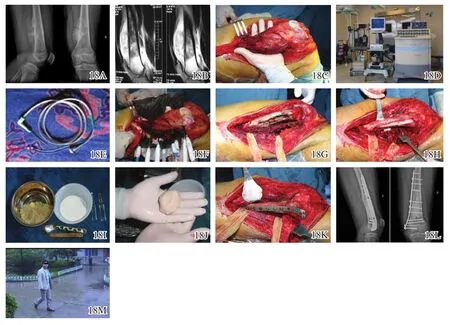
图18 股骨远端成骨肉瘤的典型微波消融保肢手术治疗前后图片 18A,18B影像学显示股骨远端成骨肉瘤 18C在保证安全界限的前提下,将荷瘤骨段从周围正常组织中分离 18D,18E微波发生器和天线 18F将电磁波能量引入瘤体 18G切除或刮除失活的松脆瘤组织 18H自体腓骨移植 18I~18K 用异体骨骨屑与骨水泥的混合物充填剩余间隙,恢复股骨正常轮廓并给予钢板螺钉预防性内固定 18L术后X线片 18M 术后11年功能完好,恢复至运动级
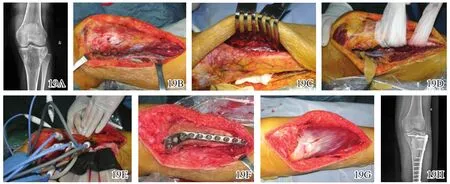
图19 胫骨近端恶性纤维组织细胞瘤的典型微波消融保肢手术治疗前后图片 19A术前X线片 19B打开比目鱼腱弓,暴露至胫前、胫后血管分叉处 19C分离胫前肌群,切开骨间膜 19D游离胫后肌群,完成荷瘤骨段的分离 19E微波灭活 19F加固 19G转移腓肠肌内侧头覆盖灭活骨19H术后X线片
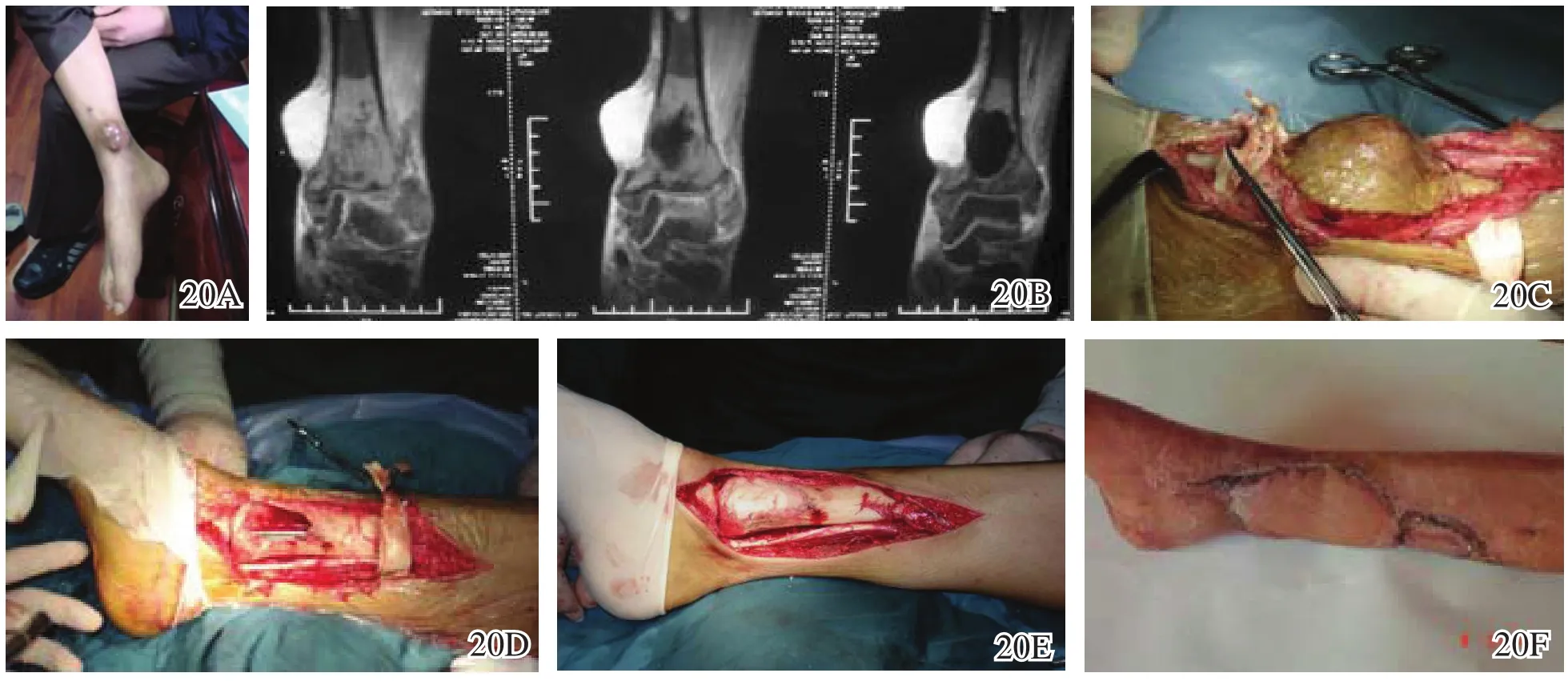
图20 胫骨远端复发性恶性纤维组织细胞瘤的微波消融手术前后图片 20A术前患肢图片 20B术前MRI 20C~20E微波灭活后采用游离皮瓣移植覆盖伤口 20F术后伤口愈合图片
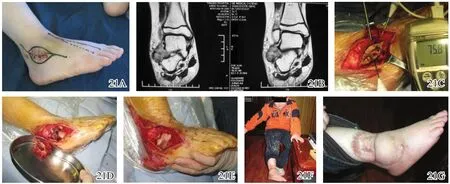
图21 跗骨窦滑膜肉瘤的微波消融保肢手术治疗前后图片 21A术前患肢图片 21B术前MRI 21C~21E微波消融后局部皮瓣转移覆盖伤口 21F,21G术后患肢图片
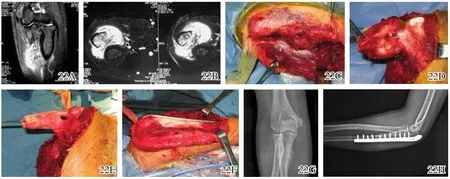
图22 尺骨近端成骨肉瘤的微波消融保肢手术治疗前后图片 22A,22B术前MRI 22C~22F术中完好保留重要的桡神经深支,并对荷瘤骨进行微波消融治疗 22G微波灭活后X线片 22H内固定术后X线片

图23 股骨近端甲状腺癌孤立性转移灶微波消融治疗前后图片 23A术前X线片 23B术中消融 23C术后X线片,髋关节功能良好
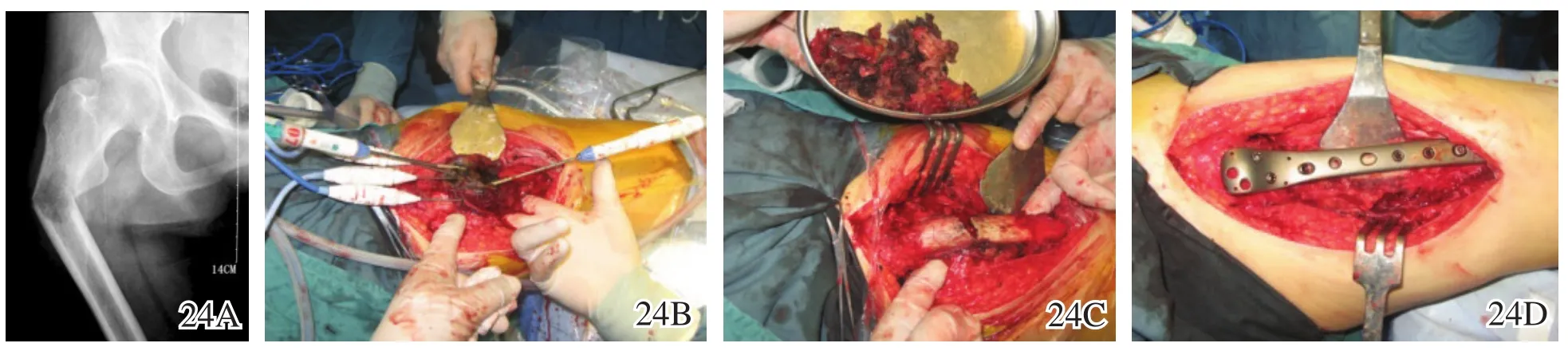
图24 股骨近端转移癌伴病理性骨折的微波消融保肢手术术前、术中图片 24A术前X线片 24B~24D治疗过程
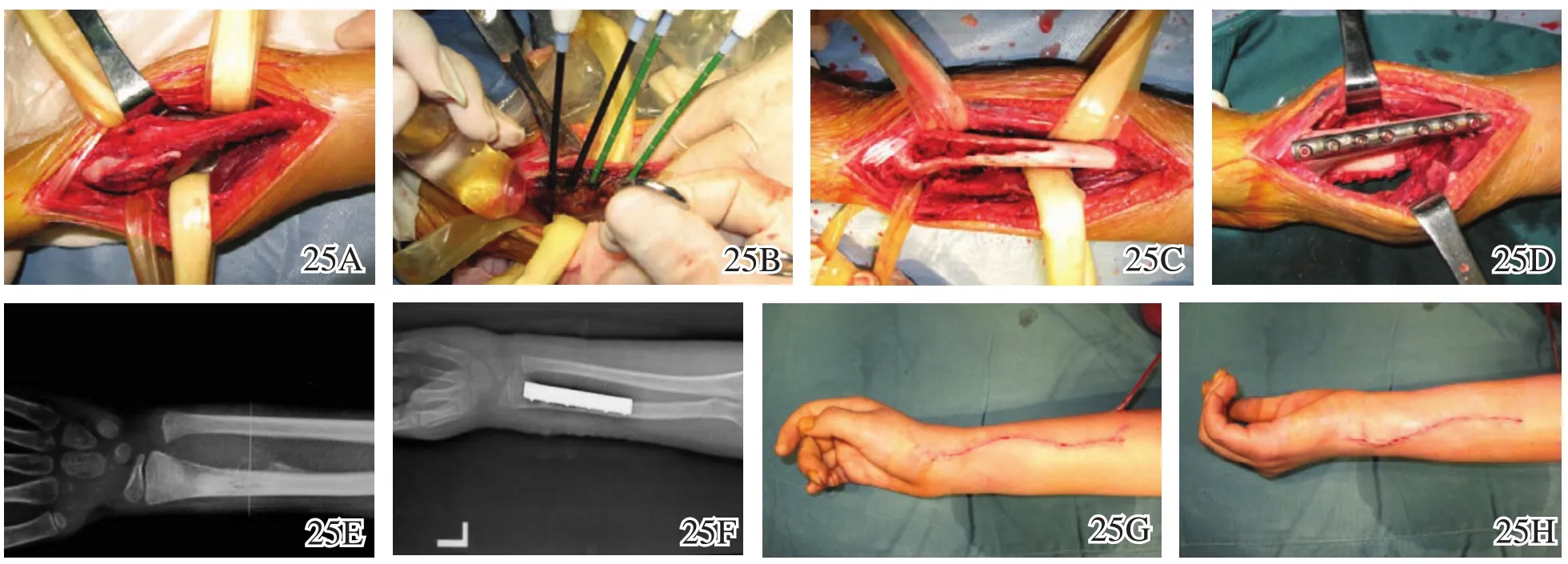
图25 桡骨远端成骨肉瘤微波消融保肢手术术中、术后图片 25A内外侧纵形切口完好地暴露荷瘤骨段 25B~25D治疗过程 25E微波灭活后X线片 25F术后X线片 25G,25H 术后患肢图片

图26 微波消融截骨病例(骨轮廓外肿瘤包块过大,重要结构分离困难)图片 26A~26C股骨近端巨大骨肉瘤术前影像学及术中图片 26D~26F胫骨近端巨大成骨肉瘤术前影像学及术中图片 26G胫骨、腓骨均需截骨的术中图片 26H肱骨近端需要截骨的术中图片(保留腋神经和桡神经)26I~26P需截骨的胫骨近端巨大软骨肉瘤术前影像学、术中显露与灭活、术后小腿外观以及术后X线片

图27 肩胛骨恶性肿瘤保肢手术前后图片 27A,27B术前DSA 27C,27D术中微波消融治疗 27E术后肩关节稳定,功能尚满意,可外展70°,保留完好的肘和手
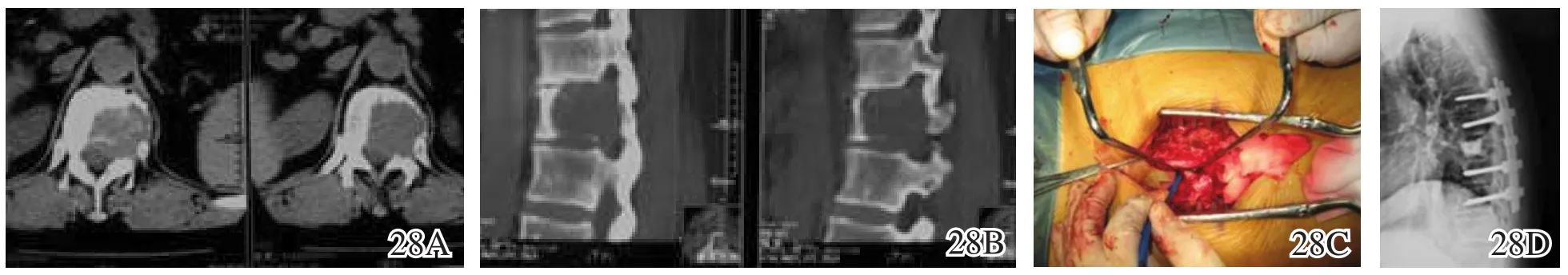
图28 T9血管瘤微波消融手术前后图片 28A,28B术前影像学 28C拉开脊髓,向瘤体内插入1根软天线,在消融的同时用生理盐水滴注脊髓,以免过热;灭活后以刮勺刮除松脆的灭活组织,然后以骨屑水泥混合物充填瘤腔 28D术后X线片

图29 骶骨脊索瘤微波消融截骨手术切除图片 29A,29B手术截除正面、背面观(可见经S2水平的截骨线)29C病理学检查示截骨线上仍有微型病灶 29D牵开双侧S1、S2神经根,结扎切断马尾 29E预定截骨线处,微波消融处理 29F三叶草样手术切口和切除标本
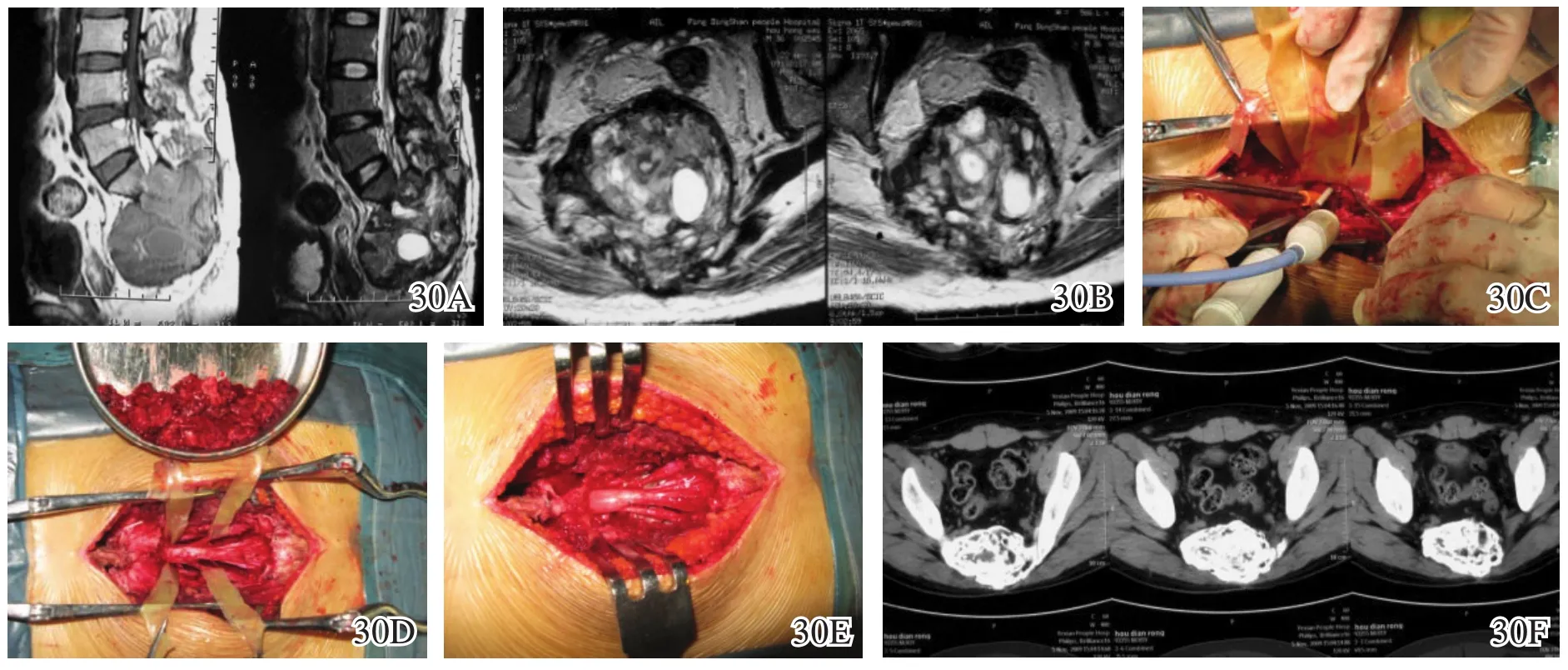
图30 高位骶骨肿瘤的微波消融刮除术图片 30A,30B术前MRI显示高达S1平面的巨大骨巨细胞瘤 30C瘤腔内微波消融 30D刮除肿瘤 30E用顺铂干粉和明胶海绵植入残腔,对神经根无损害 30F术后18个月CT示瘤腔已高度硬化,肿瘤治愈
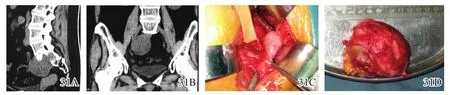
图31 S1平面的神经鞘膜瘤手术切除图片 31A,31B术前影像学示肿瘤起源于S1、S231C经腹腔入路,牵开输尿管,暴露髂内血管 31D完整摘除的肿瘤标本
R738.1,R454.1
A
1674-666X(2011)03-0304-14
2011-11-01;
2011-11-29)
10.3969/j.issn.1674-666X.2011.04.013
710038西安,第四军医大学唐都医院全军骨肿瘤研究所
E-mail:bonetm@fmmu.edu.cn

