骨水泥的遗传毒性研究
胡燕平,宋捷,马锐,王欣,郭隽,王 雪中国食品药品检定研究院国家药物安全评价监测中心,北京, 100176
骨水泥的遗传毒性研究
【作者】胡燕平,宋捷,马锐,王欣,郭隽,王 雪中国食品药品检定研究院国家药物安全评价监测中心,北京, 100176
目的检测医疗器械进口产品骨水泥的遗传毒性。材料与方法以骨水泥粉体浸提液与其液体混合液为供试液,采用细菌回复突变试验(Ames 试验) 和小鼠淋巴瘤细胞试验(MLA),在非代谢活化(-S9)和代谢活化(+S9)条件下检测。Ames 试验采用平板掺入法,检测了25、50、100 μl /皿 3个剂量组诱发鼠伤寒沙门氏菌(S.typhimurium)TA98、TA100、TA1535、TA1537及大肠杆菌(E.coli)WP2 uvrA的回变菌落数;MLAT采用微孔法检测了终浓度0.125%、0.25%、0.5% (V/V) 3个浓度组,在+S9/3 h、-S9/3 h、-S9/24 h三种处理条件下诱发L5178Y细胞tk+/-基因突变频率(MF)和小集落突变百分率(SC%)。结果Ames试验,50、100 μl /皿剂量组在加入磷酸缓冲液或S9混合液后略有沉淀产生,并对TA100、TA1535、WP2 uvrA产生不同程度的抑菌作用,无抑菌剂量诱发五株菌的回变菌落数对比DMSO溶媒(阴性)对照组,均无明显增加;MLA,各浓度组在三种处理条件下诱发的MF、SC%与其溶媒(阴性)对照组比较,无明显增加(P>0.05)。结论本实验条件下,骨水泥对测试菌株his-/trp-无明显诱变作用,对测试细胞tk+/-及染色体无明显损伤作用。
骨水泥;细菌回复突变试验;小鼠淋巴瘤细胞试验;遗传毒性
骨水泥主要用于关节成形术、创伤型的关节损伤、骨关节炎及骨质疏松中假体与活体骨组织的固定[1]。为确保产品的使用安全,本文按照医疗器械产品检测的相关标准及要求[2-4],采用细菌回复突变试验(Bacterial Reverse Mutation Assay, Ames test)[5]和小鼠淋巴瘤细胞试验(Mouse Lymphoma Assay, MLA)[6],对骨水泥进行了遗传毒性检测。
1 材料与方法
1.1材料
1.1.1 样品与对照品
骨水泥由法国Teknimed SAS公司生产、北京劲健昌达医疗科技有限公司提供,批号043G/0823,型号Gentafix3 (货号T040340G)。1套骨水泥包括41.6 g粉体和16.4 g液体,粉体含84.3%聚甲基丙烯酸甲脂、2.3%过氧化苯甲酰、9.6%硫酸钡、3.8%硫酸庆大霉素;液体含 84.4%甲基丙烯酸甲脂、13.2%甲基丙烯酸丁脂、20 ppm氢醌。将粉体按照0.2 g/ml浸提比例加入介质二甲基亚砜(DMSO),在37℃±1℃、水浴摇床18~20 r/min条件下浸提24 h ±1 h,所得浸提液再与其液体混合,以此混合液作为供试液。阴性对照品(即浸提介质) DMSO,TEDIA生产;阳性对照品叠氮钠(NaN3),MERCK-Schuchardt生产;9-氨基吖啶(9-AA),ACROS ORGANICS生产;2-氨基蒽(2-AA),Fluka生产;呋喃基糠酰胺 (AF-2)、苯并芘 (B〔a〕P),日本和光纯药工业株式会社生产;甲基甲烷磺酸酯(MMS)、环磷酰胺(CP)及突变选择剂三氟胸苷(trifluorothymidine,TFT),均购自SIGMA。
1.1.2 菌株与细胞
Ames 试验选用鼠伤寒沙门氏菌组氨酸营养缺陷型(his-)菌株(S.typhimurium) TA98、TA100、TA1535、TA1537和大肠杆菌色氨酸营养缺陷型(trp-)菌株(E.coli) WP2 uvrA,菌种引自日本(株)生物科学中心(JBS INC.)。菌种经本实验室分离筛选、扩大培养、特性鉴定合格者置-80℃超低温冰箱保存。试验前定量接种细菌冻融液,水浴摇床37℃、120 r/min培养10 h。培养结束,测定新鲜菌液光密度(OD),经计算确认活菌数浓度达1×109/ml以上的菌液用于试验。MLA选用小鼠淋巴瘤细胞L5178Y tk+/--3.7.2C,细胞引自日本国立医药品食品卫生研究所,经过纯化及支原体检查,合格者扩大培养,置液氮保存,复苏后传代5次以内使用。
1.1.3 培养基与试剂
Ames 试验:营养肉汤 (CM0067 Nutrient broth No.2),英国OXOID生产;琼脂粉(Agar Powder),购自日本。MLA完全培养基由RPMI 1640培养基(GIBCO)、NaHCO3(北京化学试剂公司,终浓度0.2% W/V)、青链霉素混合液(KeyGEN,终浓度1%)、丙酮酸钠(Amresco,终浓度200 μg/ml)配制而成。根据用途不同,分为含10%马血清(传代、处理培养)、20%马血清(96孔板培养)和不含马血清(稀释)的培养液。TFT,终浓度3 μg/ml。
1.1.4 代谢活化剂
S9由苯巴比妥钠与β-萘黄酮联合诱导处理大鼠肝而获得,本实验室自制。Ames 试验用S9混合液(S9mix)中的S9含量为10%[7],MLA所用S9在处理液中的终浓度为2%,检测时,S9与180 mg/ml的Glucose-6-Phosphate、25 mg/ml的NADP、0.15 mol/L的KCl等辅助因子溶液,按2:1:1:1(ml)的比例配制成S9mix。
1.2方法
1.2.1 细菌回复突变试验[7]
采用标准平板掺入法。设立骨水泥(粉体浸提液与其液体混合物)3个剂量组25、50、100 μl/皿,同时设立DMSO溶媒(阴性)对照组及阳性对照组,每组平行3皿,在-S9和+S9条件下同时检测。平板置37℃培养48 h,计数回变菌落数,实验数据以x±s表示。若在-S9和/或+S9条件下,在所设剂量范围内,一株以上试验菌的回变菌落数呈现剂量相关性增加,或一个以上剂量诱发的回变菌落数呈现可重复性并有统计学意义时,判为阳性,反之则为阴性。
1.2.2 小鼠淋巴瘤细胞试验[8-9]
采用微孔法设立骨水泥 (粉体浸提液与其液体的混合液) 终浓度0.125%、0.25%、0.5% (V/V) 3个浓度组,同时设立DMSO溶媒(阴性)对照组和阳性对照组(+S9:CP; -S9:MMS),每组平行2支处理管,在+S9/3 h、-S9/3 h、-S9/24 h三种处理条件下分别进行检测。+/-S9条件下的3 h处理,各组供试液-细胞处理液于37℃振荡培养箱中作用3 h;-S9条件下的24 h处理,各组供试液-细胞处理液于37℃、5%CO2孵箱中静置作用24 h。处理、清洗后的细胞于37℃、5%CO2孵箱中培养2 d进行表达,制备检测接种效率的PE0、PE2平板,于37℃、5%CO2孵箱分别培养9~10 d、7~8 d;检测基因突变频率的MF平板于表达结束后制备,37℃、5%CO2孵箱培养12~14 d。培养结束,计数含与不含接种效率细胞克隆的孔数并计算PE0和PE2、细胞相对存活率(RS%)、相对悬浮生长率(RSG)、相对总生长率(RTG);观察并分别计数含有突变细胞大集落(LC)、小集落(SC)及大、小集落(LC/SC) 并存的孔数,计算基因突变频率(MF)以及小集落突变百分率(SC%)。采用“Poisson分布两样本均数的比较”方法,将处理组的突变率与溶媒对照组进行比较、分析。如果一个或多个浓度组出现浓度依赖性和/或可重复性的突变率增加,且任意浓度组MF值>阴性对照组MF值+126 (总体评价因子,GEF)[10-11],则判定为阳性结果,反之则为阴性。
2 结果
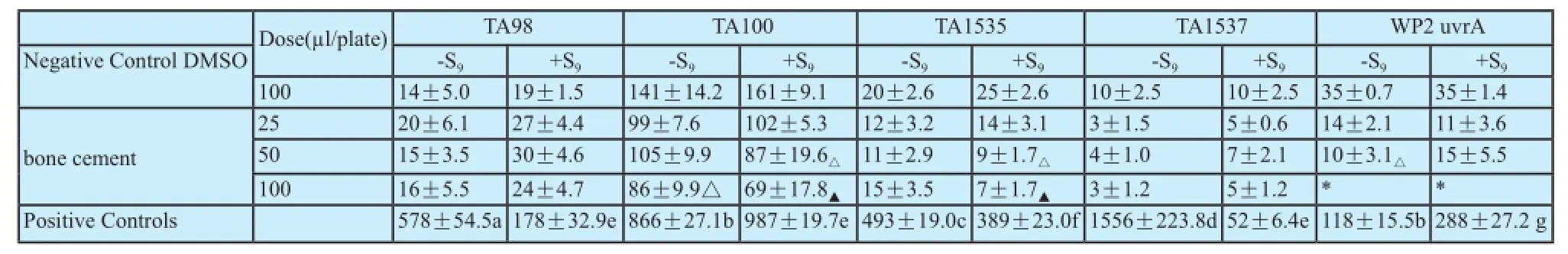
表 1 骨水泥的Ames试验结果Tab.1 Results of Ames test on bone cement (χ±s )
2.1细菌回复突变试验
如表1所示,+/-S9条件下,DMSO阴性(溶媒)对照组的回变菌落数平均值均在文献[12]报道的背景数据范围内,阳性对照组诱发的回变菌落数均达到阴性对照组的3倍以上,显示出明显的诱变能力。骨水泥(粉体浸提液与其液体混合物)的3个剂量组中,50、100 μl/皿剂量组在加入磷酸缓冲液或S9混合液后略有乳白色沉淀产生,并在培养48 h后表现出对TA100、TA1535、WP2 uvrA三菌有不同程度的抑菌作用,无抑菌剂量诱发五株菌的回变菌落数,对比阴性对照组均无明显增加。
2.2小鼠淋巴瘤细胞试验结果
如表2表3和表4所示,阴性对照组的PE、MF均在本实验室的背景数据范围内(PE:50~160%;MF:110×10-6~250×10-6);阳性对照组诱发的MF达到阴性对照组的3倍以上(P<0.01),并以小集落突变体为主。骨水泥(粉体浸提液与其液体的混合液)各浓度组,在三种处理条件下得到的RTG均大于30%,符合本试验方法中细胞毒性小于90%的要求;与DMSO溶媒(阴性)对照组比较,诱发的MF未见明显增加(P>0.05)。
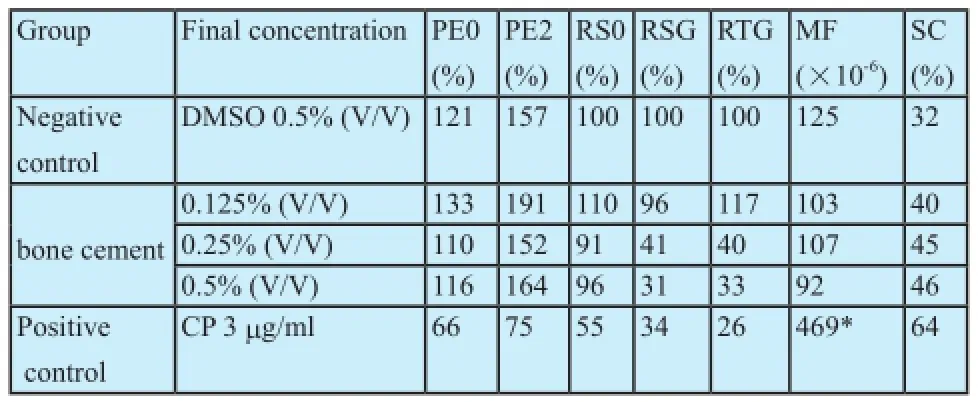
表2 +S9/3 h条件下骨水泥的MLA试验结果Tab.2 Results of MLA on bone cement with S9at 3 h
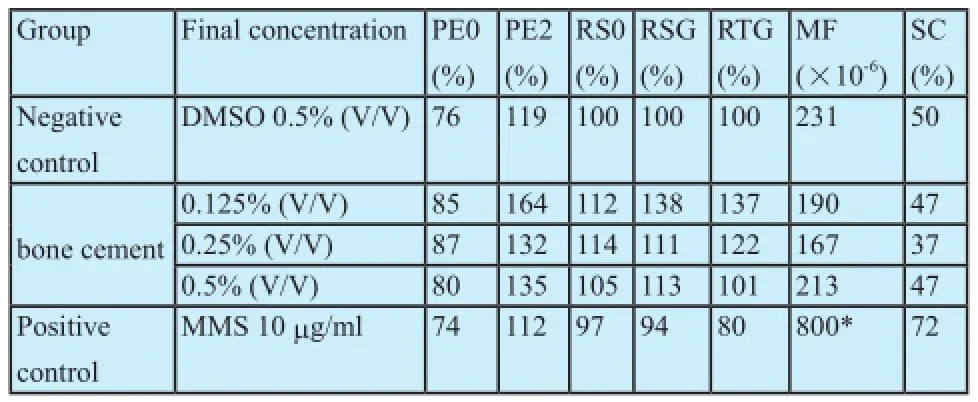
表 3 -S9/3 h条件下骨水泥的MLA试验结果Tab. 3 Results of MLA on bone cement without S9at 3 h
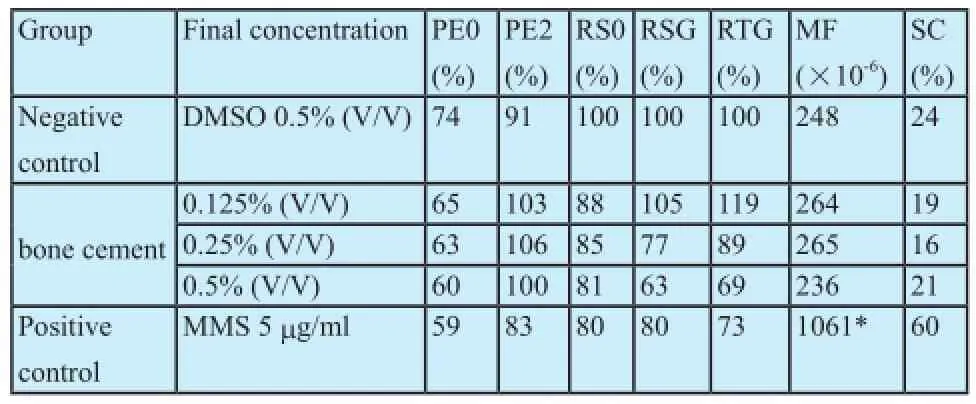
表 4 -S9/24 h条件下骨水泥的MLA试验结果Tab.4 Results of MLA on bone cement without S9at 24 h

3 讨论
骨水泥的成分较为复杂,多为不溶于水的有机物质,为此本文在实施检测前首先对浸提介质进行了选择:骨水泥的粉体部分经生理盐水浸提后呈浑浊状态,而经有机溶剂DMSO浸提后固、液分层清晰;骨水泥的液体部分与生理盐水混合后分层而与DMSO相溶。因此,本研究选用了DMSO作为骨水泥的浸提介质,而非通常使用的生理盐水。Ames试验所用5株测试菌可检测his-/trp-不同点突变,MLA试验的灵敏度高、可检测tk+/-基因突变和诱裂性两个遗传终点。研究结果表明,骨水泥对检测碱基置换型突变的三株菌TA100、TA1535、WP2 uvrA具有不同程度的抑菌作用,可能是试验菌对产品含有的硫酸庆大霉素或其它抑制细菌生长成分的敏感性不同所致(批号043Z/0836、不含硫酸庆大霉素的同类产品骨水泥未出现抑菌现象,资料另发表)。骨水泥在+S9/3 h、-S9/3 h、-S9/24 h三种处理条件下,诱发的tk+/-基因突变率及小集落突变百分率,均与阴性对照组相近。另外,该产品中含有文献报道的致突变/致癌物氢醌[13-15],可能因其含量极少而未对研究结果造成明显影响。在本实验条件下,未检测出骨水泥对his-/trp-具有明显诱变作用和对tk+/-及染色体具有明显损伤作用。
[1] 法国Teknimed SAS公司. 医疗器械注册产品标准YZB/Teknimed 0001-2009[S]. 2009
[2] 中华人民共和国国家标准GB/T 16886.3—2008/ISO 10993-3:2003《医疗器械生物学评价第3部分: 遗传毒性, 致癌性和生殖毒性试验》[S].
[3] 中华人民共和国国家标准GB/T 16886. 12—2005/ISO 10993-12: 2002《医疗器械生物学评价第12部分: 样品制备与参照样本》[S].
[4]《药物遗传毒性研究技术指导原则》课题研究组. 药物遗传毒性研究技术指导原则[S].2007
[5] OECD TG 471, Bacterial Reverse Mutation Test[S]. 1997
[6] OECD TG 476, In Vitro Mammalian Cell Gene Mutation Test[S]. 1997
[7] 日本バイオアッセイ研究センター 微生物实验室. 微生物を用いる変异原性试验手法解説[M]. 第1刷. 神奈川県秦野: 中央労働災害防止協会 日本バイオアッセイ研究センター, 1999: 16-17.
[8] 谢 明.小鼠淋巴瘤细胞基因突变试验方法[J].癌变·畸变·突变, 2003. 15(3):183-186.
[9] 赵 洁, 胡燕平, 宋 捷, 等. 小鼠淋巴瘤细胞基因突变方法的建立与应用[J]. 毒理学杂志, 2006. 20(4):268-269.
[10]Martha M.Moore,et.al. mouse lymphoma thymidine kinase gene mutation assay: follow-up meeting of the international workshop on genotoxicity testing—aberdeen, scotland, 2003-assay acceptance criteria, positive controls, and data evaluation[J]. Environmental and Molecular Mutagenesis. 2006, 47: 1-5.
[11]Martha M.Moore, et.al. Mouse lymphoma thymidine kinase gene mutation assay: Meeting of the International Workshop on Genotoxicity Testing, San Francisco, 2005, recommendations for 24-h treatment[J]. Mutation Research, 2007, 627: 36-40.
[12]胡燕平, 宋捷, 李波. 细菌回复突变试验背景数据的采集[J]. 中国新药杂志, 2009, 18 (22): 2110-2112.
[13]McGregor D. Hydroquinone: an evaluation of the human risks from its carcinogenic and mutagenic properties[J]. Crit Rev Toxicol. 2007,37(10):887-914.
[14]Luo L, Jiang L, Geng C, et.al. Hydroquinone-induced genotoxicity and oxidative DNA damage in HepG2 cells[J]. Chem Biol Interact. 2008, 173(1): 1-8.
[15]Regev L, Wu M, Zlotolow R,et.al. Hydroquinone, a benzene metabolite, and leukemia: A case report and review of the literature[J]. Toxicol Ind Health, 2011, Apr 21. [Epub ahead of print]
Genotoxicity Study of Bone Cement
【Writers 】HuYanping, Song Jie, Ma Rui, Wang Xin, Guo Jun, Wang Xue National Center for Safety Evaluation of Drugs, National Institute for Food and Drug Control, Beijing, 100176, China
bone cement, bacterial reverse mutation test (Ames test), mouse lymphoma assay (MLA), genotoxicity.
Q355
A
10.3969/j.issn.1671-7104.2011.06.008
1671-7104(2011)06-0425-03
2011-09-25
胡燕平,副主任药师;研究方向:遗传毒性研究。E-mail: huer64@126.com
【 Abstract 】ObjectiveTo investigate the genotoxicity of bone cement.Material and MethodsTest article was mixed of liquid and the powder extract of bone cement. Using bacterial reverse mutation test (Ames test) and mouse lymphoma Assay (MLA) with and without metabolic activation S9. Ames test was performed by the plate incorporation method for its ability to induce reverse mutations in three treatment dosage groups: 25 μl/plate, 50 μl/plate, 100 μl/plate using S.typhimurium TA98、TA100、TA1535、TA1537 and E. coli WP2 uvrA; In MLA, the mutation frequency (MF) and the percentage of small colony mutants (SC%) of L5178 tk+/-cells induced by bone cement at final concentration of 0.125%, 0.25% and 0.5% (V/V) were calculated and assayed with +S9/3 h, -S9/3 h, -S9/24 h.ResultsSlight precipitations of two dosage group 50 μl /plate and 100 μl/plate were observed after phosphoric acid buffer solution or S9mix added. Growth inhibition effect exists in TA100, TA1535 and WP2 uvrA to varying degrees. Other groups did not cause obvious increases in the mean number of revertant per plate compared with negative control (DMSO). The result of MLA indicated no significant MF or SC% increases (P>0.05) observed comparing with negative control under all test conditions.ConclusionsThe bone cement did not induce reverse mutation at his-/trp-and there was no obvious damage effect to gene tk+/-or chromosome under this study condition.

