浅谈化学思想方法的迁移在解题中的应用
王瑞俊
(江苏省华罗庚中学 江苏 金坛 213200)
作为全国第一批试点——江苏省已于2005年秋在全省实施了高中新课程,到现在已经整整6年时间,已有三届学生参加了新课程实施后的新高考。作为化学教师,对新课程实施前后新老教材特点的差异深有体会——老教材更强调化学知识体系的完整性和学生对“双基”的学习;新教材则强调“从生活中学习化学”,强调化学课堂中学生的探索精神、探究能力的培养,更符合现代社会的“人才观”。
高中化学新课程实施过程中,教师、学生特别是教师已经由“不适应”到“适应”,打破课堂旧有的“以教师教为中心”的理念,更新观念,成为新课程中“学生学习的组织者和引导者”,还时间给学生,充分体现“学生的主体性”,发展学生的兴趣、爱好。在新课程标准中给我们化学老师的时间并不多,除了完成新课教学任务外,几乎没有多少时间来进行习题训练。怎样提高学生的课堂听课效率,怎样提高习题训练课的授课效率成为摆在化学教师面前的一项重要课题。
化学这门学科的特点本身就是以实验为基础的学科,特别是高中化学很多的理论是根据实验得到的经验规律,没有数学、物理逻辑性强。这给初学化学的同学一种印象——化学知识比较琐碎,不容易系统地概括和记忆。部分同学所以会出现孤立地看问题,不能做到灵活应用。我们可以通过以高中化学的主干理论如质量守恒定律、氧化还原反应得失电子守恒等等为线索跨模块地进行复习来让我们化学的知识体系更为紧密,使学生更容易掌握。除了把握主干理论进行复习以外,善于发现解决不同模块问题方法的共同点,用同一化学思想方法解决不同问题也是提高习题训练课的授课效率的好方法。下面通过应用高中经典化学思想方法的迁移解决实际问题的两个例子,希望起到抛砖引玉的作用,打开大家智慧的“潘多拉盒子”。
例1:在如图所示的容器中发生下列可逆反应xA+yB⇌zC。达到平衡时,试填空:
(1)若A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z关系是______;
(2)若C是气体,并且x+y=z,在加压时化学平衡可发生移动,则平衡必定是向______方向移动;

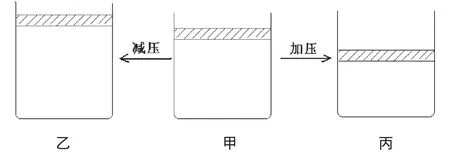
该模型中以下两个问题需要明确:对于反应 xA(g)+yB(g)⇌zC(g),其中甲→乙减压过程可以采取哪些手段?答案是直接扩大容器体积或充入与反应无关的气体。前者不难理解,后者则通过A、B、C三种气体的总压强减小来解释。那甲→丙增压过程可采取哪些手段?答案是压缩容器体积或保持容器体积不变加入C气体或保持容器体积不变成比例的加入A和B。后面两种情况分两步来理解,先将容器扩大一倍容器中的气体的物质的量也扩大一倍后压缩至原容器体积(等效平衡的思维方法)。该模型可以解决大部分气体反应中的平衡移动问题。
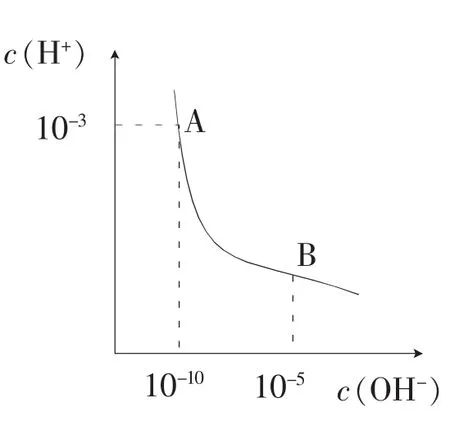
能不能将该模型运用到其他非气态的平衡体系中呢?答案是肯定的。如下图所示容器装有醋酸溶液,存在如下平衡CH3COOH⇌CH3COO-+H+,H2O⇌H++OH-,若在其中加水,平衡怎样移动?根据平衡常数不变,不难理解两个平衡都正移,醋酸和水电离度都增大。若将醋酸的电离平衡抽象成A(g)⇌B(g)+C(g),则加水稀释不就是在气体平衡体系中通过增加与反应无关的气体扩大容器体积吗?因此可以认为是气体的减压;但对水的电离平衡H2O⇌H++OH-则不能抽象成A(g)⇌B(g)+C(g),原因是溶液中主要存在的是水分子水的浓度为定值,加水稀释对水的浓度影响不大,因此不能认为是增加反应物浓度对平衡产生的影响;可以抽象成A(l)⇌B(g)+C(g),然后减压。 若在醋酸溶液中加入冰醋酸,醋酸的电离度怎样变化?该问题可以抽象成对气态平衡A(g)⇌B(g)+C(g),加压,A的转化率减小,即电离度减小。
例2:某温度下,在某稀硫酸溶液中逐滴滴入NaOH溶液,DIS系统测出溶液c(H+)、c(OH-)在滴定过程中变化如图。
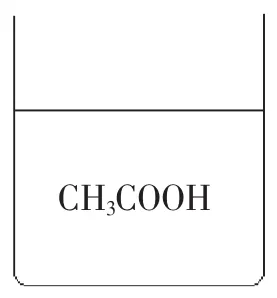
求:(1)B点时溶液的pH;
(2)在图中画出中和滴定的理论终点;
(3)若升高温度在坐标中画出c(H+)、c(OH-)在滴定过程中变化关系图。
这是一道关于中和滴定的图像题,(1)根据滴定过程中水的离子常数Kw不变不难求出B点时c(H+)=1×10-8mol/L此时pH=8。(2)根据理论终点的定义当H++OH-=H2O正好完全反应c(H+)=c(OH-)时就是该反应的理论终点,即图中曲线与函数y=x图像的交点处。(3)升高温度水的离子积常数Kw增大,因此应将该曲线沿函数y=x直线向右上方平移。
该图像题能否建立数学模型?根据水的离子积常数Kw=c(H+)·c(OH-),只要温度不变关系式变形得到c(H+)=Kw/c(OH-),即y=Kw/x,因此该函数图像为双曲线的一部分。所有的问题归集为关于函数图像的讨论。能否将关于该模型的解题方法应用于其他化学试题呢?
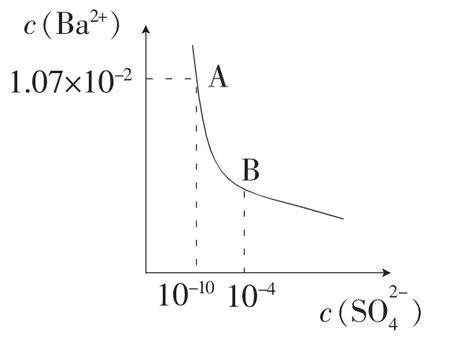
例2变形:已知某BaCl2溶液与Na2SO4溶液进行滴定并测定滴定过程中c(Ba2+)、c()并画在坐标上。 求:
(1)B点溶液中c(Ba2+);
(2)在10mL0.1mol/L的BaCl2溶液中滴入10.2mL 0.1mol/L 的Na2SO4溶液时在该图中标出该点;
(3)当BaCl2和Na2SO4恰好完全反应,若升高温度在该坐标中画出可能的位置。
无需分析,大家一看便知由于BaSO4的溶度积Ksp=c(Ba2+)·c()与水的离子积常数表达式相似且升高温度两常数都增大。因此图像问题函数化,将化学问题转变为数学问题,对于同学们扩大视野,选择更好的解题方法大有裨益。
新教材中相似模型还有很多,有待于有心人去发现和归纳。在新课程背景下,找出不同问题的相同模型、熟悉解决相关模型的化学思想方法是解决课时紧张和提高学生能力这对矛盾的一种方法,能起到事半功倍的效果,关键是善于观察问题的本质,养成这种思维习惯。

