牛奶中头孢噻呋残留消除规律及弃奶期试验
张玉洁,仲 锋,李 丹,李 倩,汪 霞,黄耀凌,何 燕,薛 毅
(1.中国兽医药品监察所,北京海淀 100081;2.华南农业大学兽医学院,广东 广州 510642;3.中国动物疫病预防控制中心,北京朝阳 100026)
头孢噻呋(Ceftiofur),其分子式为C19H17N5O7S3,化学名为[6R-[6α,7β(z)]]7-[[(α-氨基-4-噻唑基)(甲氧亚氨基)乙酰]氨基]-3-[[(2-呋喃羰基)硫代]甲基]-8-氧代-5-硫杂-1-氮杂双环[4,2,0]辛-2-烯-2-羧酸。该药是由Bernardlabeeuw 等人于1984年首次合成,其后美国法玛西亚-普强公司(Pharmacia&Upjohn)将其研制成钠盐的冻干粉及盐酸盐的混悬液,用于动物疾病的治疗。1988年,美国药品与食品管理局(FDA)批准头孢噻呋钠用于治疗牛呼吸道细菌性疾病。由于其优良的抗菌活性和药动学特点,陆续被美国、加拿大、日本及欧洲一些国家正式批准用于肉牛、奶牛、马、猪、羊的呼吸道疾病的治疗[1-2]。
目前,国内外对于头孢噻呋在各种动物体内的药物代谢动力学研究已有广泛报道[3-10],试验证明,头孢噻呋安全范围大,体内残留量低,FDA已确定其无宰前停药期和牛奶弃奶期。
国内该药物在牛奶中残留消除规律的报道不多,本文通过对牛用头孢噻呋晶体注射液在牛奶中的残留消除规律以及弃奶期的确定进行试验,旨在为该药物在我国的正确使用提供科学参考依据。
1 材料与方法
1.1 试验动物 北京市沧达农工商有限公司奶牛场6头健康荷斯坦系黑白花泌乳期奶牛。年龄2.5~8岁,体重450kg左右。试验前未使用过头孢噻呋。
1.2 试验动物用药 头孢噻呋晶体注射液(牛用)100mL:20g;批号:LotOA4AK;辉瑞国际贸易(上海)有限公司提供。
1.3 仪器与试剂 Agilent1100高效液相色谱仪(配紫外检测器和二元梯度洗脱系统);SPE柱:BondElutC18,1g/6mL;BondElutSCX100mg/10mL;恒温水浴振荡器;固相萃取装置;pH值计;冷冻离心机。
头孢噻呋标准品(中国兽医药品监察所 以C19H17N5O7S3计,含量 87.5%)、乙腈(色谱纯)、甲醇(色谱纯)、二硫赤藓醇(DTE)(含量 99%)、碘乙酰胺(含量97%)、冰醋酸、氢氧化钠、醋酸铵、三氟乙酸(TFA)(含量99%)、超纯水。
1.4 溶液配制 头孢噻呋标准液(5.0g/mL):量取0.5mL头孢噻呋标准储备液(1mg/mL),于10 mL容量瓶中,用0.1mol/L醋酸铵缓冲液溶解并稀释至刻度。
醋酸铵溶液1.0mol/L:称取77.1g醋酸铵,加水溶解并稀释至1000mL。
醋酸铵溶液0.1mol/L:称取7.71g醋酸铵,加水溶解并稀释至1000mL。
NaOH 溶液1.0mol/L:取NaOH40g,加水溶解并稀释至1000mL。
2%醋酸溶液:取20mL醋酸,加水溶解并稀释至1000mL。
DTE提取液:20mg/mL(2.0%)将 100mg DTE溶于5mL0.1mol/L醋酸铵缓冲液中,用1.0 mol/LNaOH 调pH 值至8.9。试验中,每1.0g牛奶样品需5mL提取液。需现用现配。
碘乙酰胺溶液40mg/mL(4.0%,w/v):将200 mg碘乙酰胺溶于5mL0.1mol/L醋酸铵缓冲液中。需现用现配。
C18洗脱液:乙腈∶2%醋酸(20∶80)。
SCX洗脱液:甲醇∶1.0mol/L醋酸铵(15∶85)。
流动相A(0.1%TFA水溶液):取1mL三氟乙酸,加水至1000mL。
流动相B(0.1%TFA乙腈溶液):取1mL三氟乙酸,加乙腈至1000mL。
1.5 给药 以6.6mg头孢噻呋/kg体重剂量耳根皮下1次给药。给药前,每个药瓶内容物摇晃20~30s,确保混合均匀。
1.6 取样 乳头消毒后,挤净4个乳区,取奶样50 mL;采样时间点为 0、6、12 、24、30、36、48、54、60、72、78、84、96、102h 和 108h,共 15 个时间点 。采样后立即于-20℃保存,直至样品分析。
1.7 色谱条件 色谱柱:ThermoscientificC18,4.6mm×250mm,5m;检测波长:266nm;柱温:30 ℃;进样体积:40μL。
梯度程序:流动相A(TFA水溶液)为主要成分,流动相B(TFA乙腈溶液)梯度增加。完全梯度洗脱和再平衡的时间为25min,流速为1.0mL/min。梯度洗脱程序见表1。

表1 梯度洗脱程序表
1.8 样品处理 用高效液相色谱法[7]对所取的牛奶样品进行测定。称取5±0.05g牛奶样品于50 mL离心管中,每个样品中加5mLDTE提取液,充分混合。50C水浴振摇培养15min。于4C下10000r/min离心20min,将上清液转入另一离心管中,备用。依次用 5mL甲醇、10mL0.1mol/L醋酸铵缓冲溶液预洗C18柱,将上清液转移至预洗过的C18柱中,并确保溶液慢慢流过C18柱。用5 mL0.1mol/L醋酸铵冲洗两次,在柱上衍生化以前排干洗涤液。每个C18柱上加5mL碘乙酰胺溶液,使该溶液的过柱时间至少保持30min,保证衍生化反应充分进行。用5mL0.1mol/L醋酸铵缓冲液冲洗两次,再用5mL2%醋酸溶液冲洗,保持柱子湿润。再依次用2mL甲醇、2mLC18洗脱液冲洗SCX柱。将C18柱直接放在相应的SCX柱上,用6mLC18洗脱液将C18柱上的衍生化物直接洗脱到SCX柱中。使溶液以适当的速度慢慢通过SCX柱。用1mL甲醇、2mL2%醋酸溶液洗SCX柱,挤干柱子和接口中的溶液。用2.0mL SCX洗脱液洗脱衍生物,收集洗脱液,充分混匀,过0.45μm微孔滤膜,用HPLC进行分析。
2 结果
2.1 标准曲线测定 取 0.02、0.05、0.1、0.3、0.5、1.0μg/mL6个浓度点进行检测。其浓度范围包含了头孢噻呋在牛奶样品中的最高残留限量及实际样品测定结果。经测定,线性方程为y=0.0729x+0.4511,R2=0.9998。
2.2 实际样品测定 每天各取6头牛同一个时间点的牛奶样品进行测定,每个样品做平行样,同时做标准、阴性、阳性对照,并计算其残留量。共测定九个时间点,测出的最高残留量为53.6μg/kg,测至72h样品时,4个奶样已测不出头孢噻呋残留量。为此,其余时间点不再检测。以采样时间点为横坐标,测得的每一时间点残留量平均值为纵坐标,分别绘制6头奶牛9个时间点牛奶样品中头孢噻呋残留标志物的消除规律曲线,再绘制出6头奶牛的平均消除规律曲线。
空白牛奶样品、实测牛奶样品与头孢噻呋残留标志物的标准溶液色谱图见图1A~1C。
6头奶牛6~72h牛奶样品中头孢噻呋残留标志物残留量见表2,按时间、残留量绘制的残留消除曲线图见图2、图3。
3 讨论
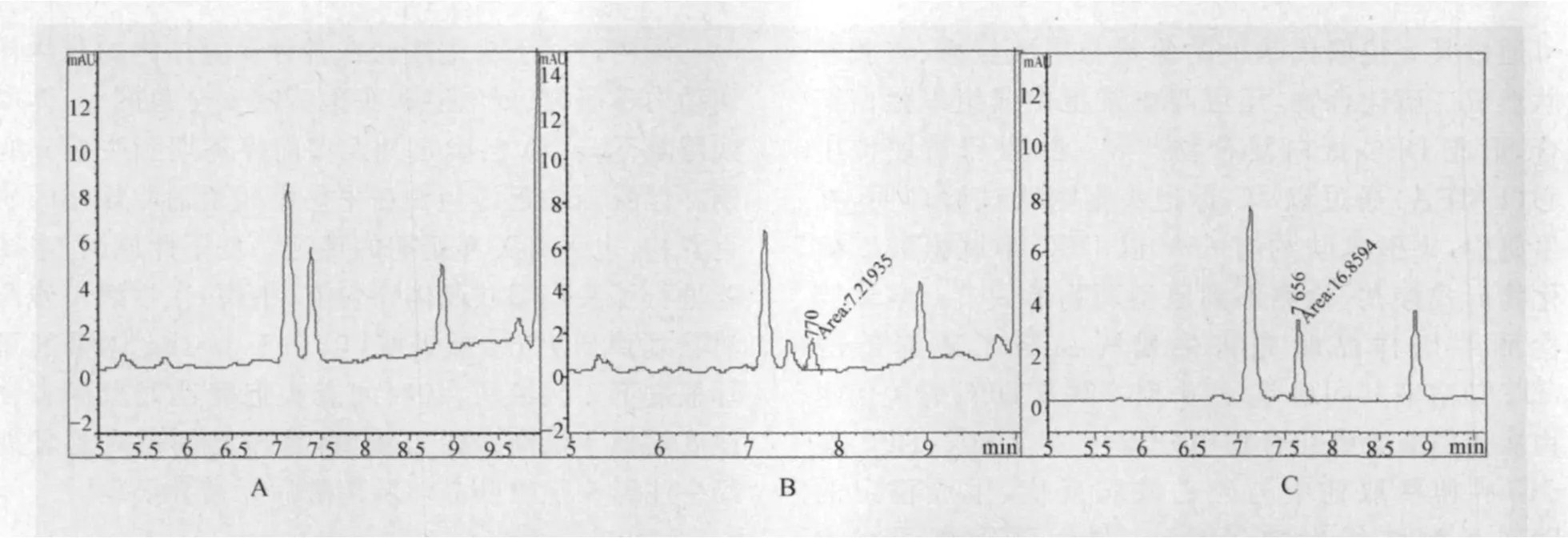
图1 空白牛奶样品、实测牛奶样品与头孢噻呋残留标志物的标准溶液色谱图

表2 6~72 h样品中头孢噻呋残留标志物残留量

对头孢噻呋在肉牛、奶牛、猪、绵羊等动物体内生物转化进行的广泛研究表明,仅有少量头孢噻呋的β-内酰胺环被破坏,生成极性代谢物,绝大部分头孢噻呋很快脱去3位硫代基上的呋喃羰基,转化成去呋喃羰基头孢噻呋(DFC),DFC含未受破坏的β-内酰胺环,是头孢噻呋有抗菌活性的代谢物。DFC在血浆、尿液和组织中极少以游离状态或原形存在,可通过其3位取代基上的巯基与半胱氨酸、谷胱甘肽形成二硫化合物,还可与血浆蛋白或组织蛋白结合,形成DFC-蛋白复合物[10-12]。欧盟药物评价中心(EMEA)通过以14C标记头孢噻呋试验证明,在牛奶中,头孢噻呋约有65%以DFC-半胱氨酸二硫化物形式存在,检测不到原型药物形式[4]。本试验检测牛奶样品时先将牛奶样品与二硫赤藓醇(DTE)溶液共同培养,使头孢噻呋及DFC有关代谢物从蛋白或含硫化合物中分离,产生DFC。DFC在C18固相萃取柱中与碘乙酰胺反应,生成稳定的DFC乙酰胺衍生物(DCA),再用强阳离子交换(SCX)柱进行净化。采用梯度HPLC紫外检测对DCA衍生物进行分析[7]。保证了试验结果的科学性和可靠性。
PremSJaglan等曾报道[13]给奶牛肌肉注射头孢噻呋,每日1次,连用5d,于每一计量后12、24h收集牛奶样品,直至最后1个剂量后5d。应用Delvotest-P和CharmtestII两种检测法对奶样进行检测。结果显示,应用Delvotest-P检测法未检到头孢噻呋残留;应用CharmtestII方法检测则可检测到牛奶样品中的头孢噻呋残留,最后1个剂量后24h,阴性样品达到90%。但所有阳性奶样中的头孢噻呋残留量均低于当时FDA规定的安全限量。
EMEA也进行了类似的试验研究[4],给药时间和采集样品时间与PremS.Jaglan等人的试验方案相同。经检测,第五个剂量后的12h为牛奶中14C-头孢噻呋残留最多的时间点,平均残留量为115 μg/kg,到第24小时和48小时迅速将为60μg/kg和20μg/kg。在另一试验中,按照相同剂量和用法,给奶牛注射未被14C标记的头孢噻呋,于最后1个剂量后每隔2h收集奶样一次,经检测,第五个剂量后的10h牛奶中头孢噻呋残留最多,残留量为71 μg/kg,到第12h时降为 40μg/kg。
本试验中,按照头孢噻呋晶体注射液(牛用)说明书规定,以6.6mg/kg体重剂量耳根皮下1次给药后,30h~36h奶中的头孢噻呋残留标志物浓度达到峰值,最高值为53.6μg/kg;72h时,66.7%奶牛牛乳中已检测不到头孢噻呋残留标志物。本试验在试验动物的选择方面注重了年龄大小和日产奶量的差异性,具有一定的代表性。相同时间点测得各样品中头孢噻呋残留量略有不同,消除速度有快有慢,分析原因可能与奶牛的年龄以及日产奶量等个体差异有关。但总体残留消除趋势及残留量水平与国外其他报道基本相符。包括残留最高点在内的各时间点残留量均低于我国农业部2002年第235号公告的规定的100μg/kg。
国内外对于头孢噻呋在各种动物体内的药物代谢动力学研究已经证明,头孢噻呋安全范围大,体内残留量低,FDA已确定其无宰前停药期和牛奶弃奶期。但我国缺乏该药物在牛奶中残留消除规律的研究资料,也无有关弃奶期的规定。基于此原因,本试验进行了头孢噻呋晶体注射液(牛用)在牛奶中残留消除规律研究,结果表明,以6.6mg/kg体重剂量耳根皮下1次给药,各时间点头孢噻呋残留标志物浓度均低于最高残留限量值,且按此剂量对泌乳期奶牛注射头孢噻呋晶体游离酸后无需弃奶期。
[1] 丁焕中,陈杖榴.兽用抗生素头孢噻呋的研究进展[J].中兽医医药杂志,2000,4:17-21.
[2] 朱阳,许峰.头孢噻呋的合成[J].中国医药工业杂志,2001,32(6):241-242.
[3] William A Moats , Marjo rie B .Medina .Vet erinary drug residues:food safety[ M] .Library of Congress Cataloging-in-Publication Data .Washin gton DC , USA .1996 :71-84 .
[4] Committee for veterinary medicinal products ceftiofur summaryreport[R].EMEA/MRL/498/98-FINAL.7,1999.
[5] 常建宇.盐酸头孢噻呋注射剂在猪体内药代动力学及安全性的研究[D].北京:中国农业大学,2006.
[6] 申春红.盐酸头孢噻呋在鸡体内的药物动力学研究[D].武汉:华中农业大学,2009.
[7] 农业部1025号公告-13-2008.动物性食品中头孢噻呋残留检测高效液相色谱法[S].2008.
[8] Souza MJE , Noguei ra D R, Silva LM, et al .Developmentan d Validation of an HPLC Method for Dterminati on of Ceftiofur Sodium[ J] .Ch romat ograp hia, 2007 , 65 :401-406
[9]Dri llich M, Arlt S , Kers ting S , et al .Cef ti ofur Derivatives inSerum , Ut erine Ti ssues , C ot yledons , and Lochia af ter Fet alMem brane Ret en tion[ J] .J ou rnal of Diary Sci ence, 2006 , 89 :3431-3438 .
[10]Makesw aran S , Pat t erson I , Point s J .An analyti cal method t odetermine conjugat ed residues of ceftiofur in milkusing liquidch romatography with tandem mas s s pectrometry[ J] .Analyt icaChimi ca Acta , 2005 , 529 :151-157 .
[11]Brown SA , Chest er ST , Speedy AK , et al .Comparison ofplasm a pharmacokineti cs and bioequivalence of ceft iofur s odiumin catt leafter a single intram uscular or subcu taneous in jection[ J] .J Vet Ph armacol Therap , 2000 , 23 :273-280 .
[12]Prem S Jaglan , Mavc F Kubicek , Thomas S , et al .Metabolismof cefti ofur .Nature of Urinry and Plasma Metabolism in Ratsand Cattle[ J] .Journal of agri cultural and food chemistry , 1989(37):1112-1118 .
[13]Prem S Jaglan , Fed S Yein , Res E Homish .Depleti on of intramuscularly inject ed ceft iofur from the milk of dairycattle[ J] .Diary Science , 1992 , 75 :1870-1876 .

