人工全膝关节置换术后胫骨侧有限元模型的建立
赵斌修,王坤正,王春生,田振兴,陈晓亮
(1.南京医科大学附属淮安第一医院骨科,江苏淮安 223300;2.西安交通大学第二医院骨一科,陕西 西安 710004; 3.西安久和能源科技有限公司,陕西西安 710008;4.青岛大学医学院附属医院骨科,山东青岛 266003)
有限元分析(finite elements analysis,FEA)是随着计算机技术进步而逐渐发展起来的一种数字模拟研究方法,其优点为省时快捷,费用低廉,应用面广,适应性强,可以反复应用,无损耗,能够通过模拟分析方法研究经典实验法所不能研究的工况,得到客观实体实验法所难以得到的实验结果,目前已经成为研究人体生物力学的最常用的分析工具。人工全膝关节置换术(total knee replacement,TKR)是目前治疗终末期骨关节炎等疾病有效的治疗方法,在术中术后胫骨侧假体可由于多种原因出现松动,由此影响手术疗效。应用有限元分析方法分析人工膝关节置换术后胫骨侧假体的应力应变情况是目前较理想的仿真力学分析方法,其可在持续性研究中重复及改变任何质量与定量变化,同时提供经典力学实验不能得到的局部以及内部的机制反应。
计算机断层成像(computed tomography,CT)对骨骼与周围软组织对比度高,能够精确地描述骨骼几何形态[1]。同时 CT值与骨骼表观密度具有近似的线性关系,骨骼表观密度与骨骼材料特性存在幂指数关系的经验公式,够较精确地描述骨骼材料特性[2,3]。本文以CT数据建立人工膝关节置换术后胫骨侧有限元模型,为有限元分析人工膝关节置换术后胫骨侧假体的应力应变情况奠定基础。
1 材料设备与实验对象
1.1 材料与设备 美国通用公司 GE Speed Light 16型 16排螺旋 CT扫描机1台;微型计算机1台(配置:CPU,PentiumIV/2.4;内存,2 GB;硬盘,160 GB;显存,128 MB;显卡, Geforce4;操作系统,Windows XP);主要相关软件:Mimics10.0(比利时 Materalise公司)、有限元软件 AN SYS11.0 (美国 Ansys公司)、ProENGINEER(美国 PTC公司)。
1.2 实验对象 国人健康志愿者1名,男性,35岁,汉族,身高1.73米,体重75 kg,下肢无骨性外伤病史及肿瘤病史。临床人工全膝置换术中常用的 6种柄体形状的胫骨侧假体。
2 方 法
2.1 胫骨有限元模型的建立 志愿者取正常解剖位,以 GE Speed Light 16型螺旋 CT机对其右股部中下1/4处至足尖进行螺旋扫描,得到0.625mm层厚的连续断层图片867张,编号,以Dicom格式存储于光盘。将第103层至第620层图像数据导入软件Mimics10.0软件,以矢状面、轴状面与冠状面三个视图角度显示数据,设定的不同阈值标准提取皮质骨、松质骨与骨髓的像素,将其蒙罩处理,得到较为粗略的三维外形。利用mimics10.0软件进行光滑处理,在 Ansys有限软件中通过布尔运算,将皮质骨、松质骨以及骨髓腔三层实体模型组装成模拟度较高的胫骨实体模型。在此模型上端的胫骨平台内外髁间嵴之中点与下端的踝穴最高点之间做连线,作为胫骨的纵向机械轴线[4],以此做为修正模型坐标的基准。为了减少数据量,提高计算的速度,在实际计算和建立几何实体模型时,仅留下胫骨模型上中2/3部分。
2.2 不同柄体形状胫骨侧假体及聚乙烯衬垫模型的建立对于临床人工全膝置换术中常用的 6种柄体形状的胫骨侧假体,通过实际测量得到假体柄的有关几何数据,6种不同柄体形状的胫骨侧假体,包括以下几种。a)圆柱形柄:柄长 40 mm,柄体直径10 mm,末端呈半球形;b)方柱锥形柄:柄长 40 mm,柄基底部12mm×12mm,柄体末端8mm×8mm; c)圆柱锥形柄:柄长40 mm,柄基底部直径10 mm,柄末端直径 6mm;d)十字锥形柄:柄长 40mm,柄体同圆柱状柄,十字锥翼展基底部7mm,锥翼末端止于柄体末端,锥翼厚度为2 mm;e)梯翼形柄:柄长 40 mm,柄体同圆柱状柄,最大翼展15mm,锥翼厚 2.5mm,侧翼平面与冠状面呈15°角;f)柱翼形柄:柄长40mm,翼展11.5mm,锥翼厚2mm,侧翼平面与冠状面呈 15°角。
依据既往文献,假体平台部的厚度设为 4 mm,设定假体平台覆盖胫骨截面的面积形状与胫骨截面面积形状相同[10]。根据手术实际,在假体与胫骨骨质之间设立骨水泥层,骨水泥覆盖胫骨截面与金属假体平台部相接触的部分厚度为2mm,在胫骨髓腔内与假体柄相接触的部分厚度为1mm。将各数据输入软件ProE,即可建立6种不同柄体形状的胫骨侧假体实体模型。参考高分子聚乙烯垫实物,以ProE软件建立高分子聚乙烯垫的实体模型。其中央部着力点(即平台凹陷最深处)位置厚度设为4 mm[11]。
将在 ProE建立的模型数据储存为iges格式,导入到 Ansys中,依据手术时的实际工况,在合适位置与原来建好的胫骨模型通过 Ansys中的布尔运算功能进行组装,使聚乙烯垫、金属假体、骨水泥、胫骨成为一体。这一过程中,模拟手术实际,胫骨近端截骨。将此组装实体模型利用 Ansys11.0软件选用十节点四面体单元(solid92单元)进行有限元网格的划分。十节点四面体的每个节点具有6个方向的自由度,能够较好体现人体骨组织的力学特性[5]。划分网格的 TKR术后胫骨侧有限元模型如图 1所示。
图1 TKR术后胫骨中上段有限元模型
3 结 果
不同柄体形状的胫骨侧假体中,各组件的节点和单元数见表1。
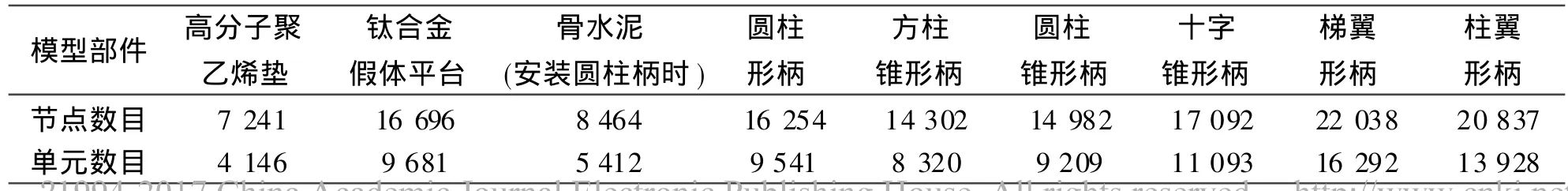
表1 模型中各部件的节点和单元数
将根据查阅文献所得各种材料的弹性模量、泊松比等材料系数以及特征值输入模型的相应部分。钛合金弹性模量及泊松比参考自 Mitsuo等[6-8]研究结果,骨皮质、松质骨及骨髓的弹性模量与泊松比参考自 Lengsfeld等[9]研究结果,具体参数见表 2。

表2 有限元模型的材料物理参数
4 讨 论
骨科手术治疗方法的选择以生物力学理论为基础,传统的生物力学研究方法因为取材越来越困难,经济费用投入较大。有限元法是目前骨科仿真生物力学研究中常用的方法。1943年,Courant首创了有限元法,其基本原理是将连续的弹性体分割成有限个单元,化整为零又积零为整地分析实验对象。其单元划分越细,计算结果越精确,但是计算量也越大,所以在实验中需要考虑计算机的运算能力和对于精度的要求程度合理地划分网格数量。
本研究与前人研究的比较来说,此模型的重要特点不仅在于其分为三层结构,即皮质骨、松质骨、骨髓(骨髓腔)三层而更加接近于胫骨的实际情况,而且更重要的是对于 TKR术后的胫骨侧部分各组件仿照真实手术状况进行了组装。
以往的长骨的有限元模型多为不规则的柱状,不分层,后来有人作出带髓腔的长骨三维有限元模型,但是仍然没有区分松质骨与皮质骨。本文中的实体模型和有限元模型分为三层,这样就更好地与实物相符合,模型的计算结果也更加接近真实情况。据现有研究结果,由于在人体下肢长骨各向异性表现不明显,模型中赋予各向同性或者正交各向异性,对于分析结果差别很小,因此模型材料取各向同性[12]。在准静态载荷下(多半是在体载荷),无论皮质骨还是松质骨,尽管它们是各向异性和非均质的,却都近似为线弹性材料。因此,我们赋予模型为分层均质各向同性线弹性材料。
鉴于当今国内膝关节置换术中胫骨侧假体形状的不同,我们选取了常用的 6种不同形状胫骨侧假体(主要区别在于假体柄的形状不同),根据实际测量数据及产品说明书,将各假体几何数据输入软件生成数字模型。根据文献,规定假体平台及高分子聚乙烯垫的厚度以及骨水泥层的厚度,建立模型。假体各部模型与胫骨模型组合成为膝关节置换术后的胫骨侧数字模型,根据现有文献赋予模型各材料以相应的物理参数,为比较应用不同形状假体后膝关节胫骨侧的生物力学特性奠定了良好基础。
本膝关节术后胫骨侧模型按照力学分析要求可模拟临床实际工作中的各种假体与胫骨髓腔各种不同相对位置情况,并可根据实际情况施加力的大小与方向,可作为进一步仿真力学分析的可靠基础,具有实用、可信度高、经济的特点。
[1] Lengsfeld M,Schmitt J,Alter P,et al.Comparison of geometry-based and CT voxel-based finite element modeling and experimental validation[J].Med Eng Phys,1998,20(7):515-522.
[2] Rho JY,Hobatho MC,Ashman RB.Relations of mechanical-properties to density and ct numbers in human bone[J].Med Eng Phys,1995,17(5):347-355.
[3] Wirtz DC,Schiffers N,Pandorf T,et al.Critical evaluation of known bone material properties to realize anisotropic FE-simulation of the proximal femur[J]. J Biomech,2000,33(10):1325-1330.
[4] 卢世璧.坎贝尔骨科手术学[M].第10版.济南:山东科技出版社,2006:237.
[5] 苏再发.颈椎前路椎体次全切除钛网植骨的三维有限元研究 [D].上海:第二军医大学,2007.
[6] Niinomi M.Recent research and development in titanium alloys for biomedical applications and health care goods[J].Sci Technol Advan Mater,2003,4:445-454.
[7] Vazquez AA,Lauge-Pedersen H,Lidgren L,et al.Finite element analysis of the initial stability of ankle arthrodesis with internal fixation:Flat cut versus intact joint contours[J].Clin Biomech(Bristol,Avon), 2003,18(3):244-253.
[8] Sonoda N,Chosa E,Totoribe K,et al.Biomechanical analysis for stress fractures of the anterior middle third of the tibia in athletes:nonlinear analysis using a three dimensional finite element method[J].J Orthop Sci,2003,8(4):505-513.
[9] Lengsfeld M,Schmitt J,Alter P,et al.Comparison of geometry-based and CT voxel-based finite element modelling and experimental validation[J].Control Eng Practice,2002,10(1):83-90.
[10] Godest AC,Beaugonin M,Haug E,et al.Godest.Simulation of a knee joint replacement during a gait cycle using explicit finite element analysis[J].J Biomech, 2002,35(2):267-275.
[11] Liang P,Jing B,Xiaoli Z,et al.Comparison of isotropic and orthotropic material property assignment on femoral finite element models under two loading conditions[J].Med Eng Phys,2006,28(3):227-233.
[12] Au AG,Liggins AB,Raso V J,et al.A parametric analysis of fixation post shape in tibial knee prostheses[J].Med Eng Phys,2005,27(2):123-134.

