双酚A在纳米羟基磷灰石修饰碳糊电极上的电化学行为及分析应用
吴云华,殷 明
(1中南民族大学生命科学学院,武汉430074;2中南民族大学药学院,武汉430074)
双酚A(BPA)是一种很重要的化工原料,用于生产环氧树脂、聚碳酸酯和聚氧酚等,属于环境激素,即使痕量的BPA也会对人类生殖及后代生存能力产生负面影响[1].因此,需建立高效率检测BPA的方法.
目前已报道的BPA检测方法有液相色谱法、荧光法、极谱法及酶联免疫吸附法(ELISA)等[2-5].液相色谱和ELISA等方法虽灵敏度高,但仪器设备昂贵,检测过程耗时,前处理较繁琐.较之上述方法,电化学方法则因具有灵敏度高、分析速度快、仪器低廉、操作简便及成本低廉等特性,目前已成为一种重要的分析手段.
近年,随着化学修饰电极的迅速发展,化学修饰碳糊电极(CMCPEs)的应用广受关注,碳糊电极具有价格便宜、制造简单、电位窗口宽、表面容易更新、敏感度高以及稳定性好的优点,深受电分析工作者的青睐[6]; 纳 米 羟 基 磷 灰 石 (Nano-HAP, Nano-Ca10(PO4)6(OH)2)是生物活性陶瓷,立体化学结构和独特的多吸附位点使其广泛用于催化领域[7].目前,BPA在碳糊电极上电化学行为已见报道[8],但Nano-HAP修饰碳糊电极测定BPA却尚未见报道.
本文制备了纳米羟基磷灰石修饰碳糊电极(Nano-HAP-CPE),研究了BPA在pH 7.0的磷酸盐缓冲溶液(PBS)中的电化学行为,并将其应用于聚碳酸酯塑料瓶中BPA含量的测定.
1 实验部分
1.1 仪器和试剂
CHI660C电化学工作站(上海辰华仪器有限公司;采用三电极系统:碳糊电极(CPE)为工作电极,铂丝电极为对电极,饱和甘汞电极为参比电极).
双酚A标准溶液:0.1 mol/L,准确称取2.28 g BPA标准品,用无水乙醇溶解,用水定容至100 mL,并黑纸包妥于4℃阴暗处保存,用时逐级稀释至所需浓度.
0.1 mol/L PBS(pH 7.0)缓冲溶液.
石墨粉(化学纯),硅油(分析纯),BPA和Nano-HAP购自Sigma公司,其它试剂均为分析纯,实验用水为二次蒸馏水.
1.2 CPE和Nano-HAP-CPE的制备
CPE电极制作:分别称取1.00 g石墨粉和0.25 g石蜡油混合(质量比4∶1)均匀后,装入直径为3 mm的碳糊电极,电极表面在硫酸称量纸上磨平抛光;Nano-HAP-CPE电极制作相似于裸碳糊电极制作方法,其不同处为Nano-HAP与石墨粉按质量比例混合.
1.3 实验方法
将Nano-HAP修饰碳糊电极置于10 mL pH 7.0的PBS中,在空白溶液中循环伏安(CV)法扫描至基线稳定,差分脉冲伏安(DPV)法扫描空白溶液,记录0~0.8 V的DPV曲线,再于空白溶液中加入样品溶液0.10 mL,再DPV扫描,记录0~0.8 V的DPV曲线,通过扣除背景得到结果.每次测定后,用刀片小心刮去表面,重新制作新的Nano-HAP-CPE.
2 结果与讨论
2.1 Nano-HAP-CPE的电化学行为特征
Nano-HAP-CPE的电化学行为以K3[Fe(CN)6]作为氧化还原探针,通过CV法进行研究.图1为CPE 和Nano-HAP-CPE 在1 mmol/L K3[Fe(CN)6]的0.1 mol/L KCl溶液中的CV图.图1曲线 a为裸CPE的CV曲线,有一对氧化还原峰,其氧化峰电位Epa=0.392 V,还原峰电位Epc= -0.130 V,峰电位差 ΔEp=0.520 V.图 1 曲线 b 为 K3[Fe(CN)6]在Nano-HAP-CPE的CV曲线,其Epa=0.315 V,负移77 mV;Epc= -0.0290 V,正移101 mV;峰电位差ΔEp=0.344 V,且峰形较对称,电极过程的可逆性提高很大,峰电流也显著增大.由此表明Nano-HAP对K3[Fe(CN)6]的氧化还原有显著促进作用.
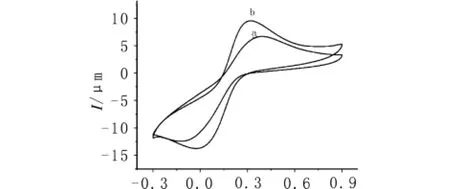
图1 铁氰化钾在裸CPE(a)和Nano-HAP-CPE(b)的CV图Fig.1 Cyclic voltammograms of 1 mmol/L K3[Fe(CN)6]at bare CPE(a)and Nano-HAP-CPE(b)
2.2 BPA的电化学行为
在pH 7的PBS溶液中,用 CV法比较了BPA在CPE和Nano-HAP-CPE电极上的电化学行为(见图2插图).在不含BPA的PBS溶液中,未观察到裸CPE(a)的氧化还原峰,而在0.7 V附近则观察到Nano-HAP-CPE电极(b)的一个氧化峰,电流较低,该氧化峰可能系Nano-HAP自身所引起的.BPA的电化学行为见图2主图,裸CPE(c)与Nano-HAPCPE(d)电极上均有一个氧化峰,氧化电位分别为0.465、0.468 V.而与裸 CEP 相比,BPA 在 Nano-HAP-CPE电极上的氧化电流显著增大,原因为Nano-HAP具有大的比表面积,对BPA有较强吸附能力和较高富集效率,增加了它在电极表面的浓度,使得氧化峰电流增强.在循环扫描过程中,未观察到还原峰,说明BPA在Nano-HAP-CPE电极上的电极反应是一个完全不可逆过程.这与文献报道相符[6-8].BPA在CPE和Nano-HAP-CPE上的连续CV扫描特征见图3.图3中,BPA在裸CPE电极上氧化电流经第2次循环电位扫描后完全消失,而在Nano-HAP-CPE电极上氧化电流则显著降低但未完全消失,并随扫描次数增加其氧化电流逐渐减小而氧化电位增加,最终趋于稳定.造成该现象的原因是BPA生成的氧化产物在电极表面发生了吸附,覆盖电极表面部分活性点位,影响了BPA在电极表面的电子交换,从而导致在以后扫描时的氧化电流大为降低.因此,本实验以第1圈的氧化峰电流作为测定信号.

图2 双酚A在裸CPE和Nano-HAP-CPE的CV图Fig.2 Cyclic voltammograms of BPA at bare CPE and Nano-HAP-CPE
2.3 实验条件的优化
2.3.1 Nano-HAP 比例的选择
取5%~70%不同质量百分比的Nano-HAP/石墨粉与硅油混合制作CPE,在相同BAP浓度下,分别在0.1 mol/L PBS(pH7)的缓冲溶液中进行线性扫描.实验表明:随着 Nano-HAP的比例增大,BPA的氧化峰电流也随之增大,且相应的氧化电位发生正移.但0.7 V电位处的氧化杂峰也随之增大.本实验选Nano-HAP/石墨粉质量百分比为10%.
2.3.2 支持电解质
在相同BAP浓度下,分别以0.1 mol/L NaCl、KCl、NaNO3、KNO3、K2SO4、Na2SO4、CH3COONa、CH3COOK和PBS溶液为支持电解质进行实验.考察其对BAP峰电流Ipa的影响,结果表明:以0.1 mol/L PBS溶液测定BAP的支持电解质,可得到最灵敏的测定信号.
2.3.3 pH 值的影响
在pH 4~10范围介质pH对BPA氧化峰电流Ipa的影响见图4a.当pH值由4增至7时,BPA的氧化峰电流逐渐增大;当pH值续由7增至10时,则氧化峰电流反而降低.考虑到检测BPA的灵敏度,故选择pH7为起始进行测试.
BPA的峰电位与pH关系见图4b.在pH 4~10范围,BPA峰电位随pH值增大而负移,电位与pH存在线性关系Epa(V)= -0.05261pH+0.8492,相关系数为r=0.9922,当pH逐渐增大时,氧化峰电位以52.61 mV/pH的速率负移,该值非常接近电子数和质子数相等电化学反应理论值(25℃时,为59 mV/pH),因此说明BPA氧化过程中质子参与反应,而且质子数和电子数相等.
2.3.4 溶剂的选择
由于BPA几乎不溶于水,本实验选用了5种有机试剂作为BPA的溶剂,分别为甲醇、乙醇、异丙醇、乙腈和丙酮.在电位窗口0~1V内,相同BAP浓度下以DPV法进行分析,结果表明以甲醇和乙醇作为溶剂时,分别具有最高氧化峰电流和最低氧化电位.本实验选用乙醇作为BPA的溶剂.
2.3.5 扫速的影响
扫速在20~400 mV/s范围的变化见图5.由图5知,BPA的氧化峰电流Ipa随扫描速率v的增加而增大,当扫速过高时,背景电流增大,峰形变宽,故选择扫速为100 mV/s.扫描过程中发现Ipa与v成线性关系,线性方程Ipa(μA)=0.2382v+12.39(r=0.9935)说明BPA在此修饰电极上的氧化过程受吸附控制.
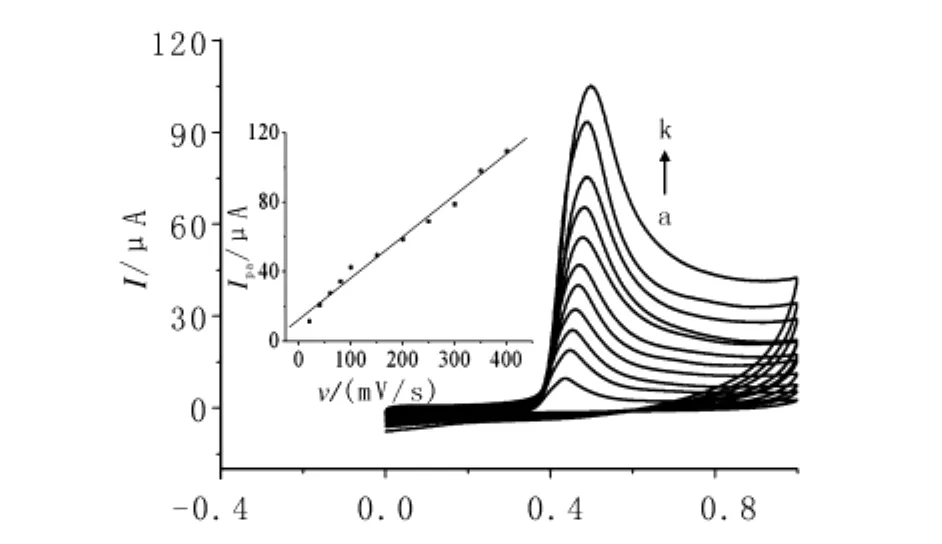
图5 BPA在不同扫速下的CV安图Fig.5 Cyclic voltammograms of BPA at different scan rate
2.3.6 富集电位与富集时间
当 pH=7,0.1 mol/L PBS 溶液时,2.5 mol/L BPA在不同富集电位下,以相同测试条件进行DPV法测试.结果见图6.由图6知,峰电流富集电位在-0.5 V时最大,测定选择富集电位为-0.5V.

图6 富集电位对BPA氧化峰流的影响Fig.6 Effect of accumulation potential on the oxidation peak current
不同的富集时间对峰电流的影响见图7.随富集时间增加峰电流升高.当富集时间150 s时,峰电流最大,超过150 s峰电流反而下降,因此选择150 s为富集时间.

图7 富集时间对BPA氧化峰流的影响Fig.7 Effect of accumulation time on the peak current
3 BPA在Nano-HAP-CPE电极上的电化学动力学参数
3.1 电荷转移系数α
在0~1 V的电位窗口下,用 CV法研究了扫描速率(20~400 mV/s)对BPA电化学行为影响并得Epa-lnν关系,见图8.其线性回归方程Epa(V)=0.02029lnν+0.3725(r=0.9920) 根根据 Laviron理论,峰电位和扫描速度遵循Epa=E0+(RT/anF)ln(RTk0/anF)+(RT/anF)lnν[11].式中,a为电荷转移系数,n为电子转移数,ν为扫速.由曲线斜率得RT/anF=0.02029(T=298,R=8.314,F=96480),由此得an=1.26.前人实验证明,对于大多数体系,0.3 <a<0.7,因而n=2,则有电荷转移数a=0.63.
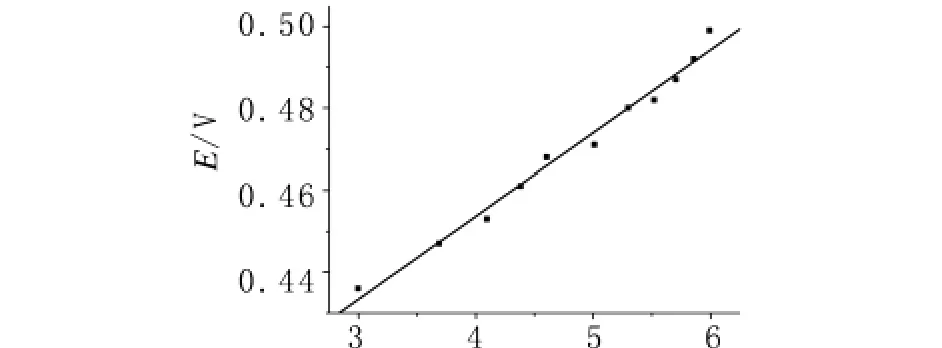
图8 双酚A氧化电位Epa与ln v的关系Fig.8 Plot for the oxidation peak potential Epa of BPA vs.ln v
3.2 有效表面积A,扩散系数D和表面吸附浓度Γs
根据电位阶跃计时电量法[12]:
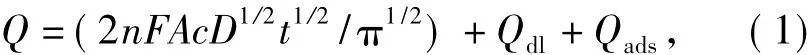
其中,A为工作电极有效表面积,c为底物浓度,D为扩散系数,Qads为法拉第容量.其他参数均有其固定值.采用计时库仑(CC)法测定BPA的D值(实验条件与 CV法相同).以 0.1 mmol/L[Fe3(CN)6]为模型化合物 (在 1.0 mol/L KCl溶液中其扩散系数D=7.6 × 10-6cm2/s[12]).由式(1)可知Q与2t1/2成线性关系(见图9).由图9插图知,Q与t1/2的斜率在 CPE(c)和 Nano-HAP-CPE(d)分别为2.40 ×10-6和 2.67 ×10-6.由此可求得裸CPE和Nano-HAP-CPE有效表面积分别为A=0.0397 cm2和A=0.0442 cm2.结果表明 Nano-HAPCPE电极的有效表面积较裸CPE电极大,因而可提高BPA吸附能力,从而导致增大BPA的氧化电流,降低检测限.

图9 铁氰化钾的CC图(扣除背景)Fig.9 Chronocoulomety of Fe3(CN)6 after background subtracted
基于公式(1)通过CC法得到BPA的扩散系数D和法拉第容量Qads.图10主图为双酚A在Nano-HAP-CPE上电量Q和时间t的关系图,通过扣除背景,电量与时间的平方呈现一定的线性关系(见图10插图),求其斜率为8.79 ×10-6和Qads=3.49 ×10-7c.因此,当n=2,A=0.0442 cm2,c=0.100 mmol/L,D=5.12 ×10-5cm2/s,通过公式Qads=nFAΓS,可得 ΓS=4.30×10-11mol/cm2.
3.3 反应级数
由BPA氧化峰电流Ipa与其浓度关系,依据电化学动力学原理[13]以 lgIpa对 lgc作图 ,在 Nano-HAP-CPE电极上电催化氧化过程中lgIpa与lgc呈良好的线性关系,见图11.由图11知,线性方程lgIpa=0.5350lgc-3.174,相关系数r=0.9976,曲线斜率为0.5350,表明在0.1 mol/L PBS溶液中 BPA在Nano-HAP-CPE电极上电催化氧化为半级反应.

图10 双酚A的CC图(扣除背景)Fig.10 Chronocoulomety of BPA after background subtracted
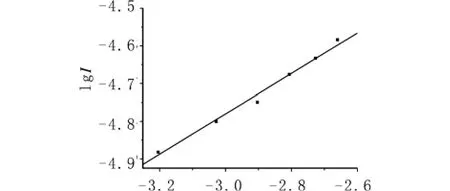
图11 氧化峰电流的对数与BPA浓度对数的关系Fig.11 Plot between the dependence of lg I pa vs.lg cBPA
4 分析和应用
4.1 干扰及重现性
测定一些常见无机离子对BPA干扰实验的结果表明,1.25 × 10-3mol/L 的 Fe3+、Ca2+、Cu2+、Mg2+、Pb2+、Cd2+、Zn2+、CL-、SO2-4、NO3-在1.25×10-5mol/L BPA溶液中基本不干扰BPA的测定.每次测定之后,用刀片小心移去电极末端用过的糊状物质,重新制作新的Nano-HAP-CPE电极,平行测定6次1×10-4mol/L BPA,相对标准偏差为1.86%,结果说明修饰电极有很好的重现性.
4.2 线性范围及检测限
用DPV法测定不同浓度BPA,并讨论了Ipa-cBPA关系.结果表明,其峰电流与BPA浓度在8.00×10-8~1.25×10-5mol/L 范围内呈线性关系(见图12).检测限为4.50 ×10-8mol/L.Ipa与浓c遵循Ipa(μ A)=0.05547cBPA(μmol/L)+0.008230,R=0.9984.
4.3 实际样品的测定及加标回收实验
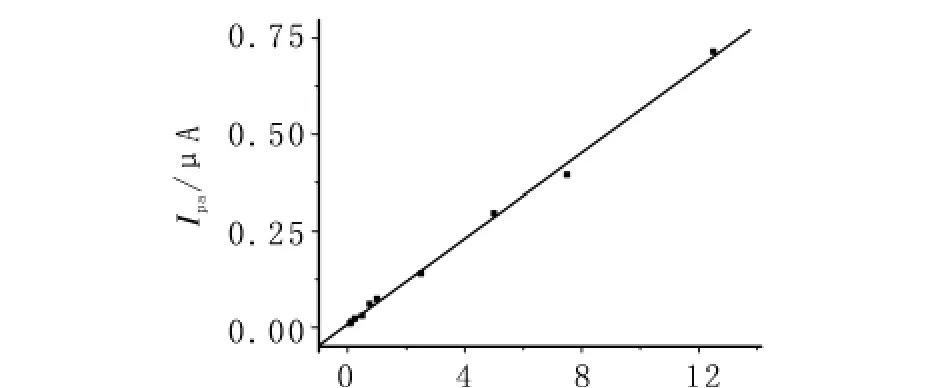
图12 氧化峰电流与BPA浓度关系Fig.12 Plot for the oxidation peak current of BPA vs.cBPA
取聚碳酸酯塑料瓶,剪碎后烘干再准确称取11.00 g放于烧杯中,加150 mL二次蒸馏水,放入超声波仪器中超声30 min,再置于70℃的烘箱中,放置48 h,过滤2次后收集滤液,最后用去离子水定容[14].在最佳实验条件下,用 DPV方法测量样品,然后进行加标回收实验.结果见表2.
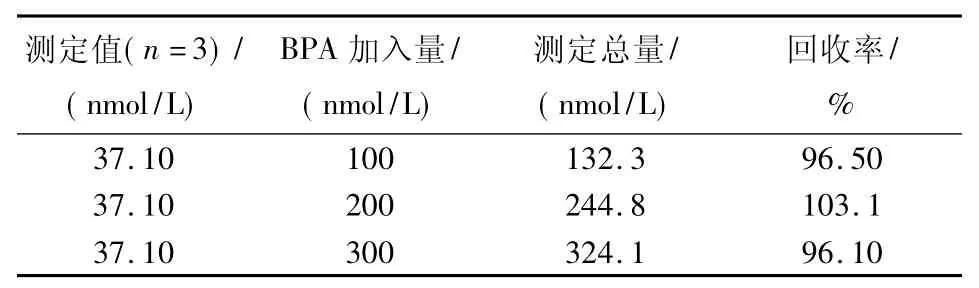
表2 聚碳酸酯塑料瓶中BPA的测定Tab.2 Determination of BPA in plastic sample
5 结语
本文研究了BPA在Nano-HAP-CPE电极上的电化学行为,结果表明,该修饰电极能增强BPA在电极表面的电化学响应,基于此构建了简便、灵敏检测BPA的电化学方法,将该方法应用于聚碳酸酯塑料瓶中BPA的测定,结果令人满意.
[1]LiW,SeifertM,Xu Y,et al.Comparative study of estrogenic potencies of estradiol tamoxifen,bisphenol-A and resveratraolwith two in virto bioassasys[J].Environ Int,2004,30(3):329-335.
[2]张学俊,吴仁安.高效液相色谱法分析矿泉水中酚类化合物[J].色谱,1998,16(6):530.
[3]唐舒稚,庄惠生.荧光法测定水中双酚A残留的研究[J].工业水处理,2006,(3):74-76.
[4]张文德,马志东,郭 忠.食品包装材料中双酚A的极谱测定[J].分析化学,2003,31(2):249.
[5]孙仕萍,马志东,张文德.单扫示波极谱法测定食品包装材料中双酚A的研究[J].分析科学学报,2002,18(6):490-492.
[6]谢红旗,李益恒.茜素紫修饰碳糊电极阳极溶出伏安法测定痕量银的研究[J].湘潭大学学报:自然科学版,2003,25(3):69-71.
[7]高玉莲,田燕妮.血红蛋白在纳米羟基磷灰石修饰的热解石墨电极上的直接电化学[J].化学研究与应用,2007,19(6):590-592.
[8]易 兰,花 田,费俊杰,等.碳糊电极阳极吸附伏安法测定双酚 A[J].化学世界,2010(4):207-209.
[9]LiQ,Li H,Du G F,et al.Electrochemical detection of bisphenol Amediated by[Ru(bpy)3]2+on an ITO electrode[J].Electrochimica Acta,2010,55:603-610.
[10]何 琼,常艳兵,张承聪.双酚A在多壁碳纳米修饰电极上电化学性质及其测定研究[J].云南大学学报:自然科学版,2004,26(1):70-74.
[11]Zeng B Z,Huang F.Electrochemical behavior and determination of fluphenazine atmulti-walled carbon nanotubes/(3-mercaptopropyl)trimethoxysilane bilayermodified gold electrodes[J].Talanta,2004,64:380-386.
[12]GolabiSM ,Zare H R.Electrocatalytic oxidation of hydrazine at glassy carbon electrodemodified electrodeposited film derived from caffeic acid[J].Electroanalysis,1999,11(17):1297-1298.
[13]吴辉煌.电化学[M].北京:化学业出版社,2004:84-85.
[14]Yin H S,Zhou Y L,Ai SY.Preparation and characteristic of cobalt phthalocyaninemodified carbon paste electrode for bisphenol A detection[J].Journal of Electroanalytical Chemistry,2009,626:80-88

