减毒流感病毒A/California/07/2009ca疫苗候选株在雪貂上的保护性研究
段跃强 李晓楠 曹 东 魏 澍 杨鹏辉 邢 丽 王希良 李培锋
(内蒙古农业大学兽医学院,呼和浩特010018)
甲型流感病毒是一类可导致高发病率和高死亡率的传染性病毒,甲型 H1N1(A/California/07/2009)流感病毒是爆发于墨西哥和美国的流感大流行的病原体,自爆发后蔓延全球,引起世界的恐慌[1-3]。截至2010年底,全球已有213个国家报道确诊病例17 410例。
流感病毒在雪貂间的传播与人类传播最为相似,因此,目前雪貂被认为是检测流感病毒最理想的动物模型[4-6]。通常情况下,研究人员选择具有代表性的H1N1流感病毒在雪貂间进行传播试验,以评估这些病毒经飞沫传播的可能性,同时也通过接种病毒,来观察雪貂的发病情况[7-9]。
本实验应用减毒A/California/07/2009ca病毒及BJ501病毒免疫雪貂,通过对雪貂的各生理指标、各器官的病毒载量的检测,来评价减毒A/California/07/2009ca病毒的弱毒性及免疫保护性。
1 材料与方法
1.1细胞、鸡胚、毒株及动物 MDCK细胞,购自ATCC公司;减毒A/California/07/2009ca流感病毒本室拯救;野毒株BJ501由中国疾病预防控制中心提供;雪貂购自江苏无锡。
1.2主要试剂 DMEM、TPCK胰酶购自Sigma;胎牛血清购自浙江天杭生物科技有限公司;96孔细胞培养板购自CORNING公司。
1.3TCID50的测定 用MDCK细胞铺96孔板,每孔4×104个细胞,待长成单层后,病毒按101、102、103……倍数稀释。每孔200 μl,稀释液为MEM 无血清培养基(含TPCK胰酶1 μg/ml),5天后电镜下观察结果,用Reed-Muench法计算TCID50,TCID50=高于50%感染病毒稀释度的对数+(高于50%感染百分数-50)/(高于50%感染百分数-低于50%感染百分数)。
1.4A/California/07/2009ca、BJ501病毒的毒力研究 10~12周雌性雪貂每组3只,共2组,分别滴鼻免疫A/California/07/2009ca、BJ501病毒,每只免疫107TCID50/200 μl,连续14天观察雪貂的死亡率、体重、精神状态,并在1、2、3、4、5、7 天时应用咽拭子取鼻腔病毒[应用无血清 MEM(50 μg/ml庆大霉素)洗脱],过滤;应用96孔细胞培养板检测鼻腔中病毒的TCID50。
1.5A/California/07/2009ca的各器官病毒载量的研究 10~12周雌性雪貂3只,滴鼻免疫A/California/07/2009ca,每只免疫 107TCID50/200 μl,免疫 3天后取雪貂鼻、肺、脾、脑、肾等器官研磨匀浆后,离心收集病毒,应用96孔细胞培养板检测各个器官中的病毒TCID50。
1.6A/California/07/2009ca免疫保护性研究10~12周雌性雪貂每组3只,共2组,实验组1、21天滴鼻免疫 107TCID50/200 μl A/California/07/2009ca病毒,21、35天采血。实验组免疫35天后和空白对照组都给予107TCID50/200 μl BJ501病毒,免疫3天后取雪貂鼻、肺、脾、脑、肾等器官研磨匀浆后,离心收集病毒,应用96孔细胞培养板检测各个器官中的病毒TCID50。HI抗体的滴度利用4单位病毒在U型96孔血凝板上用0.5%鸡红细胞检测。
1.7统计学处理 使用SPSS13.0统计软件进行数据分析,数据以±s表示。以t检验及线性回归分析检查不同组间差异性及其相关性,采用单因素方差分析,P<0.05为差异显著界限。
2 结果
2.1病毒的TCID50检测 MDCK细胞铺96孔板,每孔2×104~4×104个细胞,待长成单层后,A/California/07/2009ca、BJ501 病 毒 按 101、102、103……稀释;每孔 200 μl,MEM 无血清培养基稀释,同时以TPCK胰酶(1 μg/ml)为对照组,5天后观察结果见表1,BJ501加胰酶前后基本没有变化,而A/California/07/2009ca变化较大,加胰酶较不加胰酶高1.25 TCID50。
2.2滴鼻免疫A/California/07/2009ca、BJ501病毒后雪貂的生理指标检测 A/California/07/2009ca、BJ501病毒免疫雪貂后,由表2~4可知,A/California/07/2009ca病毒免疫后雪貂精神状态正常,没有死亡,体重有轻微下降后又迅速恢复。而BJ501却在3天时出现了感冒症状,没有死亡,体重有小幅度的下降。
2.3滴鼻免疫A/California/07/2009ca、BJ501病毒后雪貂鼻腔病毒载量的检测 A/California/07/2009ca、BJ501病毒免疫雪貂后,由表5可见,A/California/07/2009ca病毒在鼻腔内有较低的复制,4天后检测不到病毒;BJ501病毒7天内都保持较高的病毒滴度。

表1 H1N1病毒的TCID50检测Tab.1 Detection of TCID50of H1N1 virus

表2 H1N1病毒免疫雪貂后精神状态的变化Tab.2 Mental status changes of ferrets immunized with H1N1 virus

表3 H1N1病毒免疫雪貂后死亡率的变化Tab.3 Mortality changes of ferrets immunized with H1N1 virus

表4 H1N1病毒免疫雪貂后体重的变化Tab.4 Body weight changes of ferrets immunized with H1N1 virus

表5 H1N1病毒免疫雪貂后在不同时间段鼻腔病毒载量的变化Tab.5 The nasal viral load changes of ferrets at different time points immunized with H1N1 virus

表6 A/California/07/2009ca病毒免疫雪貂后不同器官的病毒载量Tab.6 The viral load in different organs of ferrets immunized with A/California/07/2009ca virus
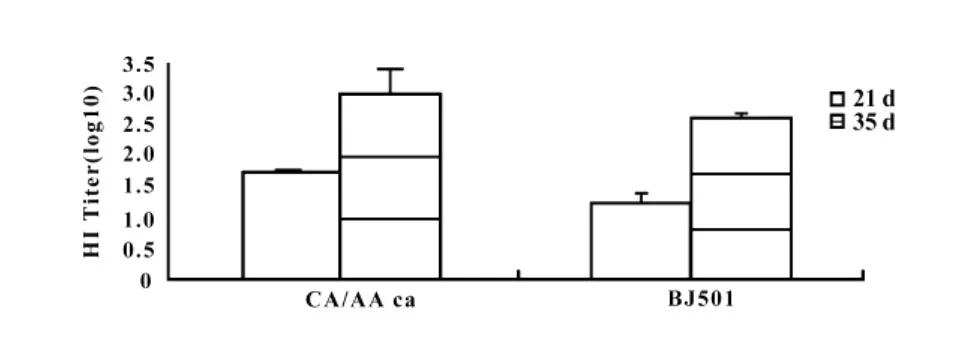
图1 免疫后雪貂血清的HI实验Fig.1 HI test of serum of immunized ferret
2.4A/California/07/2009ca病毒免疫雪貂后各器官病毒载量的检测 A/California/07/2009ca病毒滴鼻免疫雪貂3天后,处死雪貂,由表6可见,A/California/07/2009ca病毒在鼻、肺有少量复制,脾、肾、脑中没有检测到病毒。
2.5A/California/07/2009ca病毒在雪貂上的免疫保护性
2.5.1HI实验 A/California/07/2009ca病毒滴鼻免疫雪貂,采集血清样本,分别对A/California/07/2009ca病毒及BJ501病毒做HI检测,由图1可见,抗体对 A/California/07/2009ca病毒及BJ501病毒都具有很好的中和效果,并且两病毒HI结果之间无差异(P>0.05)。
2.5.2BJ501病毒免疫雪貂后各器官病毒载量的检测 A/California/07/2009ca病毒二免14天的雪貂和空白对照组的雪貂滴鼻免疫BJ501病毒,3天后处死雪貂;由表7可见空白对照组的雪貂在鼻、肺中检测到较高的病毒复制,TCID50分别达到了6.9和4.6,并且脑中也检测到1.3TCID50的病毒,肾、脾中没有检测到病毒。A/California/07/2009ca病毒组的雪貂在鼻、肺中检测到少量BJ501病毒复制,脾、肾、脑中没有检测到病毒。

表7 BJ501病毒免疫雪貂后各器官病毒载量Tab.7 The viral load in different organs of ferrets immunized with BJ501 virus
3 讨论
流感病毒具高传染性,每年在很多国家都会造成区域性的流行,20世纪曾发生过4~5次世界大流行,每次间隔9~39年。其中以1918~1919年期间H1N1流感病毒造成4 500万人的死亡最为严重。从数次大流行情况来看,H1N1爆发次数最多[10,11]。
自1998年应用流感病毒基因片段构建质粒转染细胞得到流感病毒用以研制疫苗以来,直到现在这种方法得到的病毒株都是流感疫苗株的主要来源。减毒流感疫苗2002年首次出现报道,并在以后的发展中因其诸多优点越来越引起人们的重视,减毒流感疫苗具有抗原用量小的特点,且效果很好。适用于5~17岁健康少年儿童以及18~49岁健康成人[12]。
本实验应用减毒A/California/07/2009ca流感病毒以BJ501病毒为对照,由表1可见,A/California/07/2009ca病毒在加入TPCK胰酶后,TCID50升高1.25倍,而BJ501病毒没有变化,这说明A/California/07/2009ca病毒对TPCK胰酶敏感,TPCK胰酶能够提高对A/California/07/2009ca病毒的检测灵敏度。
A/California/07/2009ca流感病毒滴鼻免疫雪貂后,对雪貂的精神状态(表2)、死亡率(表3)、体重(表4)等生理指标进行检测。A/California/07/2009ca流感病毒组没有出现异常生理反应,而BJ501病毒免疫后,雪貂出现感冒症状,这说明A/California/07/2009ca流感病毒毒力不足以引起雪貂机体的生理变化,同时可见A/California/07/2009ca流感病毒呈现弱毒的特征,而BJ501病毒呈现强毒的特征。
在此基础上我们对病毒在雪貂鼻腔中的复制情况进行检测,减毒A/California/07/2009ca流感病毒(表5)在雪貂鼻腔中4天后即检测不到,而BJ501病毒在免疫1~7天都保持着较高的病毒滴度;从各器官病毒载量来看减毒A/California/07/2009ca流感病毒(表6)在鼻、肺中有低量复制,在脾、肾、脑中没有病毒复制。BJ501病毒(表7)除在鼻、肺中有较高复制外,在脑中也有复制。这说明减毒A/California/07/2009ca流感病毒是弱毒的,而BJ501病毒具有较强的毒力。
A/California/07/2009ca流感病毒免疫雪貂后,从HI实验(图1)结果来看,A/California/07/2009ca病毒的抗体对BJ501病毒具有较好的中和效果,与A/California/07/2009ca病毒无差异;二免两周后,BJ501病毒免疫雪貂,通过对不同器官BJ501病毒的检测(表7)我们可以看到,和空白对照组相比,雪貂鼻、肺的病毒载量都显著降低,脑中没有检测到病毒。这说明减毒A/California/07/2009ca流感病毒产生的抗体是有效的,对雪貂具有一定的免疫保护作用。
本实验应用减毒A/California/07/2009ca流感病毒及BJ501病毒免疫雪貂,通过对雪貂机体各项生理指标的检测及不同时间点鼻腔的病毒载量、各个器官的病毒载量、攻毒后的各个器官病毒载量的检测,证明减毒A/California/07/2009ca流感病毒具有减毒性、不致病性及一定的免疫保护性。这些数据的获得为今后减毒疫苗株的研发提供了实验数据参考。
1 杜 宁,王大燕,舒跃龙et al.2009新甲型H1N1流感病毒病原学概述[J]. 病毒学报,2009;25(6):479-483.
2 Centers for Disease Control and Prevention(CDC).Swine influenza A(H1N1)infection in two children-Southern California,March-A-pril 2009[J].MMWR Morb Mortal Wkly Rep,2009;58(15):400-402.
3 史芳芳,李红叶,刘玉霞et al.多重RT-PCR方法检测甲型流感病毒[J].免疫学杂志,2011;27(2):162-165.
4 Dybing J K,Stacey S C,Swayne D E et al.Distinct pathogenesis of Hong Kong-origin H5N1 viruses in mice compared to that of other highly pathogenic H5 avian influenza viruses[J].J Virol,2000;74(3):1443-1450.
5 Banks J,Speidel E C,McCauley J W et al.Phylogenetic analysis of H7 haemagglutinin subtype influenza A viruses [J].Arch Virol,2000;145(5):1047-1058.
6 杨松涛,高玉伟,夏咸柱et al.虎源H5N1亚型禽流感病毒感染小鼠模型的建立[J].中国病毒学,2006;21(4):253-357.
7 Munster V J,de Wit E,van den Brand J M et al.Pathogenesis and Transmission of Swine-Origin 2009 A(H1N1)Influenza Virus in Ferrets[J].Science,2009;325(5939)1126-1177.
8 Maines T R,Jayaraman A,Belser J A et al.Transmission and Pathogenesis of Swine-Origin 2009 A(H1N1)Influenza Viruses in Ferrets and Mice[J].Science,2009;325(5939):484-487.
9 Forrest H L,Khalenkov A M,Govorkova E A et al.Single-and multiple-clade influenza A H5N1 vaccines induce cross protection in ferrets[J].Vaccine,2009;(27):4187-4195.
10 鲍琳琳,占玲俊,秦 川et al.雪貂感染流感病毒H3N2动物模型的建立[J].中国比较医学杂志,2011;21(8):5-9.
11 Amorsolo L,Suguitan Jr,Josephine M et al.Live,attenuated influenza A H5N1 candidate vaccines provide broad cross-protection in mice and ferrets[J].Plos Medicine,2006;360(9):154-169.
12 Yang P H,Duan Y Q,Wang C H et al.Immunogenicity and protective efficacy of a live attenuated vaccine against the 2009 pandemic A H1N1 in mice and ferrets[J].Vaccine,2011;29(4):698-705.
- 中国免疫学杂志的其它文章
- 幽门螺杆菌VacA、CagA及BabA蛋白的二级结构和免疫表位预测分析①

