油酸钠改性对凹凸棒黏土理化性能的影响
徐继香,康玉茹,王爱勤
(1.中国科学院兰州化学物理研究所,甘肃 兰州 730000;2.中国科学院研究生院, 北京100049)
凹凸棒黏土(Attapulgite, APT)是一种含水富镁铝的硅酸盐矿物,独特的棒晶结构使其成为聚合物材料理想的功能填料。然而,APT在形成过程中,由于类质同晶置换现象,使其呈亲水性,与聚合物的相容性差,限制了在塑料、油性涂料和橡胶等方面的应用。为了解决APT在聚合物基质中的分散问题,需对其进行物理化学改性。由于APT的阳离子可交换性和富含硅羟基,用阳离子或非离子表面活性剂和偶联剂进行有机化改性是常用的处理方式[1-4],而直接采用阴离子表面活性剂改性APT的研究报道较少。采用阴离子表面活性剂改性APT,通常是在其表面先包覆金属氧化物,使表面带正电后再用阴离子表面活性剂改性[5];也可以先使APT在酸性或碱性条件下质子化或去质子化,从而使黏土表面带正电或负电[6],然后进行阴离子表面活性剂有机改性。由于在APT表面先包覆金属氧化物后有机化涉及到二步反应,因此,本文采用阴离子表面活性剂油酸钠为改性剂。通过调节悬浮液pH值,探讨了油酸钠用量、pH值和反应温度对APT有机化程度的影响;同时,通过红外光谱、流变和ζ电位的测定,考察了最优pH和反应温度条件下,研究了不同油酸钠用量对APT理化性能的影响。
1 实验部分
1.1 试剂及仪器
凹凸棒黏土(APT),江苏玖川纳米材料科技发展有限公司,使用前粉碎过200目筛。油酸钠(化学纯,国药集团化学试剂有限公司)。实验中所用其他试剂皆为分析纯。Thermo Nicolet NEXUS TM FTIR 型红外光谱仪(美国)、 Anton paar Physica MCR301流变仪(奥地利)、 Malvern Nano-ZS 激光粒度仪(英国)、SRJX-4-13型高温箱式电阻炉(北京市永光明仪器厂)、GJB-B12K型变频高速搅拌机(青岛海通达专用仪器)。
1.2 油酸钠改性凹凸棒黏土(O-APT)的制备
取一定量的APT,按固液比1∶15,在600 r/min下搅拌均匀后,用1 mol/L的盐酸溶液调悬浮液pH值,然后在设定温度下反应60 min。之后,分别缓慢加入0、2.28%、4.56%、9.13%和18.3%(基于APT质量百分比)的油酸钠,继续搅拌60 min,产物过滤后用50 ℃的温水洗三次,除去未反应的油酸钠,在70 ℃烘干样品,粉碎过200目后放入干燥器备用。
1.3 有机化度测定
分别准确称取0.5000 g APT和O-APT于坩锅中,置于马弗炉中在600 ℃焙烧4 h至恒重。把样品转移至干燥器中冷却至室温后称重,有机化度按以下两个方程式来计算:
OD=h-p
(1)
h,p=[(m1-m2)/m1]×100%
(2)
式中,OD为O-APT的有机化度 (%);h和p分别为APT和O-APT的重量损失;m1和m2分别为煅烧前后样品的重量 (g)。
1.4 流变性测量
在30 mL蒸馏水中加入1.0000 g样品,在11000 r/min时分散20 min后,25 ℃下测量悬浮液黏度随剪切速率的变化。
1.5 ζ电位测量
在100 mL蒸馏水中加入0.5000 g样品,在11000 r/min时分散20 min后,25 ℃下测量电荷随pH值的变化情况。采用0.25 mol/L的盐酸和氢氧化钠调悬浮液pH值。
2 结果与讨论
2.1 油酸钠用量对有机化度的影响
在60 ℃和pH为3时,O-APT的有机化度随油酸钠用量的变化曲线,如图1所示。由图1可见,当油酸钠加入量为APT用量的2.28%时,O-APT的有机化度为1.16%。随油酸钠含量增加,O-APT的有机化度逐步增大,当加入9.13%油酸钠时,O-APT的有机化度为7.30%。继续增大油酸钠用量为APT用量的18.30%时,O-APT的有机化度增加不明显,趋于平衡。这是因为APT的交换能力是一定的;另一方面,高浓度下悬浮液中形成的胶束离子,也不利于表面活性剂在颗粒表面的吸附[7]。
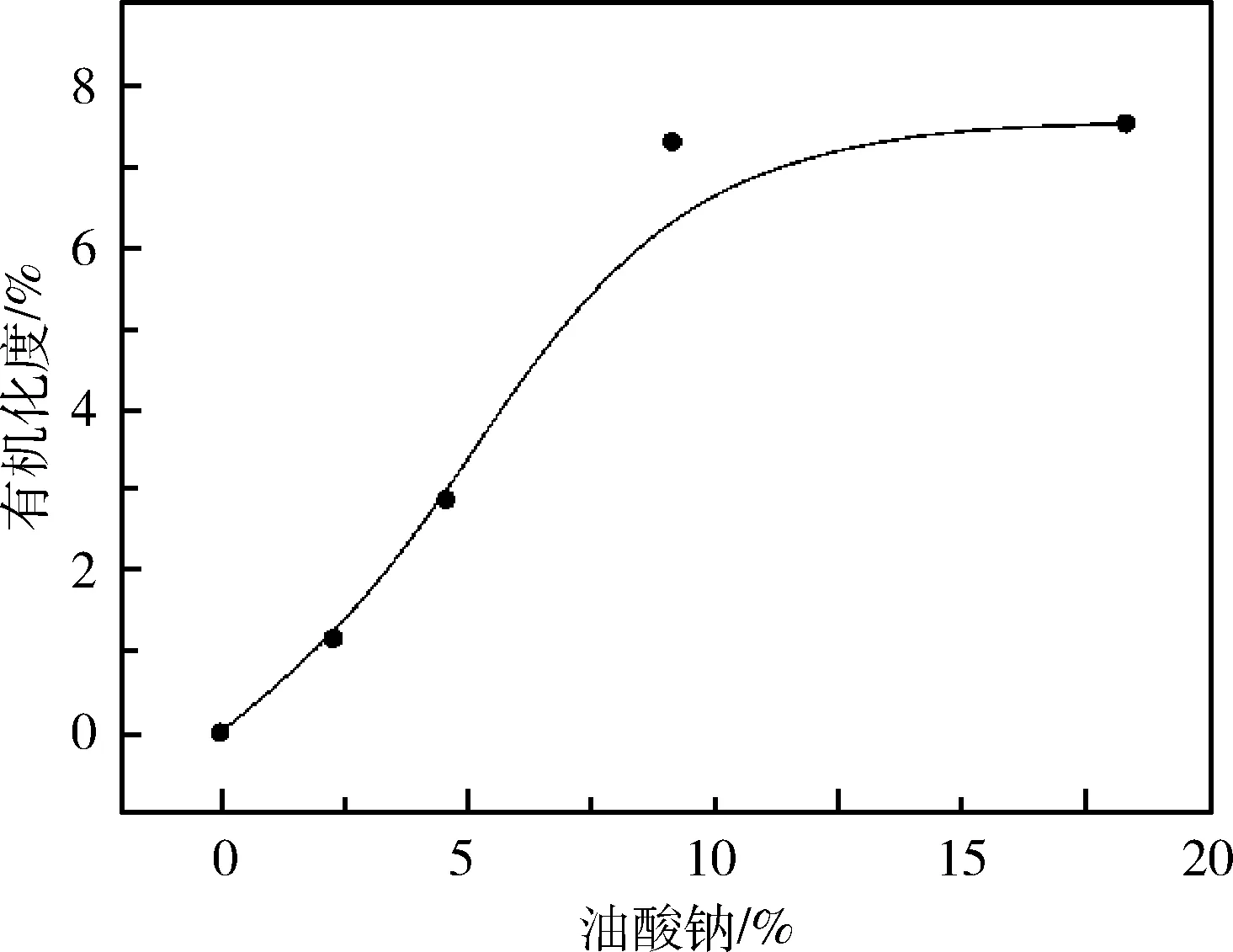
图1 油酸钠用量对O-APT有机化度的影响
2.2 溶液pH值对有机化度的影响
在60 ℃和油酸钠为APT用量9.13%时,O-APT的有机化度随溶液pH值的变化曲线,如图2所示。由图2可见,随pH值的增大,O-APT的有机化度呈现先增加后减小的趋势。当悬浮液pH为3时,O-APT的有机化度最大;当pH值进一步增大时,O-APT的有机化度又呈减少趋势。APT中具有可交换的Na+、Mg2+、Ca2+和Fe3+等金属离子,当用酸处理时,H+可交换这些金属离子,由于APT棒晶的微结构会发生变化,因而对其他阳离子物质有较大的吸附量[8]。随着pH值的增加,H+交换Na+、Mg2+、Ca2+和Fe3+等金属离子的能力减弱,因而油酸钠吸附量减少。当pH值大于APT等电点后,对油酸钠的吸附更弱,所以O-APT的有机化度更小。
2.3 反应温度对有机化度的影响
在pH为3和油酸钠为APT用量9.13%时,O-APT的有机化度随反应温度的变化曲线,如图3所示。由图3可见,随着反应温度的升高,O-APT的有机化度呈缓慢增加的趋势,但60 ℃后又减小。可能的原因是:随反应温度升高,油酸钠的溶解度增加,悬浮液中油酸钠吸附到APT表面的几率增大。同时,在pH值一定时,油酸钠主要通过静电吸附的方式结合在APT表面,而高温不利于物理吸附[9],所以80 ℃时O-APT的有机化度降低。
2.4 红外光谱分析
油酸钠、APT和不同有机化度O-APT的红外谱,如图4所示。与APT原土相比,O-APT在2921 cm-1和2851 cm-1处出现了-CH2反对称和对称吸收峰,在1556 cm-1和1450 cm-1附近出现了-COO-对称和反对称伸缩振动峰[10],说明APT表面已结合了油酸根离子。同时,随油酸钠用量增加,上述特征峰变得越强,表明APT表面结合的油酸根离子增加。该结果与图1中有机化度的变化趋势相一致。

图2 pH值对O-APT有机化度的影响

图3 温度对O-APT有机化度的影响
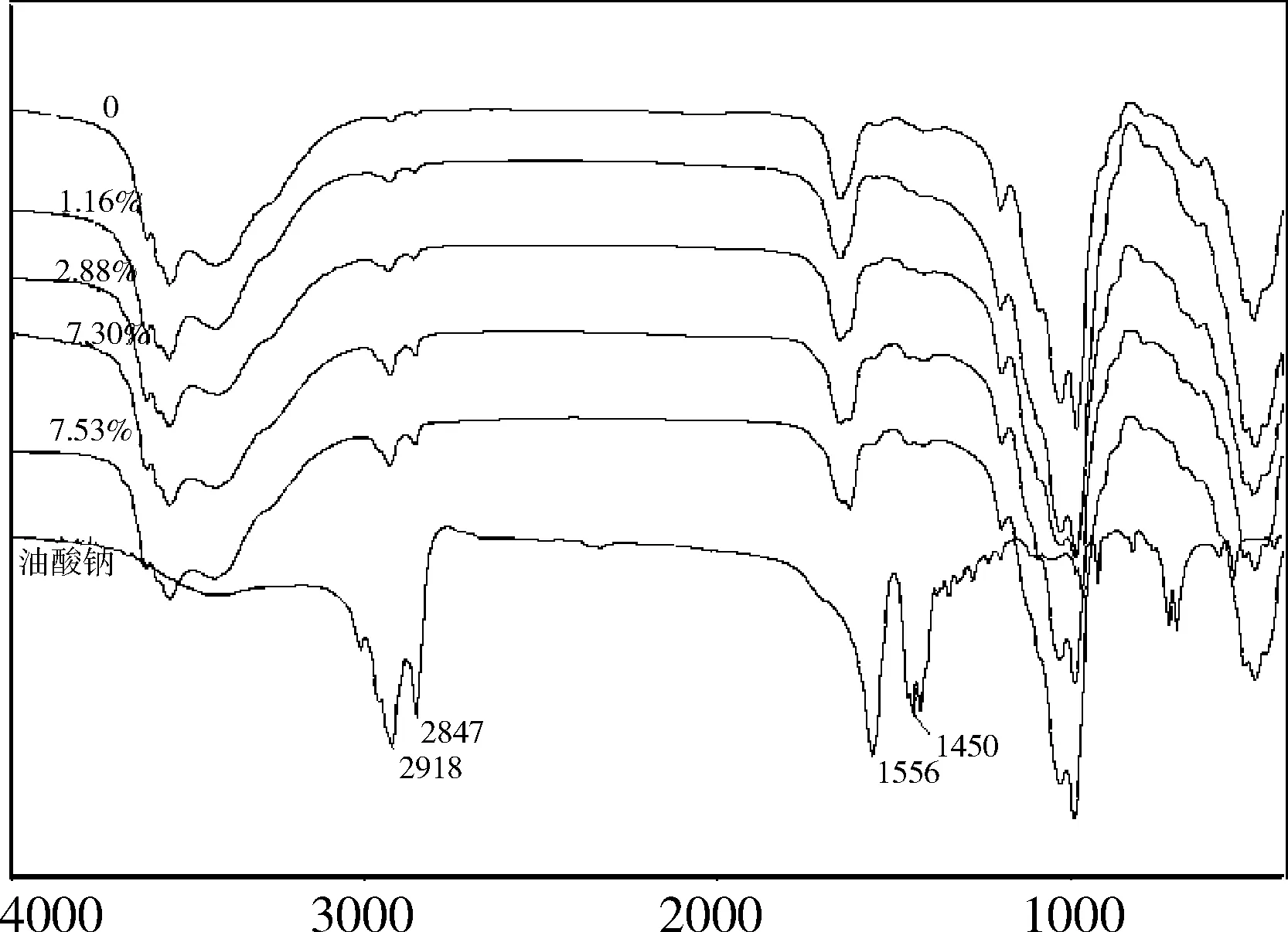
图4 油酸钠及不同有机化度O-APT样品的红外谱图
2.5 流变学性质
在APT悬浮液中,纤维状棒晶通过静电力和范德华力相互作用,使悬浮液保持一定的黏度,但随剪切力的增加,悬浮液黏度降低,表现出剪切变稀的行为。图5是在pH值为3和反应温度为60 ℃时,不同有机化度O-APT样品的黏度-剪切力曲线。与APT原土相比,有机化处理后APT悬浮液剪切黏度下降,表明油酸钠与APT发生了相互作用。当加入少量油酸钠时,APT表面部分正电荷位置结合了油酸根离子,长烷基链使APT表面疏水性增加,悬浮液剪切黏度下降。由图5可见,加入油酸钠用量为APT的4.56%时,APT悬浮液剪切黏度达到最小值;而加入油酸钠用量为APT的9.13%时,对应O-APT的悬浮液剪切黏度增加。可能原因是APT表面吸附的长链油酸根离子在棒晶间形成桥链,进一步增加油酸钠浓度时,悬浮液剪切黏度下降,可能的原因是在APT表面形成多层吸附的油酸根离子,增加了棒晶间的空间位阻[11]。油酸钠改性APT剪切变稀行为,预示着在油性涂料方面有很好的应用前景。
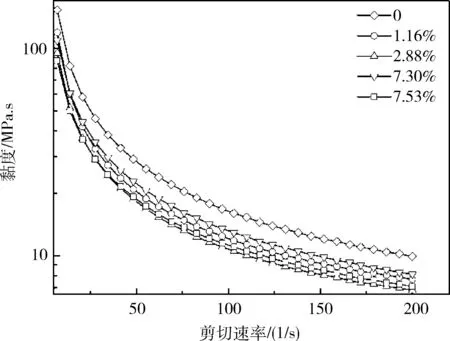
图5 不同有机化度O-APT的黏度-剪切力曲线
2.6 ζ电位分析
图6是不同有机化度O-APT表面ζ电位随悬浮液pH的变化曲线。与APT原土相比,改性处理的APT表面ζ电位更负,电位随油酸钠含量的增加而逐渐降低,表明油酸根离子结合在APT表面的正电荷位置处。当加入油酸钠用量为APT的2.28%和4.56%时,体系ζ电位与空白样品相比无显著下降,说明APT表面少量正电荷位置处吸附了油酸根离子,颗粒表面由完全亲水变为部分疏水。油酸钠用量增至APT用量的9.13%和18.30%时,悬浮液ζ电位更负,等电点的pH值分别变为2.38和1.86,表明APT表面正电荷进一步减少,大量油酸根离子结合在APT表面,表面疏水性增强。结合图5可以看出,ζ电位测量结果与样品的流变性能相一致。
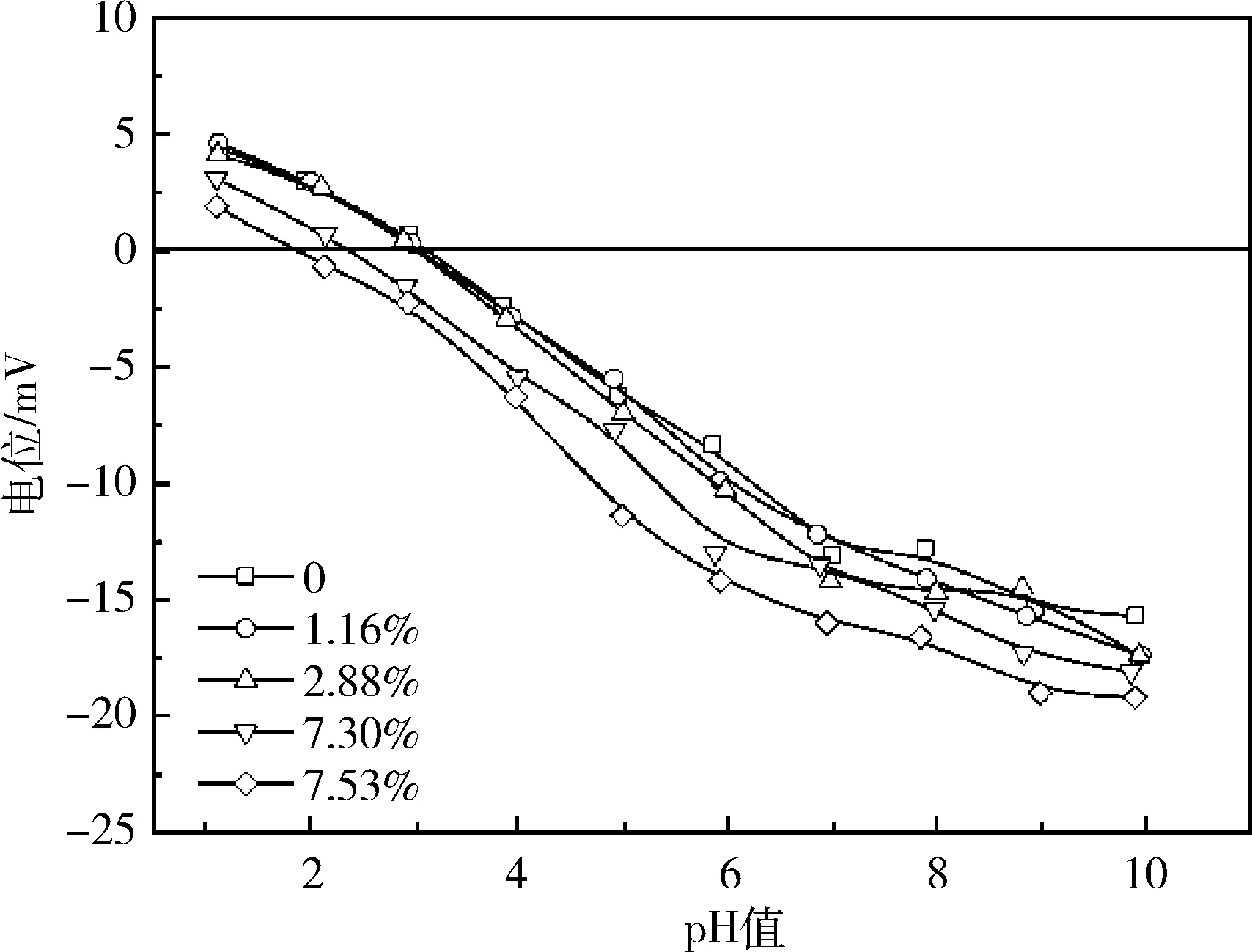
图6 不同有机化度O-APT的ζ电位随pH的变化曲线
3 结论
1) 用阴离子表面活性剂油酸钠改性APT,红外光谱证实APT表面结合了油酸根离子。反应条件对APT的有机化度有一定影响,当体系pH为3、反应温度60 ℃和油酸钠加入量为APT的9.13%时,改性样品有机化度达到7.30%。
2) 与APT原土相比,有机化处理后APT悬浮液剪切黏度下降,但随油酸钠用量增加,有机改性APT悬浮液的剪切黏度又呈现增大趋势。加入油酸钠用量为APT的4.56%时,悬浮液剪切黏度最低。
3) 随油酸钠用量增加,APT表面电荷更负,等电点逐渐减小。 油酸钠加入量为APT的18.30%时,APT表面等电点为1.86。
[1] An L., Pan Y., Shen X., et al. Rod-like attapulgite/polyimide nanocomposites with simultaneously improved strength, toughness, thermal stability and related mechanisms [J]. Journal of Materials Chemistry, 2008, 18: 4928-4941.
[2] Xue S., Reinholdt M., Pinnavai T. J. Palygorskite as an epoxy polymer reinforcement agent [J]. Polymer, 2006, 47: 3344-3350.
[3] Wang L., Sheng J.. Preparation and properties of polypropylene/org-attapulgite nanocomposites [J]. Polymer, 2005, 46: 6243-6249.
[4] 陈浩, 张俊平, 王爱勤. 有机凹凸棒黏土的制备及复合高吸水性树脂的性能 [J]. 应用化学, 2006, 23(1): 69-73.
[5] 姚超, 张国庆, 吴凤芹, 等. 硬脂酸钠对凹凸棒土有机表面改性的研究 [J]. 非金属矿, 2008, 31(6): 1-3.
[6] A. Neaman, A. Singer. Rheological properties of aqueous suspensions of palygorskite [J]. Soil Science Society of America journal, 2000, 64: 427-436.
[7] Xiao L., Xu G., Zhang Z., et. al. Adsorption of sodium oleate at the interface of oil sand/aqueous solution [J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2003, 224(1-3): 199-206.
[8] Chen H., Zhao Y. G., Wang A. Q.. Removal of Cu(II) from aqueous solution by adsorption onto acid-activated palygorskite [J]. Journal of Hazardous Materials, 2007, 149(2): 346-354.
[9] Ofor O. Oleate adsorption at a nigerian hematite-waterinterface: effect of concentration, temperature, and pH on adsorption density [J]. Journal of Colloid and Interface Science, 1995, 174: 345-350.
[10] Sivamohan R., de Donato P., Cases J. M.. Adsorption of oleate species at the fluorite-aqueous solution interface [J]. Langmuir, 1990, 6(3): 637-644.

