硫酸氢铵分解NH4Cl制备NH3和HCl工艺研究
张宪军,李树春,张振霞,崔美琴
(大连化工研究设计院,辽宁 大连 116023)
科学试验
硫酸氢铵分解NH4Cl制备NH3和HCl工艺研究
张宪军,李树春,张振霞,崔美琴
(大连化工研究设计院,辽宁 大连 116023)
对氯化铵分解的硫酸氢铵法进行了验证性的研究。同传统的专利及其它报道相比,采用本文的工艺,可使氯化铵的转化率达到95%。结果表明,当NH4HSO4:NH4Cl的摩尔比为4∶1时,反应温度在220~350℃之间,氯化铵转化率≥95%,氨气收率、氯化氢收率均≥95%。
氯化铵分解;硫酸氢铵;氨气;氯化氢
由于联碱的快速发展,氯化铵产量越来越多,面临过剩的问题。目前氯化铵主要用途是农业肥料,工业上少量使用,由于氯化铵用途的限制,开辟氯化铵新用途势在必行,这样可以促进具有自主知识产权的联碱工业健康地发展。寻求新的技术将氯化铵分解成氯化氢和氨,使氯化铵成为化工原料,将纯碱化工与有机氯化工紧密地联系到一起。所以氯化铵分解技术对于联碱的发展具有战略意义。
目前,在世界上氯化铵分解技术还没有大规模工业化应用,只有少量的专利和文献对氯化铵分解的工艺提出了一些设想并进行了初步探索。美国专利、日本专利,还有 Kessler等[1~3]提出将氯化铵固体或气体通过与硫酸铵或硫酸氢铵共混熔融后分步反应的方法进行分解。清华大学的翟广伟等人论述了硫酸铵或硫酸氢铵法[4],氯化铵的转化率不到20%,HCl收率不到20%。当然还有其它的方法,比如碱金属化合物法等等。
上述文献大多数对硫酸氢铵法分解氯化铵进行了简单的描述或有限的实验论证,缺乏详细的工艺和理论研究,并据此得出该方法的NH4Cl转化率低,操作困难,易升华,不具有可行性。本工作着重对硫酸氢铵法进行了验证性研究,最终找到了优化的工艺条件。
1 氯化铵分解原理
NH4Cl受热分解成NH3和 HCl,但同时会有大量的NH4Cl升华,为了得到NH3和HCl,一种可行的方法就是在反应物中加入一种可循环使用的酸性物质或者碱性物质,简单的说,先固定一种气体(NH3或 HCl),释放另一种气体(HCl或NH3)。无论何种NH4Cl分解方法,归结起来可表示[5]:
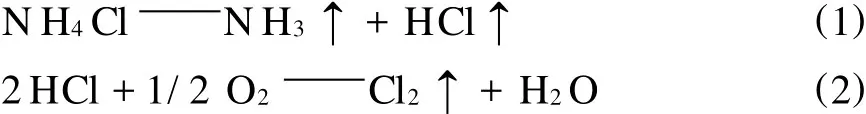
从化学热力学观点看,反应所需要的能量为状态函数,在任何一定的温度及压力下,反应物和生成物的相态一定,无论采用哪种方法及循环过程,制取NH3和Cl2(HCl)其所需能量不能小于指定条件下发生反应(1)、(2)理论所需要的能量。但是由于分解方法不同,即反应温度、压力及相态有差异,则能量的消耗不一致。在实际循环过程中有能量的损失,所以能耗远远超过理论能量。因此,不管采用哪种分解方法,在过程中能否做到能量的合理利用及降低能量的损失,是评价NH4Cl分解方法优劣的标志。当然,在选择方法时,过程的复杂程度、设备与材质的利用和腐蚀状况、反应条件的难易程度等,也是必须考虑的问题。
硫酸铵的热分解[6]已有详细研究,本文主要研究通过不同的反应方式提高氯化铵的转化率以及产物的收率。
2 试 验
2.1 试验原理
将NH4Cl加到硫酸氢铵熔融物中使硫酸氢盐温度为220~270℃,将游离态的HCl放出。此时,相当于NH3“被固定”,另一生成物基本为硫酸铵;

继续升温至330~350℃,硫酸铵分解释放出NH3,另一产物基本为硫酸氢铵。硫酸氢铵进行下一次反应,循环使用。

2.2 试验方法
试验方法分为两种反应方式。一是将一定配比的NH4Cl加入到常规反应的硫酸氢铵熔融物中;二是将一定配比的NH4Cl加入到半连续接触式反应的硫酸氢铵熔融物中。两种反应方式进行对比。
2.2.1 常规反应NH4Cl分解试验
在常规反应器中将已处理NH4HSO4加热,加入一定量的NH4Cl,继续升温到220~270℃,用pH试纸检测有 HCl气体放出,收集并计量。待无HCl放出后,继续升温至330~350℃后,用pH试纸检测有NH3放出,收集并计量。直至无NH3放出,停止反应。称重反应器,计算NH4Cl转化率。反应过程中可观察到有升华的白色NH4Cl固体结晶。试验结果如表1所示。
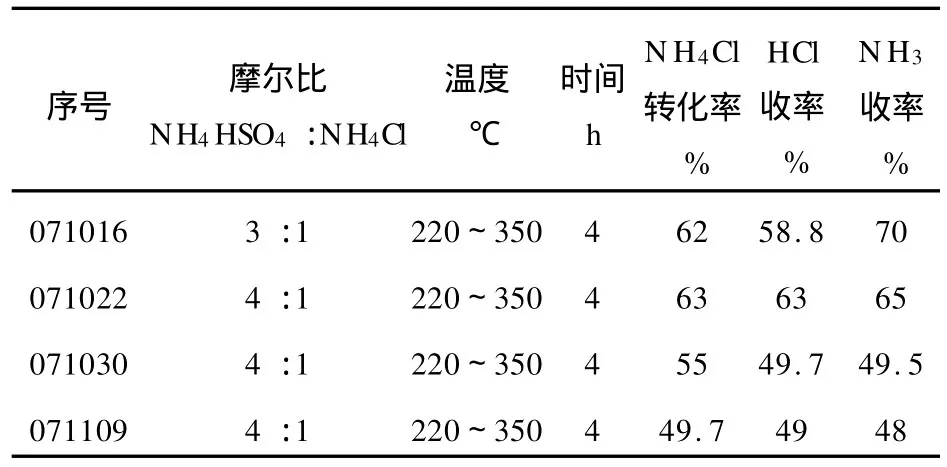
表1 NH4Cl和NH4HSO4常规反应的试验结果
2.2.2 半连续接触反应NH4Cl分解试验
在半连续接触反应器中将已处理NH4HSO4加热,通过调节加料器加入一定量的NH4Cl,升温到220~270℃,用pH试纸检测有 HCl气体放出,收集并计量生成的HCl气体。待无HCl气体放出后,继续升温至330~350℃后,用pH试纸检测有NH3气体放出,收集并计量生成的NH3气体。直至无NH3气体放出,停止反应。计算NH4Cl转化率。反应过程中没有明显观察到有升华的白色NH4Cl固体结晶。试验结果如表2所示。
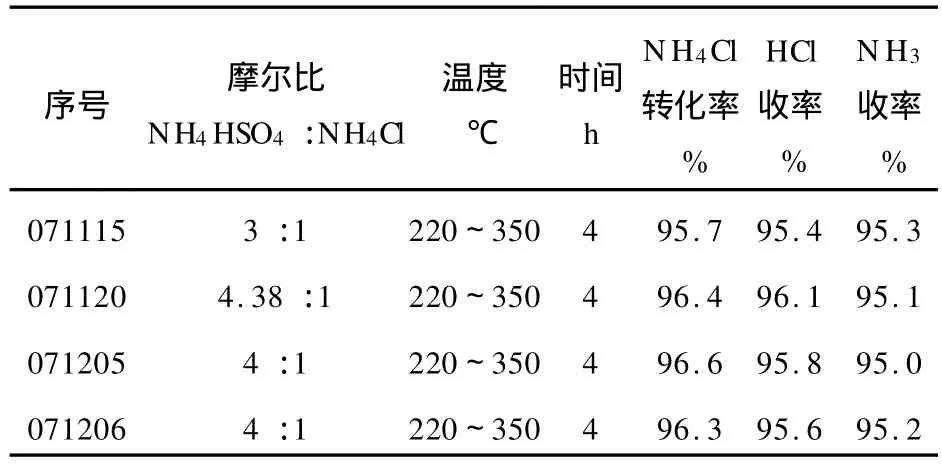
表2 NH4Cl和NH4HSO4半连续接触反应的试验结果
3 试验结果与讨论
1)硫酸氢铵法分解氯化铵的试验工艺是可行的。通过我们的半连续接触反应方法,氯化铵的转化率以及HCl、NH3收率有明显提高。
2)工业应用上需要选择能够在高温下耐酸碱腐蚀的金属材质。若解决了材质问题,工业应用就变得容易。
3)升华的氯化铵可通过回收重复利用。这样可提高氯化铵的利用率和转化率。
4)硫酸氢铵法分解氯化铵的最佳工艺条件是:
①NH4HSO4:NH4Cl的摩尔比=4∶1;
②加料方式:半连续接触法;
③反应温度:220~270℃分解回收 HCl气体; 330~350℃分解回收NH3气体;
④反应时间:4h。
在此条件下,NH4Cl转化率≥95%;NH3、HCl气体的收率为≥95%。
[1] 平贺要一.[P].JP:58-161902,1983-09-26
[2] SasakiH,TakaharaY.[P].US:4293532,1981-10-16
[3] ClaflinC.H.[P].US:2787524,1957-04-02
[4] 翟广伟,韩明汉,梁耀彰,高光华.氯化铵分解制氨气和氯化氢工艺 [J]过程工程学报.2009,9(1):59~62
[5] 张洪如.氯化铵的分解[J].纯碱工业,1982(5):41~43
[6] 刘科伟.硫酸铵的热分解[J].化学研究与应用,2002, 14(6):737~738,765
TQ113.7;TQ114.162
A
1005-8370(2011)04-03-03
2011-03-22
张宪军(1970—)大学本科,高级工程师。1996年毕业于华北工学院,现从事纯碱及纯碱生产助剂方面的研发工作。

