含三氟甲基和双希夫碱化合物的合成与表征
于赛男, 李智超, 胡英芝, 尹大学
(青海师范大学 化学系,青海 西宁 810008)
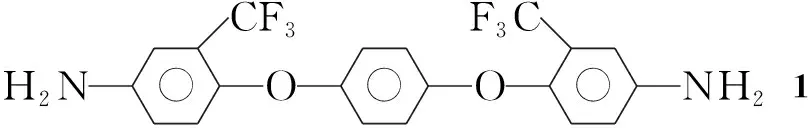
含氟化合物在杀菌、杀虫、除草领域有着广泛的应用[1]。含三氟甲基芳香化合物在农药、药物中间体等领域也有广泛的应用价值[2]。希夫碱是一类具有教好生物活性的物质,而以希夫碱为配体与金属离子形成的配合物表现出更强的生物活性[3],在抑菌、杀菌、抗肿瘤、抗病毒和解毒等独特药效[4~6]。本文利用1,4-双(4-氨基-2-三氟甲基苯氧基)苯(1)与苯甲醛(2a)或其衍生物(2b~2f)的反应,合成了一系列含三氟甲基和双希夫碱的新化合物(3a~3f, Scheme 1),其结构经UV,1H NMR, IR和元素分析表征。
1 实验部分
1.1 仪器与试剂
Lanbda 35型紫外光谱仪(CHCl3); Inova-400型核磁共振仪(CDCl3为溶剂,TMS为内标);Nexus 670型红外光谱仪(KBr压片);Elementar Vaio EL型元素分析仪。
1按文献[7]方法合成,其余所用试剂均为分析纯,使用前纯化。
Scheme1
1.2 合成(以3a为例)
在圆底烧瓶中加入2a1.7 mL(10 mmol), 1 1.08 g(5 mmol和苯20 mL,搅拌下加入适量盐酸,回流分水3 h。自然冷却至室温,析出固体,抽滤,滤饼用苯重结晶得N,N-双苯甲醛缩-1,4-双(4-氨基-2-三氟甲基苯氧基)苯(3a)。
用类似的方法合成3b~3f。
3a: 淡黄色晶体,产率62%, m.p.190 ℃~191 ℃; UV-visλmax: 317.8, 260.6 nm;1H NMRδ: 8.47(s, 2H, CH=N), 7.89(d,J=8.0 Hz, 4H, ArH), 7.55(s, 2H, ArH), 7.51~7.47(m, 6H, ArH), 7.34(d,J=8.8 Hz, 2H, ArH), 7.05(s, 4H, ArH), 6.98(d,J=6.8 Hz, 2H, ArH); IRν: 3 444, 1 627, 1 486, 1 325, 1 245 cm-1; Anal.calcd for C34H22N2O2F6: C 67.55, H 3.64, N 4.64; found C 67.72, H 3.70, N 4.65。
3b: 黄色晶体,产率81%, m.p.170.5 ℃~171.5 ℃; UV-visλmax: 324.2, 266.6 nm;1H NMRδ: 8.43(s, 2H, CH=N), 7.89(d,J=6.8 Hz, 4H, ArH), 7.52(s, 2H, ArH), 7.31(d,J=8.8 Hz, 4H, ArH), 7.17(d,J=7.2 Hz, 4H, ArH), 7.05(s, 4H, ArH), 6.95(d,J=8.8 Hz, 2H, ArH); IRν: 3 440, 1 631, 1 485, 1 323, 1 244 cm-1; Anal.calcd for C34H20N2O2F8: C 63.75, H 3.12, N 4.38; found C 63.77, H 3.15, N 4.37。
3c: 黄色晶体,产率73%, m.p.241 ℃~242 ℃; UV-visλmax: 348.6, 272.6 nm;1H NMRδ: 12.85(s, 2H, OH), 8.62(s, 2H, CH=N), 7.60(s, 2H, ArH), 7.41~7.40(m, 2H, ArH), 7.39(d,J=7.2 Hz, 2H, ArH), 7.38~7.37(m, 2H, ArH), 7.07(s, 4H, ArH), 7.03~6.99(m, 2H, ArH), 6.96(d,J=7.0 Hz, 2H, ArH), 6.94(d,J=8.2 Hz, 2H, ArH); IRν: 3 431, 1 620, 1 483, 1 326, 1 263 cm-1; Anal.calcd for C34H22O4N2F6: C 64.15, H 3.46, N 4.40; found C 64.23, H 3.50, N 4.38。
3d: 黄色晶体,产率49%, m.p.252 ℃~253 ℃; UV-visλmax: 366.2, 306.9 nm;1H NMRδ: 8.30(s, 2H, CH=N), 7.73(s, 2H, ArH), 7.49(d,J=7.2 Hz, 2H, ArH), 7.23(d,J=7.6 Hz, 2H, ArH), 7.02(s, 4H, ArH), 6.95(d,J=8.8 Hz, 4H, ArH), 6.72(d,J=8.2 Hz, 4H, ArH), 3.06(s, 12H, ArH); IRν: 3 441, 1 609, 1 482, 1 370, 1 322 cm-1; Anal.calcd for C38H32N4O2F6: C 66.09, H 4.64, N 8.12; found C 66.13, H 4.67, N 8.13。
3e: 黄色晶体,产率32%, m.p.193 ℃~194 ℃; UV-visλmax: 332.8, 279.2 nm;1H NMRδ: 8.37(s, 2H, CH=N), 7.64(s, 2H, ArH), 7.53(s, 2H, ArH), 7.32(d,J=6.4 Hz, 2H, ArH), 7.04(s, 4H, ArH), 6.97(d,J=8.4 Hz, 2H, ArH), 6.95(d,J=6.4 Hz, 2H, ArH), 3.95(s, 6H, ArH), 6.93(d,J=8.4 Hz, 2H, ArH), 3.98(s, 6H, ArH); IRν: 3 435, 1 630, 1 486, 1 320, 1 268, 1 236 cm-1; Anal.calcd for C38H30N2O6F6: C 62.98, H 4.14, N 3.87; found C 63.01, H 4.19, N 3.85。
3f: 黄色晶体,产率50%, m.p.265 ℃~266 ℃; UV-visλmax: 358.6, 275.6 nm;1H NMRδ: 8.55(s, 2H, CH=N), 8.34(d,J=14 Hz, 4H, ArH), 8.03(d,J=8.6 Hz, 4H, ArH), 7.59(s, 2H, ArH), 7.34(d,J=7.2 Hz, 2H, ArH), 7.07(s, 4H, ArH), 6.98(d,J=7.0 Hz, 2H, ArH); IRν: 3 433, 1 627, 1 524, 1 484, 1 322, 1 244 cm-1; Anal.calcd for C34H20N4O6F6: C 58.79, H 2.88, N 8.07; found C 58.78, H 2.91, N 8.06。
2 结果与讨论
2.1 结构与产率的关系
由于要形成双希夫碱,产率总体不够理想,但含有吸电子基团化合物的产率相对较高,而含有供电子基团化合物的产率较低。但2c由于分子内含有氢键使碳氧双键上的碳活性增强,有利于反应进行,从而产率升高。2f由于苯环上连有硝基形成共轭体系,使醛基活性降低,不利于反应进行,导致产率降低。在实验过程中发现,延长反应时间对产率的影响较小,主要原因是由于在化合物一端形成碳氮双键后使另一端的胺基的亲和性能降低。3a~3f的元素分析数据实测值与理论值基本吻合。
2.2 UV
对3a~3f的UV光谱分析发现,在260 nm~307 nm出现较强的苯环共轭吸收带,在317 nm~360 nm出现的吸收带为具有共轭的希夫碱C=N的π→π*电子跃迁产生的,证明了NH2与C=O完全缩合生成了C=N双键,合成了新的系列希夫碱。
与3a相比,3d的吸收波长增加最多,这是因其含有三氟甲基这个强吸电子基团使二甲胺基的供电性加强,从而使其吸收波长增大。3f由于含有生色基团硝基使吸收波长向长波方向移动较大。3c和3e由于本身含有助色基团,与3a相比向长波方向移动较小。3中的三氟甲基使吸电子基团的作用减小,而使供电子基团的作用增加。根据伍德沃德规则:卤素+5 nm,羟基+30 nm,二甲胺基+60 nm,二个甲氧基+15 nm,硝基+30 nm。
2.3 IR
3a~3f的IR谱图的共同特征是在1 632 cm-1~1 609 cm-1处有一强而尖锐的吸收峰,为碳氮双键的伸缩振动吸收;在1 487 cm-1~1 482 cm-1处有依次减小几个中强吸收峰,为苯环碳的骨架振动吸收;在1 246 cm-1~1 236 cm-1处有一个强峰,为双芳醚的特征峰;在1 327 cm-1~1 320 cm-1处有中强吸收峰,为三氟甲基的吸收峰。另外3d在1 370 cm-1处中强吸收峰,为二甲胺基的吸收峰。3e在1 268 cm-1处有一强吸收峰,为甲氧基的强吸收峰。3f在1 524 cm-1处有强吸收峰,为硝基的吸收峰。此外在3 440 cm-1附近的为羟基的吸收峰。1的胺基(3 363 cm-1)特征吸收峰已消失。
与3a的碳氮双键伸缩振动波数相比较,3f中含有强吸电子基团硝基从而抵消了三氟甲基的吸电子作用力,使共轭体系的电子云密度降低,通过链传递致使碳氮双键的电子云密度降低较小,因而向高波数的移动较小。3c和3d含有供电基团使电子云密度升高,振动能量降低,从而使波数降低。并且由于二甲胺基的供电子能力大于羟基,所以3d的波数比3c的波数更低。3e虽然带有供电子基团,但由于受到空间位阻效应的影响,使吸收频率移向高波数。3b的波长增加其原因是F的电负性较大,其诱导效应占主要地位,因此吸收频率增加。
2.4 1H NMR
分析3的1H NMR谱图数据,在δ8.70~8.30的单峰为碳氮双键的特征吸收峰,说明其在CDCl3介质中以亚胺的形式存在,证明希夫碱的生成。
3c的羟基氢质子峰出现在12.85处,原因是碳氮双键上的氮和羟基氢形成分子内氢键,使质子氢周围的电子云密度减小,质子共振磁场降低,化学位移增大。此外由于分子内氢键使碳氮双键的电子云密度降低,对质子产生去屏蔽效应,使碳氮双键上氢的化学位移向低场移动。3f中吸电子的NO2与苯环上相连时,与苯环形成共轭体系,使苯环上的电子云密度降低,通过链传递使碳氮双键上质子的核外电子云密度降低,屏蔽效应减弱,从而使质子的化学位移向低场移动。3b,3d和3e分别含有供电子氟、甲氧基和二甲胺基含有孤对电子与苯环形成p→π共轭体系,供电子效应大于诱导效应使苯环上电子云密度增加,通过链传递使碳氮双键上质子的核外电子云密度增大,屏蔽效应加强,质子共振磁场升高,化学位移降低。对于三氟甲基的取代,由于离质子较远,因此在1H NMR谱中观察不到三氟甲基上氟的影响。因此除3d外,含有三氟甲基的苯环上的相同位置上的氢的化学位移值几乎相同。3d的三个氢的位移值略有增加(δ约0.2),是由于二甲胺基的强供电子效应使三氟甲基的吸电子效应加强所致,通过偶合常数的计算,对各个有偶合效应的氢的关系理论与实际完全相符。
综上所述,在IR图谱中,3在1 632 cm-1~1 609 cm-1内出现强而尖锐的碳氮双键的伸缩振动吸收峰,是希夫碱的特征峰。在UV谱图中346 nm附近出现具有共轭的希夫碱碳氮双键吸收带,证明了胺基与醛基完全缩合生成了碳氮双键。在1H NMR中碳氮双键上CH(δ8.70~8.30)均以单峰的形式出现。系列希夫碱化合物通过谱图分析可以确定结构与预期结果一致。
[1] 刘长令. 含氟农药开发的新进展[J].精细与专用化学品,2000,6:3-6.
[2] 程隆新. 含三氟甲基农药的开发进展[J].现代农药,2004,3(3):7-11.
[3] Isse A, Gennaro A, Vianello E. Electrochemical reduction of Schiff bases ligands H2salen and H2salophen[J].Electrochemical Acta,1997,42(13-14):2065-2071.
[4] 徐莉, 徐世平. 2-吲哚醛西佛碱化合物的合成及其抗癌活性研究[J].药学学报,2000,35(4):269-272.
[5] 徐嵩,徐世平,李兰敏. 4-,6-或7-位取代苯基亚胺次甲基香豆素的合成及其抗癌活性[J].药学学报,2002,37(2):113-116.
[6] Nathan Guz, Frank S, Kim Lewis. Flavono lignan and flavone inhitions of a staphylococcus aureusmulti-drug resistance pump:Structure-activityrelationships[J].J Med Chem,2001,44:261-268.
[7] K Xie, S Y Yang, J G Liu,etal. Synthesis and characterization of soluble fluorine-containing polyimedes based on 1,4-bis(4-amino-2-trifluoromethylphenoxy)benzene[J].J Polym Sci Part A:Polym Chem,2001,39(15):2581-2591.

