锈层下碳钢的腐蚀电化学行为特征
邹 妍 王 佳,2,* 郑莹莹
(1中国海洋大学化学化工学院,山东青岛 266100;2中国科学院金属研究所,金属腐蚀与防护国家重点实验室,沈阳 110016)
锈层下碳钢的腐蚀电化学行为特征
邹 妍1王 佳1,2,*郑莹莹1
(1中国海洋大学化学化工学院,山东青岛 266100;2中国科学院金属研究所,金属腐蚀与防护国家重点实验室,沈阳 110016)
采用极化曲线、线性极化电阻(LPR)和电化学阻抗(EIS)研究了海水中带锈碳钢的电化学行为,结果发现:长期浸泡的内锈层对电极过程有较大影响;短期浸泡,LPR和EIS测定的极化电阻(Rp)逐渐增大;而长期浸泡,Rp却逐渐减小;随着浸泡时间的延长,Rp出现了先增大后减小的变化趋势.将锈层逐层剥离后研究了碳钢的电化学行为,并结合傅里叶变换红外(FTIR)光谱和横截面结构分析表明,这主要是因为长期浸泡后,内锈层中出现了具有较高电化学活性的β-FeOOH,并且其含量随着浸泡时间的延长而逐渐增加.当进行电化学测试时,在对体系进行一定程度极化的过程中,β-FeOOH参与了阴极还原反应,使电极过程不再是简单的阳极金属溶解和阴极氧还原,加快了阴极反应速度,从而导致Rp逐渐减小.
电化学行为;锈层;极化电阻;阴极还原;傅里叶变换红外光谱
锈层/金属是多相多界面复杂腐蚀体系之一,其特征是腐蚀过程涉及多个相内传质和多个相界面区迁移反应,并且腐蚀进程也会随着腐蚀产物积累而增减和转化.复杂腐蚀体系的上述特征导致测量方法和腐蚀数据变得复杂和难于解析,增加了研究工作的不确定性.锈层下的腐蚀是复杂的电化学过程,锈层覆盖金属的腐蚀电化学反应涉及锈层自身氧化还原,锈层相内传质,锈层相界面电荷迁移以及多孔锈层中微生物繁殖等多个子过程组成的复杂腐蚀过程[1-3],导致电极过程复杂化.
碳钢是海洋环境中使用的最主要的金属结构材料,其腐蚀一般为均匀腐蚀,锈层下碳钢的腐蚀是最主要的、持续时间最长的腐蚀形态,生成的铁锈主要是与铁的腐蚀有关的氧化物和羟基氧化物.锈层下的腐蚀行为与许多因素有关,如锈层的形成机制、锈层的发展变化和锈层的组成结构等.在不同环境下生成的锈层对碳钢的电极过程有不同程度的影响,因此研究其腐蚀产物与电化学行为的关系极为重要.
García等[4]认为碳钢全浸在海水中,在其表面生成的锈层可以分为两层:紧密附着的内锈层和附着不牢固的外锈层.外锈层中γ-FeOOH的含量最多,而内锈层中尖晶石相(磁性Fe3O4和磁性Fe2O3)的含量最多.β-FeOOH主要在金属的表面形成并紧紧附着在金属表面,使锈层具有多孔性并且成分不均匀,因而不具有保护性.Ma等[5]研究了在海洋大气中腐蚀生成的碳钢锈层,发现在空气中暴露3个月以后锈层开始分为两层:外层从6个月开始组成不变,由α-FeOOH、γ-FeOOH、无定形的氢氧化物和Fe3O4组成;6个月时内层只有β-FeOOH和无定形的氢氧化物,腐蚀速度增大;暴露24个月,内锈层由α-FeOOH、γ-FeOOH、无定形的氢氧化物和Fe2O3组成,腐蚀速度减小.α-FeOOH是一种比较稳定的物质,具有比较低的电化学活性,在锈层中可以起到比较好的保护作用[6].Stratmann等[7-10]研究了在干湿循环条件下纯铁的腐蚀行为,认为锈层中γ-FeOOH与Fe的腐蚀电位比较接近,γ-FeOOH是电化学活性物质,可以作为阴极参与还原反应.Nishimura等[11]认为在含有Cl-环境中形成β-FeOOH很容易发生电化学还原反应.
近年来发现,在金属/锈层复杂体系中,由于其复杂的电极过程而导致电化学方法测定的极化电阻(Rp)也受到了锈层的影响.Andrade等[12]在用电化学阻抗法研究钢筋在混凝土中的电化学行为时发现,在电位-0.7 V(vs SCE)附近,Rp会受腐蚀产物氧化还原反应的影响.González等[13]发现用传统的极化电阻方法不适合测定带锈金属的腐蚀电流密度.当锈层存在时,锈层中二价和三价铁离子的氧化还原反应会产生很大的偏离正常双电层电容数值的假电容.锈层一方面能给阴极反应提供还原物质,另一方面可以作为氧气还原的多孔电极.Flis等[14]认为钢筋经过长时间腐蚀后,界面转输电阻Rct减小,这主要是因为高价态的腐蚀产物被还原.Videm[15]用循环伏安、恒电位阶跃、恒电流阶跃、电化学阻抗等电化学方法测量了钢在碱性溶液中的腐蚀速度,发现各种电化学方法测得的结果之间有很大分歧,主要原因是腐蚀产物的氧化还原反应掩盖了金属发生腐蚀反应的法拉第电流.
为此,本文采用多种电化学方法研究了海水中锈层下碳钢的电化学行为和在自腐蚀电位附近的电极过程特征,结合锈层的组成结构分析,探讨了在电化学测试过程中碳钢阴极和阳极的反应机理.
1 实验方法
1.1 电极材料
实验材料采用Q235钢,其化学成分(质量分数(w),%)为:C 0.18,Si 0.30,Mn 0.32,P 0.04,S 0.04,Fe余量.电化学试样为厚度3 mm、直径10 mm的圆柱,一端为工作面,其余面用环氧树脂(莱阳经济技术开发区精细化工厂)封装.在实验前将所有试样用400#、600#和800#水磨砂纸逐级打磨,然后用去离子水清洗,酒精除油后在干燥器中备用.实验开始时,将电化学样品浸泡在室内海水试验箱(深圳又昭实业有限公司)中.实验所用海水取自青岛汇泉湾,室内的平均温度为20℃,在实验箱中的海水为静态海水,每个星期更换海水一次.实验开始于2007年11月,定期进行电化学测试.
1.2 红外光谱测试
用毛刷刷下外层疏松的腐蚀产物,再用刀片小心剥离内锈层,将取下的外层和内层腐蚀产物研成粉末,放入真空干燥器中以备红外测试.分析仪器为美国Nicolet公司生产的Nexus-380型傅里叶变换红外光谱仪,测量光谱区域为400-1300 cm-1,设定扫描次数为32次,实际分辨率为4 cm-1.取少量锈层样品进行测量,加入适量的KBr粉末,充分研细并混合均匀,利用模具加压制成透明样品后置于光谱仪样品室进行测试.横截面形貌采用深圳Jetet公司生产的JT-2182II彩色摄像机进行拍摄.
1.3 电化学测试
电化学测试采用三电极体系,辅助电极为铂片电极,参比电极为饱和甘汞电极,电解液为海水,使用美国Princeton公司生产的PARSTAT 2263电化学工作站进行腐蚀电化学测量,测试软件为Powersuite(美国Princeton).分别剥下不同锈层进行电化学测试的剥离方法与进行红外测试锈层的剥离方法相同.电化学阻抗(EIS)测试是在自腐蚀电位下进行的,频率范围为9 kHz-9 mHz,交流激励信号幅值为10 mV.线性极化电阻(LPR)测试的扫描速率为0.1 mV·s-1.扫描范围为相对于自腐蚀电位±10 mV.极化曲线测试扫描速率为0.1 mV·s-1,为了避免锈层的影响,极化曲线分别从自腐蚀电位向阴极和阳极扫描.极化曲线每次采用3个平行试样,挑选具有代表性的实验结果;电化学阻抗测试和线性极化测试采用5个平行试样,每次都对这5个试样进行测试,选取具有代表性的一组实验结果.测试时溶液的平均温度为20℃.
2 结果与讨论
2.1 锈层形貌
图1为在海水中浸泡不同周期碳钢的横截面形貌.可以看出,浸泡6周(图1a)时锈层只是一层比较薄的疏松黄色腐蚀产物(对应图中间的浅色部分);浸泡11周(图1b)时,锈层可以分为两层,在金属与黄色腐蚀产物之间增加了一层黑色薄而致密的内锈层(对应图中间的深色部分);随着浸泡时间的增加,从图1c和图1d看出黑色的内锈层逐渐增厚,黄色的外锈层厚度变化很小.
2.2 锈层的成分

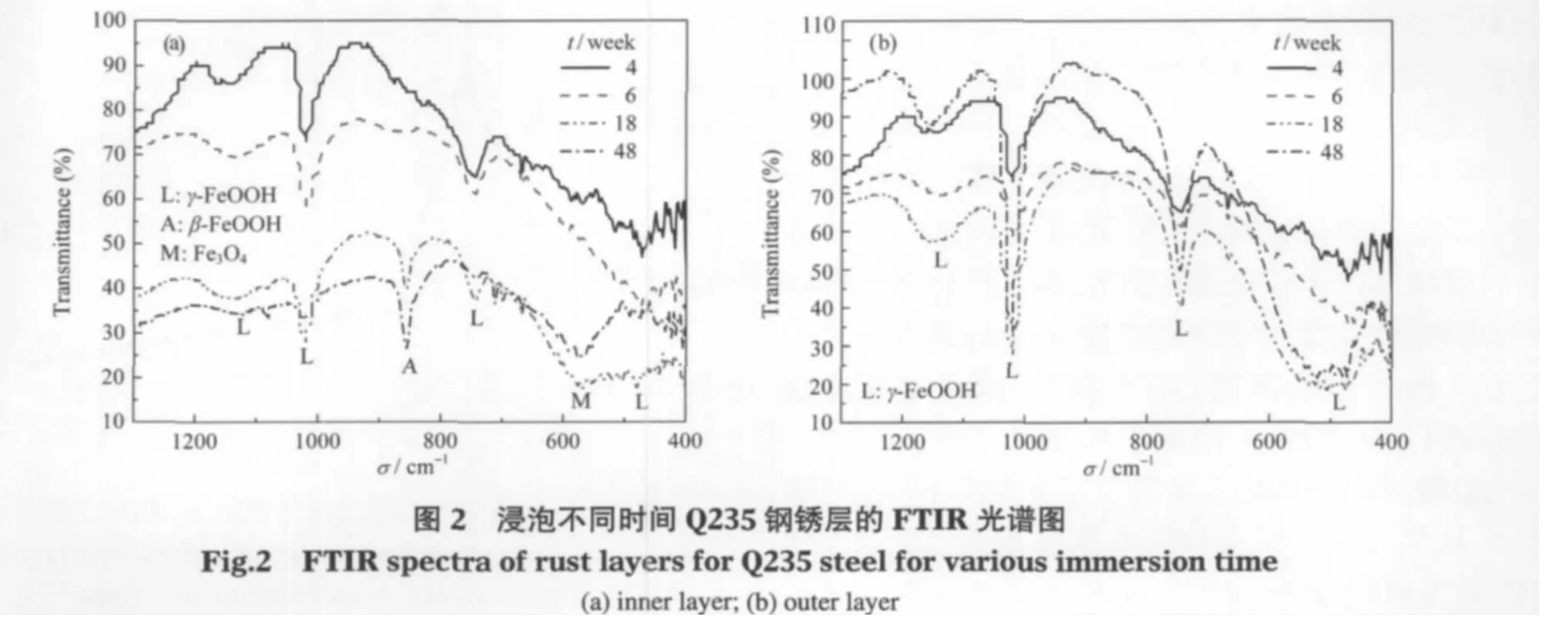
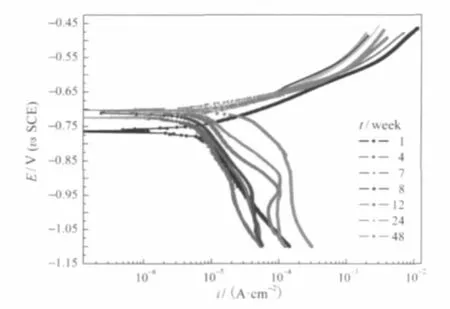
图3 在海水中浸泡不同时间Q235钢的极化曲线Fig.3 Polarization curves of Q235 steel immerged in seawater for various time
图2 为浸泡不同阶段的碳钢的红外光谱图.浸泡4周和6周时,锈层没有分层;浸泡18周和48周锈层明显分为内锈层和外锈层两层.浸泡4周的锈层在1143、1020、744和482 cm-1出现比较明显的特征峰,对应了γ-FeOOH的特征峰;浸泡6周的锈层除了有明显的γ-FeOOH的特征峰外,在861 cm-1有一个非常小的特征峰,对应了β-FeOOH中O—H的弯曲振动特征峰,这说明了此时锈层中可能有非常少量的β-FeOOH生成;浸泡18周后外锈层中含有γ-FeOOH,但没有β-FeOOH.内锈层除了γ-FeOOH的特征峰外,β-FeOOH的特征峰变得很强,说明β-FeOOH的含量明显增多.另外,在587 cm-1还有一个比较宽的特征峰,这与Fe3O4的特征峰相吻合.浸泡48周后,外锈层的成分没有发生变化,内锈层中β-FeOOH的特征峰强度超过了γ-FeOOH.这些结果表明,浸泡前期没有分层时的锈层组分与浸泡后期分层后的外锈层组分相同;8周前基本上不存在β-FeOOH,它主要形成于8周之后的内锈层中,其含量随着浸泡时间的增加而逐渐增大.
2.3 锈层下碳钢的电化学行为
2.3.1 极化曲线行为
图3为不同浸泡时间碳钢的稳态极化曲线.随着浸泡时间的增加,自腐蚀电位逐渐正移,4周以后自腐蚀电位基本稳定.阳极反应速度和斜率基本不变表明锈层对阳极过程的影响不大,锈层下阳极过程仍然是铁溶解反应.但是,锈层对阴极过程有较大影响.相比之下,8周前阴极行为变化很小,从8周开始阴极极限电流平台和阴极反应速度逐渐增加,阴极的反应机理也应该随之发生变化.
2.3.2 线性极化行为
图4为海水中浸泡48周碳钢电极的线性极化曲线.浸泡初期自腐蚀电位较负,随着浸泡时间的增加,自腐蚀电位正移并逐渐稳定,线性极化曲线也略微有点弯曲,这是由于腐蚀产物在碳钢表面的累积造成的.因此,拟合区域选在自腐蚀电位附近接近直线段的±5 mV范围内.测定的Rp变化见图5.
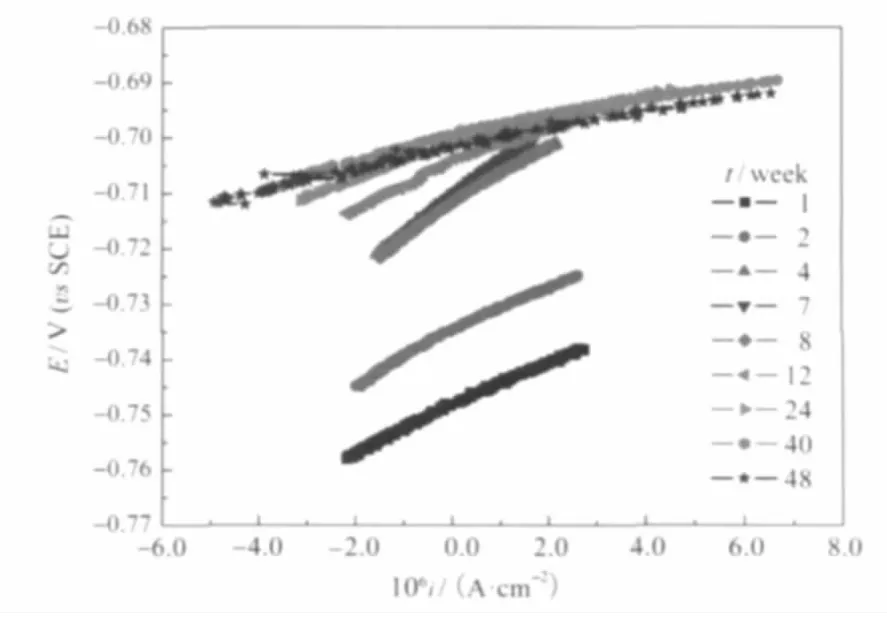
图4 浸泡不同时间Q235钢的线性极化曲线Fig.4 Linear polarization curves of Q235 steel immerged in seawater for various time
Rp随时间变化的主要特征是8周以前Rp持续增加,从第8周开始突然转为迅速减小,12周以后逐渐趋于平缓.8周前后存在截然不同的行为这一特征与图3的极化曲线变化是一致的,表明这也是阴极过程的增强引起的.由此可以表明,长期浸泡的锈层在电化学测试过程中对自腐蚀电位附近的电极过程也产生了较大的影响.
2.3.3 电化学阻抗行为
图6为浸泡48周碳钢电极的电化学阻抗响应. Nyquist图(图6(a、b))是由两个下偏的半圆构成,可能是电极表面的粗糙度导致了充放电过程的不均匀[16],因而用常相位角元件Q来代替电容元件C.高频反映了锈层的性质,低频反映了锈层/金属界面的电极过程.随着锈层的增厚,最大幅角对应的频率向低频方向移动,Bousselmi等[2]认为是锈层厚度的增加导致了这种变化.碳钢在海水中浸泡一段时间后生成的锈层可以分为内锈层和外锈层,而从极化曲线和LPR测试中发现8周前后电化学行为发生较大变化,这也可能与内锈层的生成有关,因此浸泡前8周用等效电路图7(a)[2]来拟合,8周以后(包括8周)等效电路见图7(b)[5,17],证实拟合的曲线与实验曲线吻合良好,误差在5%以内.
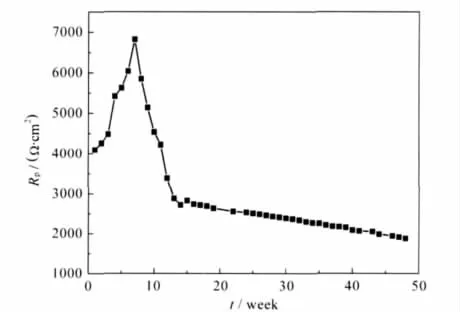
图5 线性极化法测定的极化电阻(Rp)随时间的变化Fig.5 Polarization resistance(Rp)measured by LPR with increasing of immersion time
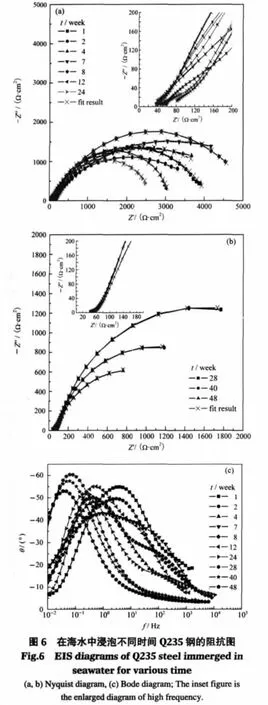
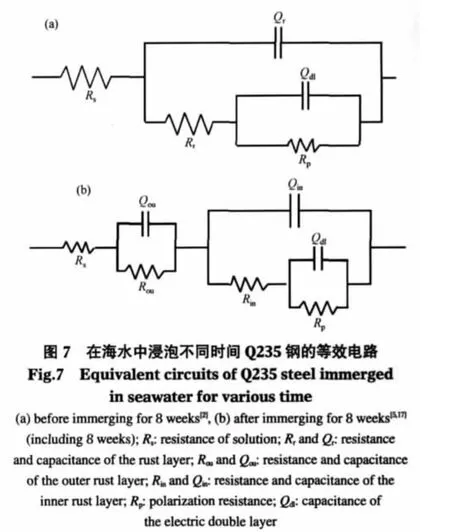
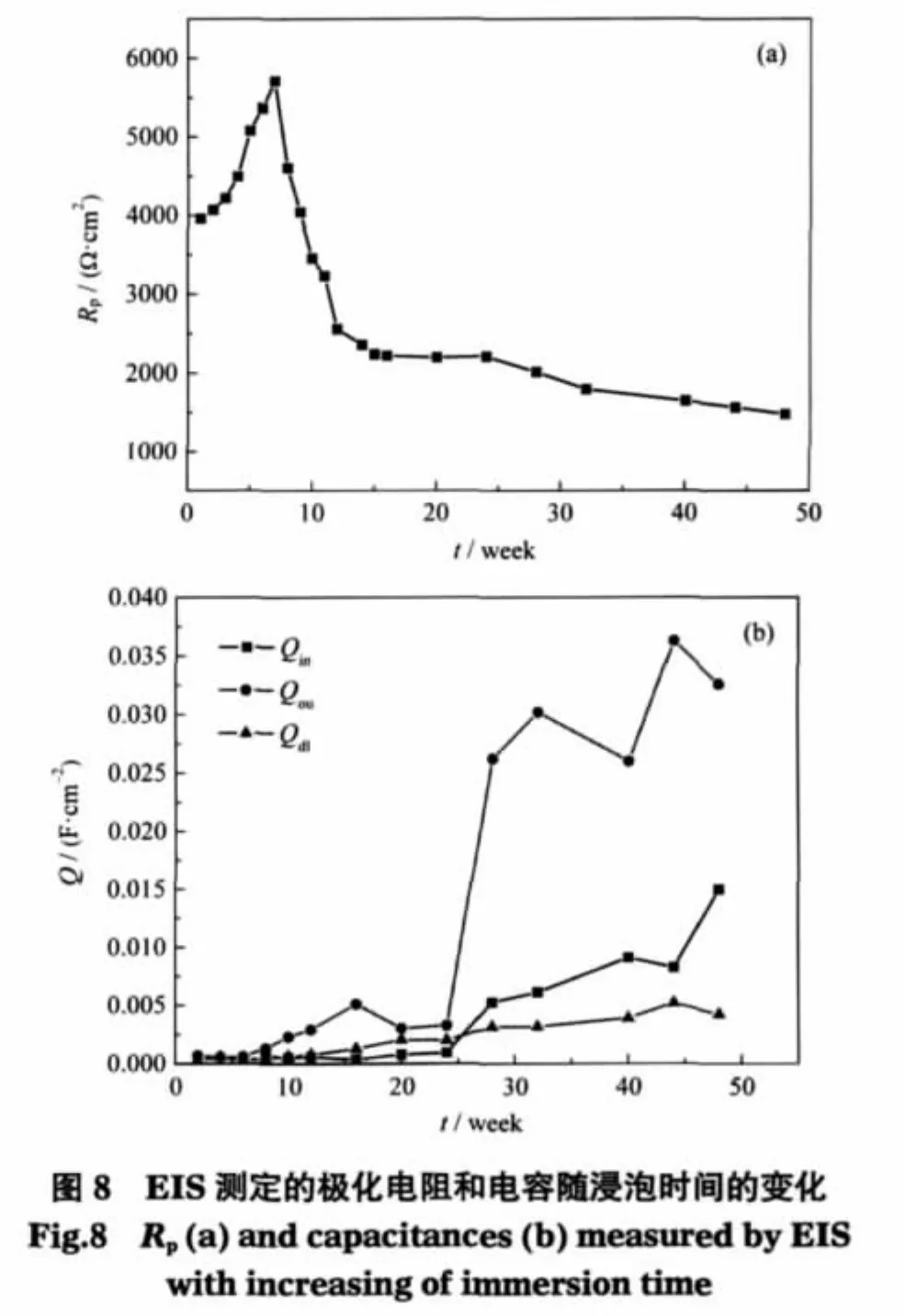
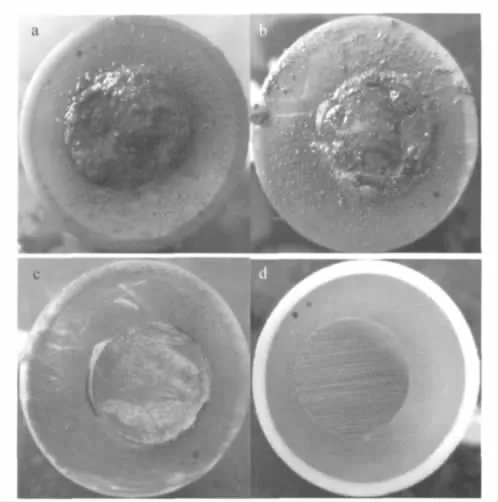
图9 在海水中浸泡20周Q235钢不同锈层覆盖的电极形貌Fig.9 Appearances of Q235 steel with different rust layers after immerging in seawater for 20 weeks(a)rust covered;(b)removal of the outer layer; (c)removal of the inner layer;(d)naked coupons
由于阴极反应是腐蚀过程的控制步骤,因此极化电阻Rp反映了在金属/锈层界面发生阴极反应的能力.随着浸泡时间的增加,Rp逐渐增大;8周以后, Rp转为逐渐减小,12周以后变化缓慢(图8(a)).EIS方法得到的Rp变化趋势与LPR方法是一致的.从电容的数值来看(图8(b)),浸泡前24周,内、外锈层电容和双电层电容变化都不大,而这段时间Rp却经历了先增大后减小的过程;24周以后内锈层和外锈层的锈层电容都显著增加,而极化电阻却变化不大,这说明了比较大的锈层电容虽然在一定程度上会影响Rp的测定,但不一定是主要因素,有可能是反应机理发生变化而导致了长期浸泡的Rp逐渐减小.
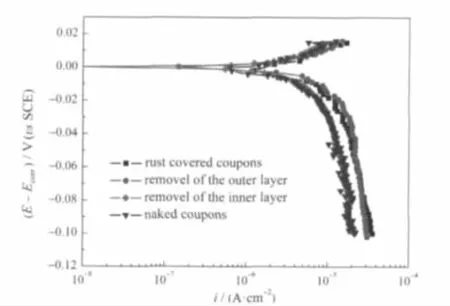
图10 在海水中浸泡20周分别除去外锈层和内锈层的阴极极化曲线放大图Fig.10 Magnified cathodic polarization curves of Q235 steel whose outer and inner rust layers were removed separately after immerging in seawater for 20 weeks
2.4 不同深度锈层的电化学响应特征
电极表面状态分为以下4种状态:带锈、去除外锈层、去除内层锈和打磨光滑的裸碳钢(图9).带锈的碳钢从表面看呈黄色(图9a中较浅的颜色),剥离外锈层后碳钢表面为黑色(图9b中较深的颜色),剥离内锈层后碳钢表面能看到腐蚀后的蚀坑.显然,除掉内锈层的碳钢和光滑的碳钢的阴极行为是相同的,仅仅清除外锈层的碳钢和带锈碳钢的阴极行为是相同的,同时比除掉内层锈碳钢和光洁碳钢阴极电流密度显著增大.这一结果表明,内锈层是导致阴极反应加速的主要原因.图10为将在海水中浸泡20周带锈电极逐层剥离锈层后的局部阴极极化曲线.
图11为在海水中浸泡20周的带锈碳钢逐层剥离锈层后的电化学阻抗图.除掉内锈层的碳钢和打磨光滑的裸碳钢试样具有相同的较高阻抗值,而被完整锈层覆盖的碳钢电极和除去外锈层的碳钢电极具有较低的相同的阻抗值.
这一行为与图10的结果是一致的.碳钢电极表面被完整锈层覆盖时的电化学阻抗谱的等效电路见图7(b).除去外锈层后只覆盖着内锈层的等效电路见图7(a).除去内锈层和打磨光滑的裸碳钢只有一个时间常数,在金属/溶液界面只发生铁的阳极溶解和氧气的还原反应,等效电路为Rs(QdlRp).按上述等效电路分别进行拟合后得到的各种电阻值列于表1,拟合曲线和实验数据能够很好地吻合(图11).
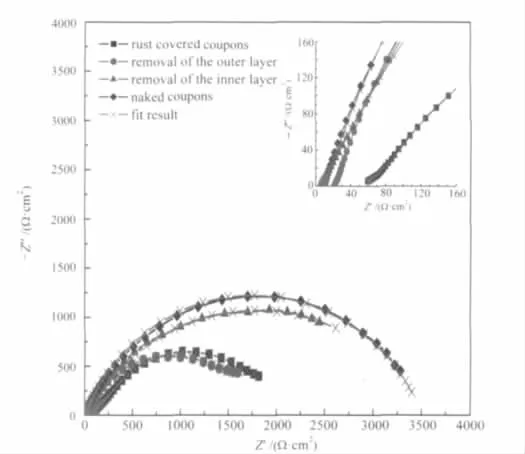
图11 在海水中浸泡20周不同锈层覆盖下的Q235钢的电化学阻抗谱Fig.11 EIS diagram of Q235 steel with different rust layers after immerging in seawater for 20 weeksThe inset figure is the enlarged diagram of high frequency.

表1 在海水中浸泡20周的不同锈层覆盖下的Q235钢的拟合电阻值Table 1 Fitted resistance values of Q235 steel with different rust layers after immerging in seawater for 20 weeks
去掉外锈层后,与完整锈层覆盖状态下的Rp相比基本上没有发生变化,说明外锈层不参与电化学反应.除去内锈层后,Rp反而增大表明在带锈体系中主要是内锈层加速了阴极反应.
2.5 电化学测试过程中碳钢的反应机理
实验中发现,浸泡前8周,碳钢表面的锈层呈棕黄色,没有分层;8周以后,锈层开始分层,表层为棕黄色,里层为黑色.
从锈层组分分析来看,浸泡8周以后锈层的组成和结构发生了较大的变化.逐渐形成的内锈层中由于含有β-FeOOH而改变了金属/锈层界面的电化学过程.Antony等[18]认为γ-FeOOH和β-FeOOH都可以发生还原反应,并且β-FeOOH比γ-FeOOH更容易被还原.当这两种成分共同存在时,β-FeOOH起主要作用加速腐蚀速度.Lair等[19]将纯的 γ-FeOOH和β-FeOOH分别与石墨混合,制成电极,外加阴极电流,测定了γ-FeOOH和β-FeOOH在不同溶液中的还原电位.结果发现,在0.1 mol·L-1、pH为7.5的NaCl溶液中,β-FeOOH的还原电位为-400 mV(vs SHE),还原效率较高;γ-FeOOH的还原电位为-450 mV(vs SHE),还原效率较低.在0.1 mol·L-1、pH为8.5的NaCl溶液中,β-FeOOH的还原电位为-440 mV(vs SHE),γ-FeOOH的还原电位为-510 mV (vs SHE).γ-FeOOH比β-FeOOH的还原电位大约负50-70 mV,还原电位越正,越容易被还原.从热力学角度看,γ-FeOOH具有较低的反应活性,β-FeOOH具有较高的反应活性.
当进行电化学测试时,需要对体系进行一定程度的阴极和阳极极化,使腐蚀电化学反应偏离腐蚀电位,这会导致锈层的电化学反应与非极化状态时不同,甚至诱发一些在平衡态时所没有的反应,致使进行测定的Rp先增大后减小.因此8周前后的锈层的电化学活性很可能是不同的.
通过极化曲线可以得知,在浸泡初期,在金属/锈层界面溶解氧的含量较高,在溶解氧供应比较充足的情况下,阴极以氧还原为主,锈层不会参与阴极反应[19].随着浸泡时间的增加,内锈层逐渐生成,锈层组分开始发生变化.具有高电化学活性的β-FeOOH大量出现并且含量逐渐增多.锈层增厚,阻碍作用逐渐增大,溶解氧越来越难扩散到金属基体表面,在电化学测试过程中锈层可以参与还原反应的能力却逐渐增强,在金属/锈层界面氧和锈层参与还原反应的比例不断发生变化.浸泡初期以氧还原为主;一段时间以后β-FeOOH开始出现并且含量逐渐增多,锈层参与还原反应的比例开始增大,氧和锈层共同控制了阴极反应速度;后期氧含量较少,而锈层中却含有大量的β-FeOOH,阴极以锈层还原为主,从而导致了电化学方法测定的Rp出现先增大后减小的情况,加快了阴极反应速度,这从极化曲线上也可以清楚的看到锈层对阴极过程的影响.
根据以上的分析并结合锈层在不同浸泡阶段的组分,可以推测出碳钢在电化学测试过程中极化电阻出现先增大后减小的变化趋势主要和内锈层中β-FeOOH的出现及其含量的变化有关.浸泡前8周,锈层组分中主要是γ-FeOOH,进行电化学测试时发生的电化学反应为
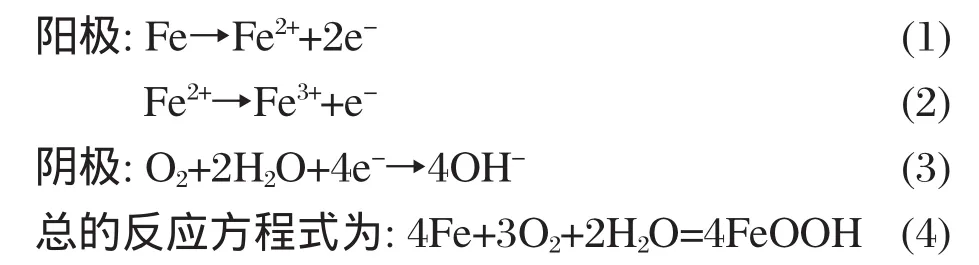
8周以后,锈层组分为γ-FeOOH、β-FeOOH和Fe3O4,进行电化学测试时发生的电化学反应为
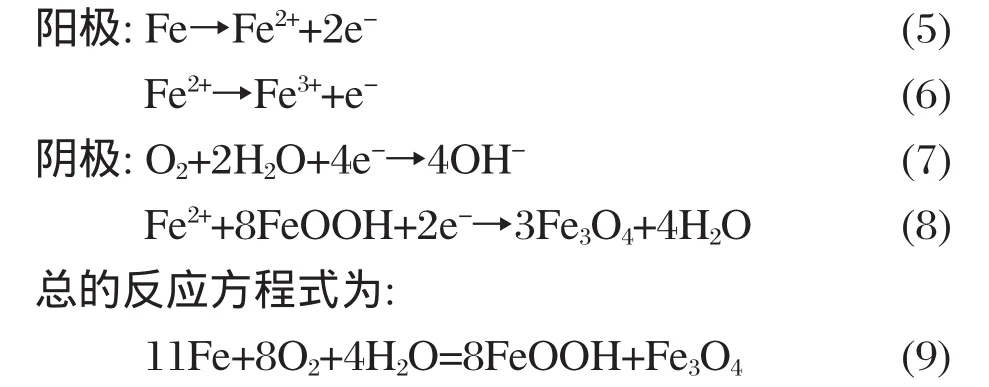
对于电化学方法来说,浸泡前8周,在进行电化学测试时阳极和阴极分别发生铁的溶解和氧的还原反应,随着腐蚀产物的增多,对氧扩散的阻碍能力增大,因此测定的Rp逐渐增大;8周以后,阴极反应增加了β-FeOOH的还原反应,增大了阴极电流密度,从而导致阴极反应加快,Rp减小.
3 结论
(1)在海水中碳钢浸泡前8周,锈层没有分层,主要成分为γ-FeOOH;8周以后,内锈层逐渐生成,主要成分为γ-FeOOH、β-FeOOH和Fe3O4.
(2)锈层在不同浸泡阶段的组成与结构不同,导致锈层下碳钢的阴极行为发生较大变化,并且使在自腐蚀电位附近测定的Rp先增大后减小.
(3)长期浸泡生成的内锈层中的β-FeOOH具有较高阴极反应活性,当进行电化学测试时,一定程度的扰动可以使锈层参与阴极还原反应,加速了阴极反应过程,导致了Rp逐渐减小.
1 Hou,B.R.Oceanologia et Limnologia Sinica,1995,26(5):514 [侯保荣.海洋与湖沼,1995,26(5):514]
2 Bousselmi,L.;Fiaud,C.;Tribollets,B.;Triki,E.Corrosion Sci., 1997,39(9):1711
3 Duan,J.Z.;Wu,S.R.;Zhang,X.J.;Huang,G.Q.;Du,M.;Hou,B. R.Electrochim.Acta,2008,54(1):22
4 García,K.E.;Morales,A.L.;Barrero,C.A.;Greneche,J.M. Corrosion Sci.,2006,48(9):2813
5 Ma,Y.T.;Li,Y.;Wang,F.H.Mater.Chem.Phys.,2008,112(3): 844
6 Yamashita,M.;Miyuki,H.;Matsuda,Y.;Nagano,H.;Misawa,T. Corrosion Sci.,1994,36(2):283
7 Stratmann,M.;Müller,J.Corrosion Sci.,1994,36(2):327
8 Stratmann,M.;Bohnenkamp,K.;Engell,H.J.Corrosion Sci., 1983,23(9):969
9 Stratmann,M.;HoVmann,K.Corrosion Sci.,1989,29(11-12): 1329
10 Stratmann,M.;Streckel,H.Corrosion Sci.,1990,30(6-7):697
11 Nishimura,T.;Tanaka,I.;Shimizu,Y.Tetsu-to-Hagane,1995,81: 1079
12 Andrade,C.;Keddam,M.;Nóvoa,X.R.;Pérez,M.C.;Rangel,C. M.;Takenouti,H.Electrochim.Acta,2001,46(24-25):3905
13 González,J.A.;Miranda,J.M.;Otero,E.;Feliu,S.Corrosion Sci., 2007,49(2):436
14 Flis,J.;Pickering,H.W.;Osseo-Asare,K.Electrochim.Acta,1998, 43(12-13):1921
15 Videm,K.Electrochim.Acta,2001,46(24-25):3895
16 Panda,B.;Balasubramaniam,R.;Dwivedi,G.Corrosion Sci., 2008,50(6):1684
17 Bousselmi,L.;Fiaud,C.;Tribollet,B.;Triki,E.Electrochim.Acta, 1999,44(24):4357
18 Antony,H.;Perrin,S.;Dillmann,P.;Legrand,L.;Chaussé,A. Electrochim.Acta,2007,52(27):7754
19 Lair,V.;Antony,H.;Legrand,L.;Chaussé,A.Corrosion Sci., 2006,48(8):2050
Electrochemical Corrosion Behaviors of Rusted Carbon Steel
ZOU Yan1WANG Jia1,2,*ZHENG Ying-Ying1
(1College of Chemistry and Chemical Engineering,Ocean University of China,Qingdao 266100,Shandong Province, P.R.China;2State Key Laboratory for Corrosion and Protection,Institute of Metal Research, Chinese Academy of Sciences,Shenyang 110016,P.R.China)
Electrochemical methods including polarization curves,linear polarization resistance(LPR),and electrochemical impedance spectroscopy(EIS)were used to characterize and investigate the electrochemical behavior of rusted carbon steel immersed in seawater.Results indicate that the inner rust layer that forms on the surface of the carbon steel after long-term immersion greatly affects the electrode process.Polarization resistance(Rp),determined by LPR and EIS, increases during the initial immersion period.After long-term immersion,it decreases.Rpinitially increases and then decreases gradually with immersion time.The electrochemical characteristics of the rusted carbon steel were studied by removing the outer and inner rust layers.The materials were analyzed by Fourier transform infrared(FTIR)spectroscopy and their cross-sectional morphologies were obtained to determine the cause.The results show that the β-FeOOH, which exists in the inner rust layer,has high electrochemical activity.Its content increases with the growth of the inner rust layer.In the electrochemical tests,even a small amount of polarization allows β-FeOOH to participate in the cathodic reduction reaction.Besides the anodic dissolution of iron and the cathodic reduction of oxygen,rust reduction is also possible.For this reason,the cathodic reaction rate is promoted and Rpdecreases.
Electrochemical behavior; Rust layer; Polarization resistance; Cathodic reduction; Fourier transform infrared spectroscopy
O646
Received:February 21,2010;Revised:March 29,2010;Published on Web:June 25,2010.
*Corresponding author.Email:jwang@ouc.edu.cn;Tel:+86-532-66781903.
The project was supported by the National Natural Science Foundation of China(50971118).
国家自然科学基金(50971118)资助项目
ⒸEditorial office of Acta Physico-Chimica Sinica

