增氧剂过氧尿素的制备及含氧量的测定
董彩霞,姜小莹
(1.中州大学 ,河南郑州 450044;2.河南科技学院 ,河南新乡 453000)
增氧剂过氧尿素的制备及含氧量的测定
董彩霞1,姜小莹2
(1.中州大学 ,河南郑州 450044;2.河南科技学院 ,河南新乡 453000)
通过添加不同纯度的稳定剂硫酸钙寻找最佳方案。探索增氧剂过氧尿素的制备工艺。利用纯度较高的硫酸钙做稳定剂有利于提高产品的产率和产品的含氧量,对原料和稳定剂进行预处理可以获得较满意的产品。
增氧剂 ;过氧尿素 ;产率
过氧化尿素中含有以无水结合的过氧化氢,相当于 H2O2含量为 33%左右,溶于水生成尿素及过氧化氢的弱酸性溶液,在室温下都可获得含 15%浓度的 H2O2溶液。过氧化尿素可溶于有机溶剂,如乙醚、乙醇、丙酮及甘油,利用这些溶剂从过氧化尿素中提取无水 H2O2。由于过氧化尿素具有上述特性,使其具有很多用途:中性洗涤剂的新型添加剂(用于漂白、杀菌);水稻根部供氧专用肥;棉花、木材、化纤、人造丝及羊毛制品的漂白剂;小禽饲料杀菌添加剂;水产养殖业用饲料消毒供氧剂;制药工业的杀菌剂;化妆品工业中染发液中的氧化剂及烫发配方中的中和剂;医用内注射给氧剂及口腔杀菌及灭臭剂;化纤类的防脱色剂及抗静电剂;水泥基础成型添加剂等。过氧尿素比过碳酸钠有很多优点,生产成本也较低。而尿素又是植物必需的营养物质,可以起到双重作用。从众多的用途来看,过氧化尿素的开发具有广阔的市场前景,将产生良好的社会与经济效益。过氧化尿素在国外的应用领域在不断地开拓和扩大。过氧化尿素的主要生产国有美国、日本等,近年来国外开发和应用已获得很大的进展。国内有大量的过氧化氢和尿素的生产厂家,但这种重要精细化工产品在工业上尚处于空白,亟待开发及应用。
过氧尿素又称作过氧化尿素、过氧水合尿素、过氧化脲、过碳酸酰胺。白色结晶或结晶性粉末,在潮湿或 40℃以上时能分解产生氧气。在65~75℃时逐渐变软融化,活性氧含量迅速下降。在 75~85℃熔融并放出活性氧,与水、酸类接触放出氧气。易溶于水、低级醇和乙二醇。乙醚或丙酮可使过氧化氢从水中萃取出来,但此溶液有爆炸性。离子状态、金属状态及氧化物状态的铁、铜、铅、锰,都能加速过氧尿素的分解。过氧尿素属于一级无机酸性腐蚀品,强氧化剂。应储存于阴凉通风库内,远离火源、热源。与可燃物、易燃物、还原性物质分存。
1 过氧尿素的制备
1.1 原料和设备
H2O2,分析纯,天津市东方化工厂;脲 (尿素),工业纯,天津市化工试剂一厂;高锰酸钾,分析纯,天津市化工试剂一厂;草酸钠,基准,北京化工厂;硫酸钙,分析纯,天津市化工试剂一厂;石膏粉,天津市化工试剂一厂。
电动搅拌机 (ED 267,12V60W,郑州杜甫仪器厂),烘箱(DHG-9070A,上海一恒科技有限公司),三口瓶(250 mL),烧杯(1 000 mL)。
1.2 过氧尿素的制备方法
在250 mL三颈瓶中加入 30%的双氧水 50 mL,开动搅拌,加入 27 g颗粒状工业尿素和 0.6986 g六偏磷酸钠,水浴加热升温到 30℃左右时,物料溶解,再恒温搅拌 10 min。加入硫酸钙石膏粉或分析纯的硫酸钙 25.5 g,再恒温搅拌 10 min。在快速搅拌条件下,在冰水浴上冷却至5℃以下。立即抽滤,滤饼在空气中吹风干燥。
1.3 有效含氧量的测定原理
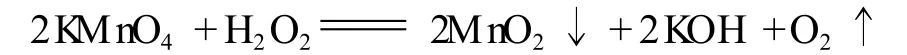
1.4 有效含氧量的测定方法
用浓度为 0.02016 mol/L的 K MnO4溶液 (用基准草酸钠标定的浓度)滴定样品,滴定时用 100 mL约 5%的稀 H2SO4调节酸度。有效含氧量用样品中含有的可放氧元素的质量百分比表示。
2 结果与讨论
数据见表1。
由表 1中表明:工业硫酸钙中的杂质离子对过氧尿素的热稳定性也有负面影响。杂质离子的存在,使尿素与过氧化氢之间的结合力减弱,很容易放出氧气。制备过氧尿素时,加入的稳定剂中如含有杂质(一般为阳离子),会使产品的产率和质量降低。在工业生产中,提高原料的利用率,除了原料配比和加入稳定剂以外,应除去体系中的杂质离子,并对原料和稳定剂进行水洗可以获得较满意的结果。
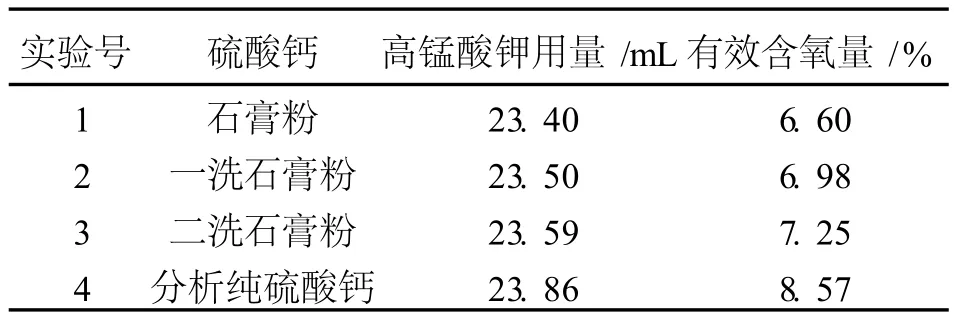
表1 实验结果
TQ441.41
A
1003-3467(2010)16-0055-01
2010-07-15
董彩霞(1968-),女,长期从事化学实验教学与研究,电话:(0371)68229079。
——过氧碳酸钠

