热电池正极材料的研究进展
苑晓宇 马伟民 闻雷 杨化仁
(1.沈阳大学机械工程学院,辽宁沈阳110044;2.沈阳化工大学材料科学与工程学院,辽宁沈阳110142;3.中国科学院金属研究所沈阳材料科学国家(联合)实验室,辽宁沈阳110016)
热电池正极材料的研究进展
苑晓宇1,2马伟民2闻雷3杨化仁1
(1.沈阳大学机械工程学院,辽宁沈阳110044;2.沈阳化工大学材料科学与工程学院,辽宁沈阳110142;3.中国科学院金属研究所沈阳材料科学国家(联合)实验室,辽宁沈阳110016)
热电池是20世纪40年代以后发展起来的一种新型高温能源电池,正极材料的发展在很大程度上决定了热电池性能的提高,研究与开发新型热电池正极材料是提高热电池性能的重要内容之一。本文主要介绍热电池的氧化物正极材料和硫化物正极材料及其合成方法和表征手段,比较了几种不同热电池正极材料的特性及存在的问题。简要叙述了在该领域的研究现状,展望并提出了不断探索新型热电池正极材料的趋势。
热电池,正极材料,CoS2,合成方法
1 引言
热电池是一种由碱金属为正极,金属盐为负极,以无机熔融盐作为电解质,利用自动激活机构点燃热源使电解质熔化,激活瞬间产生很高能量的一次储备电池,故又称为熔盐电池[1]。热电池起源于20世纪40年代,它是一种高温能源,它可在350~550℃温度下工作,而锂电池的工作温度仅为-20~60℃[2]。同时它还具有比功率大,比能量高,激活速度快,储存时间长,可靠性好,使用温度范围宽,不需维护等优点。目前,热电池已被广泛应用于高技术武器当中,如导弹、反导导弹、核武器、各种先进炸弹、炮弹、水雷以及一些作战武器的点火装置中[3-6],如俄罗斯SA-18便携式地空导弹(1985年开始服役),中国红箭-73和红箭-8导弹以及响尾蛇ATM-9L/M导弹(1956年开始服役)中均挂有热电池组点火。它还可应用在火箭的配套动力电源及军用引信电源[7]。此外,热电池在民用领域的应用中也已开始逐渐得到重视,现已有关于将其作为飞机的应急电源,地下高温探矿电源,火警电源的研究报道[8-9]。
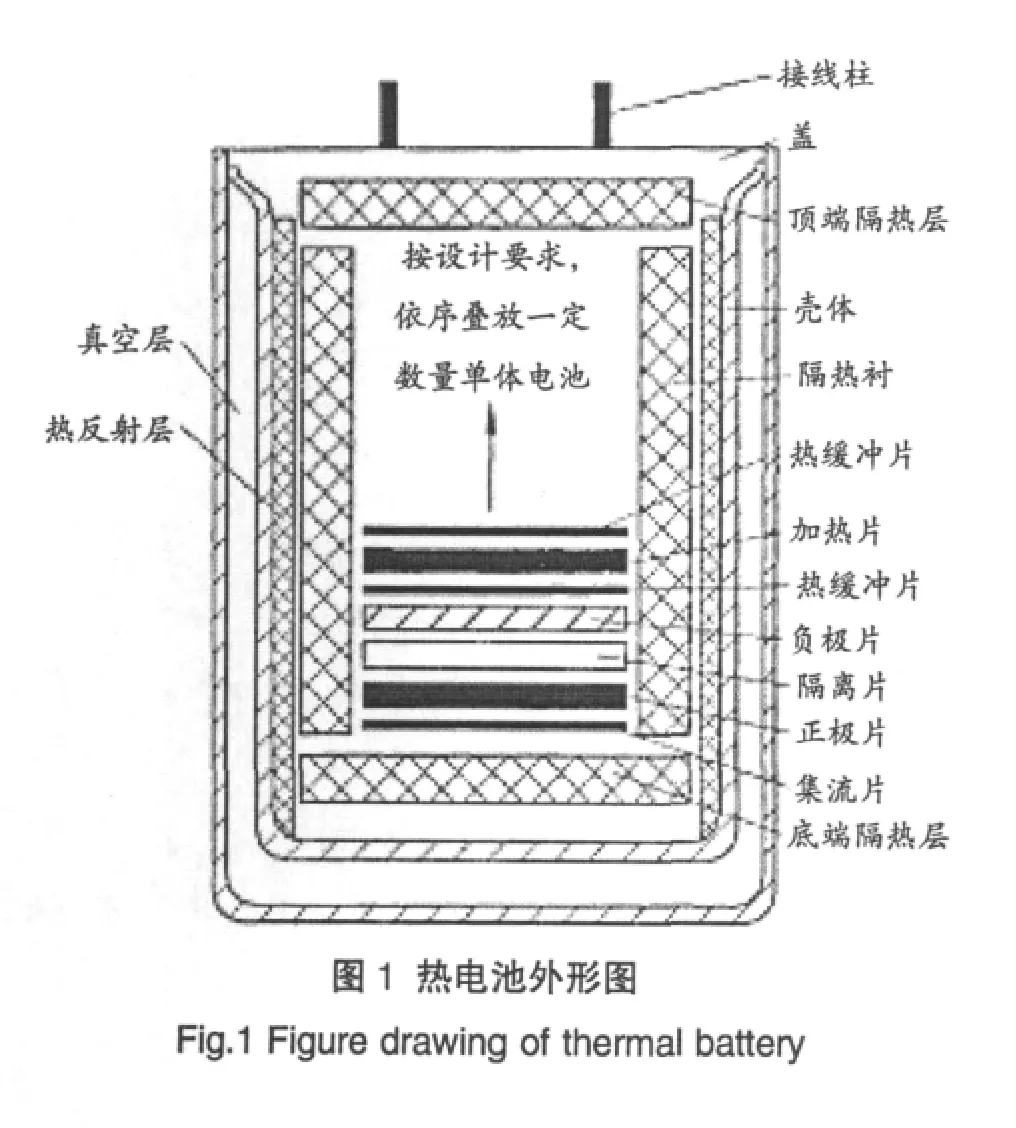
热电池根据使用负极材料的不同分为:镁系热电池、钙系热电池、锂系热电池等。热电池主要由基片、正极、负极、电解质、加热系统及保温材料组成,其中热电池的电极材料对热电池的电化学性能影响最为关键。图1[10]为热电池的外形图。理想的电极材料应具有以下一些特点:较高的工作电压,良好的热稳定性,较大的电池容量,导电性好,价格低廉。本文主要介绍热电池正极材料国内外的研究进展。
2 热电池的正极材料
作为热电池的正极材料,需具备以下一些特点[11]:(1)具有较高的电位,最好相对于锂要大于2V以上;(2)电子可导电,这样可大电流放电;(3)在600℃时可保持优良的热稳定性、化学稳定性及物理稳定性;(4)与电解质不发生反应;(5)生成的反应物能够导电或溶入电解质,以减小内阻。
原则上讲,具有氧化性的物质,如硫酸盐、氧化物、硫化物、铬酸盐、磷酸盐等均可作为热电池的正极材料,但所使用的正极材料要具有很好的性能,满足各种不同的设计要求,真正有价值的很少。
2.1 氧化物正极材料
过渡族金属的氧化物正极材料主要有V2O5、MnO2等,作为以钙、镁、锂合金为阴极的热电池正极活性物质。它具有较高的放电电压[1],但热稳定性较差,且高温时易脱氧,化学稳定性差,易于与卤化物电解质发生反应,电子的导电性差,容量较小[12]。过渡族氧化物一些单一的高价氧化物具有较高的峰值电压,但工作寿命和比能量明显降低,主要是因为放电电压下降过快。近年来锂化V2O5正极的研究越来越深入,研究发现锂化的氧化钒正极材料具有更高的电压和更好的热稳定性,但由于锂化的氧化钒正极材料的库仑比容量比较低,影响热电池的后期放电电压。
文献报道了[13]钒复合氧化物LVO研究的可行性,LVO的成分为LiV2O5+4VO2,当放电电流密度为400mA/cm2时,LVO的空载电压为2.43V,放电电压为2.32V,比同等条件下FeS2的电压高0.4V。
Clark[14]用溴化锂对VO2和VO5进行锂处理制成的锂化氧化钒作为热电池的正极材料,它的特点如下:(1)热稳定性好;(2)电极电位正极;(3)化学稳定性好。
刘效疆,陆瑞生[15]以锂化氧化钒为主,添加一定比例的二硫化铁制成复合的正极材料,其综合性能优于锂化的氧化钒和二硫化铁两种单一正极材料,将其应用于长寿命的热电池中,取得了很好的效果。
而李志友[16]则采用溶胶-凝胶法合成了锂嵌入式金属氧化物,结构稳定性好且具有高容量,放电电压平稳。但它会出现初始电压峰包及个别放电台阶的缺点。通过在合成时掺杂3.8%的Mo,可使其在500℃的放电电压提高0.3V,比容量提高300A·h/g,可解决上述缺点。
由图2(a)[16]看出,颗粒形状为棒状或条状,长端约10μm,短端约5μm;图2(b)中的颗粒形状与图2(a)中的颗粒形状一致,仍为棒状或条状,但尺寸稍小。随着Mo的适量掺杂使Li1+XV3O8的最高电压和比容量尤其是大电流放电时的比容量得到较大提高。
2.2 硫化物正极材料
金属硫化物正极材料主要分为一硫化物(如FeS、CuS等)和二硫化物(如FeS2、CoS2等),由于二硫化物较一硫化物有较高的电压,应用也较为广泛,故本文主要介绍二硫化物正极材料。过渡族金属硫化物是一类很好的热电池正极材料,通常采用较正电位的金属硫化物或盐类。用硫化物代替硫单质作为热电池的正极材料,可避免高温情况下硫蒸气逸散,同时也降低了生成多硫化物溶于电解质的发生。
2.2.1 FeS2正极材料
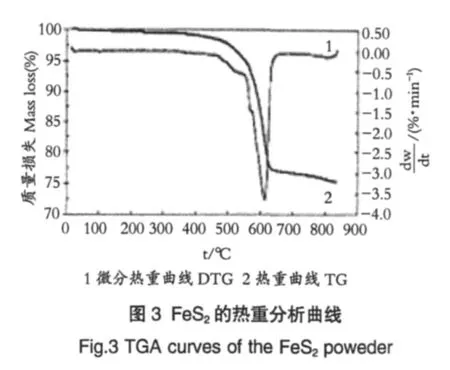
FeS2是目前应用最为广泛且技术较为成熟的与锂合金负极材料相匹配的热电池正极材料。FeS2可直接从黄铁矿中提取,资源丰富,电性能稳定,但这种正极材料制成的热电池有一个致命的缺点:它的工作温度在375~500℃,热电池放电初期电池内部的温度最高可达600℃,要满足电池的寿命长,首先要求电极材料在600℃时保持良好的热稳定性[17]。而FeS2在540℃[18]时会发生分解,最终导致温度失控,对电池极为不利。图3[18]为天然FeS2微分热重曲线及热重曲线,如图所示在样品质量为初始质量的95%时,分解温度约为540℃。
另外,使用FeS2作为热电池的正极材料,电池激活瞬间,每个单体电池会出现瞬间电压尖峰,这使电压平稳性下降,缩短了热电池工作寿命[19]。
为了解决FeS2的热稳定性问题,消除其产生的瞬间电压尖峰,目前最为有效的常规方法是采用Li2O等一些锂化剂对其进行锂化处理[1]。这样大大消除了热电池的初始电压尖峰并提高了电池寿命终结时的脉冲性能。Ming[20]则采用合成的纳米结构的FeS2作为热电池的正极,这样大大减小了热电池的体积,同时也大大提高了电极反应的速率以及热电池的利用率,从而显著提高了热电池的输出能量,其比能量高达109J/g,是常规FeS2电极的两倍,这为FeS2的应用指出了新的发展方向。一些学者[21]通过加入CoS2提高了正极的导电性,它与FeS2合成的Fe1-xCoxS2共混物作为热电池的正极取得了比单一成分材料更好的放电效果,而且Co/Fe的比例越高,放电时间越长。
2.2.2 CoS2正极材料
虽然FeS2具有很多的优点,价格低廉,放电容量大,低温性能优良,但是FeS2在温度超过540℃时会发生分解,热稳定性差,对电池极为不利,而CoS2的分解温度超过了725℃[22],对电池的长寿命较为有利。另外,要实现高功率特性,除了要求材料本身电化学极化小以外,还要求材料本身的电导率较高,以降低欧姆极化[17]。CoS2的电阻率为0.002Ω/cm,远远低于FeS2的电阻率17.7Ω/cm[23],它更有利于降低电极的欧姆极化,从而限制了FeS2在高温条件下的应用,各国学者正努力寻找FeS2的替代品。从目前发展来看,CoS2无疑将是一种较为理想的正极材料。世界上许多国家都对CoS2进行过研究,早在1995年,美国克利夫兰空军系统的Northrop Grumman公司就已经发现了CoS2这种新型的正极材料。CoS2本身具有电导率高,开路时在熔盐中化学稳定性好,热稳定性好,分解温度高,耐酸碱等优点。孙淑洋[17]采用CoS2正极材料制作的热电池,其内阻比FeS2的内阻降低了40%左右,其大电流放电、开路搁置等性能明显优于FeS2体系,放电容量却与FeS2相当。我们于20世纪90年代末开始对CoS2进行实验,到目前为止,我们已经成功将其应用在了热电池的研制上,用CoS2制作的热电池样品比能量高达52wh/L(21wh/kg),其恒流放电电流密度为0.8A/cm2,脉冲电流密度为1.6 A/cm2。CoS2有很大的研究价值,但自然界中没有CoS2晶体矿,必须人工合成CoS2晶体,通常采用化学方法制备出的CoS2大多是无定型的,因此CoS2的晶化问题就显得尤为重要。如钱逸泰等人[24]利用溶剂热法由无水氯化钴和三硫化二钠反应得到了黄铁矿结构的CoS2纳米粉体;张玲等人[25]利用晶种诱导水热合成了CoS2粉体;王明旭等人[26]利用溶剂热法由六水合氯化钴与九水合硫化钠制备出CoS2纳米粉体;另外,还可真空高温固化合成CoS2,但目前的制备方法中有一个共同的缺点:第一,必须在耐高压的密闭容器中进行,反应过程中的可控性较差,危险性较大;第二:制备的成本较高,国内尚无工业化产品,而国外也只有极少数几家公司生产,且价格较高。

2.3 硫酸盐正极材料
硫酸盐正极材料常应用于钙系热电池中。以硫酸铅为例,经X射线衍射分析证明,硫酸铅为白色单斜或斜方晶形晶体,相对密度6.2,熔点1170℃,难溶于水,有毒。
作为热电池的正极材料,其电化学反应式[11]为:

理论容量为0.177A·h/g。
2.4 铬酸盐正极材料
铬酸盐也应用于钙系热电池中。以铬酸钙为例,CaCrO4为黄色晶体,属四方晶系,在800℃以上发生分解。通常CaCrO4与LiCl-KCl电解质混合成正极活性物质,CaCrO4在LiCl-KCl熔盐电解质中呈现出很强的氧化性,其在热电池中的电化学反应式[11]为:
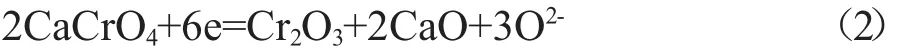
生成的不溶性还原产物对所有的水溶液都有很强的抗腐蚀性,还能抵抗电化学的再氧化对电池性能造成不良的影响。
2.5 氯化物正极材料
金属氯化物(如NiCl2、FeCl3等)是可替代二硫化铁较为理想的正极材料之一,具有较高的开路电压,理论容量高,放电电流密度大,电极电位较正。以它作为热电池的正极材料,已研制出容量大,功率大,寿命长的实用热电池,展现出了十分良好的前景。以NiCl2为例,它的稳定性好,具有优良的电化学性能,在熔盐中的电极电位很正,700℃时,在氯化物熔盐电解质中的电极电位为2.36V。但氯化物稳态放电电压较低,激活时间较长,电阻较高,技术仍不成熟,要同时输出大功率密度和能量密度仍然存在困难。赵晶[27]通过在氯化镍中添加20%的羰基镍粉对热电池放电初期激活时间起到一定改善作用。
3 常用的合成方法
热电池正极材料的电化学性能严格地受原料及制备技术的影响,为了获得性能更优异的正极材料,人们不断探索合成正极材料的技术。目前,正极材料的制备方法很多,通常采用固相合成法、水热法、溶剂热法等。
3.1 固相合成法(Solid-state reaction method)
固相合成是将固体原料按一定比例混合均匀,各原料之间处于充分接触的状态,在设定的温度下,焙烧一定时间,冷却至室温,粉碎筛分制得陶瓷粉体的一种制备方法。根据焙烧的温度不同,把焙烧在400℃以上者称为高温固相法,低于400℃焙烧者称为低温固相法。
固相法合成热电池正极材料主要有两个过程:配料和焙烧。以硫化物为例,基本步骤如下:将高纯粉体研磨并充分混合均匀,可以增大反应物之间的接触面积,使原子或离子的扩散运输比较容易进行,以增大反应速度。然后将粉末放入高温容器内进行焙烧,培烧过程的主要作用是使原料各组份间发生化学反应,形成具有一定晶格结构的基质,并且激活进入基质,焙烧的条件直接影响正极材料的电化学性能。目前有一种常压体系合成高纯二硫化钴粉末的方法[28],该方法可以得到纯度高于99%的二硫化钴粉末。另有研究人员采用钴或铁的硫酸盐,使用H2S作为硫源来制备硫化物正极材料[29]。
该方法得到的正极材料纯度较高,其电化学性能优良,但反应时间长(保温2小时以上),设备要求高,能耗高,所得产物为块状,硬度大。要得到可以应用的粉末状产品需要采用机械手段进行细化,即进行球磨,而在此过程中易引入杂质,既耗时又耗能,纯度也下降很多,严重影响了正极材料的电化学性能。
3.2 水热法(Hydrothermal method)
水热法是通过原料化合物与水在高压釜内一定温度和压力下进行的反应,并合成化合物的一种粉体制备方法。它属于湿化学方法的一种。近几年来,水热法在合成热电池正极材料中取得了很大的进展。
采用水热法制备热电池正极材料是在特制的密闭反应容器(高压反应釜)中进行,采用水溶液作为反应介质,水作为传递压力的媒介,同时在高压下,绝大多数的反应物均能部分溶解于水,促进了反应在液相或气相中进行。张玲[25]采用晶种诱导水热法制备了黄铁矿型的二硫化钴(如图4),样品晶格常数a=5.5343Å,晶粒形貌呈均匀的八面体结构[26]。
采用水热法合成的正极材料一般结晶度高,并且通过优化合成条件,可以不含有任何结晶水,粉末的大小、均匀性、形状,成分可以得到严格地控制。同时它省略了煅烧的过程,从而也省略了研磨的过程,使制得的正极材料纯度提高,晶体缺陷的密度降低,这对材料的电化学性能也起了很大的作用。但水热法只适用于实验室少量的粉体制备,若要扩大其制备量,受到很多的限制,特别是大型的耐高温高压反应釜的设计制造难度大,造价高,推广较为困难。
溶剂热法是指将反应物按一定比例放入密封的压力容器(高压反应釜)中,以有机溶剂作为介质,在高温高压的条件下进行的化学反应制得粉体的一种方法。这种方法在合成热电池正极材料应用非常广泛,王明旭等人采用溶剂热法成功合成了CoS2纳米粉体[26]。
溶剂处在高于其临界点的温度和压力下,可以溶解绝大多数物质,从而使常规条件下不能发生的反应可以进行,或加速进行。在合成正极材料时选择溶剂需要非常注意,溶剂在反应过程中控制晶体的生长,使用不同的溶剂可以得到不同形貌的产品,因此电化学性能也不同。

3.3 溶胶-凝胶(Sol-gel method)
溶胶-凝胶技术实际上是共沉淀法的一个分支,一种湿化学合成方法。它是将较低粘度的先驱体均匀的混合,制成均匀的溶胶,通过金属离子水解和凝聚作用,沉淀成胶体颗粒,经干燥成干凝胶,把干凝胶于给定的温度下焙烧得到合适的物相。
溶胶-凝胶法合成热电池正极材料的基本过程是:将金属醇盐和无机盐或其它有机盐溶解在水或其他有机溶剂中,溶质与溶剂产生水解、醇解或螯合反应形成溶胶,然后使溶胶凝胶化,再经过干燥、焙烧等过程最终得到产品。李志友等人[31]采用溶胶-凝胶法合成了LiV3O8。
采用溶胶-凝胶法合成的正极材料粒度可以达到微米级甚至更细,且均匀性较好,纯度较高,制得的正极材料高温放电性能较好。同传统的固相合成相比,它具有较低的合成及烧结温度。溶胶-凝胶技术所需设备简单,制备过程易于控制,但是溶胶-凝胶法的合成周期比较长,工业化生产的难度大。
3.4 喷雾干燥法(Spray drying method)
喷雾干燥法是将原料混合,然后加入聚合物支撑体,再进行喷雾干燥,这种方法制备得到的前驱体结晶度低,不能直接用作热电池的正极材料,但将前驱体进行高温处理后所得的正极材料性能较好。有研究人员[32]采用了热喷涂的方法直接地将黄铁矿沉积在不锈钢集流板上,形成了一层高纯的FeS2薄膜作为热电池的正极材料,这种材料即使在400~550℃的温度范围内也可获得恒定的放电电流,避免了FeS2在放电时的分解。
3.5 熔盐电解法(Molten-salt electrolysis method)
熔盐电解法[11]是利用电能加热并转换为化学能,将某些金属的盐类熔融并作为电解质进行电解,以提取或提纯金属的冶金过程。可以采用LiCl-KCl低共溶物作为电解质,CoS作负极,Al或石墨作正极,在325℃~500℃时进行电解,在阳极可生成CoS2,经适当分离后可得到纯净物,但负极电解电压不能过高。此方法可适用于正极材料CoS2的大量生产。
4 热电池正极材料的展望
热电池主要应用于当今高新技术武器中,日益发展的现代化武器对热电池也提出了更高的性能和使用的要求:一是进一步提高热电池的性能,如比功率、比能量、激活时间、热稳定性、化学稳定性等;二是进一步提高热电池的使用寿命;三是减小热电池的体积及质量;四是要求热电池具有较短的激活时间。
这就对热电池的组成材料提出了更高的要求,尤其是对热电池的正极材料,近些年来,对热电池正极材料的开发、应用和研究都有了长足的进步,但仍存在不少问题亟待解决。综合了热电池正极材料的现状研究,我们要进一步做以下工作:(1)进一步优化正极材料的制备技术,不断尝试新的制备方法,克服以往制备方法的不足;(2)不断探索新的热电池的正极材料,以满足日益增长的需求;(3)优化现有热电池正极材料,使其具有更优良的性能;(4)不断探索对环境污染小,价格低廉的正极材料。
1许小静,段柏华,曲选辉等.热电池电极材料的研究进展.稀有金属与硬质合金,2006,34(3):55
2马荣骏.锂离子电池及其正极材料的研究进展.有色金属, 2008,60(1):1
3 Linden D,et al.Handbook of Batteries (3rd edition).USA: McGnaw-Hill,2002
4 Wells J,et al.Thermal battery performance demonstration for advanced tactical and strategic application.Proceedings of the 34th International Power Sources Symposium,IEEE,1990:156
5武器系统最佳电源--热电池.新季刊,1982,10(4):146~151
6安德宇.弹上电源系统测试技术研究.航空兵器.2006,10(5): 30~33
7赵广波,徐莹,汴纪庆等.热电池技术进展及在引信中的应用.探测与控制学报,2008,30(6):64~68
8 Kaufmann S,et al.Thermal battery for aircraft emergency power.IEEE,1992:227
9侯满义等.热电池作为飞机应急系统电源应用研究.火工品, 2003,(1):33
10高俊丽,蒋立.热电池技术发展评述.第九届中国宇航学会空间能源学术年会,2005:375~383
11陆瑞生,刘效疆.热电池.北京:国防工业出版社,2005
12高俊奎,黄来和.现代热电池电极材料现状及展望.电源技术, 2009,9(6):25
13赵宝兴,皇诚德,董树本等.钒复合氧化物作热电池正极材料的可行性研究.电源技术,2006,5(5):398~402
14 ClarkAJ,etal.Lithiatedvanadiumoxide(LVO)andvanadium dioxides(VO2)as thermal battery cathode materials.In:The 19th International Power Sources Symposium.Crowborough, UK:Int.Power Sources Symposium Committee,1995:488
15刘效疆,陆瑞生.锂化的氧化钒阴极材料的研究.电源技术, 2002,2:26~28
16曹笃盟,李志友,周科朝.掺杂Mo对Li1+XV2O3物象和高温阴极放电性能的影响.中南大学学报,2005,36(5):766
17孙淑洋,刘延东,曹军记等.二硫化钴作高功率热电池正极材料的研究.电源技术,2003,27(1):28~30
18种晋,曹军记,赵晋峰等.热电池正极材料.电源技术,2004,7 (7):419~422
19何德军,刘鸿雁.导弹主电源技术的发展.兵器材料科学与工程,2009,32(1):93~96
20 Ming Au.Nanostructured thermal batteries with high power density.Journal of Power Sources,2003,115(2):360
21 Awano A,et al.Li/Fe1-xCoxS2system thermal battery performance.IEEE,1992:219
22 Briscoe J D.An improved thermal battery for military applications.Proceedings of the Power Sources Conference, 1998,38:235~239
23 Dallek S,Murphy T C and Nguyen T.Evaluation of transition -metal-sulfidecathodematerialsforthermal battery.Proc.36th Power Sources Conf.,1994,36:329~332
24 Qian X F,Zhang X M,Qian Y T,et al.Journal of Alloys and Compounds,1998,278:110~112
25张玲,郑毓峰,孙言飞等.晶种诱导水热合成二硫化钴CoS2粉体.四川大学学报,2005,42(2):197~199
26王明旭,岳光辉,耿中荣等.溶剂热法合成CoS2纳米粉体.人工晶体学报,2007,36(3):650~652
27赵晶.热电池正极材料氯化镍的性能研究.电源技术, 2006,30(8):665~667
28李明,唐威.常温体系合成高纯二硫化钴粉末的方法.中国专利:03156711,2005:2~4
29刘杰,种晋,高文明.热电池硫化物正极材料制备研究进展.电源技术,2009,33(2):148~151
30李志友,黄伯云,汤春峰等.LiV3O8的溶胶凝胶法合成及500℃阴极放电性质.功能材料,2001,32(2):181~183
31张玲,郑毓峰,孙言飞等.晶种诱导水热合成二硫化钴CoS2粉体及结构精修.新疆大学学报,2006,23(1):47~52
32 Patrick J.Masset,Ronald A.Guidotti.Thermal activated ("thermal")battery technology PartⅢ a:FeS2cathode material.Journal of Power Sources,2008,177:595~609
33王明旭,岳光辉,耿中荣等.溶剂热法合成CoS2纳米粉体.人工晶体学报,2007,36(3):650~652
34董静,种晋.影响热电池用矿物二硫化铁热稳定性的因素.电源技术,2008,32(3):147~150
35黄思玉,刘心宇,种晋等.黄铁矿薄膜电极在热电池中的应用.电源技术,2006,30(7):574~575
Abstract
Thermal battery is a new kind of high temperature power battery developed after 1940s,and its enhanced performance owes considerably to cathode material.The study and development of new cathode materials for thermal battery is of importance to improving the performance of thermal battery.In this paper,the oxides and sulfides used as cathode materials are introduced,and their synthetic methods and characterization means are reviewed.Characteristics and existing problems of different thermal battery cathode materials are compared,and the research actuality and prospects of new thermal battery cathode materials are described.
Keywords thermal battery,cathode material,CoS2,synthetic method
RESEARCH PROGRESS OF THERMAL BATTERY CATHODE MATERIALS
Yuan Xiaoyu1,2Ma Weimin1Wen Lei3Yang Huaren2
(1.College of Mechanical Engineering,Shenyang University,Shenyang Liaoning 110044,China;2.School of Material ScienceandEngineering,ShenyangUniversity of Chemical Technology,Shenyang Liaoning 110142,China;3.Shenyang National Laboratory for MaterialsScience,Metal Research Institute,Chinese Sciences Academy,Shenyang Liaoning 110016,China)
TQ174.75
A
1000-2278(2010)04-0663-07
2010-05-30
辽宁省教育厅重点实验室项目(编号:20008S181);辽宁省科技计划项目(编号:2008224001);沈阳市科技计划项目(编号:1081236-1-00)
马伟民,E-mail:maweimin56@163.com

