壳聚糖接枝胍乙酸缓蚀剂的研究
曾 涵,胡 鑫,孙向涛,杜军刚
1新疆师范大学生命科学与化学学院,乌鲁木齐 830054;2新疆大学化学系,乌鲁木齐 830000
壳聚糖接枝胍乙酸缓蚀剂的研究
曾 涵1*,胡 鑫1,孙向涛2,杜军刚1
1新疆师范大学生命科学与化学学院,乌鲁木齐 830054;2新疆大学化学系,乌鲁木齐 830000
本文以 1-氯胍乙酸和自制壳聚糖为原料,合成了一种良好的酸洗缓蚀剂-胍乙酸壳聚糖。以失重法研究了其对N80碳钢的缓蚀性能,并以交流阻抗谱研究了其在N80钢表面的吸附行为,得出缓蚀剂分子在N80钢表面吸附满足 Langmuir模式,同时算出了其吸附热。本文还采用色谱-质谱联用仪研究了缓蚀剂在酸中的降解规律,分析了其较长时间维持较高缓蚀作用的机理。
天然高分子;酸缓蚀剂;长效缓蚀
添加缓蚀剂是一种工艺简便、成本低廉、适用性强的腐蚀控制方法[1]。目前主流的有机缓蚀剂虽然使用效果较好,毒性低,但它们的分子量单一,使用量大,不容易降解,投药后缓蚀效果持续时间短,使用的性价比低。近些年来国内外学者指出[2]:今后研究的重点是探索从各种天然动植物中,提取、分离、加工其中的有效成分并进行改性,制备绿色缓蚀剂以实现资源的优化利用。目前天然产物及其改性物在金属防腐方面的应用已有文献报道[3],但它们都存在着使用温度范围窄,使用量大,溶解度不够高(特别是直接施放于弱酸性或水介质中时),长效缓蚀性能欠缺。因此对天然高分子进行进一步的结构修饰使其更好地满足实际需要成为当务之急。
本文研究了以甲壳素为原料生产壳聚糖并且以胍乙酸接枝壳聚糖的工艺,得到了一种对 N80钢具有良好缓蚀效果的改性天然高分子可降解长效缓蚀剂-胍乙酸壳聚糖 (GAAC)。它与其他含氮杂环缓蚀剂相比[4],具有以下优势:原料来源广泛,成本低廉;使用时投药量较低,缓蚀剂可生物降解,对环境无污染;投药后缓蚀效果持续时间较长。在此基础上还通过交流阻抗谱证实此缓蚀剂分子在金属表面的吸附满足LANG MU I R等温吸附模式,具有较高的吸附能,在腐蚀介质中可适用的温度范围较宽。
1 实验部分
1.1 仪器及材料
自制壳聚糖,1-氯胍乙酸,氢氧化钠,盐酸,草酸,高锰酸钾,二氯甲烷,丙酮,无水硫酸钠,甲醛,冰乙酸(均为AR)。
WP-750A型微波炉;WNZK-01温度控制仪; NDJ-1型旋转式粘度计;数字式电子天平 (梅特勒公司生产);CH I660B型电化学工作站;红外光谱仪(德国 BRUKEREQU INDX-55型 ),JEOLJNM-ECP600M型核磁共振仪;1100series LC/S MSD Trap SL型高效液相色谱-质谱联用仪 (包括四元泵;在线真空脱气机;柱温箱;自动进样器及大气压化学电离源(APCI,美国 Agilent公司);全玻璃溶剂过滤器(美国WATERS公司);HGC-24型氮吹仪 (天津恒奥科技有限公司);M ILL I-Q纯水系统 (美国M ILL IPORE公司)。
1.2 实验方法
1.2.1 壳聚糖的制备
将虾壳经过水洗后,用 2 mol/L氢氧化钠溶液经微波处理后,冷至室温浸泡 12 h后,以除去虾壳中的蛋白质,水洗至中性,再用 2 mol/L盐酸溶液在室温下浸泡24 h,使碳酸钙转化为氯化钙,用水洗至中性,干燥,粉碎后,加入 2%的高锰酸钾溶液,浸泡1 h脱色,水洗后以 60%~70%草酸处理 20 min,可得白色片状结晶甲壳素。
将甲壳素在 35%的氢氧化钠溶液中以微波处理,温度保持在 90~100℃,处理 12 h后完成脱乙酰基操作,脱乙酰基后的壳质加 2%稀醋酸后可溶解,过滤去除杂质后,滤液加入碱即可析出壳聚糖。
1.2.2 合成胍乙酸壳聚糖
称取约 3.8 g干燥壳聚糖固体,加入 10 mL质量分数为 50%的 NaOH溶液碱化,再依次加入约 20 mL异丙醇及 1-氯胍乙酸约 3 g,室温反应 2 h,并不时搅拌,壳聚糖固体缓慢溶解,然后加热 (60~70℃)反应 2 h,继续搅拌,冷却至室温 (约 30 min),加无水冰醋酸调至中性,有白色粘稠状固体生成,充分搅拌,加无水乙醚搅拌,抽滤,于 80℃烘箱干燥,研碎,得胍乙酸壳聚糖,白色或灰白色粉末 (若用盐酸保护胍基,所得胍乙酸壳聚糖呈白色或灰白色,发亮,片状,晶体)。
1.2.3 缓蚀剂对N80钢缓蚀性能的测试
采用静态失重法测试了合成化合物的缓蚀性能。钢片经过打磨,除油,脱脂,吹干后置于干燥器中,称重后使用。试片浸入待测体系中,密封。恒温24 h后,取出试片,用滤纸轻轻擦拭,再用水,无水乙醇,丙酮依次擦洗,冷风吹干后称重。依式 (1.1)计算缓蚀剂的缓蚀效率:
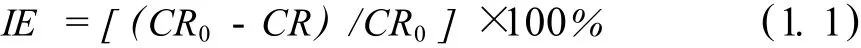
式中,CR0为未加缓蚀剂时 N80钢的腐蚀速率, CR为加入缓蚀剂后N80钢的腐蚀速率。
1.2.4 缓蚀剂分子在N80钢表面吸附行为的研究
采用电化学法研究缓蚀剂分子在 N80钢表面的吸附行为。电化学法采用三电极体系:研究电极由 N80钢片加工而得,除电极工作面 (0.24 cm2)外,其余部分均用环氧树脂密封。大面积铂电极为辅助电极,饱和甘汞电极 (SCE)为参比电极。使用前,工作电极经过用 260#砂纸抛光,除油,脱脂,用蒸馏水洗净吹干后置于温度恒定的待测溶液中 (含或不含缓蚀剂),测试温度:(28±1)℃。待自腐蚀电位 (EC)稳定后 (电化学阻抗谱 EISΔEC<5 mV),继续浸泡 4 h进行测试,测试所得的电位均为相对于 SCE的值。电化学阻抗谱的频率测试范围为 10-1~105Hz,交流激励信号幅值为 5 mV。阻抗数据采用 EQU IVCRT软件拟合处理。
由于缓蚀剂的缓蚀作用是通过在电极表面的吸附而实现的。按Langmuir吸附等温规律,在一定条件下缓蚀剂在电极表面的覆盖度θ与介质中缓蚀剂的活度间的关系可表示为:

式中,θ为覆盖度,Ka为吸附平衡常数,a为溶液中的缓蚀剂的活度 (浓度极低时以浓度代替)。而θ又可由双电层电容求得:

式中,和分别为添加缓蚀剂前后的界面电容,为电极表面完全被缓蚀剂所覆盖时的界面电容。对于一给定体系,(-)应为一定值,故令λ=(-),且令ΔCd=(-Cd),代入式(1.3),并与式 (1.2)联立,而且考虑到缓蚀剂浓度很低时,浓度C与活度a近似相等,整理后可得:
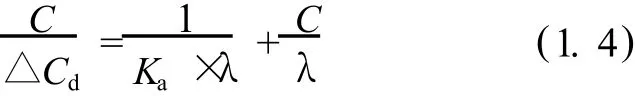
利用交流阻抗谱解析结果,计算出C/ΔCd值,并对C作图,从而可以求出其在N80钢电极表面的标准吸附自由能ΔGa。可以根据前述方法求出 1/ λ,1/Kaλ,θ。再由交流阻抗谱经过拟合后的数据计算出不同温度下的 1/λ,1/Kaλ,θ,ΔGa。其中ΔGa的计算公式如下:

而按照下面给出的公式可以算出缓蚀剂在金属表面的吸附热ΔHa。
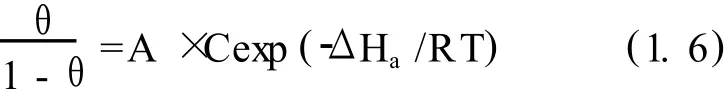
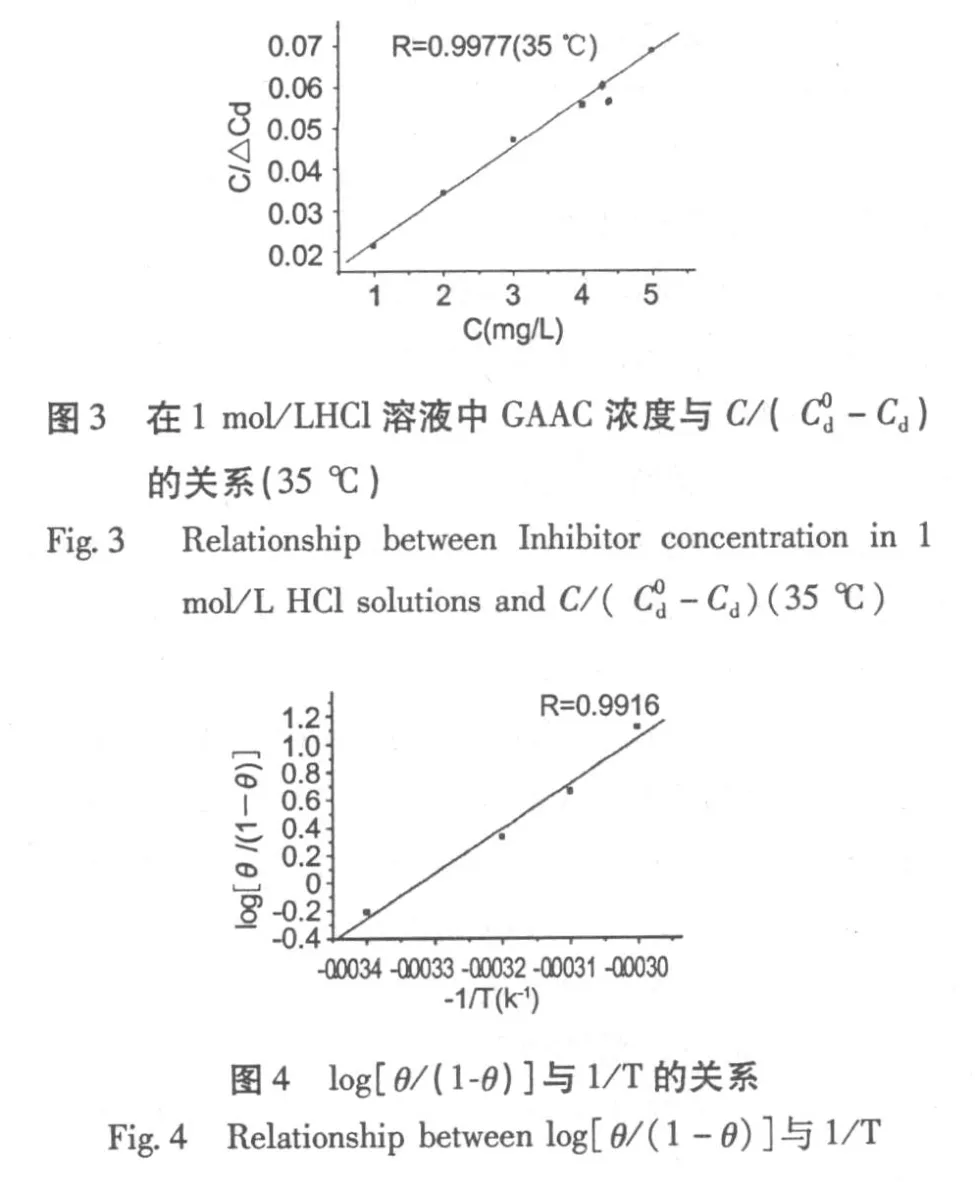
以 log[θ/(1-θ)]对 1/T作图,从线性拟合所得的斜率即可求出该化合物在 N80钢表面的吸附热。
1.2.5 缓蚀剂在酸中降解行为的研究
先使用 NDJ-01型旋转粘度计测定用 1 mol/L HCl配制的质量分数为 0.5%的缓蚀剂溶液的相对粘度(相对于水),并将之与对应的时间作图以表征两者之间的变化关系。
为进一步研究降解规律,本文采用色谱-质谱联用仪,对 1 mol/L HCl中溶解药剂 GAAC后的组分及在酸中存放一个月后的组分进行鉴定分析。在 1 mol/L HCl中加入药剂 GAAC配制成浓度为 50 mg/ L的酸溶液,样品 1为 30℃下存放一个月后的酸溶液,样品 2为当天配制的酸溶液。取样品 1及样品2各 150 mL以二氯甲烷进行萃取,将萃取所得的二氯甲烷以无水硫酸钠进行脱水处理和蒸馏处理以脱除二氯甲烷,得萃取的抽提物,再对萃取产物进行色谱-质谱联用仪分析。色谱条件:色谱柱 XDB-C18柱 (150 mm×4.6 mm i.d 5μm,美国Agilent公司),预柱 XDB-C18柱(150 mm×4.6 mm i.d 5μm,美国Agilent公司);0.05%醋酸-醋酸铵溶液 /甲醇为流动相 (25:75,V/V);流速:600μL/min柱温:35℃;进样量:20.0μL;质谱条件:APCI离子化模式:负离子;扫描范围 (m/z):150~500,毛细管电压:3.5 kV,毛细管出口电压-130V,电晕针电流:4.0μA,干燥温度:325℃,干燥气流速:5.0 L/min,雾化温度: 440℃,喷雾器压力:65.0 psi,延迟时间:200 ms,定量模式:选择粒子监测 (S M),内标:m/z[M-H2+ CH3COOH-H]-419.2。
2 结果与讨论
2.1 脱蛋白质与脱乙酰度的测定
用 PHS-25型 PH计进行测定,采用文献[4]所描述的甲醛滴定氨基氮法。甲醛可以与氨基酸的氨基相互作用,使滴定终点至 9.0左右,R-NH2+2HCHO→R-N(CH2OH)2,脱蛋白液中氨基氮含量测定如下:微波脱蛋白液中氨基氮含量为 1.642 mg/mL。
用DDS-L型电导率仪进行测量,以电导率仪的读数为纵坐标,氢氧化钠溶液的消耗量 (体积:毫升)为横坐标作图,通过一阶,二阶微分图求拐点,按文献[5]给定方法求出壳聚糖的脱乙酰度,测定结果如图 1。
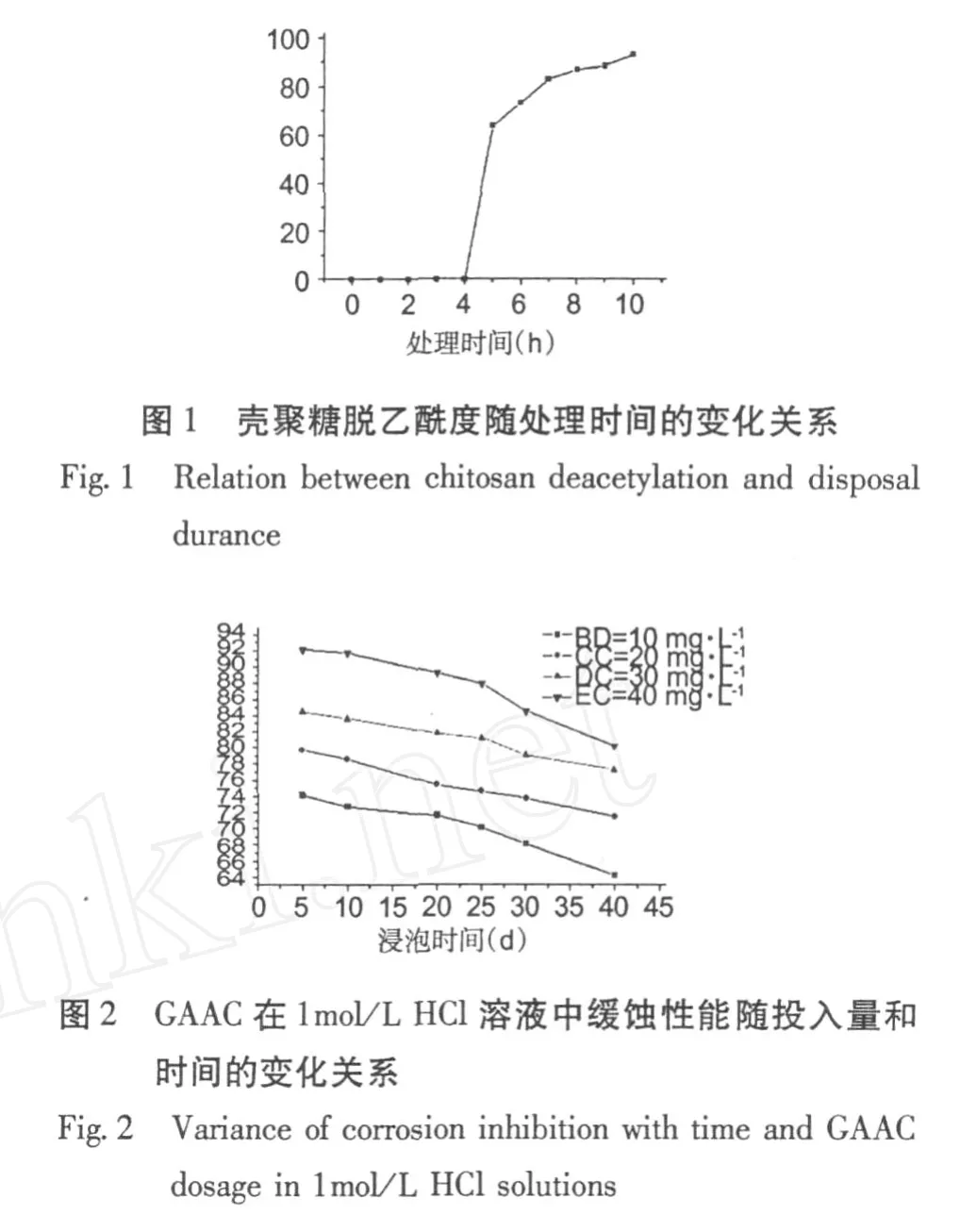
由图 1可以明显地看出:在开始的一段时间内,反应很慢,乙酰基没有被脱除;而随着处理时间延长,脱乙酰度越高,10 h以后可以认为甲壳素上的乙酰基已经全部被脱除。
2.2 特性粘度及分子量的测定
将干燥试样溶解于 0.1 mol/L NaCl溶液中,样品浓度为 0.053 g/mL。使用 NDJ-1型旋转式粘度计,按一点法进行特性粘度的测定 (此时温度恒定为 30℃)。测得胍乙酸壳聚糖的粘度为 292 m Pa·s,在此温度下用文献[6]所给方法计算其分子量,可得分子量为 4282。
2.3 GAAC的结构分析
将GAAC粉末(60目)与KBr压片,在BRUKER红外光谱仪上扫描。所得结果如下:IRvKBr max cm-1:3480(N-H),1425,1620.85(COO-),1560(guanyl),924(sugar ring,C1-H)。将 GAAC做 NMR分析,所选用溶剂为 D2O,所得结果如下:3.4~4.2 (m,5H,sugar ring2,3,4,5,6-H);4.46~5.06(m, 3H,sugar ring-OH);9.70(d,J=9.0 Hz,1H,NH); 4.56(t,J=9.3 Hz,1H,sugar C1-H)。
2.4 药剂的长效缓蚀性能
在1 mol/L HCl溶液中,加入不同剂量的 G AAC,测定它们在不同时间的缓蚀效率,测定结果如图 2。实验条件:测试温度 35℃。从图 2结果可知,不同浓度的药剂在盐酸溶液中均具有较好的缓蚀效能,在一个半月内均可保持较为良好的缓蚀效果,证实合成的缓蚀剂的确具有持久的缓蚀效能。
2.5 GAAC分子在N80钢表面的吸附行为
利用 EIS图谱解析结果,计算出C/△Cd值,并对C作图,示于图 3。通过图 3,可以看出该种缓蚀剂 35℃时在电极表面的吸附在测试的浓度范围内满足Langmuir等温吸附规律,从而可以求出其在N80钢电极表面的标准吸附自由能ΔGa。可以根据前述方法求出 1/λ,1/Kaλ,θ,CSd。其中ΔGa的计算公式如下:

而按照(2.2)给出的公式可以算出缓蚀剂在金属表面的吸附热ΔHa。
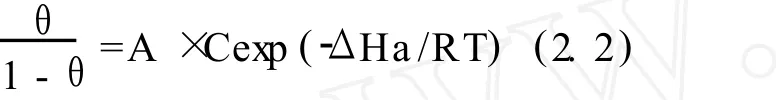
以 log[θ/(1-θ)]对 1/T作图,可得图 4。从线性拟合所得的斜率即可求出该化合物在 N80钢表面的吸附热为 26.91 kJ/mol,从吸附热数据和图 4中相同缓蚀剂浓度条件下温度对吸附自由能的影响两个方面综合考虑,此缓蚀剂在金属表面的吸附应以化学吸附为主。
2.6 药剂在酸中的降解规律

图 5 GAAC在 1 mol/LHCl溶液中相对粘度随时间的变化关系Fig.5 Variance of the relative viscosity with time of GAAC in 1 mol/L HCl solutions
天然高分子甲壳素改性后的缓蚀剂 GAAC在盐酸溶液中不可避免地会发生酸降解作用,使水溶性高分子降解为中低分子量的组分。现以图 5表示1 mol/L HCl溶液配制的一定质量百分数 (0.5%)的 GAAC溶液相对粘度 (相对于水的粘度)与时间的变化关系。
色谱-质谱联用仪的分析结果如下:为计算简便,对色谱图中的波峰直接采用面积归一化进行近似定量分析,使用质谱对降解产生的化学物质进行鉴别,分析结果如表 1所示。
由表 1可以看出,样品 1的低分子量组分浓度高,而样品 2的高分子量组分浓度较高。这与图 5一样,都证明随着时间延长,高分子量的组分逐渐降解为小分子量的组分。由于表 1中不能给出分子量超过 500的组分含量结果,分子量小于 500的组分经降解后则可被检测出,故样品 1的检出总量高于样品 2。
多数具有缓蚀作用的分子都含有未成对电子的N,P,S等杂原子,而从表 1还可以看出,就检出的含氮化合物的组分总量来看,样品 1高于样品 2,特别是低分子量的组分,样品 1的含量明显高于后者。这是药剂在酸中积存较长时间 (一个月)后仍然具有较好的缓蚀性能的主要原因。
3 结论
以自制壳聚糖 (脱乙酰度较高)与 1-氯胍乙酸为原料合成了胍乙酸壳聚糖,并且对其结构进行了表征,由于胍基的加入,使此化合物与壳聚糖相比,亲水性有所增强。
该天然高分子改性后产品对 N80钢有较好的长效缓蚀性能。在实验浓度范围内 GAAC分子在
N80钢表面上的吸附满足Langmuir等温吸附规律。由于放置较长时间后,GAAC降解产物中仍然含有相当高含量的含氮小分子组份,所以具有良好的长效缓蚀效能。

表 1 样品 1和样品 2的高效液相-质谱联用仪分析结果Table 1 Results from the analysis on HPLC-MS of sample 1 and sample 2
1 Li YT(李言涛),Hou BR(侯保荣),et al.Progress on natural environmental friendly corrosion inhibitors for metals.Corro Sci&Pro Tech(腐蚀科学与防护技术),2006,18: 37-40.
2 Wang XJ(汪晓军),Xiao J(肖锦).An acid corrosion inhibitor based on grafting natural polymer with quarternary pyridine salt.M od Chem-Eng(现代化工),1998,4:23-25.
3 Minha A.The effect aqueous extracts of some leaves and fruit-peels on the corrosion of steel in acid.Corro Prev&cont,1999,4:32-36.
4 ZhangWQ(张文清).The application on cosmetics of chitosan and its derivatives.Poly Bull(高分子通报),1999,2: 73-76.
5 Wu ZJ(吴仲几),Experiment of Food Chemistry(食品化学实验).Guangzhou:The Press of Jinan University,1995.85-88.
6 Feng KC(冯开才),Li G(李谷),Fu RW(符若文),et al. Experiment of Polymer Physics(高分子物理实验).Beijing: Chemistry Industry Press,2004.12-16.
An Inhibitor of Corrosion Based on Grafting Natural Polymer with Guan idine Acetic Acid
ZENG Han1*,HU Xin1,SUN Xiang-tao2,DU Jun-gang1
1Academ y of Life Science and Chem istry,Xinjiang Nor m al University,U rum uqi 830054,China;2Departure of Chem istry,Xinjiang University,U rumuqi 830000,China
A kind of acid inhibitor-Guanidine acetic acid chitosan(GAAC)has been synthesized by 1-chloro guanidine acetate and self-made chitosan.Effect of inhibitor on N80 steel is measured by weight-loss method and its adsorption mode is derived by amplitude circuit spectrum.Experimental results indicate its behaviorof adsorption confor ms to Langmuirmono-layermode and its adsorption enthalpy is obtained subsequently.This article also adopts GC-MS to study the disciplinarian of degradation in acid solutions and analyze itsmechanism of sustainably long-term inhibitory function.
natural polymer;acid corrosion inhibitor;long-ter m corrosion inhibition
R284.1;0636.1
A
1001-6880(2010)03-0383-05
2008-09-27 接受日期:2008-11-14
*通讯作者 Tel:86-991-4332417;E-mail:zenghan1289@163.com

