蔗渣半纤维素的热裂解特性研究
彭云云 武书彬
(华南理工大学制浆造纸工程国家重点实验室,广东广州,510640)
研究论文
蔗渣半纤维素的热裂解特性研究
彭云云 武书彬*
(华南理工大学制浆造纸工程国家重点实验室,广东广州,510640)
以从蔗渣中分离出的半纤维素为研究对象,利用TGA和Py-GC/MS研究了其热裂解特性。结果表明,蔗渣半纤维素的主要热失重区间在200~315℃之间,并在230℃左右出现一个肩状峰,700℃时焦炭产量在25%左右。Py-GC/MS分析结果表明,在低温段,半纤维素仅发生侧链断裂和解聚反应,半纤维素的热解产物主要是乙酸、醛类和酮类;温度升高,半纤维素热裂解程度加剧,热裂解产物主要为CO2、乙酸、1-羟基丙酮、1-羟基-2-丁酮、糠醛及环戊烯酮类化合物等。
蔗渣;半纤维素;热重分析;Py-GC/MS
我国生物质资源丰富,产量巨大,其中每年的农业废弃物(如秸秆、蔗渣、花生壳等)产量约为6.5亿t,到2010年,产量可达7.3亿t[1]。基于能源利用以及环境保护的双重要求,生物质热化学转化利用成为近年来的研究热点[2]。生物质热裂解是将生物质能源转化为高品位资源和化工产品工艺的核心技术,掌握生物质热解特性和机理对相关技术的发展具有基础性作用。近年来,研究者们采用各种先进的手段深入研究生物质的热解特性及热解机理。
生物质是由纤维素、半纤维素和木质素组成的高聚物,它的热裂解行为可以认为是这3种主要组分热裂解行为的综合表现[3-4]。同时由于各个组分的热裂解途径随温度变化呈现不同规律,因而分别对其进行研究是有必要的。关于纤维素和木质素的热解特性及机理[5-7]已经研究的非常深入。相对而言,半纤维素是植物纤维原料中结构最为复杂的不均一聚糖[8],由于其不易获得且结构复杂,因而针对植物原料中半纤维素的热裂解研究较少。Koufopanos等[4]和Colomba等[9]均采用木聚糖作为模型物研究半纤维素的热裂解特性及动力学。Ivan S等[10]采用4-O-甲基葡萄糖醛酸木聚糖为模型物进行了热裂解机理研究。但不同的生物质中,半纤维素的含量不同,糖基组成也不同,模型物与真实半纤维素大分子在化学结构和物化性质等方面存在很大的差别。
1 实 验
1.1 原料
蔗渣由江门甘蔗化工厂提供。经过植物粉碎机粉碎后,使之通过孔径为0.1 mm的筛,在60℃带通风的烘箱中烘干16 h,用密封袋封好,于5℃冰箱中保存待用。
1.2 蔗渣半纤维素的分离和提纯
将原料用苯-醇溶液(苯与乙醇体积比为2∶1)在索式抽提器中抽提6 h,以脱除有机溶剂抽出物再置于带通风的60℃烘箱中烘干16 h。
用亚氯酸钠溶液在pH值3.5~4.0、75℃条件下处理苯-醇抽提后的蔗渣,以脱除木质素,制备综纤维素。用10%KOH溶液处理综纤维素(1.2 g/100 mL,原料/抽提剂),过滤。用冰乙酸中和碱抽提液至pH值为5.5左右。加入3倍体积的95%乙醇,使半纤维素充分沉淀。然后离心过滤,用酸化乙醇(pH值5.5)、95%乙醇分别多次洗涤。最后冷冻干燥,备用。
1.3 半纤维素的化学结构分析
参照文献[12]的方法将半纤维素水解,采用离子色谱(D IONEX I CS-3000,美国戴安公司)测定其单糖及糖醛酸组分。
取80 mg半纤维素溶于1 mL D2O中,在400 MHz的工作频率下,采用BRUKER DRX400核磁共振仪测定半纤维素的碳谱(13C-NMR)。
其次,要敢于担当,善于担当。要将人民拥护不拥护、赞成不赞成、高兴不高兴、答应不答应作为工作的出发点和落脚点。习近平总书记号召各级领导干部要学习焦裕禄“敢叫日月换新天”的精神,始终做到心中有党、心中有民、心中有责、心中有戒。党的十九大给我们制定了任务书、路线图和时间表,我们要不忘初心、牢记使命,将实现个人梦想与实现国家的发展战略同频,用奋斗书写历史,用奋斗书写幸福。
1.4 热重和Py-GC/MS分析
在Q500TGA热重分析仪(TG公司,美国)上进行蔗渣半纤维素的热失重实验。热重分析仪以高纯度氮气(99.99%)为载气,流量为60 mL/min。5 mg样品置于铂坩埚上,在连续通氮的情况下,采用20℃/min的升温速率从室温加热至700℃。
裂解气相色谱-质谱联用由CDS5150裂解器和QP2010 Plus GC-MS(日本岛津)组成。裂解温度分别为250℃、350℃、500℃、700℃,加热时间为1 min。载气(氦气)流量为1.22 mL/min,柱子先在50℃保温5 min,然后以10℃/min升至终温280℃;进样口温度为250℃;EI-MS扫描范围为45~600 amu,扫描时间0.5 s;EI离子源能量为70 eV。
2 结果与讨论
2.1 半纤维素的化学结构
采用离子色谱测定半纤维素水解液中单糖组分及含量,结果表明:木糖的含量最高,其含量为76.14%,是半纤维素中最主要的单糖组分,其次为阿拉伯糖、葡萄糖,分别为9.06%、10.72%,此外还有少量的半乳糖(2.37%)、葡萄糖醛酸(1.20%)和半乳糖醛酸(0.51%)。没有检测到甘露糖,说明其含量极少。
图1是蔗渣半纤维素的13C-NMR谱图,其中显示了半纤维素典型的特征信号峰。大部分的信号峰根据参考文献[13-16]来解释。化学位移δ为101.7、77.4、73.7、64.6处有较强的共振峰,分别对应于1,4-连接的β-D-木糖单元的C1、C4、C3、C5。化学位移δ为107.49、78.1、63.0的信号峰,对应于与β-D-木聚糖连接的α-L-呋喃式阿拉伯糖残基中的C1、C3、C5。化学位移δ为13.5、72.9处的信号峰对应于葡萄糖醛酸中的C3、C5。

图1 蔗渣半纤维素的13C-NMR谱图
以上分析说明,本实验所分离得到的半纤维素主要由阿拉伯糖、木糖及糖醛酸组成,具有草类原料中典型的半纤维素结构。
2.2 蔗渣半纤维素的热裂解特性
图2为蔗渣半纤维素在升温速率为20℃/min下的热失重曲线及热失重速率曲线。从蔗渣半纤维素的TG曲线及对应的DTG曲线中可以看出,蔗渣半纤维素热解过程分为4个阶段。在190℃以前为第一阶段,样品在这一阶段只发生物理变化,主要是蔗渣半纤维素的失水过程;200~280℃为第二阶段,在此阶段,半纤维素开始发生失重,半纤维素的侧链开始断裂,聚糖发生解聚反应,对应DTG曲线的第一个肩峰;第三阶段在280~350℃之间,这是蔗渣半纤维素热解的主要反应阶段,在该温度区间内蔗渣半纤维素热解生成小分子气体和大分子的可冷凝挥发分而造成明显失重,并且其失重速率在300℃左右达到最大值,这一主要反应阶段的失重率为60%左右;第四阶段(大于400℃)主要为炭化阶段,物质失重逐渐
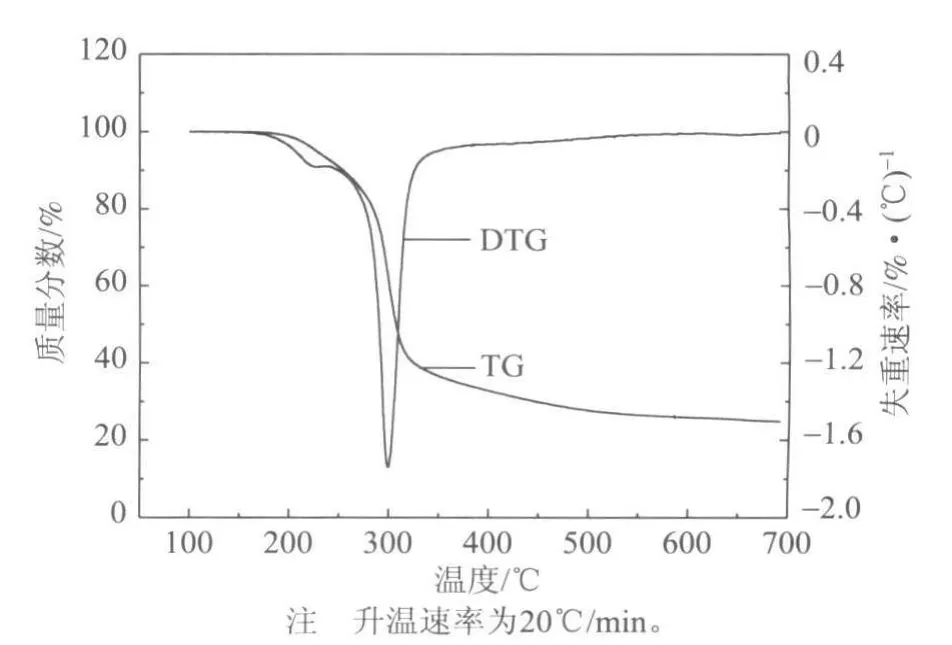
图2 蔗渣半纤维素的TG和DTG曲线

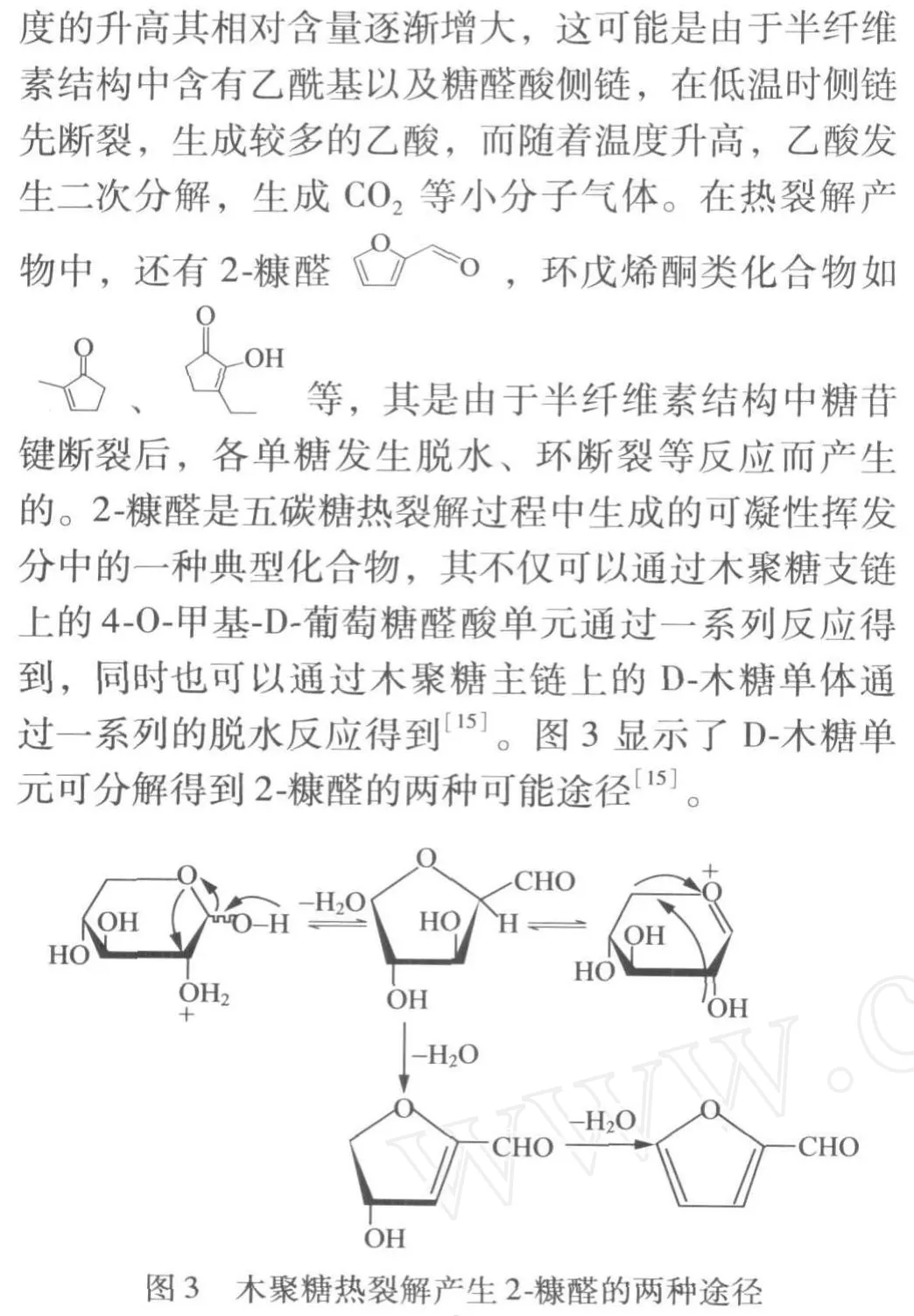
此外,热裂解产物中还存在苯、苯酚等芳香化合物,这与谭洪[19]、董宁宁[20]的热裂解研究结果一致。由于在植物细胞结构中,半纤维素和木素存在酯键连接,不可能完全将两种组分分开,因此分离得到的半纤维素可能还存在LCC连接。苯及苯酚等芳香化合物可能来自于LCC的热分解。另外,由于高温提供大量的能量,或通过自由基反应[21],使低温裂解的小分子化合物产生聚合,形成稳定性好的苯及同系物、稠环化合物,同时也形成一些杂环的芳香化合物。相关产物的生成机理尚需进一步的实验研究论证。
经研究发现,半纤维素热裂解产物中大部分成分均可用作生物能源,可提炼出十余种产物用作重要的化学品。产物中富集乙酸、1-羟基丙酮、1-羟基-2-丁酮、2-糠醛、2-甲基-2-环戊烯酮、1,2-环戊二酮、3-甲基-1,2-环戊二酮、3-乙基-2-羟基-2-环戊烯酮、2, 5-二甲基环戊酮、戊醛等。乙酸是一种非常重要的有机化工产品,可用于有机合成等。2-糠醛是呋喃环系最重要的衍生物,是制备多种药物和工业产品的原料。其主要用作溶剂,它可有选择性地从石油、植物油中萃取其中的不饱和组分,也可从润滑油和柴油中萃取其中的芳香组分。1-羟基-2-丙酮、1-羟基-2-丁酮、丙酮、2-甲基-2-环戊烯酮、1,2-环戊二酮、3-甲基-1,2-环戊二酮、3-乙基-2-羟基-2-环戊烯酮、2,5二甲基环戊酮、戊醛等可用作香料和生产食用调味品的原料。苯酚等芳香化合物也是常用的化工原料。
因此,根据以上分析,热解产物受温度影响明显,可将半纤维素的热解特性及产物生成规律,与纤维素、木素的热解规律相结合,根据生物质主要组分的热解区间和热解产物的差异,通过控制不同的热解温度,或采用分级热解工艺,选择性热解,从而获得目标产物,实现糠醛、乙酸、酮类等的有效分离。将生物质分级热解等技术与生物质原料和产品用途对应起来;把适宜的反应器、反应工艺和反应条件有机地结合起来;针对产物内含有的物质及可能发生的化学反应,尝试将热裂解产物中有价值的成分在简单装置上通过适合的反应将其转化为高附加值产品;把生物油作为能源和提取化工产品进行整合,达到最佳的经济可行性,真正实现可持续发展。
3 结 论
3.1 半纤维素的热重分析表明,半纤维素的热稳定性较差,其在200℃就开始热分解,在700℃热解已经趋于完全。热解过程可分为脱水、热解初期、主要热裂解阶段和炭化阶段。
3.2 半纤维素的Py-GC/MS分析结果表明,半纤维素在不同热解温度下的热裂解产物有较大差异,如随着温度升高,在热裂解产物中乙酸的相对含量降低,而CO2的相对含量逐渐增大。在低温段,半纤维素的热解产物主要是乙酸、少量醛类和酮类,说明热裂解初期半纤维素仅发生侧链断裂和解聚反应;高温段,半纤维素热裂解程度加剧,热裂解产物主要为CO2、乙酸、1-羟基丙酮、1-羟基-2-丁酮、糠醛及环戊烯酮类化合物。
3.3 半纤维素的热裂解产物中富含乙酸、羟基丙酮、羟基丁酮、糠醛等许多有用的化学品。若采用合适的仪器装置和工艺条件将其转化为高品位能源,对于进一步研究生物质可再生能源的应用具有重要的意义。
[1] 赵 军,王述洋.我国生物质能资源与利用[J].太阳能学报, 2008,29(1):90.
[2] Kendry P M.Energy production from biomass(Part 2):Conversion technologies[J].Bioresource Technology,2002,83:47.
[3] Bassilakis R,Carangelo R M,WojtowiczM A.TG-FTIR analysis of biomass pyrolysis[J].Fuel,2001,80(12):1765.
[4] Koufopanos C A,Maschio G,Lucchesi A.Kinetic modeling of the pyrolysis of biomass and biomass components[J].Canadian Journal of Chemical Engineering,1989,67:75.
[5] Yang H P,Yan R,Chen H P,et al.In-depth investigation of biomass pyrolysis based on threemajor components:hemicellulose,cellulose and lignin[J].Energy&Fuels,2006,20(1):388.
[6] Varhegyi G,Michael J A Jr.Kinetics of the thermal decomposition of cellulose,hemicelluloses,and sugar cane bagasse[J].Energy&fuels,1989,3(3):329.
[7] 谭 洪,王树荣,骆仲泱,等.木质素快速热裂解试验研究[J].浙江大学学报:工学版,2005,39(5):710.
[8] Wedig C L,Jaster E H,Moore K J.Hemicellulose monosaccharide composition and in vitro disappearance oforchard grass and alfalfa hay [J].Journal ofAgricultural Food Chemistry,1987,35(2):214.
[9] Colomba D B,LanzettaM.Intrinsic kinetics of isothermal xylan degradation in inert atmosphere[J].Journal of Analytical and Applied Pyrolysis,1997(40/41):287.
[10] Ivan S,Varhegyi G,AntalM J.Thermogravimetri/mass spectrometric characterization of the ther mal decomposition of 4-O-methyl-D-glucurono-D-xylan[J].Journal of Applied Polymer Science,1988, 36:721.
[11] Saha B C.Hemicellulose bioconversion[J].Journal of Industrial Microbiology and Biotechnology,2003,30(5):279.
[12] 杨淑蕙.制浆造纸分析与检测[M].北京:中国轻工业出版社,2003.
[13] KováP,Hirsch J.Sequential synthesis and13C-N.m.r.spectra o methylβ-glycosides of(1→4)-β-D-xylo-oligosaccharides[J].Car bohydrate Research,1982,100(1):177.
[14] EbringerováA,HromádkováZ,Alföldia J,et al.Structural and so lution properties of corn cob heteroxylans[J].Carbohydrate Poly mers,1992,19(2):99.
[15] Ivan S,JurajA,MáriaM.A13C-N.M.R study of the alkaline deg radation products of polysaccharides[J].Carbohydrate Research, 1986,152(1):137.
[16] LawtherJM,Sun R C,BanksW B.Extraction,fraction,and char acterization of structural polysaccharides from wheat straw[J].Jour nal ofAgricultural Food Chemistry,1995,43:667.
[17] Maschio G,KoufopanosC,LucchesiA.Pyrolysis,a promising rout for biomass utilization[J].Bioresource Technology,1992,42 (3):219.
[18] 宋春财,胡浩权.秸秆及其主要组分的催化热解及动力学研究[J].煤炭转化,2003,26(3):91.
[19] 谭 洪.生物质热裂解机理研究[D].杭州:浙江大学,2005.
[20] 董宁宁.碳水化合物的热裂解气相色谱-质谱研究[J].质谱学报,2004,25(1):24.
[21] 甘孝贤.自由基开环聚合[J].化学通报,1986(11):18.
Abstract:The pyrolysis characteristics of hemicellulose isolated from sugarcane bagasse were studied by ther mogravimetric analysis(TG) and pyrolysis GC/MS.The results showed that themajor reaction stage of hemicellulose pyrolysiswaswithin 200~315℃.A shoulder-shape peak appeared at about 230℃.The last remnants of coke accounted for about 25%or so at 700℃.The Py-GC/MS analysis showed that th main productsof hemicellulose pyrolysis at lower temperaturewere acetic acid and a little ketone and aldehyde,butmany kindsof compound like 1-hydroxy-2-acetone,1-hydroxy-2-butone,2-furanal and cyclopenetene were produced at higher temperature which were produced from the fragmentation of the main structure.The products of hemicellulose pyrolysis consists of acetic acids,furanal and ketones which can b used as important chemicalmaterials.
Keywords:sugarcane bagasse;hemicelluloses;ther moanalysis;Py-GC/MS
(责任编辑:常 青)
The Pyrolysis Characteristics of Hem icellulose from Sugarcana Bagasse
PENG Yun-yun WU Shu-bin*
(State Key Lab of Pulp and Paper Engineering,South China University of Technology,Guangzhou,Guangdong Province,510640)
(*E-mail:shubinwu@scut.edu.cn)
TK6;X793
A
1000-6842(2010)02-0001-05
2009-12-10(修改稿)
国家重点基础研究发展计划项目(项目编号2007CB210201);国家863计划资助课题(批准号2007AA05Z456);中科院天然气水化合物重点实验室开放基金项目(批准号0807K1)。
彭云云,女,1985年生;在读硕士研究生;研究方向:生物质热化学转化为清洁燃料与化学品。
*通信联系人:武书彬,E-mail:shubinwu@scut.edu.cn。

