氨基磺酸镍合成工艺的研究
江 波,周枚花
(1.江西陶瓷工艺美术职业技术学院,江西 景德镇 333001;2.华东交通大学,江西 南昌330013)
氨基磺酸镍[1]溶液,分子式为[Ni(H2NSO3)2◦4H2O],外观为绿色溶液。它是一种优良的镀镍主盐[2],优点为电沉积速度快,分散能力强,镀层应力小,电流效率高,可达90%以上。另外,还有溶解度大,无污染等优点。现已广泛应用于电子、汽车、航天、兵器、造币、冶金镍网、无线电、彩色铝合金等行业。
传统的合成工艺有两种:一种工艺是将镍粉与氨基磺酸在引发剂的作用下直接反应制得[3],这种工艺虽然简单直接,但有两个缺点:一是必须要求高质量的镍粉原料才能保证得到高质量的氨基磺酸镍,因为一般的镍粉含有铁,钴,铜,锌等15种杂质元素,杂质太多影响氨基磺酸镍的电镀效果;二是由于引发剂的加入,使得产品中不可避免的有引发剂的残留,从而在一定程度上影响了电镀效果;另外一种工艺是先将硫酸镍与碳酸钠发生反应生成碳酸镍,再加入氨基磺酸生成氨基磺酸镍,这种工艺也有两个缺点:一是由于选择的原料必定会产生硫酸根离子和钠离子,这两种杂质离子都会很大程度上影响产品的电镀效果;二是后一步反应中会产生二氧化碳气体,必须时刻监测,否则因为大量气泡的生成,反应液有可能溢流出来,降低产率。
综合考虑传统的合成工艺的优缺点,本文提出了一种制取氨基磺酸镍的新工艺,其反应流程为:第一步用镍盐溶液与氨水反应生成氢氧化镍,第二步将氨基磺酸与氢氧化镍反应生成氨基磺酸镍。经过长期实验发现,使用该工艺制取氨基磺酸镍关键是第一步合成氢氧化镍,因为氢氧化镍颗粒越大效果越好,这样不仅易于沉降,且得到的产品纯度就越高。结果表明,使用该工艺所制得的氨基磺酸镍溶液,杂质含量低,特别是SO42-含量低,当其应用于电镀时,沉积速度快,镀层内应力低,在适当的电镀条件下,甚至可得零应力镀层[4]。其品质优于国内其它品牌,可与国外先进企业的产品处于同一水平。
1 实验工艺
1.1 反应原理
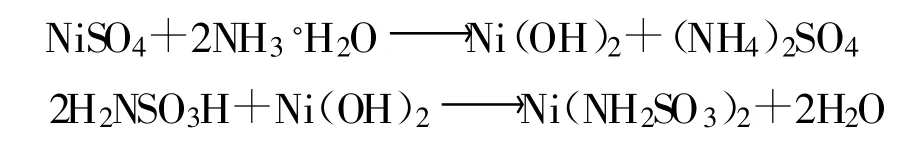
1.2 试验步骤
先在镍盐溶液中加入氨的物质量为镍离子3~6倍的氨水,控制溶液的pH值在9.5~12.0,搅拌下加热溶液使其温度维持在40℃~90℃,体系中有球形Ni(OH)2生成;当溶液pH值下降至8.5~10.5中某一确定值时,向体系中缓慢加入NaOH溶液至母液蓝色褪去,此过程中控制加碱速度,维持溶液pH值稳定;经搅拌、陈化、抽滤,则镍盐完全转化为球形氢氧化镍[5]。然后,将氢氧化镍充分洗涤去除钠离子和硫酸根离子等杂质,再将氨基磺酸分多批加入合成氨基磺酸镍[6],反应温度控制在80℃内,最后,经浓缩、过滤,得产品。
1.3 试验流程示意图
试验工艺流程示意图如图1。
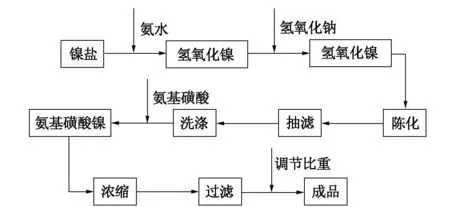
图1 试验流程示意图
2 最佳试验条件的控制
2.1 合成氢氧化镍工艺条件的控制
合成氢氧化镍是新工艺的关键步骤,对工艺条件的控制直接影响到氢氧化镍的量,工艺条件包括反应温度、反应体系的pH值、搅拌强度、镍氨比等[7]。
1)反应温度
在镍盐溶液中加入氨水生成氢氧化镍的过程中,为了提高产率,必须确保镍离子完全转化成氢氧化镍,但是如果反应温度较低时,镍离子和氨水可以络合生成镍氨络合物,例如[Ni(NH3)4]2+,并且形成的镍氨络合物会溶解在氨水里,这样,镍离子有所流失,势必会降低氢氧化镍的产量,也就会降低氨基磺酸镍的产量。因此,在制备氢氧化镍时,反应温度是个至关重要的因素[7]。反应过程中温度太高时,氨水受热分解会挥发一部分,造成氨水有所损失;反应过程中温度太低时,反应速度很缓慢,最重要的是镍离子会形成镍氨络合物而损失一部分。必须抑制镍氨络合物的形成,确保镍离子尽可能与氨水中的氢氧根离子结合生成氢氧化镍。
在其它条件相同的情况下,不同反应温度所产生的氢氧化镍如表1所示。

表1 温度对产品氢氧化镍浓度的影响
从表1可知,反应温度过低,反应速度缓慢,且生成了镍氨络合物而降低了氢氧化镍的量;反应温度过高,氨水受热分解损失一部分,产量也不高。反应温度应当控制在40℃~90℃较为适宜。
2)反应体系的pH值
为防止反应液产生局部过碱,影响氢氧化镍的成核形状[8],需进行反应液pH值的均匀性试验。
第一个均匀性试验是加氨水时反应体系的pH值控制:经过反复的试验总结,为了得到球形的氢氧化镍,需控制溶液的pH值在9.5~12.0,每隔一分钟分别测量反应液上部、中部、下部的pH值,并记录下来。
钠离子是杂质,会影响氨基磺酸镍的电镀效果,反应体系的pH值会直接影响到溶液中杂质钠离子的百分含量,如下图2,pH值小于8.0时,溶液中钠离子的百分含量相当高;pH值介于8.0~8.5时,钠离子的百分含量急剧下降接近零;pH值大于8.5时,钠离子的百分含量有少量提升。所以,应该尽可能缓慢的分批次加入氢氧化钠,并且保持pH值不小于8.5较好。
第二个均匀性试验是加氢氧化钠时反应体系的pH值控制:随着氨水的不断消耗,pH值逐渐变小,当pH值下降至8.5~10.5中某一确定值时,缓慢加入氢氧化钠提升pH值至8.5~10.5并保持稳定,在这个过程中每隔一分钟分别测量反应液上部、中部、下部的pH值,维持稳定值,否则 pH值一旦小于8.5,杂质钠离子的百分含量将会急剧上升。
3)搅拌强度
加大搅拌速度对生成球形氢氧化镍必不可少[9]。为了增大镍盐与氨水的接触面积,避免局部过浓现象,保持溶液在一个均相的环境中,在加热的过程中用磁力搅拌器高转速的搅拌,如果在低转速搅拌下,形成絮状的氢氧化镍,无法形成球形的氢氧化镍,对于后续的陈化过程不利,所以,为了生成球形的氢氧化镍,必须在高转速下搅拌。
4)镍氨比
从反应方程式来看,镍离子与氨水发生反应的摩尔比是1:2,也就是说氨水的物质量是镍离子的2倍,但为了使镍盐完全转变成氢氧化镍,很显然氨水应该过量;但是,镍离子与氨水又会形成银氨络合物且溶于过量的氨水中,若氨浓度太大,将会损失部分镍离子而降低产量,所以,氨水的量要适中。不同镍氨比所产生的氢氧化镍如表2所示。
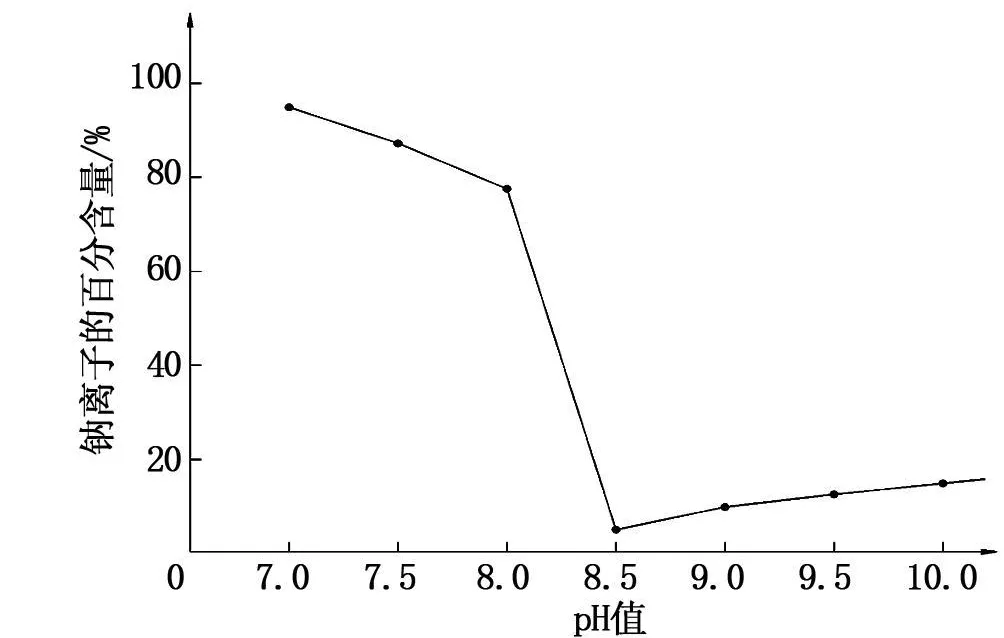
图2 钠离子随pH值变化的百分含量

表2 镍氨比对氢氧化镍浓度的影响
从表2可以看出,选择加入氨的物质的量为3~6倍的镍离子较为适宜。
5)氢氧化镍洗涤过程条件控制
将合成好的氢氧化镍进行洗涤除杂,去除杂质Na+,SO42-。
(1)影响洗涤效果主要因素有
洗涤水流量:加大洗涤水,能有效带走杂质元素。
洗涤时间:洗涤时间理论上是越长越好,但洗涤时间越长,镍的流失也越大,从而降低回收率,不利于生产成本。
洗涤水路:洗涤换边次数6次,洗涤时间为30 min,洗涤过程中多次轮换出水水路,洗涤效果比较好。
(2)简单检测监控洗涤效果的方法
测量洗涤水的pH值(或者测其电导率)。由于(NH4)2SO4是强酸弱碱盐,Na2SO4是强酸强碱盐,所以,如果洗涤水里这两种盐少,则pH接近7,说明洗涤效果好。因此只要通过简单的pH测量,就可以大体知道洗涤效果如何,可以买台电导仪,测量更准确。
通过上述的一些简单方法,就可以检测监控洗涤效果及氢氧化镍的合格性。
2.2 合成氨基磺酸镍工艺条件的控制
(1)氨基磺酸分批加入
氢氧化镍与氨基磺酸的反应是放热反应,一次性加入氨基磺酸,反应不均匀,温度骤升,对温度无法控制。所以,氨基磺酸应该分多批加入,反应较均匀,温度易于控制。
(2)反应温度
为制备高纯度的氨基磺酸镍,抑制水解产物是最主要的条件之一。H2NSO3H和H2NSO3-遇水均发生水解:
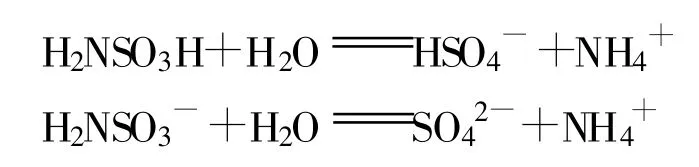
从化学反应热力学分析,升温对水解有利。因此,在制备氨基磺酸镍时,反应温度是个至关重要的因素。反应过程中,温度越高,反应速度越快,但相应地氨基磺酸镍的水解越明显,产生的也就越多,而是氨基磺酸镍产品最主要的控制指标之一,也是影响电镀效果的关键杂质。温度越低,反应越慢,从而也影响反应进程。在其它条件相同的情况下,不同反应温度所产生的量如表3所示。
表3 温度对产品中的影响

表3 温度对产品中的影响
样品号 温度t/℃ SO2-4/ppm 1 30 300 2 50 320 3 60 330 4 70 340 5 80 345 6 90 500 7 100 1 600
从表3可知,氨基磺酸分多批加入时,反应温度应当控制在80℃内较为适宜。
3 结果与讨论
3.1 与同类产品的性能比较
将按上述工艺所合成的氨基磺酸镍与国内外同类产品的性能进行比较,结果如表4所示。
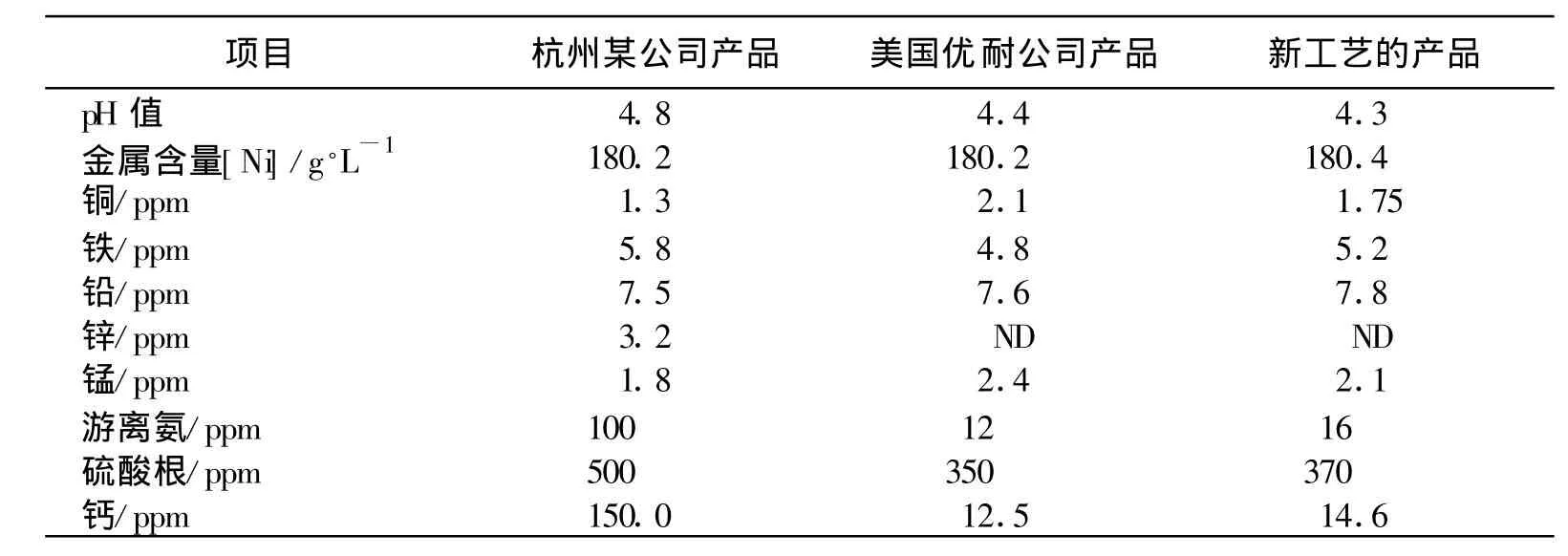
表4 新工艺合成的氨基磺酸镍与国内外同类产品的比较

续表
由表4的数据可以看出,用该工艺所合成的氨基磺酸镍的品质明显优于国内其它品牌,同美国优耐公司的产品也处于同一水平。
3.2 需要改进的问题
在试验中,因为氢氧化钠的加入,使得产品中不可避免有硫酸钠的残余,从而在一定程度上影响了电镀效果[10]。如何使产品中的硫酸钠的含量降到最低,得到更加优质的产品,有待进一步研究。
4 结论
氨基磺酸镍是镀镍、电铸镍所必需的精细化工原料,研究其制备方法与工艺有实际应用与理论价值。本研究提出了一种合成氨基磺酸镍的新工艺,同传统的合成工艺相比,该工艺简单易行,质量和产量都大有提高,但是,新工艺和传统工艺都有一个共同的缺点,即由于杂质离子的存在影响电镀效果。如何减少杂质离子是今后重点考虑的问题。如果使用本工艺生产,成本低,方法简单,生产效率高,产品质量稳定。分析检验表明,该种氨基磺酸镍纯度高,杂质含量低,可以考虑投放市场。
[1]蔡剑秋,周连江,乐志强,等.无机盐工业手册[M].北京:化学工业出版社,1979:434-437.
[2]卫中领,陈秋荣,张韬.氨基磺酸镀镍液和镀镍方法[P].中国专利:CN 200910044980,2009-08-05.
[3]徐强.一种氨基磺酸镍的制备方法[P].中国专利:CN 200410025138,2005-12-28.
[4]禹茂章.精细化学品辞典[M].北京:化学工业出版社,1989:18-19.
[5]张强,赫文秀,张永强,等.球形氢氧化镍的制备及表征[J].内蒙古石油化工,2009,3(13):33-34.
[6]陈兆斌,陈淑丽,薛鹏冲.氨基磺酸镍制备的研究[J].精细化工,2001,18(9):22-28.
[7]安晓君,焦红忠,李志,等.制备条件对球形Ni(OH)2电化学性能的影响[J].宁夏工程技术,2005,4(2):15-20.
[8]陈腾飞,龚伟平,贺万宁,等.制备条件对球形Ni(OH)2物理性能的影响[J].云南冶金,2002,31(2):46-48.
[9]彭美勋,沈湘黔,危亚辉.搅拌型式对球形Ni(OH)2物理性质的影响[J].硅酸盐通报,2008,27(2):30-33.
[10]曾华梁,吴仲达,秦月文,等.电镀方法手册[M].北京:机械工业出版社,1989:220-225.

