用于心脏起搏器的经皮能量传输系统
周 煜 于歆杰 程锦闽 王崇慧 王 琳
(1. 清华大学电机系电力系统国家重点实验室 北京 100084 2. 中国医学科学院北京协和医院 北京 100730)
1 引言
心脏起搏器这一应用于人体的诊疗装置在医学中越来越发挥着不可替代的作用。受惠于此,很多患者延长了生命多达数十年。同时,心脏起搏器的临床应用也面临了许多难题。其中一个亟待解决的问题就是如何保证设备所需能量的持续、稳定、长期供给。由于该设备需要数十年在人体内稳定地运行,故能量供应的突然中断会带来严重的后果[1]。现有的供能方式主要有两种:①由一根线连接到体外电池,这样不用担心能量的耗尽,但是无疑会使患者大大增加被感染的几率,也会给平时生活带来诸多不便。②使用一次性电池供电[2]。目前应用比较广泛的是锂碘电池。虽然采用此种方案不会带来感染和行动的受限,但是大约6~8年就需要去重新做手术更换起搏器脉冲发生装置,而且每年要定期去医院检查电池状况。有没有一种方案能够规避这两种困扰呢?基于法拉第电磁感应原理的非接触式经皮能量传输装置(Transcutaneous Energy Transmission System,TETS)应运而生。能量的无线传输技术配合已有的锂离子可充电电池不仅可以突破电池的容量限制,也使术后易感染的难题迎刃而解。此外,TETS的研制对于人工耳蜗、人工心脏等需要持续供能的诊疗设备同样具有临床价值。
国外对于TETS的研究始于20世纪80年代。目前,日本、美国以及欧洲少数国家对TETS已进行深入研究[3-6]。日本 Tohoku大学研究小组已有实验室样机问世,但是距离临床应用仍有很多需要解决的难题[7-10]。我国在这一领域的研究尚处于起步阶段,研究大多以理论分析为主,主要集中在系统后续电路模块的方案,对于频率的选取没有统一的标准[11-14]。因此研制一套具有我国自主知识产权的TETS具有重要意义。
2 TETS的工作原理和组成概述
TETS的工作原理如下:由法拉第电磁感应定律和麦克斯韦电磁理论,交变的电场可以转化为交变的磁场,反之亦然。将体外的无接触式松耦合变压器的一次线圈通入频率恒定的交流,在其周围产生一个交变磁场,位于体内的二次线圈将感应到的磁场转化为一次侧同频的交变电场,能量得以传入后续电路。后续电路将得到的能量经过整流、稳压等手段的处理,使其电压、功率满足诊疗设备供电电池的充电要求。这样整套系统就可以维持体内诊疗设备的持续运转。
如图1所示,本文阐述的TETS由经皮变压器和二次侧电路两部分组成。作为能量转化装置的经皮变压器分为体外一次线圈和体内二次线圈两部分,分别作为磁场的发射和接收装置。能量由电能转化为磁能再转化为电能对心脏起搏器进行供电。作者对TETS进行了设计和改进,做出了罐型铁氧体磁心线圈和集成后续电路的PCB电路板,可以与二次电池和心脏起搏器整合成一体。
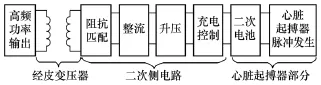
图1 TETS结构图Fig.1 Structure of TETS
3 TETS经皮变压器的研制
TETS的核心在于经皮变压器的研制。TETS的二次侧部分以及心脏起搏器是完全植入人体的,位于真皮层和胸大肌之间。由于病人形体各异,且呼吸状况和健康程度不同,经皮变压器两个线圈的间隙距离并不固定。经皮变压器必须在这样复杂的条件下为后续电路提供平稳的电压和足够的功率,同时还要满足小体积和高效率等相互制约的因素,这就需要综合各种矛盾加以分析取舍。诸如线圈的形状、材料的选取、线圈的绕制以及同后续电路之间的配合提出了不小的挑战,必须要全面综合考虑才能得出一个相对满意的方案。作者将在下文分频率的选择,线圈的绕制,等效的电路模型三个方面加以论述。
3.1 频率的选择
高频乃至超高频电磁波具有良好的指向性,但是透入深度较低,不能更好地进入人体皮肤传递到二次侧线圈;而且系统的频率越高能量的热效应也越高,对于人体是不安全的。低频(1kHz及以下)电磁波虽然较为安全但容易发散,会使二次侧接收不到预期的功率而无法驱动电池的充电电路。
对于效率的选择还要重点考虑国内和国际上对于电磁环境标准的严格限制。
由美国 ACGIH 辐射标准[15],在 0.01~3MHz这个频率范围,人体每 cm2可承受的电磁辐射为0.1W,所以只要保证每平方厘米的辐射能量在0.1W以下,电流所激发的交变磁场对生命体都是安全的。按下文可算得,TETS经皮变压器线圈面积约为27cm2,考虑TETS的效率因素在内,对于几百mW能量需求的人体内置电装置是很容易满足的。根据国家环保总局的国内电磁辐射标准[16],对公众在0.1~3MHz频率范围内电磁波照射不超过 40W/m2的标准推算可知,在 110mW 以内的辐射总量对人体是安全的。但如果考虑效率因素,则这样的能量供应不能满足TETS二次侧的要求。此标准制定于1988年,并未考虑到日后科技方面的诸多应用,标准的制定较为保守。对比现今手机辐射的影响,TETS系统的影响要小很多,所以在较低的频率下,TETS对人体是安全的。
用仿真软件 Comsol Multiphysics 3.3的 Static模式得到的经皮变压器线圈的磁通密度建模图形如图2所示。
利用软件得到 1kHz~10MHz频段下的电流数据,计算得到在各频率下的一、二次侧电流比,数据见表1。
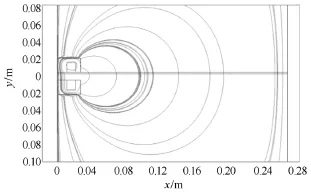
图2 经皮变压器磁通密度仿真图(含磁心)Fig.2 Simulation of magnetic flux density of transcutaneous transformer(magnetic core included)
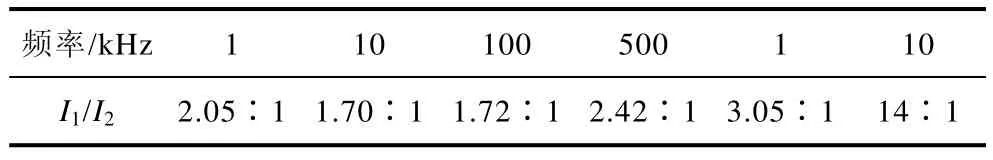
表1 常用频率下TETS特性Tab.1 TETS characteristic under common frequencies
可以看出,随着频率的升高,一、二次侧电流比先减小后增大。在10kHz时为1.70∶1,100kHz时为1.72∶1,变化不大。电流比越小,说明相同结构下,一二次耦合效率越高,一次侧通入较小的电流就可以耦合到二次侧得到较大的电流,所以,一、二次电流比越小,变压器效果越好。
理论表明,系统频率越高,能量辐射的穿透性越好。由上面仿真结果,考虑植入设备效率和温升之间的矛盾(频率越高,效率提高,但温升也随着增加),选择系统的工作频率为 100kHz,这个频率的电磁波既能使足够的能量传递到二次侧又能确保人体安全。
此外,选择该频率也可以较好地减小日常电器对于TETS的影响。对于作为能量接收和转换装置的 TETS而言,其经皮变压器的二次线圈需要接收到持续稳定且有一定强度的电磁波辐射才能启动充电过程。平时生活中的电器所辐射的电磁波频率多为MHz乃至GHz级别,发散且易衰减,持久辐射到人体胸部(TETS所处位置)的机会非常小,对于患者而言是较为安全的。另外,针对心脏起搏器而言,患者遵照医嘱回避发电厂和高压装置等强辐射装备更是必需的。
3.2 经皮变压器的研制
为削弱高频集肤效应,电路往往使用多股相互绝缘细导线编织成束来代替同样截面积的粗导线,即Litz线(利兹线或称漆包绞和线)。
由于两线圈分别位于体内和体外,对于电磁波的传递是不利的,特别在间隙较大的情况下更突出。如果不选用磁导率较高的材料协助导磁,将使二次侧接收到的能量过低而导致实验失败。此外,二次侧线圈位于体内也对导磁材料的体积提出了很高的要求。
软磁材料方面,不但新兴材料非晶合金、纳米合金、磁性薄膜迅速发展,而且传统材料硅钢、软磁铁氧体、坡莫合金近年来都有明显的进步[17]。本项目确定了以下五个选择准则,并对市面上已有的软磁材料进行了筛选:
(1)磁导率要高。高磁导率材料可以降低外磁场的励磁电流值,从而降低磁元件的体积。
(2)具有很小的矫顽力和狭窄的磁滞回线。低矫顽力材料使得磁化和退磁容易,磁滞回线狭窄,在交变磁场中磁滞损耗就小。
(3)电阻率要高。高电阻率材料可以大幅度降低涡流损耗,提高系统效率。
(4)具有较高饱和磁感应强度。磁感应强度高,相同的磁通需要磁心截面积小,磁性元件体积小。
(5)满足实验要求的特定频率。
软磁材料有其最佳的适用范围,必须加以取舍,具体如下:
(1)硅钢适用频率为工频左右,故不适合该项目。
(2)非晶材料具有体积小,效率高等特点,其中钴基非晶材料具有最高的导磁率和较低的饱和磁感应强度,200kHz下应用优势明显,是良好的备选材料。但缺点是造价昂贵且加工难度大,国内生产厂商有限。实验曾尝试使用钴基非晶带材附于线圈表面,对于导磁性能提升有限。作者分析这是由于带材本身延展性差不能像成品磁心那样质地紧密,性能打了很大折扣。
(3)在中高频下,软磁铁氧体占领的市场份额最大。它的优点是适用频率较高,具有低损耗因子、高品质因数、稳定的磁导率。价格相对新型材料而言十分低廉,是首选材料。软磁铁氧体磁心有Mn-Zn、Cu-Zn等多种,形状也有 E形、环形、U形等多种。
系统最终采用罐型磁心作为变压器一次侧和二次侧,是磁导率约为 2000的 Mn-Zn材质,型号为GU 59×36,即铁心外径和内径分别为 59mm 和36mm。基于这种铁心,Litz线绕制了与之紧密结合的变压器线圈并用环氧树脂进行了封装,如图3所示。

图3 经皮变压器线圈实物图Fig.3 Transcutaneous transformer coils
需要说明的是,采用这种线圈是对比市面上现有的铁氧体磁心形状的结果。很明显,E形、环形、U形等铁氧体线圈形成的磁路不利于两个线圈的对正和电磁波的有效传递。只有截面圆形的线圈才能更好地利用空间,并使线圈的对正问题最小化。最终没有采用非晶合金材料是由于目前国内开模制造小型钴基非晶铁心的成本高,制造工艺难度大,行业标准内的钴基磁心的形状均不符合要求。后文实验可以看出,空气间隙对于实验结果的影响非常大。
3.3 经皮变压器的等效模型
通过对比变压器等效模型下计算得到的负载实验数据和实验测得数据的一致性可以验证模型的正确性。
不同于一般变压器,此种经皮变压器带有空气间隙,所以不能等效为理想变压器和全耦合变压器,如果忽略铁磁材料的非线性特征,则可以初步考虑空心变压器模型[18],如图4所示。
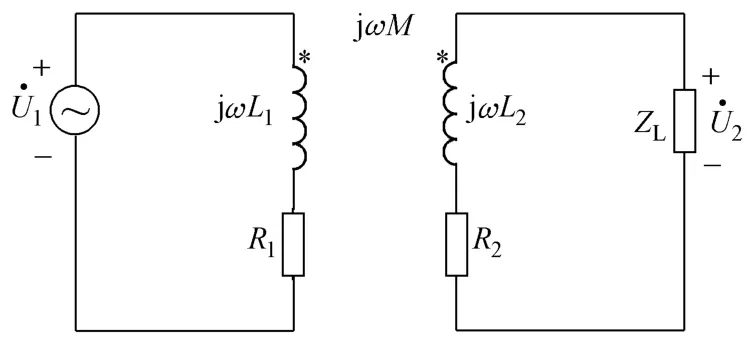
图4 经皮变压器的等效电路Fig.4 Equivalent circuit of transcutaneous transformer
图4中,1U˙代表一次侧输入交流电压,ZL代表负载阻抗,2U˙代表ZL的电压,ωL1和R1代表一次侧线圈的自感感抗和电阻,ωL2和R2代表二次侧线圈的自感感抗和电阻,ωM 为线圈间的互感感抗。由于两侧线圈完全一致,故具有相同电路参数,可以令ωL1=ωL2=ωL,R1=R2=R。从二次侧电负载端看入的戴维南等效电路由图5所示。
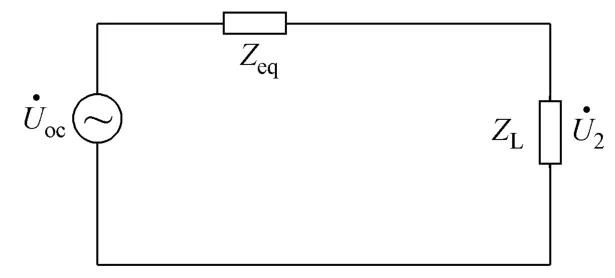
图5 经皮变压器的简化电路Fig.5 The simplified circuit of transcutaneous transformer
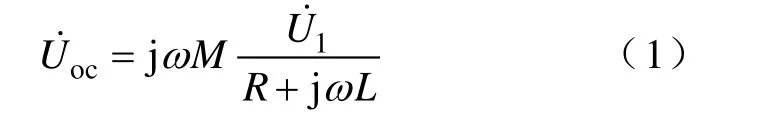
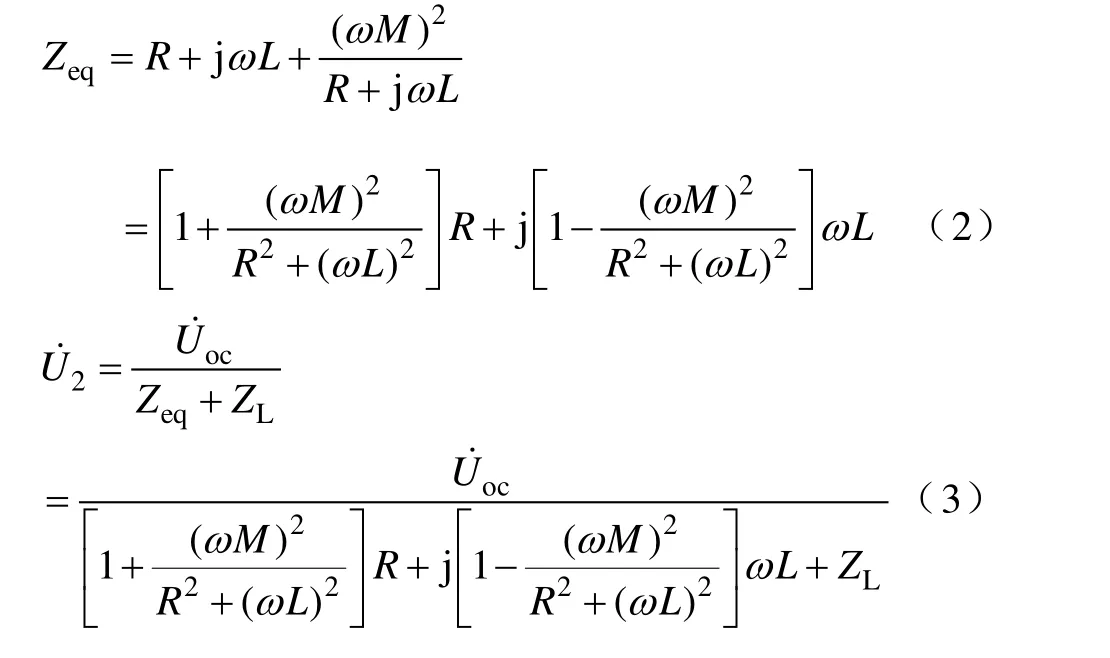
由式(3)可看出,在已知 U1的情况下,只要测得R、ωL、ωM和ZL四个参数即可算出U2。
为确保测量不受 100kHz交流下集肤效应的影响,本实验采用HP4284A精密LCR参数表测量不同间隙下线圈的自感和电阻;互感感抗ωM 利用不同间隙下测得的二次侧开路电压和一次侧电流的有效值的比值求得;实验用负载 ZL经实测阻抗值为(5.00+j3.64)Ω。
为验证空心变压器模型的准确性,只要将算得的 U2与直接测得的 U2进行比较即可。选取 2~10mm共 5组线圈间隙进行实验。根据测得数据和式(2)可算得不同间隙下负载侧看入的前端等效阻抗Zeq。测得数据和算得的阻抗数值见表2。
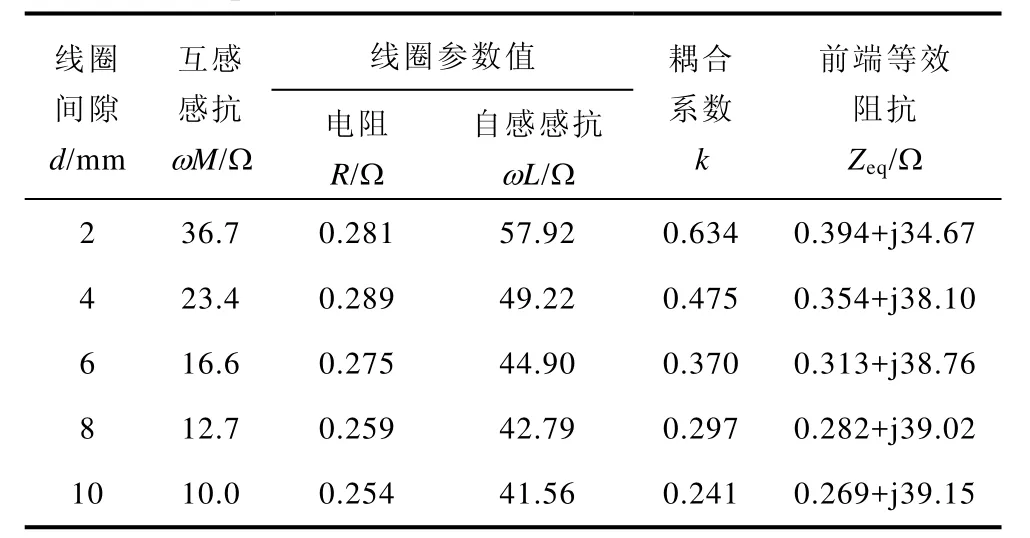
表2 经皮变压器实验测定数据Tab.2 Experimental data of transcutaneous transformer
在一次侧通入5V有效值,100kHz频率的交流电,分别测得在对正情况下5组间隙的二次侧负载电压的有效值。表3列出了二次侧负载电压的实测结果、根据表2数据和式(3)计算得到的结果以及二者的误差。
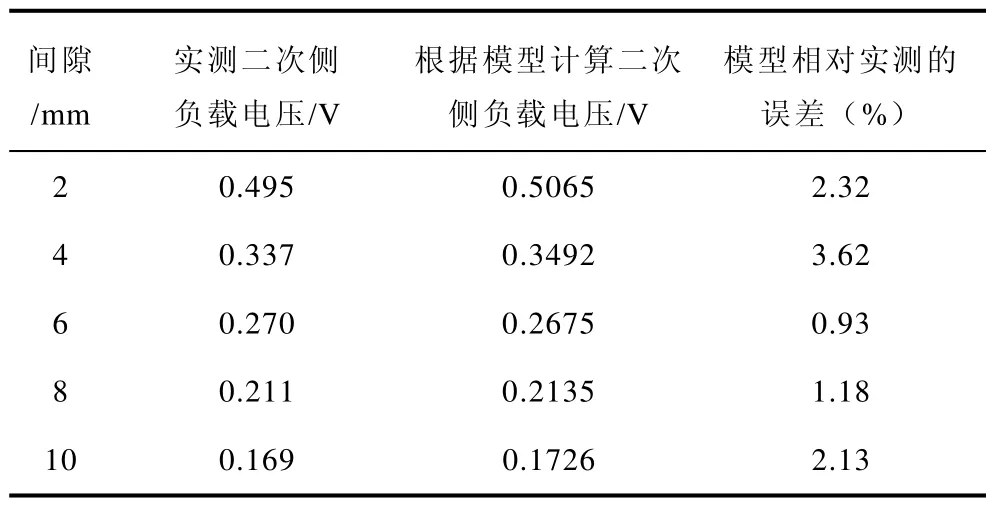
表3 经皮变压器实测和模型数据对比Tab.3 Contrast between the measure data and model
可以看出,模型数据与实验数据吻合得很好,这证实了该变压器模型的正确性,即带有空气间隙的经皮变压器可由空心变压器模型来等效,也就是说在经皮变压器应用中忽略铁磁材料的非线性特征是可取的。
由表2和表3可看出:①间隙增大带来两变压器线圈之间的耦合变弱。从表征两互感线圈耦合强弱的耦合系数k的变化趋势可以明显看出这一点。②随着变压器线圈间隙的增大,在一次侧电压不变的情况下二次侧电压呈下降趋势,这与理论分析相一致。③一次侧电压限定为5V,且负载阻抗不大的情况下,如不施加任何补偿则二次侧得到的电压非常低。即使将一次侧电压提高至20V(此时变压器线圈的磁特性仍处于线性未饱和状态),二次侧电压最高只能到 2V(2mm间隙下)左右,送出的功率不到 1W,这对于充电实验的完成不利。这也证明了施加补偿的必要性。
4 二次侧电路的研制及相关实验
4.1 二次侧电路的研制和分析
图1经皮变压器后续的二次侧中,整个电路分为四部分,即阻抗匹配、整流、升压和充电控制。
阻抗匹配环节主要是利用了电容的串并联手段抵消经皮变压器的电感对于后续电路带来的影响。由表2可以看出,前端等效阻抗的感抗部分随间隙增加而增大。感抗增大的影响主要表现在电压的分配上。电感虽然不会消耗功率,但是它会分得相当一部分电压,无形中使得整个TETS的带载能力有了较大下降。
整流环节是将交流 100kHz转变为直流,而且希望整流器件在开关上消耗尽量小的能量。不控整流电路因为电路结构简单,无需产生控制信号因而应用普遍。在不控整流方式中又以半桥整流和全桥整流研究最多。由于两相半波整流方式需要在变压器二次侧为三端输出,增加了变压器绕制难度,且效果和全桥整流相似,因而采用不控整流中的全桥整流。为了进一步降低开断损耗,本项目使用肖特基二极管。
升压环节是为适应前面环节的输出电压而确定的。前级电压如能保证后续电池充电芯片的正常工作且输出电压波动较小就可忽略此环节;如前级电压过小或输出电压的波动大到不足以维持芯片的正常工作则需保留该环节。
充电控制环节是心脏起搏器供能电池的前级输入环节。该环节使用市场上成熟的充电控制芯片,其优点是具有较大范围的输出电压和成熟的充电控制模式,可有效延长二次电池的使用寿命。
4.2 TETS的实验测试和分析
研究小组将经皮变压器及其后续电路整合在一起,构成完整的TETS后,据此进行了大量实验。以下选取两个典型的充电实验来验证该系统的可行性。
实验1线圈间隙为8mm,使用纸张作为模拟。充电的时间-电压曲线如图6所示。
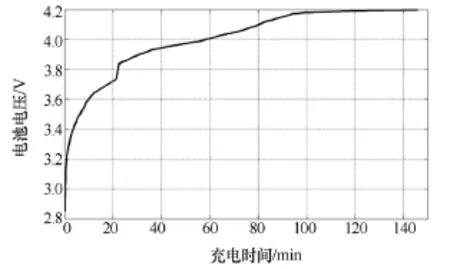
图6 TETS在8mm纸质间隙下的完整充电曲线Fig.6 Charge curve of TETS under 8mm paper interval
二次侧电路串入35.3nF电容,使得TETS达到谐振。需要说明的是,35.3nF电容可以补偿 45.1Ω感抗,略大于表2中8mm间隙下的39.02Ω,这是由于为使整个TETS谐振,电容同时补偿了后续二次电池引入的电感。即使如此,需补偿电感的主要部分仍是前级经皮变压器,所以表2的数值仍具有指导意义,后续实验对于选取的电容可参照表中的数值进行细微调整。
实验1充电时间总共为150min,电池从不足电量的10%的2.8V充至满电电压4.2V。值得注意的是曲线在电压上升到 3.7V时短时间跃升到 3.8V。这是因为充电芯片的内部检测电路检测到电池达到额定电压3.7V以后,充电模式由恒流方式变为了恒压方式,电压短时间提升至一个较高水平。随着充电电流逐渐下降,充电过程逐步放缓至整个过程完毕。
实验2使用了4.85mm厚度的猪皮作为线圈间隙,这与人体皮肤厚度和磁介质参数和厚度非常近似,具有更高参考价值,图7是完整的充电曲线示意图。
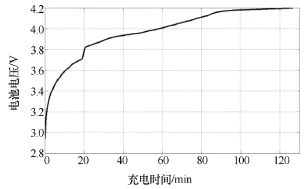
图7 TETS在4.85mm猪皮间隙下的完整充电曲线Fig.7 Charge curve of TETS under 4.85mm pig-skin interval
实验中,二次侧电路串入 36.6nF电容,TETS达到谐振。整个实验耗时126min。
5 结论
本文研究了利用感应式电能传输原理的 TETS作为心脏起搏器供能的方案。结合国内国际电磁标准,作者提出了使用 100kHz作为经皮变压器的工作频率;随后阐述了TETS的工作原理和组成部分,提出了经皮变压器的等效模型并对系统样机进行猪皮间隙的充电实验。结果表明,TETS在一次侧输入较低交流电压的情况下可以使锂离子二次电池在150min内从电力不足10%的2.8V充电至满电电压4.2V,从而维持心脏起搏器的正常运转。
[1]Robert E Fischell. The invention to the rechargeable cardiac pacemaker vignette[J]. IEEE Engineering in Medicine and Biology, 1990, 9(2): 77-78.
[2]Dr Orhan Soykan. Power sources for implantable medical devices[J]. Devices Technology & Applications Electronics, 2002(6): 76-79.
[3]Hideaki Abe, Hiroshi Sakamoto, Koosuke Harada. A noncontact charger using a resonant converter with parallel capacitor of the secondary coil[J]. IEEE Transactions on Industry, 2000, 36(2): 444- 451.
[4]Richard P Phillips. A transcutaneous energy transport system with voltage input for power control[J].Cardiovascular Mechanics, 1991, 13(5):2131-2132.
[5]David B Geselowitz, Quynh T N Hoang, Roger P Gaumond. The effects of metals on transcutaneous energy transmission system[J]. IEEE Transactions on Biomedical Engineering, 1992, 39(9): 928-934.
[6]Puers R, Vandevoorde G. Recent progress on transcutaneous energy transfer for total artificial heart systems[J]. Artificial Organs, 2001, 25(5): 400-405.
[7]Matsuki H, Shiiki M. Investigations of coil geometry for transcutaneous for artificial heart[J]. IEEE Transactions on Magnetics, 1992, 28(5): 2406-2408.
[8]Matsuki H. Transcutaneous DC-DC converter for totally implantable artificial heart using synchronous rectifier[J]. IEEE Transactions on Magnetics, 1996,32(5): 5118-5120.
[9]Hidekazu Miura, Shinsuke Arai, Fumihiro Sato, et al.A synchronous rectification using a digital PLL technique for contactless power supplies[J]. IEEE Transactions on Magnetics, 2005, 41(10): 3997-3999.
[10]Hidekazu Miura, Shinsuke Arai, Yasuyuki Kakubari,et al. Improvement of the transcutaneous energy transmission system utilizing ferrite cored coils for artificial hearts[J]. IEEE Transactions on Magnetics,2006, 42(10): 3578-3580.
[11]樊华,郑小林,皮喜田,等. 一种用于体内诊疗装置的无线能量传输方案[J]. 北京生物医学工程,2004,23(3): 168-170.Fan Hua, Zheng Xiaolin, Pi Xitian, et al. The application of wireless energy transmission in the micro-device inside human[J]. Beijing Biomedical Engineering, 2004, 23(3): 168-170.
[12]曹玉珍,武文君,范增飞. 植入式电子装置经皮感应充电方案[J]. 电子测量技术,2006,29(4): 19-20,32.Cao Yuzhen, Wu Wenjun, Fan Zengfei. Inductive charging design for implantable electronic device[J].Electronic Measurement Technology, 2006, 29(4):19-20, 32.
[13]陈海燕,高晓琳,杨庆新,等. 用于人工心中的经皮传能系统耦合特性及补偿研究[J]. 电工电能新技术,2008,27(2): 59-62.Chen Haiyan, Gao Xiaolin, Yang Qingxin, et al. Study on coupling characteristics and compensation of transcutaneous energy transmission system for artificial heart[J]. Advanced Technology of Electrical Engineering and Energy, 2008, 27(2): 59-62.
[14]陶发. 植入式生物遥测装置无线电能传输系统研究[D]. 南京:南京航空航天大学,2005.
[15]ACGIH[S]. Radiation Standard of America, 1984.
[16]电磁辐射防护规定[S]. 国家环境保护局, 1988.
[17]田民波. 磁性材料[M]. 北京:清华大学出版社,2001.
[18]于歆杰,朱桂萍,陆文娟. 电路原理[M]. 北京:清华大学出版社,2007.

