新型口服碳青霉烯类抗菌药物—泰吡培南酯
张文君 吴文芳 冯小龙
泰吡培南酯(Tebipenem Pivoxil)是日本明治制药株式会社研究开发的世界上第一个口服碳青霉烯类抗生素,于2009年8月26日在日本上市。泰吡培南酯是泰吡培南的前药,对革兰阳性和革兰阴性菌均具有较强的抗菌活性,对金黄色酿脓葡萄球菌、链球菌属、肺炎球菌、粘膜炎莫拉菌(布兰汉氏球菌属)、流感菌敏感,对青霉素敏感或耐药肺炎链球菌和流感嗜血菌的疗效较好,用于儿科患者耳鼻喉和上呼吸道感染的治疗,包括持续性中耳炎和细菌性肺炎,本文将该药介绍如下。
1 药品基本信息
1.1 中文化学名 新戊酰氧基甲基(1R,5S,6S)-6-[(1R)羟乙基]-1-甲基-2-[1-(1-(2-噻唑啉-2-基)氮杂环丁烷-3-基硫代]-1-碳青霉-2-烯-3-羧酸脂。
1.2 英文化学名 (1R,5S,6S)-6-[1(R)-Hydroxyethyl]-1-methy-2-[1-(2-thiazolin-2-yl)azeti-din-3-ylsulfanyl]-1-carba-2-penem-3-carboxylic acid pivaloylo-Xymethyl ester。
1.3 化学结构式
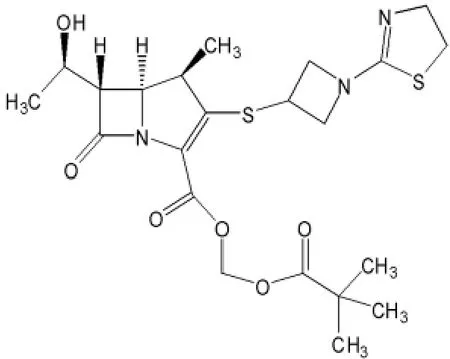
1.4 分子式 C22H31N3O6S2。
1.5 分子量 497.6302。
1.6 产品性状 本药品为结晶性粉末,易溶于甲醇和乙腈中,难溶于水,无吸湿性。
1.7 用法与用量 正常情况下,儿童用泰吡培南酯每日服用2次,每次4 mg(滴定率)/kg,饭后口服。必要时可增至一次6 mg(滴定率)/kg。
1.8 适应证 肺炎、中耳炎、副鼻腔炎。
2 合成路线
2.1 第1种合成路线 由化合物Ⅰ(1R,5R,6S)-6-[(1R)-1-羟乙基]-2-[(二苯基磷酰基)氧基]-1-甲基-碳青霉-2-烯-3-甲酸对硝基苄酯与化合物Ⅱ3-巯基-1-(1,3-噻唑啉-2-基)氮杂环丁烷盐酸盐反应生成化合物Ⅲ,化合物Ⅲ经氢化还原生成化合物Ⅳ,化合物Ⅳ和特戊酰碘甲酯或特戊酰氯甲酯反应生成目标化合物Ⅴ[1-4]。

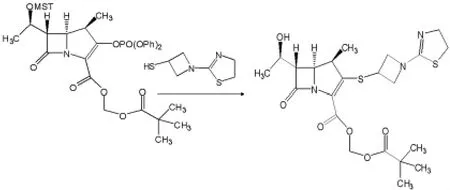
2.2 第二种合成路线 由化合物Ⅵ(1R,5R,6S)-6-[(1R)-1-羟乙基]-2-二苯基磷酰氧基-1-甲基-碳青霉-2-烯-3-羧酸新戊酰氧基甲酯与化合物3-巯基-1-(1,3-噻唑啉-2-基)氮杂环丁烷盐酸盐反应生成目标化合物Ⅴ[5,6]。
3 药效学研究
泰吡培南酯是泰吡培南的前药,是一种对呼吸道、泌尿道具有高效、广谱的新型的口服碳青霉烯抗菌素。给大鼠服用泰吡培南酯和泰吡培南的生物利用度分别为 38.1%,0.8%[1,7]。和β-内酰胺类抗生素相比,泰吡培南对肺炎链球菌显示了高效的抗菌活性。泰吡培南对青霉素易感菌株、青霉素中度敏感菌株以及耐青霉素菌株的MIC 90值分别为0.002、0.004~0.016和 0.063 μg/ml。对耐药菌株显示了杀菌活性[8]。
在体外实验中,泰吡培南对厌氧菌的抗菌活性和亚胺培南、头孢妥仑酯、阿莫西林/克拉维酸和克拉霉素进行了比较。在所有的抗微生物药物试验中,泰吡培南显示了最好的活性,分离株的MIC 90值小于(0.03~2)μg/ml,不包括痤疮丙酸杆菌、艰难梭菌、狄氏拟杆菌。尤其是泰吡培南对消化链球菌属、芽胞杆菌属、梭杆菌属和韦荣球菌属的临床分离株的抗菌活性比亚胺培南高2~16倍。接种体大小对泰吡培南的活性有很小的影响,它对脆弱杆菌产生的β-内酰胺酶稳定[7]。
在泰吡培南对临床分离株的体外活性试验中,其中包括耐万古霉素的金黄色葡萄球菌,将泰吡培南对青霉素结合蛋白的亲和力与头孢托仑和其他抗菌药物进行了比较。在所有菌体试验中,泰吡培南再次表现出良好的活性(MIC 90=0.025~6.25 μg/ml),除了对耐万古霉素的屎肠球菌(MIC 90=100 μg/ml);泰吡培南对各类青霉素结合蛋白(PBPs)的抑制机制与亚胺培南相似,但是其中PBP2和PBP3有所不同,泰吡培南对耐甲氧西林金黄色葡萄球菌的PBP2和大肠杆菌中的PBP3的活性分别比亚胺培南高10倍和5倍[9]。
泰吡培南对呼吸道感染的临床分离株的抗菌活性也在体外进行了研究,包括肺炎链球菌(52例)、化脓性链球菌(19例)、流感嗜血杆菌(50例)和肺炎杆菌(53例)。泰吡培南的抗菌活性(MIC 90 <0.006 ~0.39 μg/ml)比亚胺培南、头孢地尼和法罗培南高2~64倍。泰吡培南对各种产生β-内酰胺酶的菌株也显示了较强大的活性,不包括产生碳青霉烯酶菌株,并且对耐青霉素的肺炎链球菌和流行性感冒杆菌有强的浓度依赖的亚抑菌后效作用(PAE)(分别为1/4的最低抑菌浓度为6 h和1/2的最低抑菌浓度为9.2 h)。泰吡培南对青霉素结合蛋白1A,1B,2A/2X,2B和PRSP(耐青霉素肺炎链球菌)HSC-3 的亲和力很高,半抑菌浓度值分别为 0.12、0.08、0.16、0.05和 0.01 μg/ml。泰吡培南对青霉素结合蛋白 1B,2,3A,和流行性感冒杆菌Lj5的3B也有很高的亲和力,IC 50值分别为0.05、0.01、0.12 和 0.10 μg/ml。泰吡培南对尿道感染引起的病菌比如大肠杆菌,也显示了很好的活性(MIC 90=0.05 μg/ml)。泰吡培南相比于亚胺培南对肾二肽脱氢酶的水解相当稳定。因此,研究显示泰吡培南比亚胺培南、法罗培南和头孢地尼对呼吸和尿路感染引起的大多数病菌具有更强大的活性[10,11]。
用415个耐β-内酰胺酶的肠杆菌菌株测定对泰吡培南、头孢泊肟、环丙沙星、四环素、磷霉素和复方磺胺甲基异恶唑的敏感性。临床分离株的生长被1 μg/ml或更少的泰吡培南抑制,而对比者的抑制率范围为从磷霉素的23%到头孢泊肟的99.5%[12]。
泰吡培南、亚胺培南和头孢托仑对PRSP(耐青霉素肺炎链球菌)、甲氧西林敏感菌和耐甲氧西林金黄色葡萄球菌、大肠杆菌、肺炎克雷伯菌、弗氏柠檬酸杆菌、摩氏摩杆菌、流感嗜血杆菌和粘膜炎微球菌临床菌株活性被进行了对比。泰吡培南相比于其他抗生素,抗菌活性更高,MIC 90值为 0.025~6.25 μg/ml,该药具有杀菌活性[13]。
泰吡培南、亚胺培南和口服头孢菌素对来自呼吸道感染的儿童的肺炎链球菌、流感嗜血杆菌、酿脓链球菌、无乳链球菌和粘膜炎微球菌菌株的活性进行了比较。泰吡培南普遍具有超高活性(MIC 90=0.002 ~0.25 μg/ml)。对耐青霉素肺炎链球菌具有杀菌活性[14]。
泰吡培南、亚胺培南、头孢地尼、头孢托仑和头孢泊肟对产生β-内酰胺酶的大肠杆菌、肺炎克雷伯杆菌临床菌株的活性进行了研究。泰吡培南(0.06 μg/ml)泰吡培南(0.06 μg/ml)对产生A型和C型酶的菌株有效,不包括B型和MOX-1型酶[15]。
对肺炎链球菌、流感嗜血杆菌和黏膜炎微球菌菌株的研究表明,泰吡培南在较低的pH值环境下活性更好。大多数菌株被人类菌株杀死,泰吡培南和血清有协同作用[16]。
同法罗培南、头孢地尼、头孢托仑和阿莫西林相比较,泰吡培南对青霉素敏感菌、耐青霉素肺炎链球菌、黏膜炎微球菌和嗜肺军团菌的活性是这些药的4~256倍(MIC 90=0.032~0.125 μg/ml)。并且也显示了对流感嗜血杆菌的活性(MIC 90=0.25 μg/ml)。对患有耐青霉素链球菌的呼吸道感染的小鼠服用泰吡培南(10 mg/kg,3次/d,3 d),则小鼠的呼吸频率明显降低。虽然泰吡培南本质上在体外治疗流感嗜血上活性逊于头孢托仑,但是在患有这种菌造成的呼吸疾病的小鼠的治疗上,治疗效果相似[17]。
泰吡培南对甲氧西林敏感菌葡萄球菌、肺炎链球菌、大肠杆菌、肺炎克雷伯菌、流感嗜血杆菌、嗜肺军团菌和黏膜炎微球菌表现了强大的抗菌活性(MIC 90=1 μg/ml or less)。泰吡培南酯对青霉素敏感菌肺炎链球菌TUH39(ED50=1.95 mg/kg,口服)、PRSP TUM741和流感嗜血杆菌TUM8引起的小鼠呼吸道感染疾病,优于亚胺培南、法罗培南、头孢托仑酯、头孢地尼、阿莫西林和盐酸左氧氟沙星[18]。
在由PRSP引起的中耳炎灰鼠模型试验中,泰吡培南酯在提高其成活率方面优于阿莫西林,同样体现在细菌清除方面[19]。
4 药代动力学
呼吸道感染的小鼠的肺和血清的Cmax、AUC和t1/2分别为9.03 μg/g 和 51.24 μg/ml,31.0 μg · h-1· ml-1和142.2 μg·h-1·ml-1和 6.18 h 和 3.88 h[20]。灰鼠的临床前研究显示,泰吡培南酯的 Cmax为 7.2 μg/ml,tmax为 0.67 h,t1/2为0.43 h[19]。
通过大腿和肺部感染的小鼠对泰吡培南酯的药代特性进行了研究。在大腿和肺部感染模型试验中,AUC/MIC,Cmax/MIC和t1/2/MIC值均表现出了良好效果相关性,特别是AUC/MIC和Cmax/MIC值。这些PK/PD结果在112例患耳鼻疾患的患者Ⅱ期临床治疗中得到了证实[21]。
健康男性受试者单剂量服用泰吡培南酯25~200 mg,多剂量服用100 mg或200 mg,每天3次,服用7 d。在单剂量研究中,AUC跟剂量成线性关系,Cmax和剂量成比例关系直至150 mg,tmax和t1/2都是大约30 min。药物吸收不受食物影响。通过尿液排泄的药物占剂量的54%~73%。多剂量药动学参数同样如此,只是有部分的代谢(剂量的10%)。具有好的耐受性[22]。
5 安全性
对大鼠和小鼠的研究证实,泰吡培南酯对盲肠菌群具有很微小的影响。体外试验显示,泰吡培南酯对盲肠内容物稳定,但是它的活性代谢物被大鼠的盲肠内容物水解[23,24]。
6 临床研究
临床结果显示,泰吡培南酯在不考虑剂量的情况下可去除全部的肺炎链球菌和85.7%的流感嗜血球菌。泰吡培南酯对所有情况下的急性中耳炎有效,对93.8%情况下的剂量为500 mg的急性鼻窦炎有效。没有严重不良事件发生。最已发生的是腹泻和便溏。不良事件一般发生在推荐剂量在500 mg/d的情况下[25]。
1 Abe T,Hayashi K,Mihira A,et al.L-084,a new oral carbapenem:Synthesis and structure-activity relationships of C2substituted 1beta-methylcarbapenems.38th Intersci Conf Antimicrob Agents Chemother(ICAAC),(Sept 24-27,San Diego),1998,Abst F-64.
2 Isoda T,Sato C,Mihira A,et al.(Wyeth-Lederle Japan,Ltd.).2-(1-(1,3-Thiazolin-2-yl)azetidin-3-yl)thiocarbapenem derivatives.EP 0632039,EP 0717042,JP 1996053453,US 5534510,US 5659043,US 5783703.
3 Kumagai T.(Wyeth-Lederle Japan,Ltd.).Carbapenem-3-carboxylic acid ester derivatives.EP 0808315,JP 1999504039,US 5886172,WO 9721712.
4 Yasuda S,Okue M,Hori N.(Meiji Seika Kaisha,Ltd).Process for producing carbapenem derivative and intermediate for use in the production.WO 2004035539.
5 Nishino K,Koga T.(Kaneka Corporation).Process for producing carbapenem compound for oral administration.EP 1580191.
6 西野敬太,古贺照义.经口给药用碳青霉素烯化合物的新的合成中间体及其制造方法.CN1708504A.
7 Kato N,Kato H,Tanaka K,Watanabe K.L-084,a new oral carbapenem:In vitro activity against anaerobic bacteria.38th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Sept 24-27,San Diego),1998,Abst F-70.
8 Kobayashi R,Konomi N,Hasegawa K,et al.In vitro antivity of tebipenem,a new oral carbapenem antibiotic,against penicillin-nonsusceptible Streptococcus pneumonia.Antimicrob Agents Chemother,2005,49:889-894.
9 Hanaki H,Sasaki K,Inaba Y,et al.L-084,a new oral carbapenem:In vitro activity against clinical isolated strains including vancomycin low-restraint Staphylococcus aureus and its binding affinity to PBPs.38th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Sept 24-27,San Diego),1998,Abst F-66.
10 Hikida M,Itahashi K,Igarashi A,et al.In Vitro antibacterial activity of LJC 11,036,an active metabolite of L-084,a new oral carbapenem antibiotic with potent antipneumococcal activity.Antimicrob Agents Chemother,1999,43:2010-2016.
11 Hikida M,Itahashi K,Shiba T,et al.L-084,a new oral carbapenem:In vitro antibacterial activity.38th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Sept 24-27,San Diego),1998,Abst F-65.
12 Muratani T,Kobayashi T,Matsumoto T.In vitro activities of tebipenem against Enterobacteriaceae isolated with broad-spectrum beta-lactamase.45th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Dec 16-19,Washington,D.C.).2005,Abst F-1160.
13 Nishion T,Yoshida M.L-084,a new oral carbapenem:In vitro activity.38th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Sept 24-27,San Diego),1998,Abst F-67.
14 Igarashi A,Hikida M,Ubukata K.L-084,a new oral carbapenem:Comparative antimicrobial activity of carbapenem with other beta-lactams for clinically isolated organisms.38th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Sept 24-27,San Diego),1998,Abst F-68.
15 Inque M,Kuga A,Sato Y,et al.L-084,a new oral carbapenem:In vitro antibacterial activity against clinical isolates of beta-lactamase producers.38th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Sept 24-27,San Diego),1998,Abst F-63.
16 Hikida M,Itahashi K,Igarashi A,et al.Susceptibilities of causative organisms of respiratory tract infections to L-084,a new oral carbapenem owing to medium pH and serum.39th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Sept 26-29,San Francisco),1999,Abst 387.
17 Miyazaki S,Hosoyama T,Furuya,N,et al.L-084,a new oral carbapenem:In vitro and in vivo antibacterial activity.38th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Sept 24-27,San Diego),1998,Abst F-69.
18 Miyazaki S,Hosoyama T,Furuya N,et al.In vitro and in vivo antibacterial activities of L-084,a novel oral carbapenem,against causative organisms of respiratory tract infections.Antimicrob Agents Chemother,2001,45:203-207.
19 Sugano T,Morita J,Yoshida T,et al.Unique pharmacokinetic/pharmacodynamic property of a novel carbapenem,tebipenem in murine thigh and lung infection models.45th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Dec 16-19,Washington,D.C.),2005,Abst F-1448.
20 Itahashi K,Fukushima T,Nagura J,et al.Efficacy of tebipenem pivoxil(ME1211)on acute otitis media in chinchilla caused by penicillin-resistant Streptococcus pneumoniae(PRSP).45th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Dec 16-19,Washington,D.c.),2005,Abst B-738.
21 Totsuka K,Furukawa M,Furuya N,et al.PK/PD analysis of tebipenem pivoxil(ME1211),a novel oral carbapenem,in otolaryngological infections,a phase Ⅱ clinical trial(3).45th Intersci Conf Antimicrob A-gents Chemother(ICAAC)(Dec 16-19.Washington,D.C.),2005,Abst L-579.
22 Yokokawa M,Yano M,Nakashima M.L-084,a new oral carbapenem:Pharmacokinetics and tolerance observed in the phase Ⅰstudies.39th Intersci Conf Antimicrob Agents Chemother(ICAAC)(Sept 26-29,San Francisco),1999,Abst 388.
23 Liu CX,Kato N,Watanabe K,et al.Impact of a new quinolone,DU-6859a,and two oral carbapenems,CS-834 and L-084,on the rat and mouse caecal microflora.J Antimicrob Chemother,2000,46(5):823-826.
24 Liu C,Kato N,Watanabe K.Impact of a new quinolone and two oral carbapenems on the rat and mouse cecum flora.100th Gen Annu Meet Am Soc Microbiol(ASM)(May 21-25,Los Angeles),2000,Abst A-9.
25 Yamanaka N,Furukawa M,Furuya N,et al.Clinical efficacy of tebipenem pivoxil(ME1211),a novel oral carbapenem,in otolaryngological infections,a phase Ⅱ clinical trial(1).45th Intersci Conf Antimicrob A-gents Chemother(ICAAC)(Dec 16-19,Washington,D.C.),2005,Abst L-577.

