干扰素治疗乙肝病毒相关性肾炎的Meta分析
曹春蕊 尹胜杰 白玉如 于岩岩
HBV是具有泛嗜性的病毒,以感染肝组织为主,此外,还可感染多种组织和器官,造成相应的病变,如乙肝病毒相关性肾炎(乙肝肾),患者可出现肾功能损害,乙肝肾最常见的病理学改变是膜性肾小球肾炎及膜性增殖性肾病。对于乙肝肾的治疗,以往以糖皮质激素为主,主要目的在于降低尿蛋白,激素虽能控制尿蛋白,但长期应用,乙肝病毒复制增加,有加重肝炎的可能。中药治疗乙肝肾目前也缺乏循证医学的证据。目前,乙肝肾的治疗已经转变为以抗病毒治疗为主,抗HBV的药物主要包括两大类,即干扰素类和新的核苷(酸)类似物,干扰素是最早应用的抗HBV药物,已经有一些治疗乙肝肾的临床报道,因此我们对干扰素治疗乙肝肾的临床实验进行了Meta分析,以评价干扰素治疗乙肝肾的效果,为临床选择治疗方案提供较为合理的依据。
1 资料与方法
1.1 文献纳入标准及排除标准 文献以随机对照实验、队列研究和临床对照试验为研究对象,并提供病例入选标准[1,2]:(1)血清HBsAg阳性;(2)患肾小球肾炎,并可除外狼疮性肾炎等继发性肾小球疾病;(3)肾组织切片上有HBV抗原。其中第3条为必备条件。对肾组织切片上有 HBsAg存在,血清中HBsAg阴性者,亦可诊断为乙肝病毒相关性肾炎。排除标准:排除非病例对照试验、质量评分低的研究、重复发表及不符合纳入标准的文献[3]。研究方案:研究组为干扰素治疗,剂量可因人而异(按体表面积计算),疗程3个月以上。对照组为对症治疗。疗效判定标准以治疗结束时的结果为准,主要统计尿蛋白阴转率,随访时的疗效作为参考。文献质量要求Jadad评分≥3分。随访年限要求6个月以上。
1.2 检索的数据库及检索方法 由两名研究者独立进行文献质量评估及交叉核对。检索的数据库包括Pubmed、Cochrane、Embase、OVID、CNKI、CBM 和学位论文,手工检索现有临床资料及会议论文。文献检索方法:英文检索词为interferon,nephritis或 membranous Glomerulonephritis,并 以 human、Meta-analysis、randomized controlled trial、clinical controlled trial、cohort study 和English限制。中文检索词为干扰素、乙肝相关性肾炎、随机对照试验和临床对照试验。
1.3 异质性检验 采用STATA 9.0软件进行分析。对各研究组的尿蛋白好转率的优势比(OR)值进行异质性检验。如果OR齐性,采用固定效应模型M-H法做合并效应量估计。如果OR非齐性,则采用随机效应模型进行分析。异质性检验时,以P<0.05认为资料具有异质性。
1.4 发表偏倚的评估 以纳入分析的各研究的OR值为横坐标,logOR值为纵坐标绘制漏斗图,根据其对称性评估发表偏倚,并以Egger偏倚线性回归方法分析发表偏倚。P>0.05提示无发表偏倚。
2 结果
2.1 文献入选情况 共纳入5篇,其中队列研究3篇,随机对照实验1篇,临床对照实验1篇,涉及患者72例。各项研究的临床资料见表1、2。将各研究的数据输入STATA 9.0软件,进行Meta分析后的结果见表3。

表1 纳入分析的各研究的基本情况
2.2 发表偏倚 虽然纳入的研究较少,但漏斗图基本对称,提示存在发表偏倚的可能性较小。以STATA9.0软件进行Egger偏倚线性回归分析,P=0.668,P>0.05提示无发表偏倚。见图1。
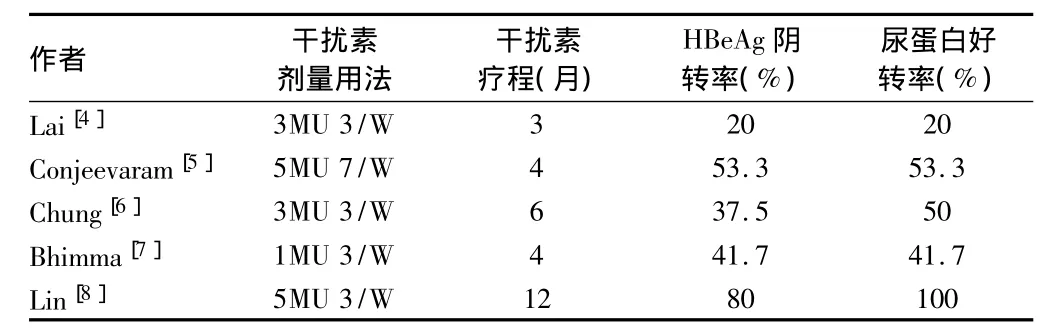
表2 临床实验设计
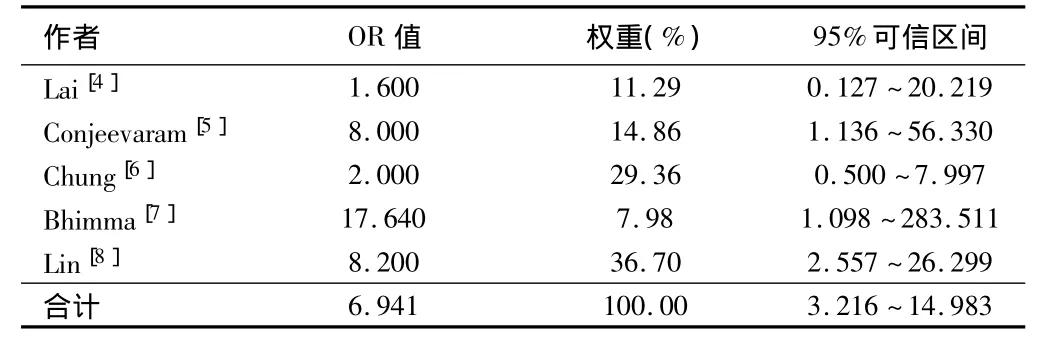
表3 各研究的OR值及95%可信区间

2.3 研究结果 总的尿蛋白好转率是53%,各研究合并的OR值为6.358,95%可信区间:3.033~13.330,应用固定效应模型检验,χ2=4.57,P=0.335 ,I2=12.4%,P >0.1,显示各研究具有同质性。即干扰素治疗乙肝肾可明显使尿蛋白好转。
2.4 敏感度分析 敏感度分析显示,较长疗程(6~12个月)及较高剂量(IFN-a 5 MU,7/W)的治疗未显示出更好的治疗效应。将Jadad评分为高质量的文献[8]排除后,其余文献进行敏感度分析,结果表明,IFN-a治疗乙肝肾的效应无显著改变。
2.5 不良反应 临床上最常见的不良反应是“流感样”症状,包括发热、寒战、肌痛、关节痛、头痛和乏力等。这些症状大多发生在治疗开始的前3 d内,并随着剂量的增加而加重,绝大部分患者能够耐受。中性粒细胞减少症及血小板减少性紫癜也有发生。其他常见不良反应包括脱发、体重减轻、情绪低落等。本组文献未报道发生失代偿期肝疾病及肝功能衰竭事件。6例患者因不良反应较重退出实验,总退出率8.3%。
3 讨论
干扰素作为免疫调节抗病毒药,治疗乙肝肾可使HBeAg阴转,HBV-DNA阴转,部分患者甚至达到HBsAg阴转。我们知道,细胞免疫低下、HBeAg和 HBV-DNA与乙肝肾的发病机制有关[9-12],故调节免疫抗病毒是治疗乙肝肾的关键。核苷类药物虽能有效降低HBV-DNA,但HBeAg及HBsAg阴转率较干扰素低,且大部分核苷类药物无儿童用药经验,对乙肝肾的疗效有待进一步的临床试验证实。我们进行的Meta分析结果表明,干扰素治疗乙肝肾可有效控制尿蛋白,疗效确切,长期随访,效果稳定,无严重不良反应出现。尿蛋白阴转还可能与HBeAg阴转有关,希望以后能进行尿蛋白阴转和HBeAg阴转(或HBV-DNA阴转)相关关系的回归分析。各研究的病例退出率极低,也说明试验方法安全有效。本研究结果可为临床治疗提供参考。但由于以下几方面原因,应用以上分析结果仍需慎重:(1)纳入的试验多质量低下,随机对照试验未描述随机化方法、随机分配方案的隐藏及盲法评估。(2)样本含量小,直接影响试验的质量,也有可能出现实验结果的偏差。(3)仅以尿蛋白作为评价肾功能的指标,未能完全统一到肾小球滤过率。(4)本研究仅检索应用中文及英文发表的相关文章,而其他语种有可能发表阴性结果的研究。
1 Johnson RJ,Couser W.Hepatitis B infection and renal disease:clinical,immunopathogenetic and therapeutic considerations.Kidney Int,1990,37:663-676.
2 Hattori S,Furuse A,Matsuda I.Presence of HBe antibody in glomerular deposits in membranous glomerulonephritis is associated with hepatitis B virus infection.Am J Nephrol,1988,8:384-387.
3 杨青,庄捷秋,林瑞霞,等.小儿乙肝病毒相关性膜性肾病临床病理特征和治疗.中国中西医结合肾病杂志,2003,4:706.
4 Lai KN,Li PKT,Lui SF,et al.Membranous nephropathy related to hepatitis B virus in adults.N Engl J Med,1991,324:1457-1463.
5 Conjeevaram HS,Hoofnagle JH,Austin HA,et al.Long-term outcome of hepatitis B virusrelated glomerulonephritis after therapy with interferon alfa.Gastroenterology,1995,109:540-546.
6 Chung DR,Yang WS,Kim SB,et al.Treatment of hepatitis B virus associated glomerulonephritis with recombinant human alpha interferon.Am J Nephrol,1997,17:112-117.
7 Bhimma R,Coovadia HM,Kramvis A,et al.Treatment of hepatitis B virus-associated nephropathy in black children.Pediatr Nephrol,2002,17:393-399.
8 Lin CY.Treatment of hepatitis B virusassociated membranous nephropathy with recombinant alpha-interferon.Kidney Int,1995,47:225-230.
9 Lin CY.Hepatitis B virus-associated membranous nephropathy:clinical features,immunologic profiles,and outcome.Nephron,1990,55:37-44.
10 Bhimma R,Coovadia HM.Hepatitis B virus-associated nephropathy.Am J Nephrol,2004,24:198-211.
11 Ohba S,Kimura K,Mise M,et al.Differential localization of s and e antigens in hepatitis B virus-associated glomerulonephritis.Clin Nephrol,1997,48:44-47.
12 Chingyuang Lin,Chiou Chyn Lin,Gwong Jen J.et al.Defect of Cell-Mediated Immune Response against Hepatitis B Virus:An Indication for Pathogenesis of Hepatitis-B-Virus-Associated membranous nephropathy.Nephron,1997,76:176-185.

