糖尿病对急性心肌梗死患者心室功能的影响
张莉 傅向华 李俊峡
随着人们生活水平日益提高,糖尿病及冠心病的发病率逐年上升,糖尿病被认为是冠心病的等位症,并且是影响冠心病预后的独立危险因素。本文就糖尿病对急性心肌梗死(AMI)患者心功能的影响进行研究。
1 资料与方法
1.1 一般资料 选取2001年12月2007年6月我院住院AMI患者126例,其中男101例,女25例;平均年龄(59±11)岁。入选患者符合下列标准:入选者根据有无糖尿病史分为糖尿病组(36例)和非糖尿病组(90例)。
1.2 入选和排除标准 (1)入选标准:连续胸痛超过30 min;心电图超过两个导联ST段抬高,心肌酶增高和(或)肌钙蛋白阳性。(2)糖尿病诊断标准:空腹血糖>7.1mmol/L;餐后2 h血糖11.1mmol/L。(3)排除标准:有陈旧性心肌梗死(包括既往有明确病史或心电图表现)者;严重的瓣膜性心脏病、扩张型和肥厚型心肌病者;中重度肾功能不全者;既往无糖尿病史,入院后血糖高于正常。
1.3 平衡法核素心血池显像判定左心室功能及心室收缩同步性。AMI发病后2~7 d采用}Tc体内红细胞标记法,被检者静脉滴注20mg亚锡焦磷酸盐(北京师范大学),30 min后再注入示踪剂99mTcO4~740 MBq(20 mci)(北京中国原子能所),待标记红细胞5~10 min,99mTc-红细胞在血液中分布达到平衡后即行平衡法核素心血池显像采集。被检者取仰卧位,以左前斜(LAO)30~450(左右室最佳分割位)进行图像数据采集,每个心动周期采集32帧,总计数8000 K,矩阵为64×64,在采集过程中剔除异常心跳或伪信号的干扰,采集完成后全部数据资料存盘。计算左心室功能并进行相位分析。
1.3.1 左心室功能参数:采用SOPHY计算机系统的心血池程序软件,半自动化勾画出左心室的舒张末感兴趣区经扣除收缩末本底后分别得出左心室时间-放射性活度曲线,按计数-容量法原理,根据心动周期舒张末期和收缩末期的计数得出左心室收缩功能和左心室舒张功能参数。左心室收缩功能参数包括左心室射血分数(LVEF),左心室峰射血率(LPER),左心室峰射血率时间(TPER)。LVDF参数包括左心室峰充盈率(PFR),左心室峰充盈时间(TPFR)。
1.3.2 相位分析及心室收缩同步性(VSS)参数:应用SOPHY心血池程序相位分析软件,以相位和振幅值表示局部室壁收缩的时间顺序和活动幅度,得到相位图和振幅图以及可供定量比较的参数。以横坐标代表一个完整的心动周期,以360°表示,纵坐标表示心室相同相位的频度,相位直方图呈正态分布并与相位图呈严格的对应关系,两者色阶呈一致性变化。测定相位直方图基底的起点与止点,得到定量的心室收缩同步性参数:心室相角程(PS);测量相位直方图的1/2高宽得到半高宽(FWHM)及峰相位标准差(PSD),单位为度。
1.4 统计学分析应用SAS 8.0统计软件,计量资料以表示,采用t检验计数资料采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 糖尿病组和非糖尿病组患者临床特点比较 2组年龄、性别比、血脂、既往史及个人史差异无统计学意义(P>0.05)。见表1。

表1 2组临床特点比较
2.2 糖尿病对左心室收缩及舒张功能的影响 伴有糖尿病的AMI患者心功能不全的发生率明显增加(55.55%vs 35.55%,P<0.05),心脏收缩及舒张功能均显著受损,而其心室收缩同步性参数比无糖尿病患者显著减低。见表2。
表2 2组左心室收缩及舒张功能比较
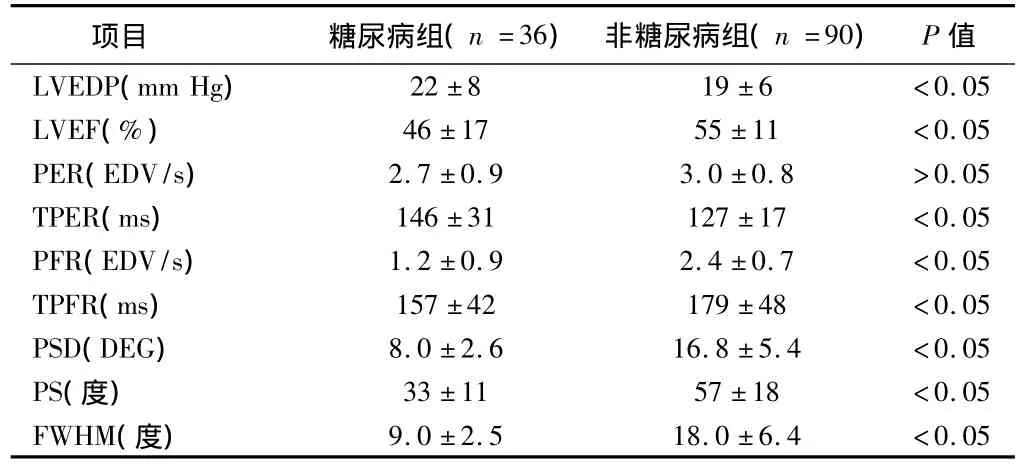
表2 2组左心室收缩及舒张功能比较
项目 糖尿病组(n=36) 非糖尿病组(n=90) P值LVEDP(mm Hg)22±8 19±6 <0.05 LVEF(%) 46±17 55±11 <0.05 PER(EDV/s) 2.7±0.9 3.0±0.8 >0.05 TPER(ms) 146±31 127±17 <0.05 PFR(EDV/s) 1.2±0.9 2.4±0.7 <0.05 TPFR(ms) 157±42 179±48 <0.05 PSD(DEG) 8.0±2.6 16.8±5.4 <0.05 PS(度) 33±11 57±18 <0.05 FWHM(度)9.0±2.5 18.0±6.4 <0.05
3 讨论
近年的流行病学调查显示,糖尿患者群高血压、心肌梗死及心力衰竭的发生率显著高于非糖尿患者群[1]。糖尿病被认为是冠心病的等位症。并且是影响冠心病预后的独立危险因素。本研究已表明:伴有糖尿病的AMI患者心功能不全的发生率明是增加(P<0.05)。且收缩功能和舒张功能全面受损。
在本研究中,伴有糖尿病的AMI患者较无糖尿病者LVEF下降17.43%,TPER延迟15.45%。这是由于AMI时部分心肌坏死,同时由于顿抑心肌、冬眠心肌的存在,心肌收缩功能显著受损,糖尿病并存的血脂异常加重了冠状动脉的损伤[2],弥漫的冠状动脉病变、多支病变和微血管瘤是糖尿病患者冠状动脉的特征性改变[3]。此外无论是胰岛素依赖型糖尿病还是非胰岛素依赖型糖尿病均由于自主神经系统功能障碍而易发生隐性心肌缺血[4,5]。因此AMI伴发糖尿病患者的非梗死区域同样存在缺血心肌,冠状动脉储备功能受损严重,因此收缩功能受损较无糖尿病者更加严重。
同时,糖尿病还可显著加重AMI患者的舒张功能障碍,使PFR减小50%。其机制可能为:(1)心肌内所有细胞都可能受蛋白糖基化作用的影响,其可使蛋白质和胶原变性,导致胶原之间以及与心肌纤维和其他结构蛋白的交联增加,降低动脉管壁及心室的顺应性,使心肌舒张功能减弱[6]。甚至在无缺血性心脏病的糖尿病患者中也可见到心肌纤维化或连接异常增殖[7,8]。(2)心脏信号转导蛋白的糖基化及其他的糖基化产物会导致活性氧化物质(ROS)增多,影响钙离子通道的平衡及线粒体功能,导致细胞凋亡[9]。(3)高血糖还使心脏局部肾素-血管紧张素系统激活,以自分泌和(或)旁分泌的方式发挥多效性作用,促进血管收缩;诱导具有生长刺激性的原癌基因c-fos、cjun、c-m yc 等和转化生长因子-β(TGF2β)基因表达,刺激心肌细胞和血管的生长,特别是胶原的合成,胶原的堆积可增加心肌舒张阻力,使心肌僵硬。(4)心肌细胞间质过碘酸-schiff(PAS)染色阳性物质、脂类物质、糖蛋白等的沉积,都可使心肌顺应性降低,从而出现以心室舒张早期充盈受损、等容舒张时间延长、心房负荷增加为特征的左心室舒张功能损害。(5)很多学者认为糖尿病患者心脏舒张功能减退还与心肌微血管病变和代谢障碍有关[10]。
心室收缩同步性同样是心室功能的重要指标,核素相位分析法能灵敏地反映心室收缩同步性[11,12],相位直方图用定量参数PS、PSD、FWHM来反映心室各局部的收缩的协调性和均匀性即整体收缩的同步性。PS反映心室最早和最晚的收缩相位差值,FWHM和PSD则反映着心室收缩的集中趋势和平均离散度,三者均是评价VSS的定量指标。通常情况下,PSD、PS、FWHM值的减低,提示心室收缩同步性增强,反之则减弱。但是我们可以看到本研究的结果是糖尿病伴AMI患者心室收缩同步性好于无糖尿病者,这是因为无糖尿病患者AMI时局部心肌坏死,甚至室壁瘤形成,因而导致心室收缩不均一,心室收缩同步性差,但是糖尿病患者除梗死区域外,心肌弥漫性受损,但是从表面看心室收缩同步性却优于无糖尿病组,这更加说明伴有糖尿病的AMI患者整体心室功能受损严重。
1 Fisher BM,Frier BM.Evidence for a specific heart disease of diabetes in humans.Diabetic Med,1990,7:478.
2 王怀祯,刘迎午,王禹.冠心病合并糖尿病患者冠状动脉造影临床分析.实用医学杂志,2005,21:2789-2790.
3 陈灏珠主编.心脏病学.第5版.北京:人民卫生出版,2000.1715-1739.
4 Sullivan J,Conroy R,MacDonald K.Silent ischemia in diabetic men with autonomic neuropathy.Br Heart J,1991,66:313-315.
5 Chipkin SR,Frid D,Alpet JS,et al.Frequency of painless yocardial ischemia during exercise tolerance testing in patients with or without diabetes mellitus.Am J Cardiol,1987,59:61-65.
6 Aljada A,Saadeh R,Assian E,et al.Insulin inhibits the exp res2sion of intercellular adhesion molecule21 by human aortic endothe2lial cells through stimulation of nitric oxide.J Clin Endocrinol Met,2000,85:2572-2575.
7 Perez JE,McGill JB,Santiago JV,et al.Abnormal myocardial acoustic properties in diabetic patients and their correlation with the severity of the disease.J Am Coll Cardiol,1992,19:1163-1164.
8 Van Hoeven KH,Factor SM.A comparison of the pathological spectrum of hypertensive, diabetic, and hypertensive-diabetic heart disease.Circulation,1990,82:848-855.
9 王燕燕,王晓,汪义军,等.血清TNF2α在胰岛素抵抗及微血管病变中的变化.医学研究生学报,2003,13:311-313.
10 Phillps RA,Goldman ME,Ardeljan M,et al.Determinants ofabnormal left ventricular filling in early hypertension.J Am Coll Cardiol,1989,14:979-985.
11 Mena I,Carmody J,Chelsy S,et al.Usefulness of phase analysis in nuclear medicine.J Nucl Med,1981,22:83-87.
12 毛焕元,曾林生主编.心脏病学.第2版.人民卫生出版社,2001.3:388-389.

