腹腔恶性纤维组织细胞瘤1例报告
马喜娟 汪秀玲 李绍东 李琳琳 徐 凯
1.徐州医学院附属医院影像科,江苏 徐州 221004 ; 2.病理科
腹腔恶性纤维组织细胞瘤1例报告
马喜娟1汪秀玲1李绍东1李琳琳2徐 凯1
1.徐州医学院附属医院影像科,江苏 徐州 221004 ; 2.病理科
腹腔;恶性纤维组织;细胞瘤
1 临床资料
患者 男,76岁,无明显诱因感右上腹胀痛不适1年余,伴反酸,呈间断性,近半月来腹胀加重,平卧后呼吸费力。查体:右中上腹部触及不规则肿块,质地较韧,囊实感,边界清,较为固定,无触痛,叩诊实音。
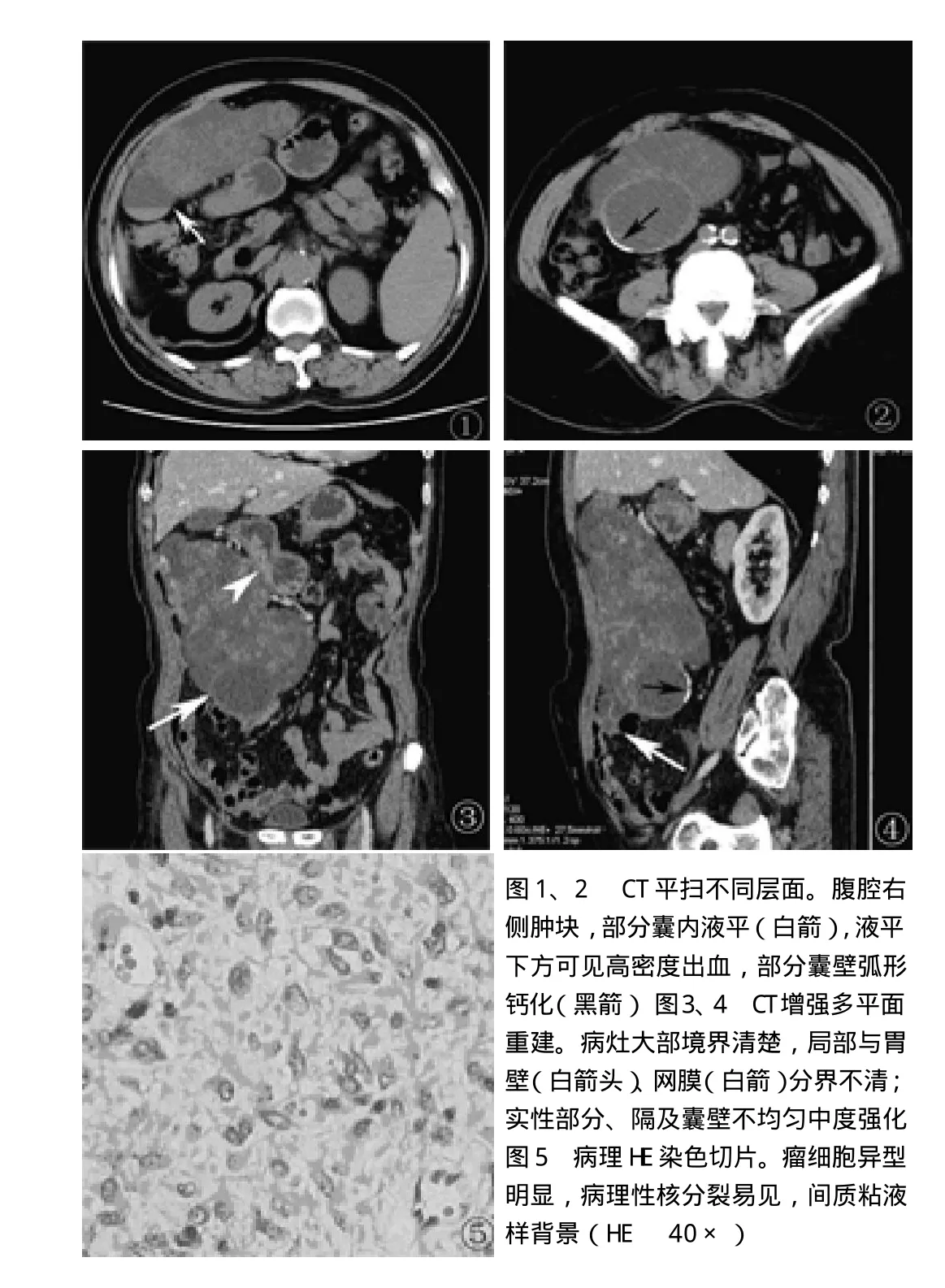
超声检查示上腹部不规则混合回声包块,边界清楚。CT检查:腹腔右侧巨大囊实性团块,约15.3cm×7.1cm×20.0cm,上自第一肝门水平,下至骶髂关节水平,部分跨中线生长,形态不规则,密度不均匀,实性部分平均CT值约55Hu,囊性部分平均CT值约16Hu,部分囊内可见液平,部分囊壁见弧形钙化(图1、2),增强扫描实性部分内示斑片样中度强化,分隔及囊壁呈中度强化(图3、4)。
手术所见:腹腔内巨大肿物,约15cm×8.0cm×20.0cm大小,境界大部清晰,较为游离,位于胃肠道的表面,肿块中下部与网膜间关系密切、粘连,肿块上部局限区域与胃前壁粘连较紧密,无法分清境界。肝脏、腹壁及盆腔未见转移结节。术后病理:巨检灰红结节样组织块,切面灰红、灰黄、灰白,部分呈鱼肉状,部分区域呈囊性,内含淡黄色清亮液体;镜下瘤细胞呈梭形或多角形,异型明显,病理性核分裂易见,间质有粘液样背景,胶原纤维及毛细血管丰富,炎细胞浸润(图5);免疫组化:溶菌酶 Lys(+),巨细胞抗体 CD 68(+),平滑肌标记物 SMA(-),结蛋白单抗 Des(-),S100(-);病理诊断:(腹腔)黏液型恶性纤维组织细胞瘤。
2 讨 论
恶性纤维组织细胞瘤(m a lignan t fib rous histiocytoma,MFH)为来源于间叶组织的恶性肿瘤,成分复杂、形态多变,多发生于老年人,以61岁-70岁为发病高峰,与性别无关,常见于四肢深部软组织,发生于腹腔者少见,文献多以个案报道介绍。组织学一般将其分为四种亚型:轮辐状-多形型、黏液型、巨细胞型、黄色瘤型MFH[1]。在各型MFH组织中,黏液变性> 50%以上即归入黏液型 MFH,该型术后复发率高,转移率低于轮辐状-多形型[1]。
M FH的影像学表现无特异性,CT平扫表现为界限不清或清楚的软组织肿块,病灶内的低密度区可以是黏液样变、出血或坏死[2],病灶内可有钙化,为多团块状或环形偏心性钙化,亦可有脂肪成分;增强扫描后病灶大部分呈中-高度强化,实性部分表现为结节样和周边的强化[3];大部分M FH为周围血管分支多重供血[2];腹腔M FH需要与畸胎瘤、脂肪肉瘤、平滑肌肉瘤鉴别。畸胎瘤通常脂肪成分和钙化同时存在,而脂肪肉瘤表现为脂肪密度及索条状与结节状软组织密度影,一般病灶内无出血,增强扫描时无明显强化,可资鉴别,但是当脂肪肉瘤分化差,其内没有脂肪成分时鉴别较困难;平滑肌肉瘤中心性坏死通常较大,很少出现钙化,增强扫描呈周边强化。
本例病灶位于肝脏下方,CT多平面重建显示其大部境界清楚,局部与网膜间及胃前壁境界不清,其邻近胃壁的形态、轮廓、密度均未见异常改变,可以排除原发于胃的可能,而应定位于网膜或肠系膜,囊性部分CT值较高部分为肿瘤黏液成分及出血改变。本例M FH供血血管为肝固有动脉和胰十二指肠动脉分支,可见到环形偏心钙化,与文献报道一致[2,3],但并未见到脂肪成分。
腹腔内较大或巨大肿块,含钙化、囊变,无或含少量脂肪,且呈不均匀中度强化时应考虑MFH,CT多平面重建(MPR)能较好显示肿块部位、形态、大小及与周围组织的关系(图3、4),MRI对显示内部出血及脂肪有特殊优势,确诊要靠穿刺活检或手术病理。
1 刘筱,江瑞康.软组织恶性纤维组织细胞瘤3例并文献分析[J], 中国误诊学杂志, 2008,8(7):1733.
2 Chen HC, Chen CJ, Jeng CM, et al.Malignant fibrous histiocytoma presenting as hemoperitoneum mimicking hepatocellular carcinoma rupture[J].World J Gastroenterol 2007; 13(47): 6441-6443.
3 陈新娟,沈文.腹腔恶性纤维组织细胞瘤 1 例[J],罕少疾病杂志,2005,12(2):42-43.
R730.262
D
2009-12-26

