采用复盐法脱除工业废水中的硫酸根
王海鹰,彭小玉,王云燕,柴立元,舒余德
(中南大学 冶金科学与工程学院,湖南 长沙,410083)
高浓度硫酸盐废水大量存在于矿山、冶金、食品及医药等行业中[1],这些废水不经处理直接排入水体,将会产生一系列危害[2-5],如:过量的硫酸根可使水体产生恶臭,影响水的感官性状及其使用;过量的硫酸根不利于作物生长,使土地盐渍化;含有硫酸盐的饮用水有苦涩味,并有致泻作用,如长期饮用,将引起腹泻和消化不良等症状。因此,水中硫酸根脱除研究越来越引起人们的关注。目前,比较成熟的脱除硫酸根的方法主要有 BaCl2法、CaCl2法、冷冻法及生物法[6-10]。BaCl2法是工业应用最广泛的化学除 SO24-方法,其工艺操作简单,去除效果好,但 BaCl2有较强的毒性,贮存条件要求高,使用成本高[11]。采用CaCl2法时,由于硫酸钙的溶度积(9.1×10-6)较大,去除SO2-的效果比氯化钡法差。采用冷冻法能耗相当大,
4目前工业上应用很少见。采用生物法处理含硫酸盐废水具有成本低、适用性强、无二次污染等优点[12],但启动时间较长、处理速度慢、效率低、有机物消耗量大[1]。近几年,人们开发出了离子交换法、膜分离法及吸附法等[10,13],其中,离子交换法具有吸附和脱附速度快、操作方便等优点。膜分离法是由加拿大Kvaerner chenetics公司开发的一种新型脱除硫酸根离子的技术,可以有效地从盐水溶液单价阴离子 Cl-中分离出 SO24-,具有硫酸根脱除率高、操作简便、成本较低等特点。目前,这些方法主要应用于氯碱生产过程中盐水中硫酸根脱除,而它们在工业废水处理领域的应用还有待进一步研究。此外,也有采用针铁矿、柱撑蒙脱石、焙烧水滑石等吸附去除水中硫酸根离子的文献报道[14-16],但此类方法受溶液pH值、操作温度等因素影响较大,且成本较高,尚处于实验研究阶段。因此,有必要开发一种有效的硫酸根脱除方法。有研究报道 SO24-能与 Ca2+和 Al3+在一定条件下形成复合物硫酸钙铝沉淀(Al2Ca3(SO4)6)[17-18]。基于这种原理,本研究以水合硝酸铝及氢氧化钙为脱除剂,脱除重金属废水中的硫酸根。探讨铝盐加入量、溶液 pH值、反应时间、反应温度及 SO24-初始浓度等因素对SO2-4脱除效果的影响,旨在为工业废水中硫酸根的脱除开辟一条新途径。
1 实验
1.1 主要仪器及试剂
主要仪器:PHS-3C精密pH计;AUY220型电子分析天平;HJ-6多头磁力加热搅拌器;HH-601恒温数显水浴;SHZ-CD型循环水式多用真空泵。
主要试剂:Na2SO4(分析纯);CaSO4·2H2O(分析纯);Al(NO3)3·9H2O(分析纯);Ca(OH)2(分析纯);NaOH(优级纯);盐酸联苯胺(分析纯);酚酞(指示剂);超纯水(电导率为 5.47×10-4S/m)。
1.2 实验方法
有色冶炼废水经中和水解及脱钙工序处理后,溶液中 Ca2+,Na+及 SO24-的质量浓度分别为300,220,720 mg/L,故采用分析纯 CaSO4·2H2O 和无水Na2SO4,配制成 SO24-质量浓度为1 720 mg/L的溶液,作 SO2-脱除的实验溶液。实验时准确称取 1.29 g4 CaSO4·2H2O和1.479 g无水Na2SO4,置入250 mL烧杯中,加入200 mL超纯水搅拌溶解,且微微加热,溶解后转入1 L 容量瓶定容以备用。每次实验取100 mL溶液置于三角瓶中,再加入一定量铝盐,用Ca(OH)2调节溶液pH值,搅拌一定时间,沉淀过滤,取滤液分析其中 SO24-残余量。
1.3 分析方法
硫酸根离子浓度采用酸碱滴定法测定[19]。在盐酸联苯胺的冷溶液中,加入含有硫酸盐的中性溶液,生成不溶性的硫酸联苯胺沉淀,反应式如下:
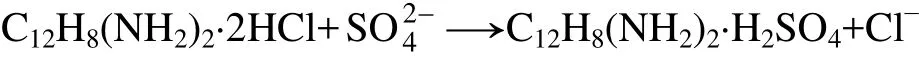
沉淀静置10~15 min后,真空过滤、洗涤,置于50 ℃以上的热水中水解为游离硫酸和联苯胺:
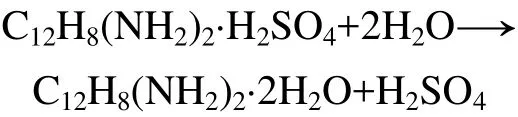
以酚酞为指示剂,用标定后的NaOH标准溶液滴定,反应终点为无色变为微红色。
2 结果与讨论
2.1 pH值对 脱除的影响
分别取100 mL初始质量浓度为1 720 mg/L的SO2-溶液置于8个三角瓶中,铝盐加入量为1.4 g,4反应温度为25 ℃,用石灰乳调节至不同的pH值,搅拌90 min,沉淀、过滤,取滤液分析其中 SO24-含量。结果如图1所示。
SO2-去除率明显依赖于溶液的pH值。当溶液pH4≤10.0时, SO24-去除率小于43.4%, SO24-残留质量浓度大于970 mg/L;当pH值为10.0~10.5时,SO24-去除率随pH值升高迅速提高,从pH=10.0的43.6%提高到pH=10.5的90.5%,当pH≥10.5时,随着pH值增大, SO24-去除率变化不明显,维持在90%~96%,SO2-4残留质量浓度低于100 mg/L。由此可见:复盐沉淀法去除 SO24-的有效pH值应大于10.5。
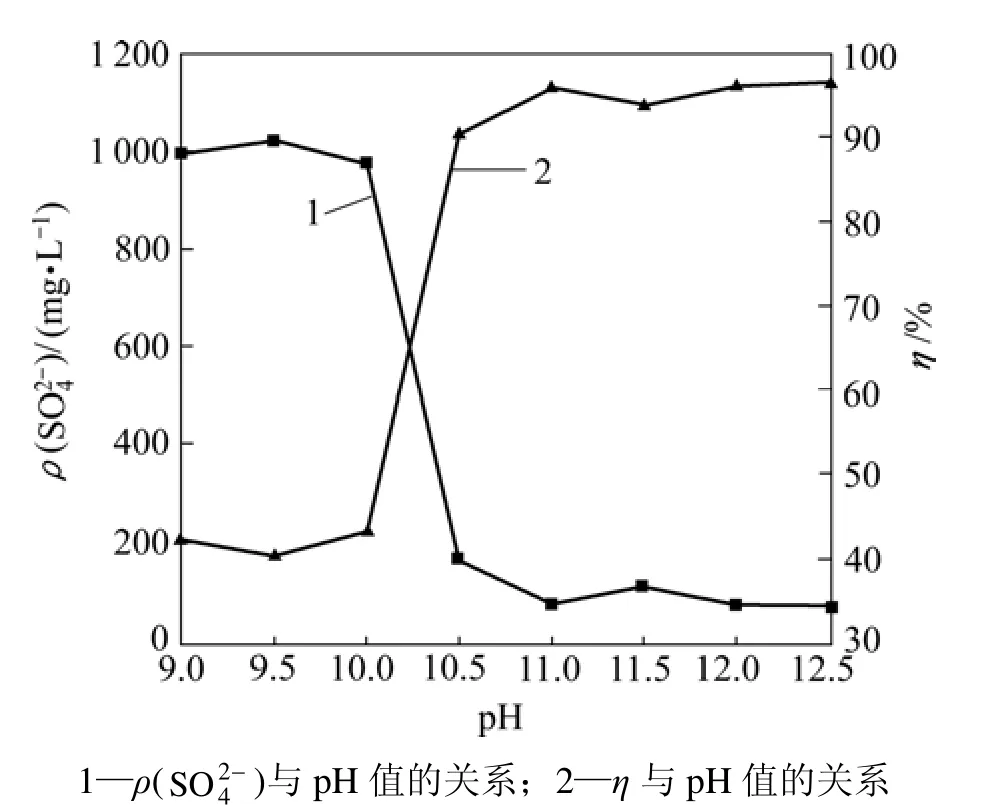
图1 pH值对 SO 24 -去除率η及其残留质量浓度ρ(S O 24 -)的影响Fig.1 Effects of pH values on removal ratio and residual concentration of sulfate
2.2 硝酸铝加入量对 SO 24 -脱除的影响
SO24-初始质量浓度为1 720 mg/L,溶液体积为100 mL,反应温度为25 ℃。加入不同量的铝盐,用石灰乳调pH值至12.0,搅拌90 min,结果如图2所示。从图2可见:当铝盐加入量小于0.62 g时, SO24-去除率随着铝盐加入量的增大基本呈直线上升,表明此时 Al3+的投加量不够, SO24-的去除率取决于 Al3+投加量,要提高 SO24-的去除率,需增加Al3+投加量;当铝盐加入量增大到 0.62 g时, SO24-去除率达到95.6%, SO24-残留质量浓度为 75.6 mg/L;继续增大铝盐加入量,SO24-去除率基本保持不变,维持在96%左右,说明此时Al3+投加量已基本满足沉淀 SO24-的需求,再继续投加Al3+,S O24-去除率增加已不明显。由Al3+投加量0.62 g对应的残留质量浓度可计算出,27 mg Al3+可以去除99.4 mg SO24-,与理论计算相比多消耗17.66 mg Al3+。这说明加入体系中的Al3+只有部分用于形成硫酸钙铝复合物沉淀。
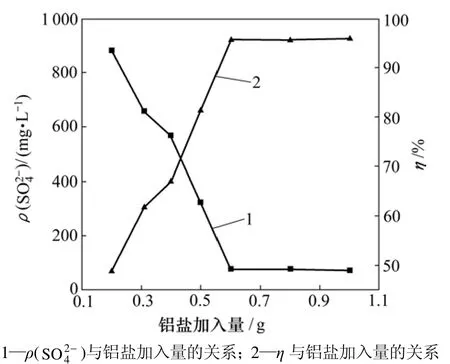
图2 铝盐加入量对 SO 24 -去除率及其残留质量浓度的影响Fig.2 Effects of aluminum salt dosage on removal ratio and residual concentration of sulfate
2.3 SO 24 -初始质量浓度对 SO 42 -脱除的影响
取100 mL浓度不同的 SO24-溶液,反应温度为25℃, SO24-与Al3+物质的量为1.1∶1.0,用石灰乳调pH值至12.0左右,搅拌90 min,研究 SO24-初始质量浓度对去除率的影响,结果如图3所示。
由图 3可见:当 SO24-初始质量浓度低于 1 300 mg/L时, SO24-去除率随其初始质量浓度的增加而增大;当 SO24-初始质量浓度高于1 300 mg/L时,对 SO24-去除率无明显影响,保持在94%~96%之间。其原因是SO24-初始质量浓度高,Ca2+,Al3+和 SO24-三者碰撞机会多,硫酸钙铝晶核容易形成,且大量硫酸钙铝在沉降过程中会吸附部分 SO24-,使 SO24-去除率增大。由图 3还可以看出:当溶液 SO24-初始质量浓度高于1 300 mg/L时,经本方法处理后,出水 SO24-质量浓度低于100 mg/L,达到生活饮用水卫生标准。
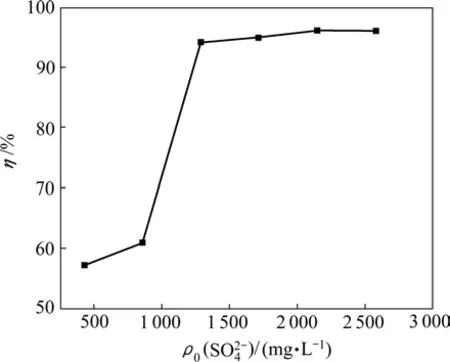
图3 SO 24 -初始质量浓度ρ0( SO 24 -)对 SO 24 -脱除率的影响Fig.3 Effect of initial concentration of sulfate ion on removal of sulfate
2.4 反应时间对 SO 24 -脱除的影响
在6个三角瓶中,分别取100 mL初始质量浓度为1 720 mg/L的 SO24-溶液,加入0.62 g铝盐,加入1.3 g Ca(OH)2调pH值至12.0左右,反应温度为25 ℃。搅拌不同时间后,沉淀、过滤,取滤液分析 SO24-含量,结果如图4所示。由图4可见:当搅拌时间小于60 min时,SO24-去除率随着搅拌时间的增长而提高,从搅拌20 min的76.8%增至搅拌60 min的95.4%;当搅拌时间达到60 min后,再增加搅拌时间, SO24-去除率无明显变化,基本维持在 96%左右, SO24-残留质量浓度约为70 mg/L,说明搅拌时间为60 min时反应基本达到平衡。可见,复盐法脱除 SO24-最佳反应时间为60 min。
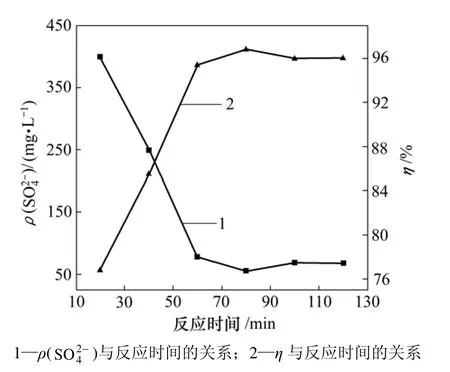
图4 反应时间对 SO 24 -去除率及其残留质量浓度的影响Fig.4 Effects of reaction time on removal ratio and residual concentration of sulfate
2.5 反应温度对 SO 42 -脱除的影响
反应所需温度是决定本方法是否适用于实际工程的重要因素之一。取100 mL初始质量浓度为1 720 mg/L的 SO24-溶液,置入三角瓶中,加入0.62 g铝盐;用0.40 g Ca(OH)2调pH值为11.0~12.0,搅拌60 min,考察反应温度对 SO24-去除率的影响,实验结果如图5所示。

图5 反应温度对 SO 24 -去除率及其残留质量浓度的影响Fig.5 Effects of reaction temperature on removal ratio and residual concentration of sulfate
由图5可见:在反应温度在25~45 ℃时,SO24-去除率无明显变化,保持在93%~95%。可见:在常温条件下,用复盐沉淀法能有效地去除溶液中硫酸根离子。
2.6 正交实验
为了分清影响因素的主次,选择各因素的最优水平,根据单因素条件实验结果,采用三因素三水平正交设计表进行正交实验,并对实验结果数据进行极差分析,结果如表1所示。

表1 正交实验结果及极差分析Table 1 Results of orthogonal experiment and range analysis
根据各因素极差的大小可以判断因素重要性顺序。表1中极差表明:pH值是影响 SO24-脱除的重要因素,当pH值大于11.0时,SO24-可以脱除到100 mg/L左右,但随着pH值降低, SO24-残余浓度增加,脱除率降低;当pH值为10.0时, SO24-只能脱除到1 200 mg/L。极差表明反应时间和铝盐加入量对 SO24-脱除未表现出明显的影响,各因素对 SO24-去除率影响由大至小的顺序依次为:溶液pH值、铝盐加入量、反应时间。较优水平组合为A3B3C3,即最佳工艺条件为:溶液pH值为12.0,反应时间为80 min,铝盐加入量为0.7 g。但由于溶液pH值为11.0和12.0时,SO24-脱除率相差较小,且考虑到成本问题,确定实际工艺条件如下:溶液pH值为11.0,反应时间为60 min,硝酸铝加入量为0.6 g。
2.7 固相XRD分析
实验条件:S O24-初始质量浓度为1 720 mg/L,溶液体积为100 mL,反应温度为25 ℃。加入铝盐的量为0.6 g,用石灰乳调pH值至11.0,搅拌60 min;过滤、沉淀烘干。固相XRD分析结果如图6所示。

图6 固相XRD谱Fig.6 XRD pattern of precipitation
由图6可以看出:固相沉淀的主要组成物相为钙矾石,其分子式为Ca6Al2(SO4)3(OH)12·26H2O,为一种常用的混凝土膨胀剂[20-22]。检测结果表明:在碱性条件下,溶液中的 SO24-可与Ca2+和Al3+形成复合物沉淀而得以脱除。
3 结论
(1) 在碱性条件下,溶液中的 SO24-可与 Ca2+和Al3+形成复合物沉淀而得以去除,其去除率随着 SO24-初始质量浓度的增大而提高。实验所用 SO24-初始质量浓度为1 300~2 500 mg/L时,经本方法处理后,出水SO2-质量浓度可以达到100 mg/L以下。
(2) SO24-去除率依赖于溶液pH值、铝盐投加量及反应搅拌时间。当pH值为11.0, SO24-与Al3+的物质的量比为1.1∶1.0,搅拌时间为60 min时,去除率可达到95%左右。此外,固相分析结果表明:其主要物相为 Ca6Al2(SO4)3(OH)12·26H2O,这说明溶液中的SO24-以复盐形式脱除。
[1] 柴立元, 刘恢, 闵小波, 等. 改性活性污泥高效处理高浓度硫酸盐废水[J]. 中南大学学报: 自然科学版, 2005, 36(3):431-436.CHAI Li-yuan, LIU Hui, MIN Xiao-bo, et al. Efficient treatment of high concentration sulfate wastewater by modified aerobic activated sludge[J]. Journal of Central South University: Science and Technology, 2005, 36 (3): 431-436.
[2] 谢杰, 洪文笔, 高玉梅, 等. 液膜分离技术提取水中硫酸根的可行性分析[J]. 吉林建筑工程学院学报, 2007, 24(4): 5-8.XIE Jie, HONG Wen-bi, GAO Yu-mei, et al. The feasibility analysis of extracting sulfate from water by liquid membrane separation technology[J]. Journal of Jilin Institute Architectural& Civil, 2007, 24(4): 5-8.
[3] Benattia C T, Tavares C R G, Lenzi E. Sulfate removal from waste chemicals by precipitation[J]. Journal of Environmental Management, 2009, 90 (1): 504-511.
[4] Lens P N L, Visser A N L, Janssen A J H, et al. Biotechnological treatment of sulfate-rich wastewaters[J]. Critical Reviews in Environmental Science and Technology, 1998, 28(1): 41-88.
[5] Ghigliazza R, Lodi A, Rovatti M. Kinetic and process considerations on biological reduction of soluble and scarcely soluble sulfates[J]. Resources, Conservation and Recycling,2000, 29(3): 181-194.
[6] 王广兴, 郭连才. 盐水中硫酸根的脱除技术[J]. 中国氯碱,2006(8): 5-7.WANG Guang-xing, GUO Lian-cai. Removal technology of sulfate anion in brine system[J]. China Chlor-Alkali, 2006(8):5-7.
[7] 苏恒熙, 王秀丽, 蔡泽坚. 无机盐复合体系脱除 SO24-的工艺研究[J]. 盐业与化工, 2006, 36(3): 1-3, 10.SU Heng-xi, WANG Xiu-li, CAI Ze-jian. Research on the process of removing SO24-from multi-component type solution[J]. Guangdong Chemical Industry, 2006, 36(3): 1-3, 10.
[8] Kabdasli I, Tünay O, Orhon D. Sulfate removal from indigo dyeing textile wastewater[J]. Water Science and Technology,1995, 32(12): 21-27.
[9] 金哲男, 熊雪松, 李席孟, 等. 吸附法深度除去氯化锂中硫酸根的实验研究[J]. 稀有金属, 2007, 31(3): 404-406.JIN Zhe-nan, XIONG Xue-song, LI Xi-meng, et al. Deeply removing sulfate radical from lithium chloride in adsorption method[J]. Chinese Journal of Rare Metals, 2007, 31(3):404-406.
[10] 曹天飚, 郭伟, 马红钦, 等. 盐卤中硫酸根脱除技术[J]. 中国井矿盐, 2006, 37(4): 19-22.CAO Tian-biao, GUO Wei, MA Hong-qin, et al. Technology of sulfate removal from brine[J]. China Vell and Rock Salt, 2006,37(4): 19-22.
[11] 祝清生. 卤水中硫酸根的去除方法[J]. 氯碱工业, 2004(12):10.ZHU Qing-sheng. Removal technology of sulfate in brine system[J]. Chlor-alkali Industry, 2004(12): 10.
[12] 常晓雷, 康勇, 冯颖. 硫酸盐还原菌与单质铁协同作用处理酸性含锌废水[J]. 中国有色金属学报, 2006, 16(9): 1647-1652.CHANG Xiao-lei, KANG Yong, FENG Ying. Treatment of acid zinc wastewater by sulfate reducing bacteria cooperated with iron[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(9):1647-1652.
[13] 袁斌. 新法脱除硫酸根技术国内外进展[J]. 氯碱工业,2000(11): 3-6.YUAN Bin. Progress of new SO24-removing technology at home and abroad[J]. Chlor-alkali Industry, 2000(11): 3-6.
[14] 李冬梅, 王海增, 王立秋, 等. 焙烧水滑石吸附脱除水中硫酸根离子的研究[J]. 矿物学报, 2007, 27(2): 109-114.LI Dong-mei, WANG Hai-zeng, WANG Li-qiu, et al. Removal of sulfate from aqueous solution by adsorption of it on layered double hydroxides[J]. Acta Mineralogica Sinica, 2007, 27(2):109-114.
[15] 刘桂荣, 廖立兵. 柱撑蒙脱石吸附水中硫酸根离子的实验研究[J]. 矿物学报, 2001, 21(3): 470-472.LIU Gui-rong, LIAO Li-bing. Removal of sulfate from aqueous solutions by adsorption on pillared montmorillonite[J]. Acta Mineralogica Sinica, 2001, 21(3): 470-472.
[16] Rietra R P J J, Hiemstra T, van Riemsdijk W H. Sulfate adsorption on goethite[J]. Journal of Colloid and Interface Science, 1999, 218: 511-521.
[17] 胡文容. 铝盐沉淀法去除酸性矿井水中 SO24-的试验研究[J].煤矿环境保护, 1996, 10(5): 18-20, 32.HU Wen-rong. Removal of sulfate from acid mine drainage by aluminum-salt precipitation technology[J]. Energy Environmental Protection, 1996, 10(5): 18-20, 32.
[18] Schaezier D J. Precipitation of calcium aluminates and sulfoaluminates from water[J]. Journal Water Pollution Control Federation, 1978, 50(7): 1821-1826.
[19] 王建国, 王瑞斌. 盐酸联苯胺分离-酸碱滴定法测定实验室废水中硫酸根研究[J]. 科学技术与工程, 2007, 7(17): 4438-4440.WANG Jian-guo, WANG Rui-bin. Study on the determination of sulfate in laboratory wastewater by benzidine hydrochloride separate and acid-base titration[J]. Science Technology and Engineering, 2007, 7(17): 4438-4440.
[20] 石云兴, 王泽云, 吴东, 等. 钙矾石的形成条件与稳定性[J].混凝土, 2000(8): 52-54.BAI Yun-xing, WANG Ze-yun, WU Dong, et al. Forming condition and stabil ity of ettringite[J]. Concrete, 2000(8):52-54.
[21] 彭家惠, 楼宗汉. 钙矾石形成机理的研究[J]. 硅酸盐学报,2000, 28(6): 511-515.PENG Jia-hui, LOU Zong-han. Study on the mechanism of ettringite formation[J]. Journal of the Chinese Ceramic Society,2000, 28(6): 511-515.
[22] 马惠珠, 邓敏. 碱对钙矾石结晶及溶解性能的影响[J]. 南京工业大学学报, 2007, 29(5): 37-40.MA Hui-zhu, DENG Min. Effect of alkali on ettringite crystallization and solubility[J]. Journal of Nanjing University of Technology, 2007, 29(5): 37-40.

