微波消解石墨炉原子吸收光谱法测定植物中的铅
吴彩霞,张洪荣
(兰州大学草地农业科技学院,甘肃 兰州730020)
铅是一种慢性和蓄积性毒物,能侵犯人的造血系统、神经系统和肾脏,引起贫血、脑病变和肾病变[1-3]。它可以通过水体、土壤、空气向生物体转移,造成全世界各种植物性食物中均有铅的存在。铅通过空气和食物链进入人类和动物体内,对生命安全构成威胁[4-5]。铅也可以影响植物的生长,使根量减少,根冠膨大变黑、腐烂,影响养分吸收,导致地上部分生物量下降[6]。但部分(如草木樨Melilotusof f icinalis)耐铅植物,在高铅环境下能正常生长,可作为铅污染土壤的生态修复植物[7]。为方便学者进行铅污染方面的研究,简洁、快速、准确的检测植物、土壤、食品等物质中铅含量非常必要。目前,铅的测定方法有火焰原子吸收法、二硫腙比色法和石墨炉原子吸收法。由于植物中铅的含量较低,比色法和火焰原子吸收法测定结果的误差较大,而石墨炉原子吸收光谱法具有较高的灵敏度。植物样品的前处理方法多采用干灰化[2,8-9]和湿法消化[3,10],操作繁琐、费时,样品消解不完全。也有学者采用 HNO3或HNO3-H2O2酸体系微波消解法处理水产品[11]、酵母[12]和酱菜[4]等样品,但用上述酸体系微波消解植物样品,消解不理想;还有学者使用HNO3-HClO4体系[13-15]消解植物样品,消解效果好,但由于HClO4体系易发生爆炸,一些公司生产的微波消解炉严禁使用该体系,如美国CEM公司生产的MARS240/50微波消解炉。研究探讨了微波消解石墨炉法测定植物中铅的样品处理酸的体系、酸的用量以及石墨炉的最佳工作条件,为微波消解石墨炉原子吸收光谱法测定植物中的铅提供依据。
1 实验方法
1.1 主要仪器 MARS240/50微波消解炉(美国CEM公司);Thermo M系列原子吸收分光光度计,GF95Z石墨炉,FS95自动进样器(美国热电公司)。石墨管(高温涂层),MILLIPORE超纯水器。
1.2 主要药品和试剂 硝酸(HNO3,优级纯),氢氟酸(HF,优级纯),硝酸铅(光谱纯),磷酸(光谱纯),20 g/L的磷酸溶液。
铅标准储备液:准确称取在105℃烘箱中烘至恒质量的硝酸铅(光谱纯)1.598 5 g置于300 mL广口烧杯中,加入5 mL硝酸(优级纯)和超纯水溶解后,转移至1 000 mL容量瓶中定容至刻度,摇匀,此标准溶液中含铅1 000 μ g/mL。水为超纯水(电阻率18.2 MΩ·cm以上)。
1.3实验处理
1.3.1 酸体系、用量 用了4种酸体系:①HNO3,②HNO3-H2O2,③HNO3-HF,④HNO3-H2O2-HF,13种组合方式进行消化试验(见表1)。
1.3.2 微波消解功率、温度和时间 实验采用了600 W和1 200 W的微波消解功率,不同的温度,升温时间和控制温度保持时间组合处理样品。
1.3.3 基体改进剂及用量的选择 在30 μ g/L Pb2+标准溶液进样量20 μ L不变的前提下,实验采用了不同加入量的H3PO4和NH4H2PO4基体改进剂。
1.4 待测液制备 称取约0.300 0 g样品置于消化管中,依次加入1 mL HF、3 mL H2O2和5 mL HNO3,盖上内盖,并旋紧外盖,于微波消解炉内600 W 消解15 min冷却,转入400 mL聚四氟广口烧杯中于120℃电热板上加热,烧杯中液体约为2 mL时,再加入约5 mL超纯水,加热使可溶性盐溶解,冷却转移至100 mL容量瓶中定容,摇匀,并迅速移至塑料瓶中保存。
1.5 回收率实验 分别称取3份同一植物样品,其中1份作参照,另2份分别加入不同量的铅,按照样品待测液制备方法制备待测液,用石墨炉原子吸收分光光度法测定待测液中Pb浓度,根据加入Pb的量计算回收率。
2 结果
2.1 微波消解条件
2.1.1 酸体系及用量 不同酸体系的实验结果表明,仅HNO3和HNO3-H2O22种酸体系消解植物样品消化液混浊;而HNO3-HF和HNO3-H2O2-HF 2种酸体系,消化液清澈透明,不混浊,因此可以使用 HNO3-HF或 HNO3-H2O2-HF体系消解植物样品(表1)。在使用HNO3-HF酸体系时,需要驱除氮氧化物后再转移定容,而HNO3-H2O2-HF酸体系则不需要此步骤,更加省时方便,故本法选用 HNO3-H2O2-HF体系。
0.3000g 样品,不同用量的 HNO3、H2O2和HF的实验结果见表1,可以看出,最佳酸用量为5 mL HNO3-3 mL H2O2-1 mL HF,消解完全,消化液清澈透明不混浊,而且用量小。

表1 酸体系及用量
2.1.2 消解功率、温度、时间 0.300 0 g样品,HNO3-H2O2-HF消解体系,微波消解炉设定不同功率、温度和时间的实验结果见表2,可以看出方法2-4均可将样品消解澄清,因微波消解仪的额定功率为1 200 W,消化管能承受的温度约为220℃,为延长消化管使用寿命及仪器安全运行,故选择方法2,即微波消解炉的功率为600 W、温度为180℃,时间为15 min,该条件下消化完全,消化液透明无残渣。
2.2 原子吸收分光光度计的工作条件
2.2.1 光谱仪工作条件 波长283.3 nm,灯电流7.5mA,光谱通带1.0nm,氩气(Ar)作保护气,氘灯扣除背景。
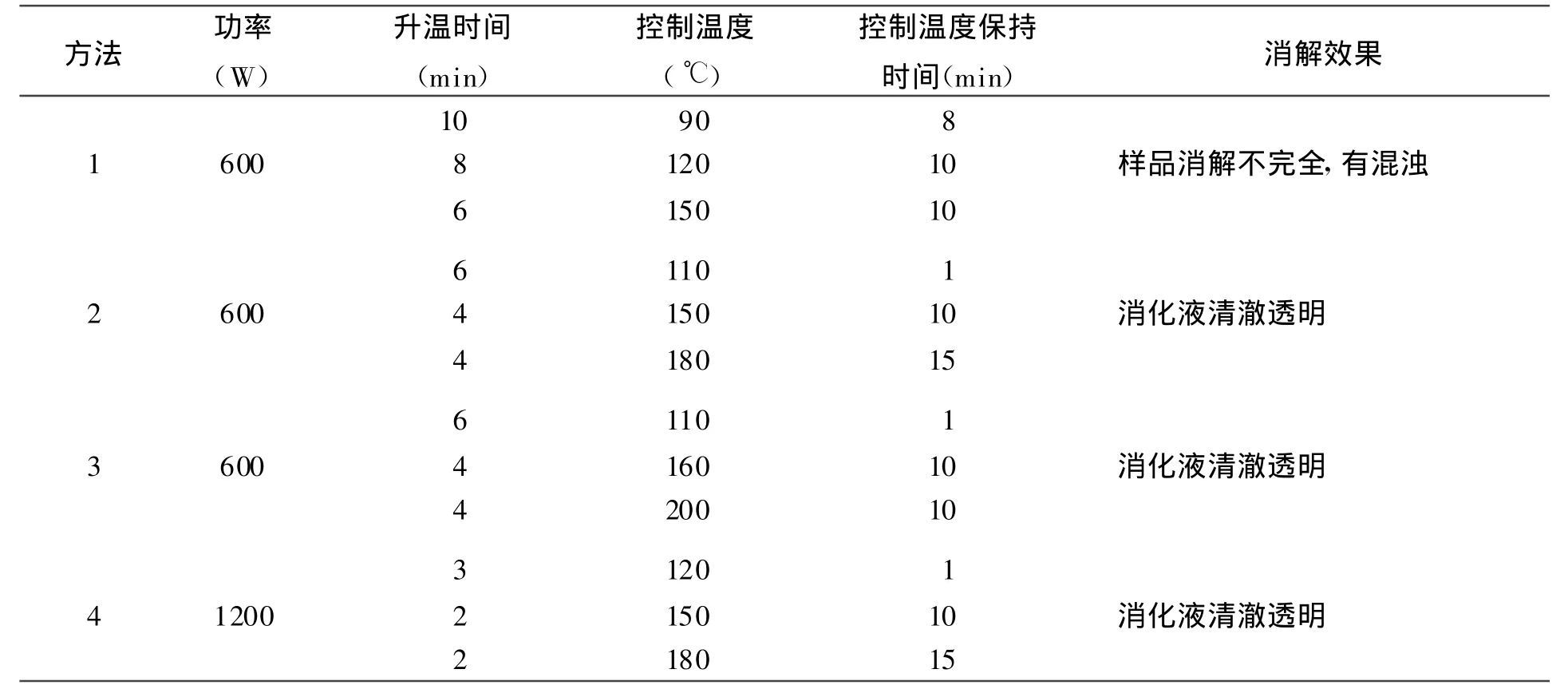
表2 微波消解功率、温度和时间
2.2.2 石墨炉工作条件的选择 铅是易挥发性元素,温度高于450~500℃易损失,加入 H3PO4做固定剂,用20 μ g/L Pb2+标准溶液测试,可提高灰化温度至900℃,原子化温度为1 400℃,样品溶液进样量为 20 μ L,基体改进剂H3PO4溶液(20 g/L)加入量为5 μ L。吸光度值最高且稳定。石墨炉工作条件见表3。
2.2.3 基体改进剂及其用量的选择 在30 μ g/L Pb2+标准溶液进样量20 μ L不变的前提下,试验了H3PO4和 NH4H2PO4的加入量,实验表明H3PO4加入量为 2 μ L,NH4H2PO4加入量 1 μ L和 H3PO4加入量为 5 μ L,NH4H2PO4加入量2 μ L时,测量结果稳定,精密度高(表4)。本研究选用H3PO4作为基体改进剂,加入量为5 μ L。
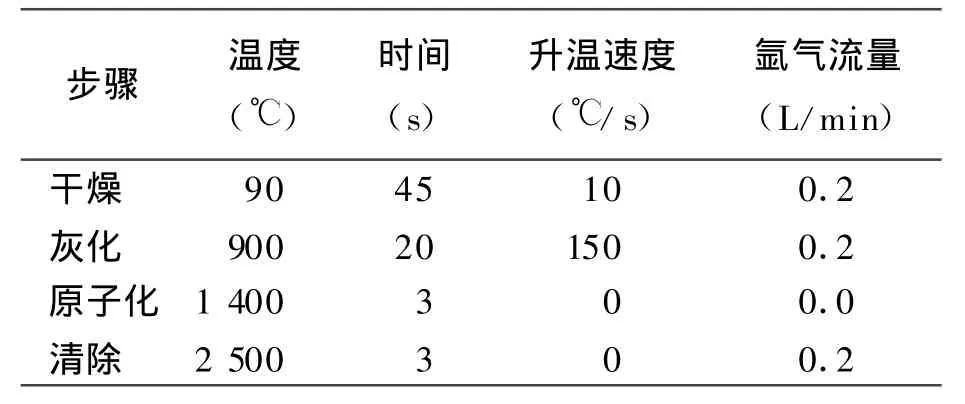
表3 石墨炉工作条件
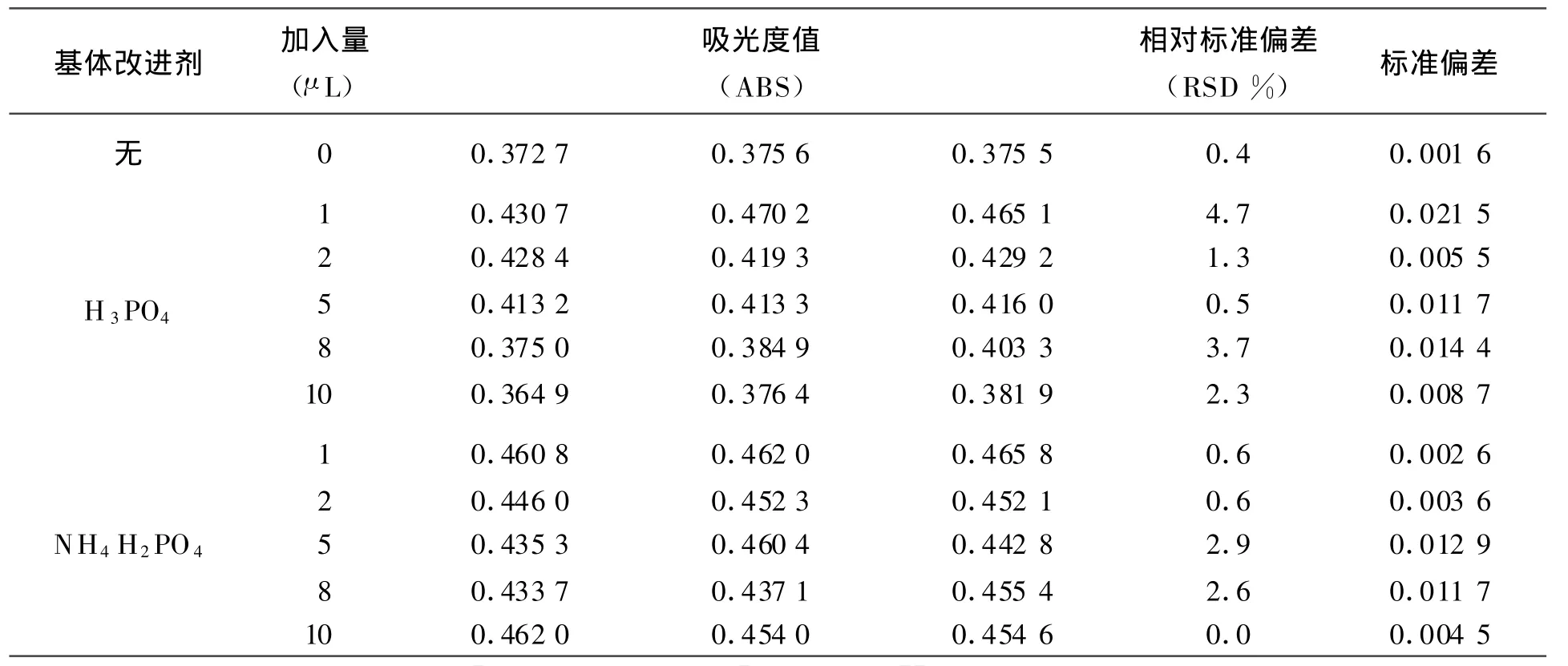
表4 基体改进剂及用量的选择
2.3工作曲线、精密度和检出限 测定0、10、20 、30、40 、50 μ g/L 铅标准溶液 ,得线性回归方程A=0.011 63 C+0.025 9(r=0.993 8,P<0.01)。
式中:A为吸光度值;C为 Pb2+的浓度(μ g/L)。对标准溶液各测定6次,其相对标准偏差(RSD)分别为:5.6%、4.1%、2.2%、1.8%、2.8%、1.2%,对试剂空白测定24次,测得检出限为0.068 4 mg/kg(n=24)。
2.4 样品测定结果和回收率 在2份植物样品中分别加入不同量的铅,进行回收率试验,测定结果见表5。
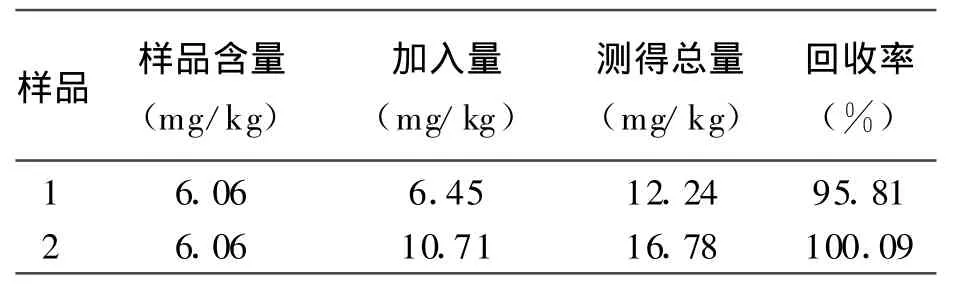
表5 样品测定结果和回收率
3 结论
3.1 HNO3-H2O2-HF体系微波消解植物样品效果优于 HNO3、HNO3-H2O2和HNO3-HF体系,最佳酸用量为 5 mL HNO3、3 mL H2O2、1 mL HF,180℃微波消解15 min,消解完全,消化液清澈透明不混浊。
3.2 H3PO4溶液做基体改进剂,在石墨炉灰化温度为900℃,原子化温度为1 400℃的条件下,测定植物中铅 。对 0、10、20、30、40、50 μ g/L 系列Pb2+标准溶液测定6次,其线性回归方程 A=0.011 63 C+0.025 9(R2=0.987 6,P<0.001)。相对标准偏差RSD为1.2%~5.6%,对试剂空白测定24次,测得检出限为0.068 4 mg/kg,样品加标回收率为95.81%~100.09%。上述实验数据说明采用实验条件测定植物中的铅,方法选择性良好,精密度和准确度高且简便、快速。
[1] 黄熠,向牡秀,周菊峰,等.石墨炉原子吸收光谱法测定鱼腥草西洋参和茯苓中的铅[J].西南民族大学学报(自然科学版),2008,34(1):149-151.
[2] 巨积红,刘俊娓.植物中低含量铅的石墨炉原子吸收测定法[J].职业与健康,2006,22(2):103-104.
[3] 杨兵兵,王铎,肖建存,等.加油站附近绿色植物中铅含量的测定[J].广东微量元素科学,2005,12(9):61-63.
[4] 康远干.微波消解石墨炉原子吸收光谱法测定番木瓜酱菜中铅[J].理化检验——化学分册,2003,39(7):391-392.
[5] 庄会荣,刘长增,陈继诚,等.原子吸收光谱法测定铅的进展[J].理化检验——化学分册,2003,39(7)430-433.
[6] 王慧忠,何翠屏,赵楠.铅对草坪植物生物量与叶绿素水平的影响[J].草业科学,2003,20(6):73-75.
[7] 周朝彬,胡庭兴,胥晓刚,等.铅胁迫对草木樨抗氧化系统的影响[J].草业科学,2006,23(13):43-46.
[8] 钟运技.石墨炉原子吸收光谱法测定茶叶中的铅[J].分析与检测,2008(1):45-47.
[9] 蒋炜,唐洪,刘中春,等.干法灰化石墨炉原子吸收光谱法测定全血铅[J].中国卫生检验杂志,2008,18(3):464-465.
[10] 冯利,陈中兰,曾淼.石墨炉原子吸收法测定美白化妆品中铅和镉[J].分析科学学报,2008,24(4):461-463.
[11] 戎江瑞,张立军,俞安复,等.微波消解——原子吸收法测定水产品中铅与镉[J].中国卫生检验杂志,2009,19(2):305-306.
[12] 程先忠,张开诚,金灿.微波消解石墨炉原子吸收法测定酵母粉中的微量铅和镉[J].分析科学学报,2008,24(1):67-70.
[13] 冯自立.微波增压溶样——原子吸收光谱法测定延胡索样品中微量铅镉[J].安徽农业科学,2009,37(4):1418-1419.
[14] 黄熠,向牡秀,王小华,等.石墨炉原子吸收法测定黄芪甘草和广藿香中的铅[J].太原师范学院学报(自然科学版),2008,7(1):110-112.
[15] 王喜全.原子吸收光谱法测定植物叶中微量重金属[J].理化检验——化学分册,2007,43(5):360-361.

