微波消解—纳氏试剂分光光度法测定土壤中总氮
古昌红
(重庆工商大学环境与生物工程学院,重庆 400067)
随着氮肥世界范围内的大量使用,因不考虑土壤的供氮能力而盲目地大量使用氮肥,一方面,使得氮素利用率低,造成了氮素的巨大损失;另一方面氨态氮和一些氮氧化物的挥发损失、硝态氮的淋失导致了严重的环境污染[1],给人们生活及健康造成了很大的危害。所以,土壤中总氮含量的测定对于评价土壤肥力价值,指导施肥,评估氮素供应的环境效益,保护生态平衡具有重要意义,而快捷、简便、准确、灵敏的测定方法已成为现实的需要[2]。
目前在土壤全氮量的测定中,一般用半微量凯氏法分解土壤样品,使土壤中的氮转化为铵态氮。消煮液中的铵态氮可以用蒸馏法、扩散法或比色法测定,最经典的是蒸馏滴定法[3],其操作繁琐。而微波技术以其简便、快速特点在土壤分析预处理中的应用已取得了较多的研究成果[4,5]。以微波消解土壤样品,用纳氏试剂分光光度法测定其中总氮量,以期获得快速、准确测定土壤中总氮量的分析方法。
1 实验部分
1.1 仪器、试剂和样品
(1)仪器设备。MDS-6微波消解炉(上海新仪微波化学科技有限公司);722分光光度计(上海光学仪器厂);具玻璃磨口塞比色管,25 mL。
(2)试剂。除非另有说明外,分析时均使用符合国家标准或专业标准的分析纯试剂。
①无氨水:在1 000蒸馏水中,加入0.10 mL硫酸(=1.84 g/mL),在全玻璃蒸馏器中重蒸馏,将馏出液收集在带有玻璃塞的玻璃瓶中。
②纳氏试剂:称取16.0 g氢氧化钠溶于50 mL无氨水中,充分冷却至室温。另称取7.0 g碘化钾和7.0 g碘化汞溶于无氨水,然后将此溶液在搅拌下徐徐注入氢氧化钠溶液中。用无氨水稀释至100 mL,贮于聚乙烯瓶中,密塞保存。
③1.00 mg/mL的铵标准储备液:用电子天平准确称取经100℃干燥的分析纯氯化铵3.817 6 g于100 mL洁净的烧杯中,加入无氨水搅拌使其溶解,用玻璃棒引流倒入1 000 mL容量瓶中,用无氨水定容至标线。
④碱性过硫酸钾溶液:称取40过硫酸钾(K2S2O8),另称取15 g氢氧化钠(NaOH),溶于无氨水中,稀释至1 000 mL,溶液存放在聚乙烯瓶内。
(3)土壤样品。土壤样品采自重庆工商大学后山,经风干、磨细、过筛(100目)、混匀、装瓶备用。
1.2 样品预处理
准确称取土壤样品0.1 g(精确到0.000 1 g)于聚四氟乙烯消解罐中,加入最佳消解混酸体系,放入微波消解炉中,设定最佳消解压力、时间。消解完全后,待消解罐冷却至室温,取出消解罐,将消解液转入100 mL容量瓶中,用无氨水稀释至刻度。
1.3 测定
移取上述是试液5.00 mL于50 mL具塞比色管中,用无氨水稀释至标线,加入1 mL酒石酸钾钠和1.5 mL钠氏试剂,混匀,静置10 min,以无氨水为参比,用10 mm比色皿,在波长420 nm处测定吸光度(GB 7479-87)。
1.4 标准曲线
准确吸取一定量的10 mg/L铵标准使用液于50 mL比色管中,加无氨水稀释至标线,再加1.00 mL酒石酸钾钠溶液和1.50 mL纳氏试剂,混匀。放置10 min,以无氨水为参比,用10 mm比色皿,在波长420 nm处测定吸光度,减去零浓度空白管的吸光度后,得到校正吸光度,绘制以氮含量C(mg/L)对校正吸光度A的标准曲线。所得线性回归方程为:A=303.68C+0.001,相关系数r=0.998 9。
2 结果与讨论
2.1 微波强度、消解时间和混酸体系的选择
微波加热是对试样进行有效地即时深层加热,并且样品是高压密闭容器内进行,强度过高,时间过长,会超出溶样杯的缓冲能力,发生危险;强度低了,消解不完全。所以要控制消解强度及消解时间,同时选择消解的混酸体系。土壤样品微波消解条件见表1。
与表4中由半微量凯氏定氮法测得的土壤样品中的总氮量233.1 mg/kg相比较,从表1可见,土壤样品在碱性过硫酸钾中,不论微波炉压强高低,时间长短都不能消解;在浓H2SO4+H2O2或浓H2SO4+H2O2+HCl的混酸体系下,不论微波炉压强高低,时间长短总不能消解完全;在浓H2SO4+HF的混酸体系下,0.7 MPa时消解10 min即可消解完全,达到快速、简便的消解土壤样品目的。由此可得微波最佳消解条件为:2 mL 浓 H2SO4和1 mL HF,于0.2 Mpa下保持 3 min,0.5 MPa下保持 2 min,0.7 MPa下保持5 min。
2.2 方法检出限
以10 mL无氨水代替试样,采用与测定完全相同的试剂、用量和分析步骤进行平行测定10次,测定数据见表2。空白平行测定算术平均值为0.034;标准偏差Sb为0.000 79;方法检出限D.L=4.6Sb=0.003 4 mg/L。
2.3 方法精密度
称取0.1 g(精确到0.000 1 g)土壤样品,加入2 mL浓H2SO4和1 mL HF,在最佳微波消解条件下进行10次平行测定,计算10次结果的平均值和相对标准偏差RSD,结果见表3。
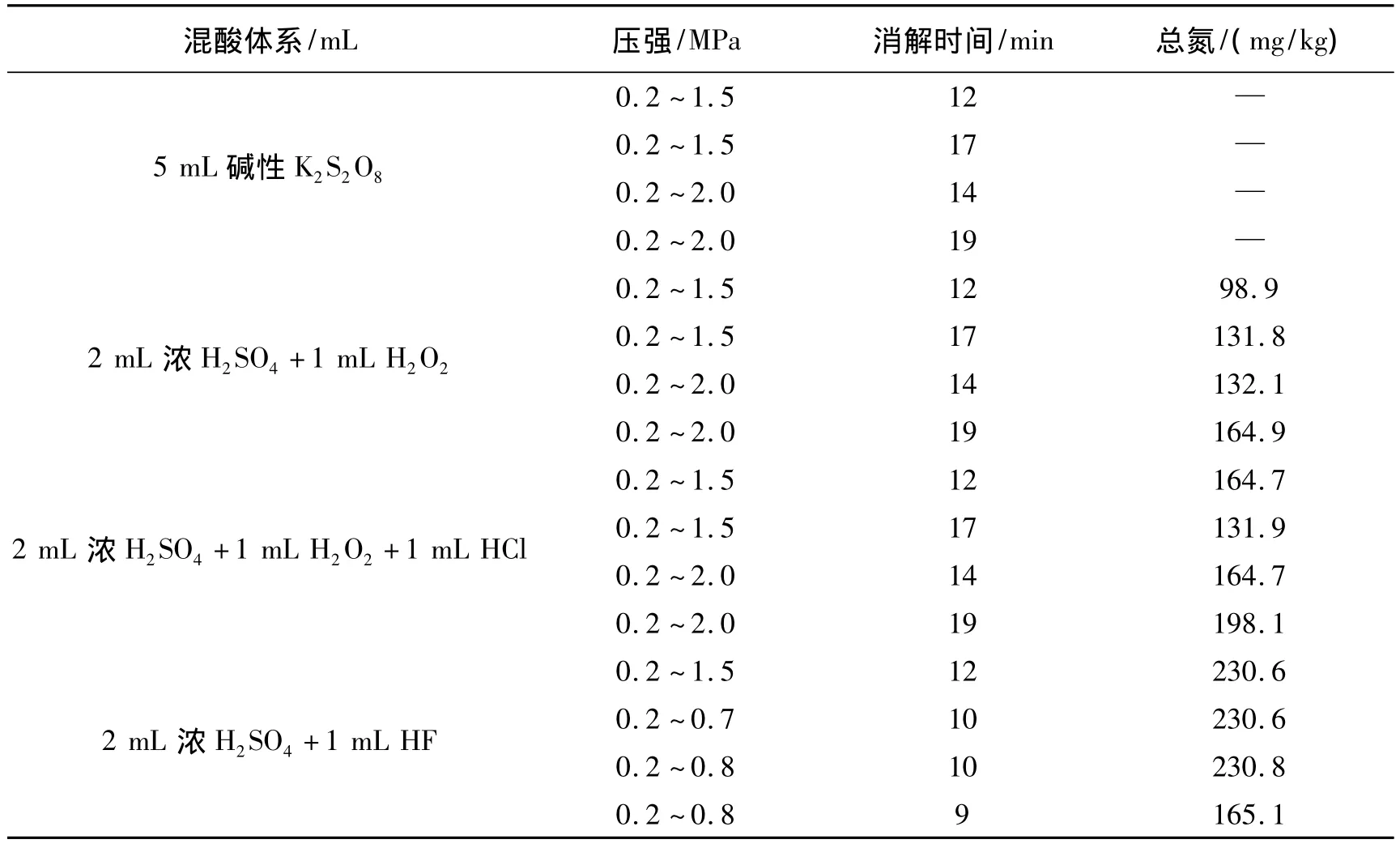
表1 土壤样品微波消解条件

表2 空白值测定

表3 土壤样品平行测定结果
从表3可见,微波消解的相对标准偏差为6.7%,小于10%,满足分析要求。
2.4 方法准确度
(1)与半微量凯氏定氮法测定值比较。称取土壤样品1.0 g(准确到0.000 1 g)用半微量凯氏定氮法(GB 7173-87)测定总氮量,平行测定5次,结果见表4,其相对误差为-1.16%。
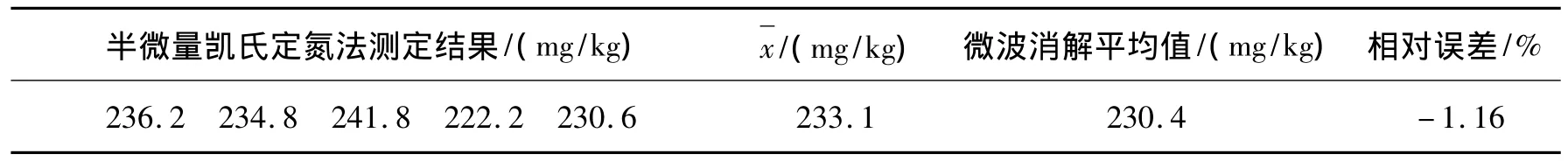
表4 国标法测定结果
(2)加标回收率实验。在已经测定出含量的土样中加入23.0 μg氮标准溶液,计算加标回收率,结果见表5,平均回收率为85.90% ~114.5%。
3 结论

表5 土壤样品加标回收率的测定结果 μg
微波消解-纳氏试剂分光光度法测定土壤中总氮的微波消解最佳条件为:用2 mL浓H2SO4和1 mL HF,于0.2 Mpa下保持 3 min,0.5 MPa下保持2 min,0.7 MPa下保持5 min;方法的检出限为0.003 4 mg/L,相对标准偏差RSD为6.7%,加标回收率为 85.90% ~114.5%,与国标法比较的相对误差为-1.16%。
微波消解法消化土壤样品测定总氮,时间短,消解试剂用量少,污染少,具有简便、快速、精密度与准确度较高的特点,可大大提高工作效率。但方法空白值较高,加标回收率也不太理想,还有待于进一步的完善。
[1]马立珊.农业氮素管理与环境质量[M].南京:江苏科学技术出版社,1992
[2]朱兆良,文启孝.中国土壤氮素[M].南京:江苏科学技术出版社,1990
[3]GB7173-87土壤全氮测定法
[4]范春蕾,梁振益,张敬迎,等.微波消解-石墨炉原子吸收法研究益智及土壤中的铅含量[J].化学分析计量,2009,18(5):24-26
[5]徐玉宏,张静,王静媛,等.微波消解-分光度法测定土壤中的全硼[J].中国环境监测,2009,25(3):43-45

