珠子参饮片质量标准研究
宋小妹, 房 方, 蔡 皓, 蔡宝昌*
(1.南京中医药大学,江苏南京 210046;2.陕西中医学院,陕西咸阳 712046)
珠子参为五加科植物珠子参(Panax japonicusC.A.Mey.var.major(Burk.)C.Y.Wu et K.M.Feng或羽叶三七Panax japonicusC.A.Mey.var.bipinnati-fidus(Seem)C.Y.Wu et K.M.Feng的干燥根茎。主产于四川、云南、贵州、甘肃、陕西、西藏等。具有补肺、养阴、活络、止血之功效,主要用于气阴两虚、烦热口渴、虚劳咳嗽、跌扑损伤、关节疼痛、咳血、外伤出血等症的治疗[1]。化学研究表明,珠子参主要活性成分为多种皂苷类[2]。药理实验表明皂苷类成分具有镇痛、镇静[3]、增强免疫力[4,5]、抗肿瘤[6]等活性。从现行各种标准来看,珠子参饮片的质量标准尚不完善。为此,本实验在对珠子参系统研究的基础上,以珠子参主要皂苷类成分人参皂苷Ro、竹节参皂苷IVa等为评价指标,对珠子参饮片进行质量评价研究,以保证其临床用药的安全有效。
1 实验材料
1.1 珠子参药材 分别购于四川、云南、贵州、湖北等地。经陕西中医学院药学院王继涛高级实验师鉴定,为珠子参Panax japonicusC.A.Mey.var.major(Burk.)C.Y.Wu et K.M.Feng的干燥根茎。
1.2 珠子参饮片 珠子参饮片为相应药材炮制的加工品(炮制方法:取原药材,挑出杂质,水洗,清水喷淋3次,放置5 h,切厚片。70℃干燥5 h,过筛,即得)。
1.3 仪器及试剂
1.3.1 仪器 Waters高效液相色谱仪;2996紫外检测器,Epower工作站;SB-3200D型超声清洗机(宁波新芝生物科技股份有限公司,180 W,40 kHz);BP-121S电子天平(北京赛多利斯仪器系统有限公司)。
1.3.2 药品与试剂 乙腈为色谱纯(SK Chemicals公司);其余试剂均为分析纯;水为娃哈哈纯净水;人参皂苷Ro对照品、竹节参皂苷Ⅳa对照品(均为自制,经1HNMR、13CNMR、HMBC、HMQC 及 HR-MS确定结构;面积归一法计算含量均大于98%,符合含量测定要求)。
2 方法与结果
2.1 饮片性状 本品为类圆形或不规则块片,直径0.2~1.8 cm。表面棕黄色或黄褐色,有皱纹;切面淡黄白色,粉性;或黄白色或黄棕色,略呈角质样。气微,味微苦、微甘。
2.2 粉末显微特征 本品粉末黄白色、灰白色或棕黄色。木栓细胞表面观呈多角形,壁薄,非木化;切面观类方形,内含红棕色分泌物。草酸钙簇晶多,整个薄壁细胞组织均有分布,直径20~76 μm,棱角多宽钝,少数较尖。导管多为网纹,直径20~46 μm,螺纹、梯纹导管可见。
2.3 薄层色谱鉴别 取本品粉末1 g,加甲醇30 mL超声处理40 min,滤过,滤液蒸干,残渣加水20 mL加热溶解,水饱和正丁醇萃取3次,合并正丁醇萃取液,蒸干,残渣加甲醇5 mL加热溶解,作为供试品溶液。另取人参皂苷Ro对照品、竹节参皂苷Ⅳa对照品适量,加甲醇制成每1 mL各含2.0 mg的对照品溶液。照薄层色谱法(附录Ⅵ B)试验,分别吸取竹节参皂苷Ⅳa对照品溶液、人参皂苷Ro对照品溶液各 2 μL,供试品溶液 2 μL 和/或 5 μL,分别点于同一硅胶G薄层板上,以正丁醇-乙酸乙酯-甲醇-甲酸-水(5∶10∶0.5∶0.3∶3.5)上层液为展开剂展开,取出,晾干,喷以10%硫酸乙醇溶液,于105℃加热至斑点显色清晰,置紫外灯(300 nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点。见图1。
2.4 检查
2.4.1 水分测定 依照《中国药典》2005年版(一部)水分测定法(附录IX H第一法)进行测定。测定数据及结果见表1。

图1 珠子参饮片薄层色谱图1、8.分别为竹节参皂苷Ⅳa对照品、人参皂苷Ro对照品 2、3.四川样品溶液(点样量分别为2 μL、5 μL)4.云南样品溶液 5.贵州样品溶液 6、7.湖北样品溶液(点样量分别 2 μL、5 μL)Fig.1 TLC chromatogram of prepared pieces of Rhizoma Panacis majoris1、8.Chikusetsusaponin IVa and ginsenoside Ro reference substance 2-7.samples
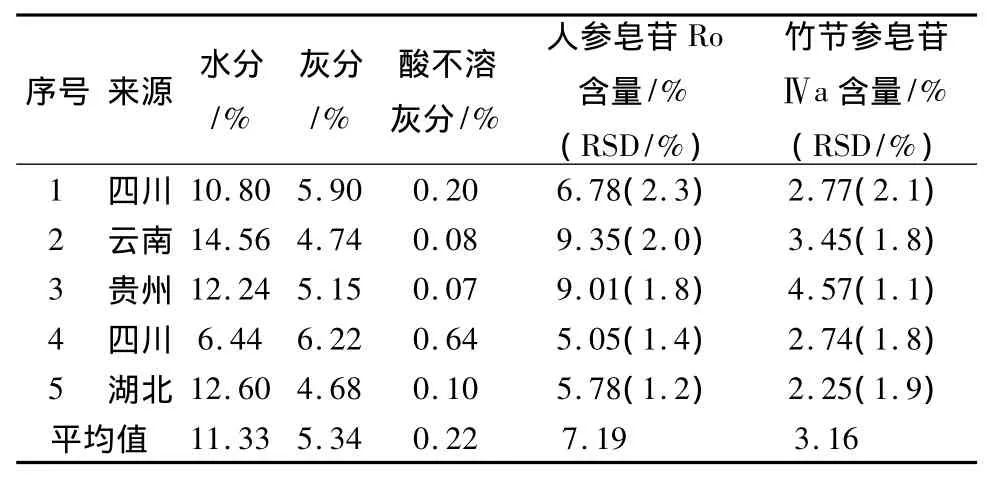
表1 珠子参饮片中水分、灰分、酸不溶灰分及人参皂苷Ro、竹节参皂苷Ⅳa含量Tab.1 Determination results of prepared pieces of Rhizoma Panacis majoris
2.4.2 总灰分 依照《中国药典》2005年版总灰分测定法(附录IX K)进行测定。数据及结果见表1。
2.4.3 酸不溶性灰分测定 依照《中国药典》2005年版一部总灰分及酸不溶性灰分测定法(附录IX K)进行测定。测定数据及结果见表1。
2.5 含量测定
2.5.1 色谱条件 色谱柱:Kromasil Column C18(5 μm,4.6 mm×250 mm);流动相:乙腈-0.2%磷酸溶液(36∶64);检测波长:203 nm;流速:1.0 mL/min;进样量:20 μL;柱温:30℃;理论板数按竹节参皂苷Ⅳa峰计算应不低于3 000。
2.5.2 对照品溶液制备 分别取竹节参皂苷Ⅳa对照品和人参皂苷Ro对照品适量,精密称定,加60%乙醇配制成竹节参皂苷Ⅳa 0.260 5 mg/mL,人参皂苷Ro 0.521 0 mg/mL的溶液,摇匀,作为对照品溶液。
2.5.3 供试品溶液配制 取珠子参粉末(过2号筛)约0.1 g,精密称定,加60%乙醇溶液30 mL,超声处理40 min,取出,加60%乙醇补足重量,滤过,取续滤液即得。
2.5.4 线性关系考察 取上述对照品溶液,分别进样1、2.5、5、10、15、20 μL,测定峰面积,分别以人参皂苷Ro和竹节参皂苷Ⅳa进样量(μg)为横坐标,峰面积为纵坐标,绘制标准曲线,并计算回归方程得:人参皂苷 Ro:Y=1.5×105X-7 909(r=0.999 9),竹节参皂苷Ⅳa:Y=3.2×105X-18 460(r=1)。结果表明,人参皂苷Ro在0.51~10.26 μg范围内、竹节参皂苷Ⅳa在0.26~5.21 μg范围内,峰面积Y与进样量(μg)X线性关系良好。
2.5.5 精密度试验 取对照品溶液10 μL,照2.5.1项下色谱条件,重复进样6次,测定人参皂苷Ro和竹节参皂苷Ⅳa峰面积。结果表明,本法精密度良好,人参皂苷Ro峰面积RSD为0.68%,竹节参皂苷Ⅳa峰面积RSD为1.07%。
2.5.6 稳定性试验 取同一供试品溶液分别于0、2、4、8、12、18、24 h 内进样,照 2.5.1 项下色谱条件测定人参皂苷Ro和竹节参皂苷Ⅳa峰面积。结果表明,供试品溶液在24 h内峰面积稳定,人参皂苷Ro峰面积RSD为0.68%,竹节参皂苷Ⅳa峰面积RSD为1.61%。
2.5.7 重复性试验 取同一批号样品,平行称取6份,按2.5.3项下方法制备供试品溶液,照2.5.1项下色谱条件测定人参皂苷Ro和竹节参皂苷Ⅳa含量。结果表明,本法具有较好的重复性,人参皂苷Ro和竹节参皂苷Ⅳa RSD分别为1.84%和1.93%。2.5.8 回收率试验 取已知含量的样品5份,各0.1 g,精密称定,精密加入人参皂苷Ro和竹节参皂苷Ⅳa对照品适量,按2.5.3项下方法制备供试品溶液,按2.5.1项下色谱条件测定人参皂苷Ro和竹节参皂苷Ⅳa含量。计算回收率,见表2、表3。结果表明,本法回收率良好,人参皂苷Ro和竹节参皂苷Ⅳa的RSD分别为0.46%和0.91%。
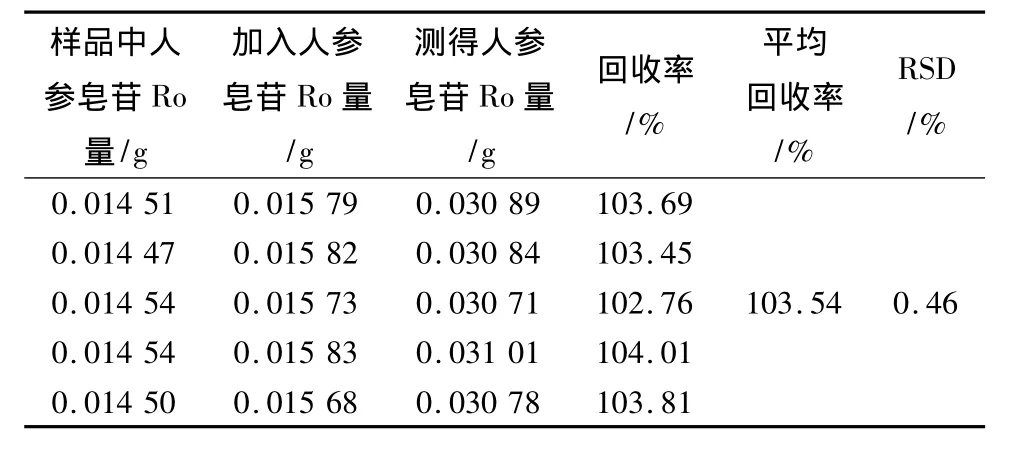
表2 人参皂苷Ro回收率试验结果Tab.2 Results of recovery test of ginsenoside Ro

表3 竹节参皂苷Ⅳa回收率试验结果Tab.3 Results of recovery test of chikusetsusaponin IVa
2.5.9 样品含量测定 取不同批次样品粉末约0.1 g(各2份),精密称定,按2.5.3项下方法制备供试品溶液,进样20 μL,按2.5.1项下色谱条件进行测定,记录色谱峰面积,计算含量,结果见表1。对照品和供试品HPLC图谱见图2。

图2 珠子参饮片HPLC图谱A.对照品 B.四川珠子参样品 C.湖北珠子参样品 1.人参皂苷Ro 2.竹节参皂苷ⅣaFig.2 HPLC chromatograms of prepared pieces of Rhizoma Pannacis majorisA.reference substances B.sample of sichuan C.sample of Hubei 1.ginsenoside Ro 2.chikusetsusaponin IVa
3 讨论
3.1 实验过程所用人参皂苷Ro对照品和竹节参皂苷Ⅳa对照品均为自制,其结构经1HNMR、13CNMR、HMBC、HMQC及HR-MS等方法予以鉴定确认;纯度检查采用HPLC法,面积归一法计算含量,纯度均在98%以上,分别达到了含量测定所用对照品的技术要求。
3.2 薄层色谱鉴别用于中药鉴别具有快速简便等特点。珠子参饮片的薄层色谱鉴别条件的确定,是在对实验条件的系统考查基础上确立的,而且经反复试验证明,该方法具有分离度好、斑点清晰、简便易行等特点,可用于珠子参饮片的鉴别。
3.3 实验过程中,对供试品溶液制备的提取方法、提取溶媒、提取时间等条件进行了实验考察。结果表明,该实验条件提取率高、杂质少、操作简便,可用于珠子参饮片的提取。
3.4 本试验首次建立了HPLC法同时测定珠子参饮片中人参皂苷Ro、竹节参皂苷Ⅳa含量的方法。该方法专属性强、灵敏度高、重现性好,可用于评价珠子参饮片的质量。
[1]中国药典[S].一部.2005:192.
[2]杨崇仁,周 俊,冯宝树,等.秦岭产珠子参根茎的皂苷成分[J].植物学报,1988,30(4):403-408.
[3]李巧云,赵 恒,岳松健,等.大叶珠子参总皂甙的镇痛镇静作用研究[J].华西药学杂志,1993,8(2):90-92.
[4]李慧兰,李存德.珠子参总皂甙对白细胞介素-1,白细胞介素-2的影响[J].云南中医学院学报,1994,17(1):27-29.
[5]朱新华,李存德,后文俊.珠子参总皂甙对脾细胞增殖效应影响的研究[J].昆明医学院学报,1994,15(1):65-67.
[6]陈 涛,崔帮平,黎家华,等.珠子参对小鼠H22肝癌抑制作用及机制[J].世界华人消化杂志,2007,15(24):2597-2601.

