五步蛇毒抗肿瘤组分X对小鼠生殖毒性及F1子代的影响
逄朝霞,鲁文清,翟瑞仁,郭廷凯
蛇毒是由蛇的毒腺分泌的一种天然毒蛋白,成分复杂,主要含蛋白质、多肽及一些酶类,具有广泛的生物学活性,可作为天然的药用资源。在抗肿瘤方面很有潜力[1],然而蛇毒中含有多种复杂成分,这些成分可能会引起临床不良反应[2]。本实验将提取的五步蛇毒抗肿瘤组分X(FX)按照低剂量组为2.5 mg/kg,中剂量组为5 mg/kg,高剂量组为10 mg/kg;第4组为生理盐水阴性对照组(CK),经尾静脉注入鼠体,通过观察五步蛇毒抗肿瘤组分X对雄鼠、孕鼠一般生殖毒性、围产期毒性的影响,提示,五步蛇毒抗肿瘤组分X在5 mg/kg剂量下应用于临床是安全的。现报告如下。
1 材料和方法
1.1 材料 五步蛇(Agkistrodon Acutus)蛇毒冻干粉,辽宁省清源县,DEAE-sepharose琼脂糖凝胶,瑞典Pharmacia公司。性成熟昆明种小鼠,体重(35±2)g,未交配过,由中国药品生物制品检定所实验动物中心提供。
1.2 方法
1.2.1 蛇毒抗肿瘤组分X的分离纯化 DEAESepharose离子交换色谱:称取五步蛇毒冻干粉20 g,用0.02 mol/L pH7.8的Tris-HCl缓冲液溶解。溶液以离心半径8 cm 4 000 r/min离心20 min,取上清,透析12 h后,以6.0 ml/min的流速上阴离子交换柱(DEAE-Sepharose)。上样完毕后以0.02 mol/L pH7.8的Tris-HCl缓冲液洗脱未吸附的杂蛋白,待透过峰下到基线时,分别用0.02 mol/L Tris-HCl含0.05 mol/L和0.1 mol/L氯化钠的缓冲液进行梯度洗脱收集活性峰。
1.2.2 一般生殖毒性实验[3]①分组与给药:选状态良好、发育正常的雄性小鼠120只,雌性120只,分别将雌雄小鼠进行随机分组,雄性4组,每组30只,雌性4组,每组30只;给药剂量参考一般毒理学实验结果[4],低剂量组为 2.5 mg/kg,中剂量组为5 mg/kg,高剂量组为10 mg/kg,第4组为生理盐水阴性对照组(CK);雄性小鼠交配前连续尾静脉给药60 d,雌性小鼠交配前连续尾静脉给药14 d,按雌雄1∶1合笼交配,观察阴栓的有无确定是否有交配行为,有交配行为的雌鼠当天定为妊娠d0,妊娠时间相同或相近的雌鼠分成一组,每组25只,共4组;对雌孕鼠继续给药至妊娠第15天;称体重1次/3 d,给药量0.1 ml/只小鼠,根据体重变化调整;②观察指标:对于雌鼠,一般综合指标包括测定动物用药期间体重和进食量,观察精神状态和活动情况,称体重1次/周,观察交配行为,计算受孕率等;对于雄鼠,测定动物用药期间体重和进食量,观察精神状态和活动情况,交配后处死,检查精子活动度、精子数量和精子形态,称睾丸和附睾重量,计算重量系数,对睾丸组织进行病理检查;在妊娠第18天处死动物并剖腹,计算受孕率,死胎数、活胎数、总着床数、吸收胎数、有死胎孕鼠数、子宫连胎重和孕0~14 d母鼠增重,观察活胎的外形,记录外形畸变率,对随机抽出的2/3胎仔用茜素红染色后做骨髓检查,记录骨髓畸变率,其余1/3胎仔经Bouin液固定后用徒手切片法检查内脏缺陷,包括肝、心、肺、肾、脑、睾丸、卵巢、子宫等脏器,记录内脏畸变率并计算总畸形率。
1.2.3 围产期毒性试验[4]①分组与投药:选状态良好、发育正常的雄性小鼠120只,雌性120只,分别将雌雄小鼠进行随机分组,雄性4组,每组30只,雌性4组,每组30只;给药剂量参考一般毒理学实验结果,设计低剂量组为2.5 mg/kg,中剂量组为5 mg/kg,高剂量组为10 mg/kg,第4组为生理盐水阴性对照组(CK);按雌雄1∶1合笼交配,观察阴栓的有无确定是否有交配行为,有交配行为的雌鼠当天定为妊娠d0,妊娠时间相同或相近的雌鼠分成一组,每组25只,共4组;从妊娠第15天开始每天用药直至分娩后21 d;②观察指标:孕鼠分娩后第7天每窝保留8只仔鼠,不足8只弃去,分别于产后第1、4、8、12、16、21天称重; 仔鼠出生后第5天测试以下指标:翻正反身:记录仔鼠腹面朝上转为四肢着地所需的时间,记录≤10 s和>10 s的仔鼠数;阴性趋地性试验:仔鼠放在倾斜25°斜面上,头部向下,仔鼠会自动转向使其头朝上,观察头部转向180°所需时间 ,以大于和小于20 s为界,记录仔鼠数;断崖回避试验:将仔鼠头部置于台面外,观测仔鼠鼻尖退回台边缘所需时间,记录大于和小于20 s的仔鼠数;游泳能力试验:用仔鼠游泳试验检测中枢神经系统发育情况,仔鼠放入26℃水中游泳15 s,记录直线游动、圆圈游动、浮在水面及下沉的仔鼠数。
随机取产后2个月F1代仔鼠雌雄各10只进行随机交配试验,观察F1代雌鼠的受孕率和胚胎发育情况。
1.3 统计学方法 采用SPSS 13.0统计分析软件,各组观察指标求出±s,组间比较用t检验。
2 结 果
2.1 一般生殖毒性实验
2.1.1 雄鼠 各组动物用药期间精神状态良好,尿、大便和皮毛未因长期用药而发生变化,饮水量和食物消耗量与对照组无显著差异。对照组、低剂量组、中剂量组和高剂量组体重增长值分别为:(9.21±2.38)、(9.40±3.12)、(9.01±1.92)、(6.93±1.87)g,给药期间,高剂量组体重增长受到限制,说明高剂量组雄鼠已产生毒性反应,高剂量组雄鼠睾丸系数与CK组比较有增加,但病理检查未见退变及坏死等病理反应,可认为睾丸系数的相对增加主要是由于体重减少,造成睾丸质量相对增加所致。精子量、精子活动度、交配频度和雄鼠的生育率未见明显差异。
2.1.2 雌鼠 试验期间各组动物精神状态良好,尿、大便和皮毛未因长期用药而发生变化,饮水量和食物消耗量与对照组无明显差别,受孕率也未见明显改变,但高剂量组雌鼠体重增长受到明显限制,说明高剂量组有中毒反应。
2.1.3 孕鼠和胎鼠 各试验组孕鼠在妊娠期间一般健康状况良好,高剂量组孕鼠体重增加和子宫连胎重两项指标与CK组比较有差别,其它指标与CK组比较均无差别,见表1。
2.2 围产期毒性试验 见表2。
2.2.1 对仔鼠体重的影响 高剂量组新生仔鼠体重与CK组相比减少,有显著性差异(P<0.05),但出生后第21天各组仔鼠体重与CK组相比较无明显差别。
2.2.2 对其它体征的影响 各剂量组仔鼠开耳、长牙、睁眼时间与CK组相比均无明显差别(P>0.05),反映神经功能的指标(翻正反向,阴性趋地试验,断崖回避试验和游泳能力)各剂量组仔鼠与CK相比也无明显差别。
2.2.3 对F1子代生殖功能的影响 与CK相比,各剂量组F1子代小鼠交配能力,受孕率,总着床数,活胎数,死胎数,吸收胎数,子宫连胎重和总畸形率无明显差别(P>0.05)。
3 讨 论
发育中的胚胎对外界毒物非常敏感,往往在对成体不产生毒性的剂量下,对胚胎就可产生毒性,从而引起发育停滞和出生缺陷[5]。有关妊娠期受毒性药品影响胚胎发育,造成着床数减少、死胎和吸收胎数增加或影响出生子代生殖系统结构和功能的报道很多[6]。孕前或孕期遭受毒物会延缓胚胎的正常发育,导致发育停滞或死亡,出现吸收胎,活胎体重减轻,胎仔脊柱裂、腭裂、性腺发育不良等畸形;本文结果表明,在高剂量组条件下胚胎体重明显低于阴性对照组,而在5 mg/kg剂量组与CK相比没有明显差异,故在10 mg/kg体重剂量下有可能对胚胎造成影响,但由于没有剂量效应关系,所以不能肯定在10 mg/kg剂量下就产生胚胎毒性,在现有条件下,该实验可以证明,在5 mg/kg剂量时未对雄鼠或孕鼠产生毒性,提示此剂量下FX应用于临床可能是安全的。
出生前暴露于外源性毒素能引起雄性子代生殖系统发育异常,如隐睾,睾丸、附睾重量减轻,精子数目减少,这是检测外源性毒素样物质作用的指标[7]。本文结果表明,FX对雄鼠睾丸无毒性反应剂量大约为5 mg/kg体重,用10 mg/kg剂量处理时对雄鼠的体重和睾丸系数都有一定的影响,但病理检查未见退变及坏死等病理反应,可认为睾丸系数的相对增加主要是由于体重减少,造成睾丸质量相对增加所致。精子量、精子活动度、交配频度和雄鼠的生育率未见明显差异。故仅凭本文结果不能断定高剂量组具有生殖毒性,但在5 mg/kg体重剂量药物应该是安全的,还有待于临床的进一步研究。
[1]吴保平,高春芳,张亚历,等.东亚钳蝎毒生物提取物对人大肠癌细胞的体外抑杀实验.中国肛肠病杂志,.1993,4(1):3-6.
[2]Kiechle FL,Zhang X.Apoptosis:biochemical aspects and clinical implications.Clinica Chimica Acta,2002,326(1-2):27-45.
[3]董伟华,臧梦维,孔天翰,等.蝎毒组分Ⅱ对人喉癌细胞毒性的研究.中国医药学报,1994,4(1):9-11.
[4]Muggia FM.Relevance of chemotherapy dose and schedule to outcomes in ovarian cancer.Semin Oncol,2004,31(6 Suppl 15):19-24.
[5]苏智广,梁爱华,袁静明.东亚钳蝎神经毒素的研究进展.山西大学学报(自然科学版),1997,20(3):343-7.
[6]郑智敏,王成裕,田中岭,等.蝎毒对人肿瘤细胞株和动物移植性肿瘤的作用.河南医科大学学报,1995,30(4):351-3.
[7]Hammou Oubrahim,Jun Wang,Earl R,et al.Molecular cloning and characterization of murine caspase-12 gene promoter.Proc Natl Acad Sci U S A,2005,102(7):2322-27.
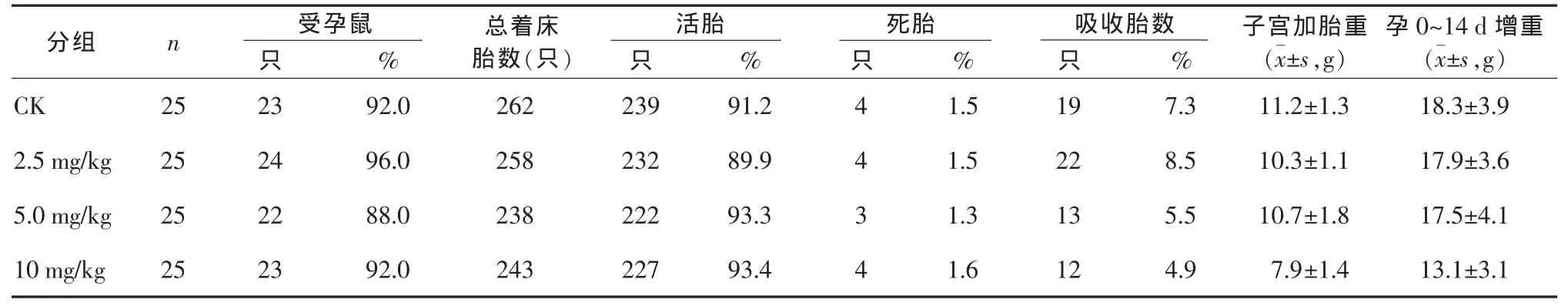
表1 FX激肽原酶对雌性小鼠F0生殖功能的影响
表2 蛇毒激肽原酶对F1仔鼠一般体征的影响(±s)
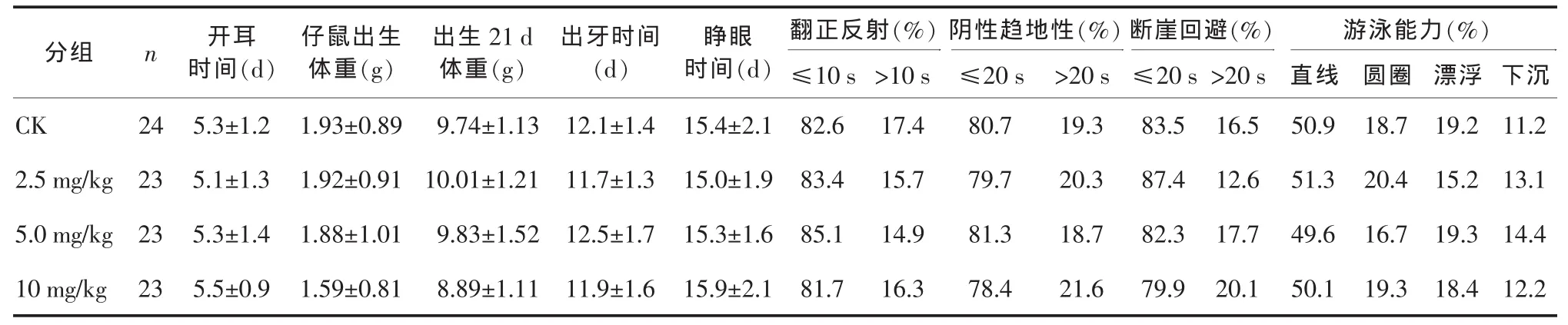
表2 蛇毒激肽原酶对F1仔鼠一般体征的影响(±s)
?

