国产化学发光分析系统检测睾酮的临床验证
林 云 ,汪先桃 ,刘 萍
(1、云南省中医医院检验科,云南 昆明 650021;2、博奥赛斯(天津)生物科技有限公司,天津 300203)
以往全自动化学发光分析系统主要以国外产品为主,而随着国内科技产业发展和卫生保健事业的需要,国内开始了全自动化学发光分析系统研发工作,并有产品推出。为评价国产Bioscience PETECK96-I全自动化学发光分析系统与罗氏电自动化学发光分析系统检测睾酮(Testosterone,以下简称T)是否等效,研究按照国家关于新药临床验证的指导原则和体外诊断试剂临床研究技术指导原则[1]、NCCLS指南文件[2],进行该系统检测睾酮的临床性能测试。
1 材料与方法
1.1 材料 对照系统:罗氏公司化学发光全自动免疫分析仪 Elecsys2010,国药管械(进)字 2002第3400335号。配套T检测试剂盒,国食药监械2008第2400661号,试剂盒批号:155387-02,参考值:男性 2.8~8ng/mL,女性 0~0.82ng/mL。 验证系统:博奥赛斯 (天津)生物科技有限公司Bioscience PETECK96-I化学发光免疫分析系统。试剂:为配套T试剂、校准品和质控品。
1.2 方法
1.2.1 临床检测样品 根据国家关于体外诊断试剂盒二类临床试验的要求,收集了120例样本,均来自本院就诊的门诊及住院病人。样本均为空腹时抽取的静脉血,自然凝血后,离心分离出血清,去除严重溶血、脂血、黄疸的样本于-20℃保存,每份标本不少于500μl。所有待测样本浓度均应≤20ng/ml,其中超出医学决定水平值样本50例。
1.2.2 临床试验对照产品的确定 罗氏公司生产的化学发光全自动免疫分析系统可以定量检测T,经国内外同行的评价,认为此系统及其配套T检测试剂盒为国际一流的水准[3],因此,本临床试验以Roche 2010电化学发光全自动免疫分析系统(Elecsys 2010)对T的测定值作为“金标准”,以此考查天津博奥赛斯公司研制的Bioscience PETECK96-I化学发光分析系统使用其配套T检测试剂盒的检测结果是否等效。
1.2.3 统计学处理 结果以x±s表示,采用SPSS 13.0统计分析软件对Elecsys2010的测定值和Bioscience PETECK96-IT的测定值两组数据进行配对t检验(检验水准α=0.05)、线性相关和回归分析并评价。
2 结果
2.1 准确性
用试剂盒对试剂盒校准品进行双孔检测,用Log(X)-Logit(Y)数学模型拟合,对两条剂量-反应曲线进行斜率t检验;以国家标准品系列为标准,计算试剂盒校准品的实测浓度,并计算5个校准品实测浓度与理论浓度比值的平均值。结果见表1。
斜率t检验结果t=1.21,∣t∣≤2.447,两条直线不明显偏离平行;实测浓度与理论浓度平均差异小于10%,说明试剂盒校准品定值准确。试剂盒校准品相关系数绝对值∣γ∣>0.99线性良好。
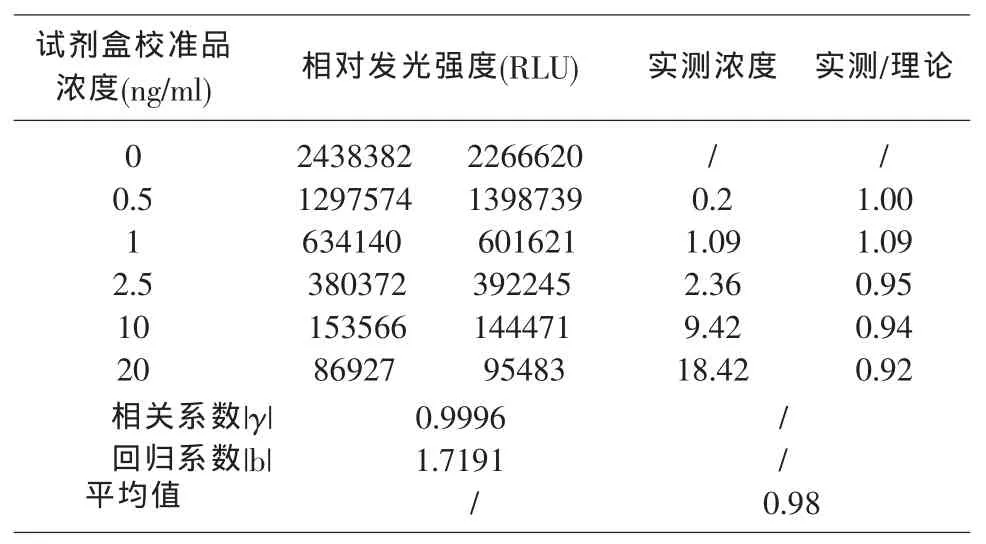
表1 准确性:试剂盒校准品检测结果
2.2 精密性
用三批试剂盒对质控品QcL和QcH进行10孔重复测定,统计实验结果的标准偏差(SD)和平均值。由SD和 的比值计算得到批内和批间的变异系数CV。结果见表2。
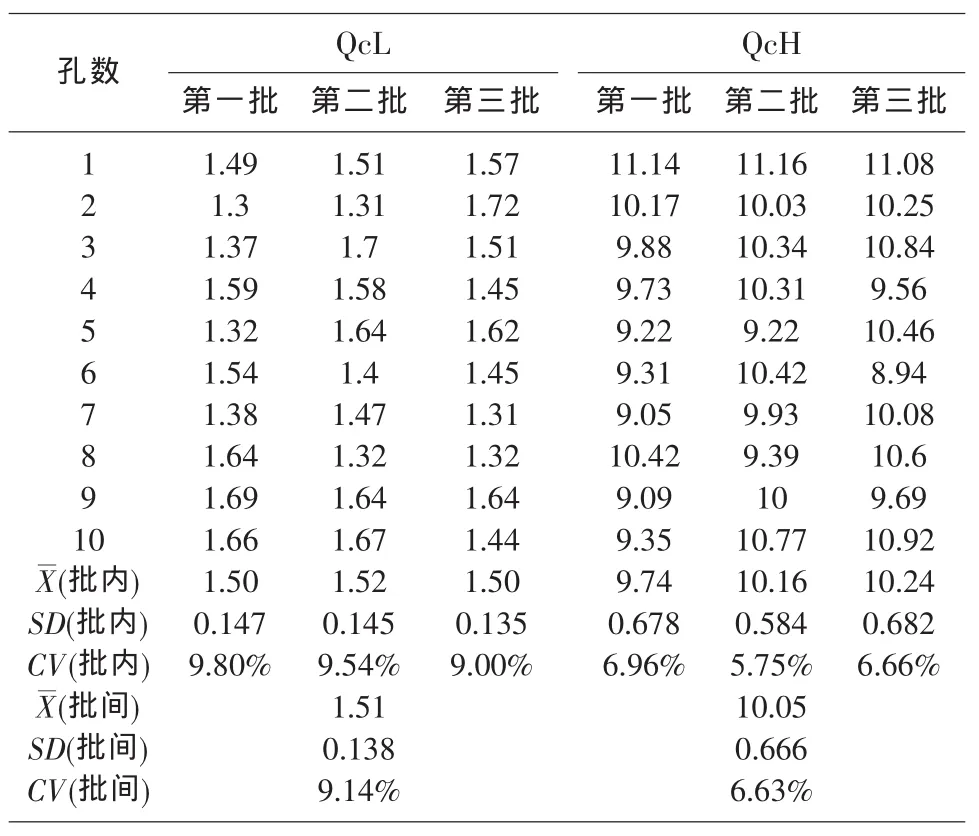
表2 精密性
由上表知本产品的批内CV小于15%,批间CV小于20%。
2.3 参考范围的测定
选择1186份健康人群血清样品,其中成年男性132例、成年女性956例和男性儿童98例,建立90%置信区间。结果见表3。

表3 参考范围
2.4 特异性测试
临床上T的主要类似物是雌三醇(E3)和雌二醇(E2),孕酮(P)。 用二甲亚砜分别溶解 E3、E2、P,然后用稀释液2#分别稀释到1000ng/mL,用试剂盒检测。结果见表4。
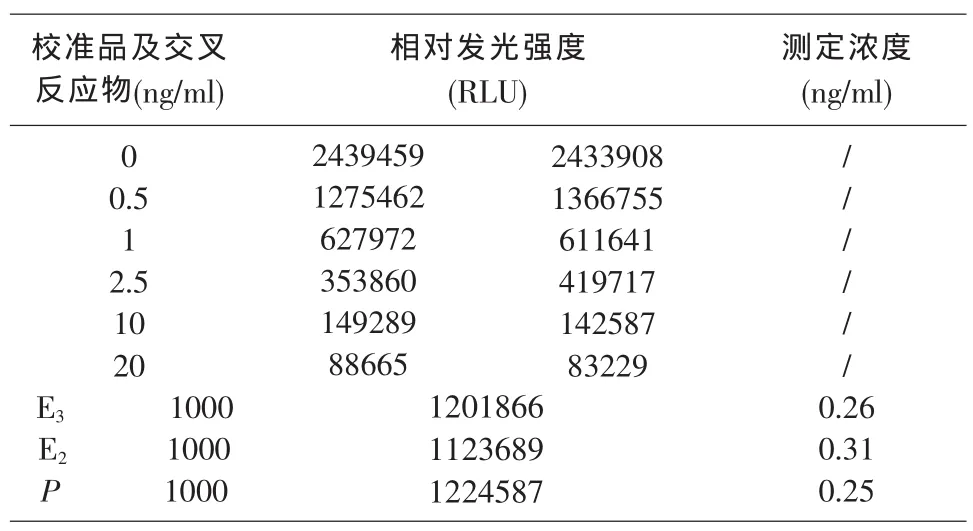
表4 交叉反应
当 E3、E2、P 的浓度分别为 1000、1000、1000ng/ml时,没有发现交叉反应。
2.5 试剂盒测定范围及最低检测限
实验方法:将T浓储液稀释成系列浓度,加样量为每孔50μl;然后每孔加入50μl的T酶结合物,37℃温育30分钟,洗涤5次,每孔加发光液100μl,5min后读数。结果见表5。

表5 试剂盒测定范围及最低检测限数据表
试剂 在0.1~20ng/mL范围内成线性发展,试剂盒最低检测限可达0.1ng/ml。
2.6 两种系统测定值配对t检验统计分析 结果见表6。

表6 两种方法测定值比较
2.7 两种系统测定值相关性分析
以Elecsys2010的测定数值为横坐标,以Bioscience PETECK96-I的测定数值为纵坐标,利用EXCEL软件做图(图1),计算相关系数γ和回归系数并进行t检验。直线方程为Y=1.0348X–0.0335,线性回归系数为1.0348,相关系数为0.9413。以SPSS 13.0对相关系数进行 t检验 (检验水准α=0.05),P<0.001,两种方法测定的T值密切相关。回归系数为1.0348,表明两种方法之间测定的T值一致性良好。

2.8 测定值不一致的分析
经对数据的统计分析,120例样本中有6例测定值结果不一致(占5.0%),对于不符合的样本,经重复性检测,测定值没有明显改变。使用Elecsys2010进行复测,复测2例与Elecsys2010结果一致,4例与Bioscience PETECK96-I结果一致(见表7)。经分析没有规律性的偏差产生,多为临界偏差,所以考虑产生不一致的原因主要可能由样本病例的个体差异、两种方法测定原理的差别及操作随机误差造成的。
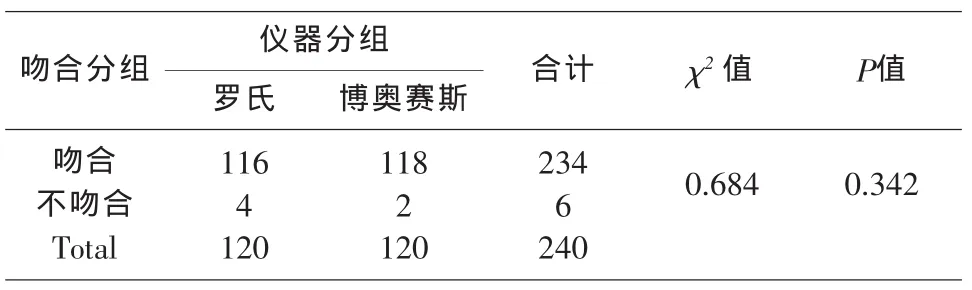
表7 两种不同检查方法吻合度对比
3 讨论
T是男性激素,T促进男性第二性征的发育,维持前列腺和精囊的功能。血循环中的T绝大多数与载体蛋白质结合[4],T在体内的含量不高。CLIA法是利用抗原抗体间免疫反应的高亲和力、高度特异性和化学发光的高敏感性建立起来的一种微量免疫定量测定技术,采用化学发光免疫分析(CLIA)法检测T浓度具有灵敏度高、线性检测范围宽、操作简单、定量和稳定的优点[5]。
Bioscience PETECK96-I的配套T定量检测试剂盒采用竞争抑制法,以辣根过氧化物酶(HRP)为标记物,样品中的T浓度依据由标准品T浓度建立的数学模型进行定量,从而检测人血清中T的含量。
检测仪器的系统性能测试数据是临床实用的重要指标,每一项测试必须按照国家关于新药临床验证的指导原则和体外诊断试剂临床研究技术指导原则和NCCLS指南文件严格操作。
Bioscience PETECK96-I测定T的精密度 CV<20%,参考范围符合临床应用,临床常见干扰物质对T的检测,无统计学意义,临床线性范围为0.1~20ng/ml,能达到临床检测要求。比对试验中,同组测试中采用Roche 2010电化学发光全自动免疫分析系统(Elecsys 2010)对T的测定值与天津博奥赛斯公司研制的Bioscience PETECK96-I化学发光分析系统使用其配套T检测进行对比试验。两组数据比较P>0.05,差异无统计学意义,两组数据线性回归系数为1.0348,相关系数为0.9413总体可比性较好。Bioscience PETECK96-I的灵敏度、特异性高,测定结果稳定。
综合研究结果分析,Bioscience PETECK96-IT定量检测与Elecsys 2010对T的测定值等效,该系统达到临床测定要求,可用于临床检测。
[1]国家食品药品监督管理局令(第3号).药物临床试验质量管理规范[S].北京:国家食品药品监督管理局,2003.
[2]Clinical and Laboratory Standards Institute.EP9-2A,Method comparison and bias estimation using patient samples,approved guideline[S].Pennsylvania.CLSI,1986.
[3]阳 苹.罗氏MODULAR E170全自动电化学发光免疫分析仪性能验证[J].重庆医学,2009,38(19):2395-2397.
[4]辛钟成.老年男性雄激素缺乏综合征和睾酮补充疗法的研究进展[J].中华老年医学杂志,2003,22(6):333-334.
[5]尹东光,贺佑丰.促甲状腺激素化学发光免疫分析的研究[J].分析化学,2004,32(7):45-47.

