喹啉、吲哚和咔唑对 Ni-Mo催化剂上4,6-DMDBT HDS反应抑制作用
韩姝娜,周同娜,柴永明,周红军,刘晨光
(中国石油大学CNPC催化重点实验室,山东青岛266555)
随着柴油燃烧后排出的废气对环境的危害日渐显现,世界许多国家和地区相继颁布了更为严格的柴油标准,而我国的柴油标准正在逐渐与国际标准接轨。在柴油标准中,硫含量是清洁柴油的重要指标,美国等发达国家要求将柴油中的硫质量分数从500μg/g降至小于15μg/g[1],而且原油劣质化、重质化的情况日益严重,所以必须对超深度加氢脱硫技术进行研究。
二苯并噻吩类物质是柴油中较难脱除的含硫化合物,其中烷基取代二苯并噻吩类化合物由于空间位阻效应,更难以脱除。原料中存在的其他杂环化合物对这些物质的加氢脱硫(HDS)反应十分敏感[2-3],有机含氮杂环化合物就是二苯并噻吩类物质超深度加氢脱硫过程的主要抑制剂[4]。柴油中的有机含氮杂环化合物分为喹啉、吖啶等碱性氮化物和吲哚、咔唑等非碱性氮化物。含氮化合物对于含硫化合物的 HDS有明显的抑制作用,而且碱性氮化物对于 HDS的抑制作用强于非碱性氮化物[5],并且部分加氢的含氮化合物物种对 HDS反应抑制作用比其母体物种更强[6-8]。
笔者以喹啉、吲哚和咔唑作为模型化合物考察了含氮化合物对4,6-二甲基二苯并噻吩(4,6-DMDBT)在Ni-Mo加氢催化剂上 HDS的反应活性和选择性的影响,并通过这3种氮化物对4,6-DMDBT加氢反应活性和反应路径的抑制作用推测氮化物抑制Ni-Mo催化剂 HDS活性中心的机理。
1 实验部分
1.1 药品
4,6-二甲基二苯并噻吩(4,6-DMDBT),自制,纯度>98%;甲苯、喹啉、吲哚均为AR试剂,国药集团产品。
1.2 催化剂制备
将Al2O3/分子筛按比例混合研磨,加入田菁粉和稀硝酸挤压成型,500℃焙烧 4 h,得到载体。MoO3、NiCO3·3Ni(OH)2·4H2O和磷酸配制浸渍液,等体积浸渍,500℃焙烧4 h制得 Ni-Mo催化剂 CK-2。其基本性质见表 1。将催化剂破碎为20~40目的颗粒后使用。

表1 加氢脱硫催化剂CK-2的基本性质Table 1 Properties of CK-2 HDS catalyst
1.3 加氢脱硫实验
采用长60 cm、直径8 mm、厚度2 mm的不锈钢反应管。将1.6 g催化剂用1.5倍体积的石英砂稀释后装填在反应管的中部,上、下部均用石英砂填实。在反应过程中,催化剂床层始终处于反应管的等温区。在2 MPa、300℃条件下,采用质量分数为2%的CS2-甲苯溶液,对催化剂进行预硫化8 h。预硫化后,在反应温度 280℃、液时空速 5 h-1、V(H2)/V(Oil)=300的条件下,进行加氢反应。反应原料中含4,6-二甲基二苯并噻吩的质量分数为0.5%,喹啉、吲哚和咔唑的质量分数分别为0.24%、0.31%和0.43%。每个加氢反应条件稳定6 h后,每隔1 h在反应器出口处取样,测定产物的组成。
1.4 原料和产物的分析方法
采 用 美 国 Finnigan 公 司 的 TRACE GC-TRACEDSQ色-质联用仪定性液相中 HDS和加氢脱氮(HDN)产物;采用agilent公司气相色谱仪定量分析其组成。FID检测器,色谱柱 HP-5 (30 m×0.32 mm×0.5μm)。气化室温度330℃,检测室温度330℃,柱温80~300℃(程序升温),分流比80,采用面积归一法定量计算产物组成。
2 结果与讨论
2.1 4,6-DMDBT加氢脱硫反应的转化率和产物组成
含硫化合物的加氢脱硫反应存在2条反应路径:先对芳环加氢再脱除分子中硫的先加氢再脱硫(HYD)路径和直接脱除分子中硫的直接脱硫(DDS)路径[9]。表 2为 280℃、2 MPa(总压)条件下, 4,6-DMDBT在CK-2催化剂上 HDS产物及其分布。

表2 在CK-2催化剂上4,6-DMDBT加氢脱硫反应产物和分布Table 2 Product distribution of 4,6-DMDBT HDS over Ni-Mo catalyst
由表2可以看出,3,3′-二甲基联苯(3,3′-DMBP)及其异构体是DDS反应路径主要产物,3-(3′-甲基环己烷)甲苯(3,3′-MCHT)及其异构体为 HYD反应路径主要产物,并且出现了3-甲基联苯(3-MBP)及其异构体和三甲基联苯(TMBP)及其异构体,说明4,6-DMDBT在催化剂上发生了甲基不对称转移反应。这是由于载体中添加了一定量的 H-USY分子筛,酸性位增强的缘故[10]。值得注意的是,在产物中,出现了相当数量的3-甲基-(5-甲苯基)-1-环己烯(3,5’-MTCH)及其异构体,其原因有待进一步研究。4,6-DMDBT部分加氢产物4,6-四氢二甲基二苯并噻吩(4,6-DMTHDBT)与4,6-DMDBT相比,电子云密度减弱,并且不是平面分子结构,减弱了硫原子附近取代甲基的空间位阻作用,有利于硫原子的端连吸附在氢解活性位上发生DDS反应,但在氮化物存在条件下,没有检测到这类化合物。在CK-2催化剂上,280℃、2 MPa(总压)条件下, 4,6-DMDBT HDS反应路径如图1所示。

图1 4,6-DMDBT在CK-2催化剂上加氢反应路径Fig.1 Reaction pathways of the hydrodesulfurization of 4,6-DMDBT on CK-2 catalyst 280℃;Total pressure 2 MPa
以4,6-DMDBT加氢生成的所有不含硫加氢产物,主要是3,3’-二甲基联苯(3,3’-DMBP)、3-(3’-甲基环己烷)甲苯(3,3’-MCHT)等的产率总和表示脱硫率(xHDS)。分别由式(1)~(5)计算该催化加氢反应中的 sDDS、sHYD、ATotal、ADDS和 AHYD。

式(1)~(5)中,F0为 4,6-DMDBT进料流速, mol/s;x(4,6-DMDBT)为反应转化率,%;m为催化剂质量,kg;sDDS为通过DDS反应路径得到的产物选择性,%;sHYD为通过 HYD反应路径得到的产物选择性,%;ADDS、AHYD和 ATotal分别为 DDS、HYD反应路径活性和总活性,μmol/(s·kg)[11]。由此计算得到的数据列于表3。
从表3可以看出,4,6-DMDBT加氢脱硫的DDS反应选择性与 HYD反应选择性的比值为0.67,说明4,6-DMDBT的加氢脱硫主要通过 HYD反应路径进行,与添加分子筛的催化剂加氢反应的结论[12]一致。
2.2 含氮化合物对4,6-DMDBT HDS转化率的影响
碱性氮化物对于 HDS有较强的抑制作用[13]。喹啉在柴油中的含量较少,但是对 HDS的抑制作用非常明显。咔唑类化合物是柴油中主要的含氮化合物,和吲哚同为非碱性氮化物。它们对 HDS的影响有不同的结论。Van Looij等[13]得到,在碱氮质量分数2~30μg/g条件下,氮化物对噻吩的抑制作用大小顺序为:吲哚、喹啉、咔唑。Laredo等[14-15]认为,非碱性氮化物咔唑对 DBT的 HDS的抑制作用比其他的碱性和非碱性氮化物例如喹啉和吲哚弱。咔唑质量分数大于50μg/g时,抑制作用不显著。笔者考察了在较高氮质量分数(200~500μg/g)条件下,喹啉、吲哚和咔唑对4,6-DMDBT HDS的抑制作用。图2为3种不同添加质量分数下,喹啉、吲哚和咔唑对4,6-DMDBT HDS转化率的影响。

表3 4,6-DMDBT在CK-2催化剂上的HDS结果Table 3 HDS results of 4,6-DMDBT over CK-2 catalyst

图2 添加氮化物前后4,6-DMDBT在CK-2催化剂上HDS反应的转化率(x(4,6-DMDBT))Fig.2 Conversion of 4,6-DMDBT(x(4,6-DMDBT))HDS with and without nitrogen compounds over CK-2 catalyst(1)Indole;(2)Carbazole;(3)Quinoline 280℃;Total pressure 2 MPa
由图2可以看出,喹啉、吲哚和咔唑对4,6-DMDBT的 HDS反应有非常明显的抑制作用。比较相似氮添加量时的 4,6-DMDBT HDS转化率得出,在CK-2催化剂上,氮化物对于4,6-DMDBT HDS的抑制作用大小顺序为:喹啉、咔唑、吲哚。脱硫率也出现与4,6-DMDBT转化率相似的规律,此处没有另列图示。
2.3 含氮化合物对4,6-DMDBT HDS反应路径的抑制作用
加入喹啉、吲哚和咔唑后,4,6-DMDBT加氢脱硫的DDS和HYD选择性之比随氮化物加入量的变化如图3所示,其3种活性的变化列于表4。由图3和表4可以看出,氮化物的加入大幅降低了4,6-DMDBT HDS总活性、DDS活性以及 HYD活性。这3种氮化物对于CK-2催化剂的4,6-DMDBT HDS总活性、DDS活性以及HYD活性的抑制作用大小顺序为:喹啉、咔唑、吲哚。喹啉和咔唑的加入增加DDS反应产物所占的比例,sDDS/sHYD增大。添加喹啉使 DDS反应选择性增加的幅度较大(图3(3)),咔唑作用较小。在添加喹啉的条件下, DDS反应成为4,6-DMDBT HDS的主要反应。当咔唑存在时,DDS和 HYD反应路径的比例很相近,当添加的咔唑质量分数(以氮计)大于258μg/g时,发生DDS反应的4,6-DMDBT的量超过发生HYD反应的。吲哚与前2种氮化物的影响不同,在吲哚质量分数(以氮计)小于403μg/g时,发生HYD反应的4,6-DMDBT的量大于发生DDS反应的;当吲哚质量分数(以氮计)为517μg/g时,DDS成为4,6-DMDBT HDS的主要反应;随着吲哚质量分数的增加,sDDS/sHYD增大。
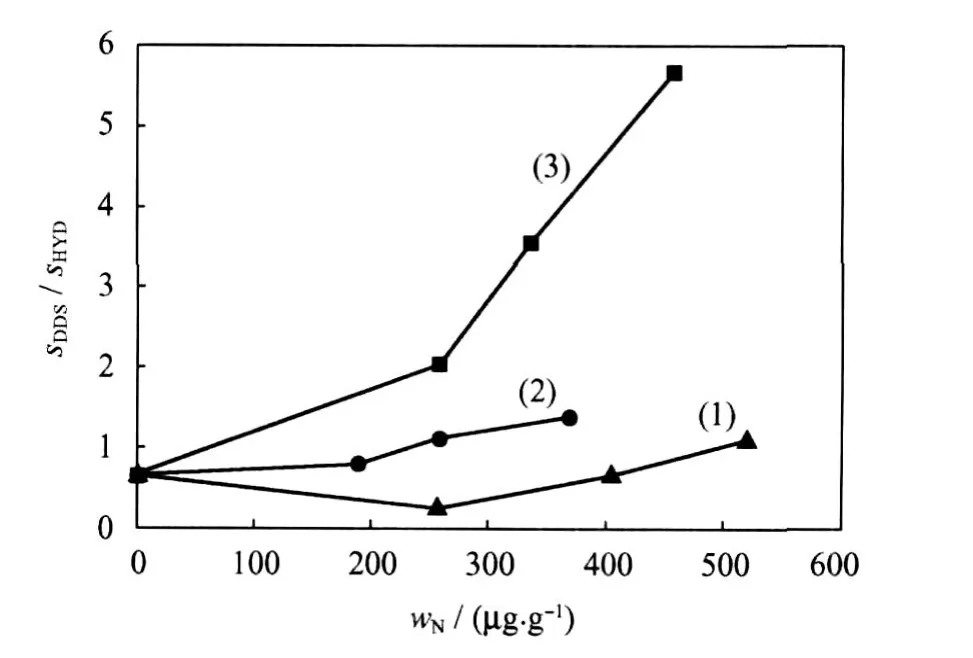
图3 加入不同量氮化物后4,6-DMDBT HDS的DDS和HYD选择性之比(sDDS/sHYD)Fig.3 sDDS/sHYDof 4,6-DMDBT HDS with different amounts of nitrogen compounds over CK-2 catalystNitrogen compound:(1)Indole;(2)Carbazole;(3)Quinoline 280℃;Total pressure 2 MPa
图4为4,6-DMDBT的 HDS产物分布随喹啉添加量的变化。可以看出,随着喹啉添加量的增加, HYD反应路径的主要产物3,3′-MCHT产率下降非常迅速,因为催化剂酸性位影响而发生甲基转移反应产生的MCHT异构体含量亦下降明显,且两者的比例明显改变,MCHT异构体的比例要少于未添加喹啉时。HYD活性也从22μmol/(s·kg)快速下降到2.7μmol/(s·kg)。DDS反应路径的主要产物为3,3′-DMBP,但是,没有检测到其异构体。DDS活性从14μmol/(s·kg)下降到5.5μmol/(s·kg)。这说明喹啉不但会抑制 HYD活性和DDS活性,而且还会抑制催化剂的烷基转移反应活性。

表4 氮化物存在下CK-2催化剂的4,6-DMDBT HDS总活性、DDS活性和HYD活性Table 4 Total,DDS and HYD activities of 4,6-DMDBT HDS with nitrogen compounds over CK-2 catalyst
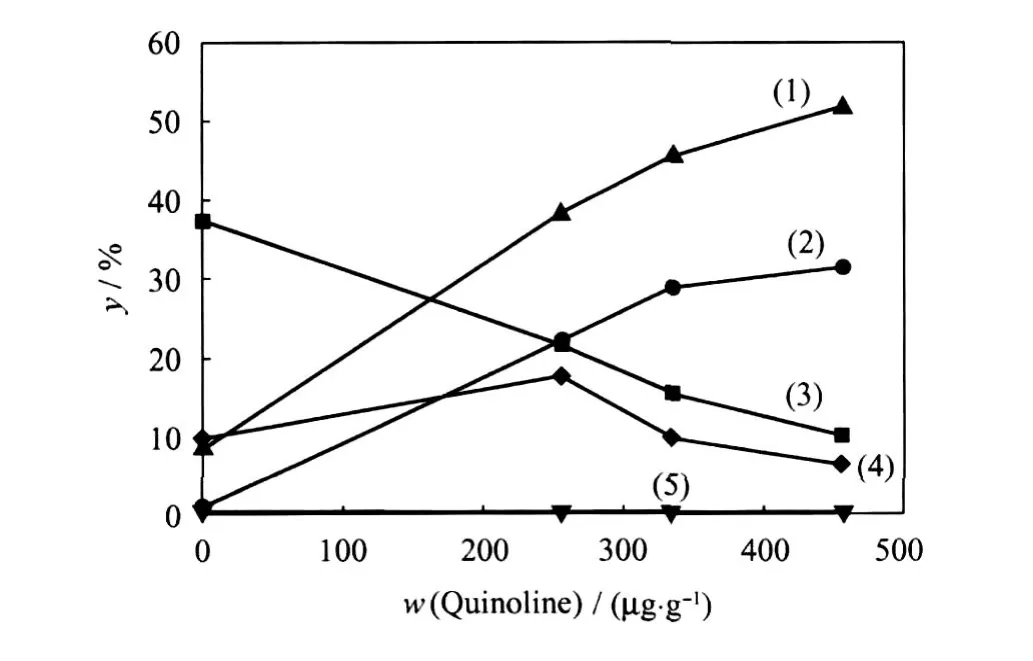
图4 4,6-DMDBT加氢脱硫产物分布随喹啉添加量的变化Fig.4 Product distribution of 4,6-DMDBT HDS over CK-2 catalyst vs the amount of quinoline added(1)3,3′-DMBP;(2)DMTHDBT;(3)3,3′-MCHT isomers; (4)3,3′-MCHT;(5)4,6-DMDBT isomers 280℃;Total pressure 2 MPa
根据实验结果,喹啉对于Ni-Mo催化剂 HYD活性位的抑制作用大于对DDS活性位,并能毒化催化剂酸性位,减少发生甲基转移和异构化反应的比例。通过分子模拟计算得出,喹啉有比4,6-DMDBT更高的键序,所以4,6-DMDBT和喹啉竞争吸附在加氢活性位上,喹啉占据大部分位置, 4,6-DMDBT的硫原子的净电荷比喹啉上的氮原子高,4,6-DMDBT相比于喹啉有更高的氢解趋势[16]。喹啉对催化剂酸性位的毒化,较大程度上抑制了异构化反应的发生,但相对提高了发生不对称(歧化)反应的比例。催化剂B酸中心的增加有利于发生异构化反应,而中等酸性则促进歧化反应的发生[17]。由此,喹啉通过形成带正电荷的物种与B酸中心相互作用,并且通过N原子的孤对电子和芳环的π电子云,能够强烈地吸附到L酸中心上,优先吸附于催化剂的较强酸位上,抑制异构化反应发生。
图5为4,6-DMDBT的 HDS产物分布随吲哚添加量的变化。与喹啉的剧烈影响不同,吲哚的抑制作用比较温和。在最初引入吲哚时,3,3′-MCHT异构体数量减少,同时,发生甲基不对称反应的产物4-MDBT和TMDBT的直接脱硫的产物3-MBP和TMBP数量有微量增加。DDS产物3,3′-DMBP的数量也有一定幅度的增加,没有检测到其异构体。四氢二甲基二苯并噻吩(DMTHDBT)的数量有少量增加,而4,6-DMDBT异构体的数量微量增加。增加吲哚添加量,3,3′-MCHT及其异构体数量有较大程度减少。
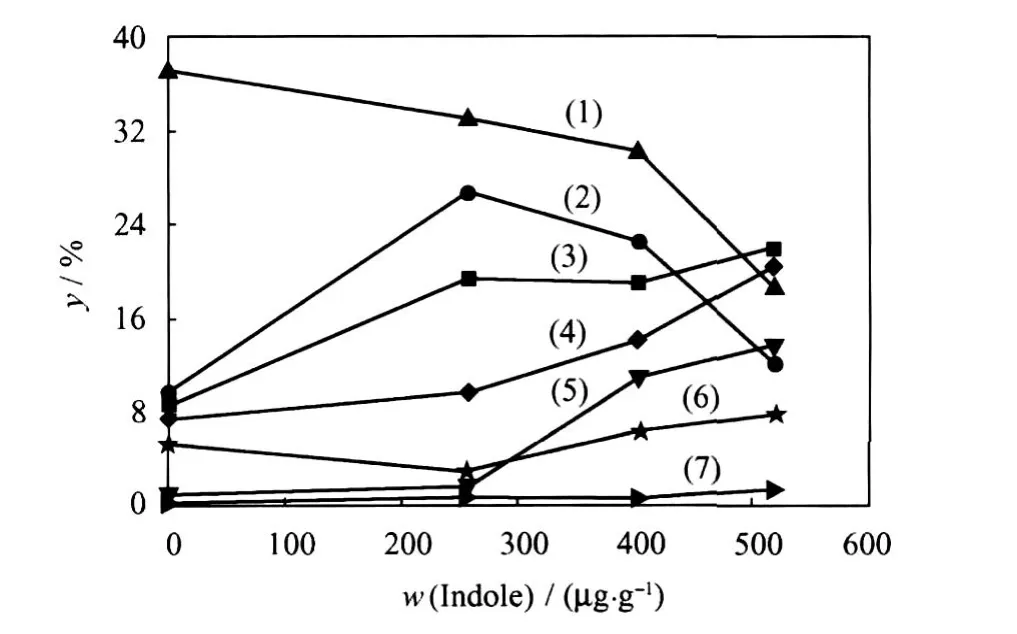
图5 4,6-DMDBT加氢脱硫产物分布随吲哚添加量的变化Fig.5 Product distribution of 4,6-DMDBT HDS over CK-2 catalyst vs the amount of indole added(1)3,3′-MCHT isomers;(2)3,3′-MCHT;(3)3,3′-DMBP; (4)3-MBP;(5)DMTHDBT;(6)TMBP;(7)4,6-DMDBT isomers 280℃;Total pressure 2 MPa
吲哚为非碱性氮化物,在4,6-DMDBT HDS中增大了 HYD反应比例,这与喹啉不同。普遍认为, 4,6-DMDBT的DDS反应与催化剂酸性位有关,而且活性的提高与酸性位促进甲基转移和不对称反应减弱4位和6位甲基空间位阻也有极大的关系[16-17],所以吲哚对于 DDS反应的抑制主要原因是吲哚或其部分加氢产物对催化剂酸性位的抑制。HDS反应中产生的异构体减少也表明了这一点。
图6为4,6-DMDBT的 HDS产物分布随咔唑添加量的变化。咔唑的抑制作用介于吲哚和喹啉之间。咔唑的存在使4,6-DMDBT HYD反应路径的产物3,3′-MCHT减少,其异构体的量下降较多; DDS反应路径产物3,3′-DMBP的数量增加,没有检测到它的异构体;4,6-DMDBT的异构体减少, DMTHDBT比例增加。在咔唑质量分数为188μg/g时,4,6-DMDBT的 HYD反应为主要反应,但是,质量分数为258和366μg/g时,DDS为主要反应。
咔唑趋向于抑制 HYD反应路径,对催化剂的酸性位也有抑制作用,与喹啉的抑制作用相比,明显偏弱。有研究得出,咔唑的影响是可逆的[18]。可见,与前2种氮化物相比,咔唑及其部分加氢产物在催化剂活性位的脱附较容易。

图6 4,6-DMDBT加氢脱硫产物分布随咔唑添加量的变化Fig.6 Product distribution of 4,6-DMDBT HDS over CK-2 catalyst vs the amount of carbazole added(1)3,3′-DMBP;(2)3,3′-MCHT isomers;(3)3,3′-MCHT; (4)DMTHDBT;(5)4,6-DMDBT isomers 280℃;Total pressure 2 MPa
目前对Ni-Mo催化剂的 HDS活性位的认识尚不统一,较多被接受的观点是,Ni-Mo-S相上不饱和位形成的硫空穴是加氢活性中心,并具有弱的氢解活性,它可以与 H2S作用转化为B酸中心,B酸中心被认为是氢解和异构化反应活性中心[19]。喹啉、吲哚和咔唑对加氢活性中心的吸附强弱取决于其电子云密度,密度越大,吸附能力越强。对于氢解活性位的抑制作用取决于氮化物的气相碱度,在相似氮化物添加量时,喹啉表现出对DDS反应路径较强的抑制作用(3,3′-DMBP的产率最低),咔唑次之,吲哚最弱。吲哚存在下,4,6-DMDBT的 HYD反应多于DDS反应,推测吲哚与其他2种含氮杂环化合物相比更易于加氢生成气相碱度比吲哚强的中间产物——二氢吲哚和乙基苯胺,它们吸附在DDS活性位,而此时吲哚已从 HYD活性中心上解离, 4,6-DMDBT主要通过 HYD反应路径脱硫。根据4-MDBT和其他产物异构体的产率变化或消失,载体的酸性位也会被氮化物中和,而且,比催化剂上与Mo有关的B酸位恢复得慢。
3 结 论
(1)在本次实验条件下,Ni-Mo催化剂上,喹啉、吲哚、咔唑对4,6-DMDBT HDS转化率的抑制作用大小顺序为:喹啉、咔唑、吲哚。
(2)3种氮化物对于4,6-DMDBT HDS反应路径的影响各不相同。喹啉主要抑制 HYD反应活性,增加DDS反应的比例,并且,对催化剂的酸性位有较强的抑制作用。吲哚存在下,4,6-DMDBT发生HYD反应的占大多数,吲哚部分加氢产物主要抑制催化剂的酸性位,而不是 HYD反应活性位。咔唑的抑制作用介于吲哚和喹啉之间,DDS和 HYD反应选择性与不添加氮化物时4,6-DMDBT加氢反应相近,DDS反应路径比例略有提高。
(3)载体的酸位被氮化物或其加氢中间产物中和,而且比催化剂上与 Mo有关的B酸位恢复得慢。
[1]李大东,蒋福康.清洁燃料生产技术的新进展[J].中国工程科学,2003,5(3):6-14.(LI Dadong,J IANG Fukang.The new evolution of technology for clean fuel production[J].Engineering Science,2003,5(3):6-14.)
[2]MIZUTANI H,GODO H,TAKAYU KI O,et al. Inhibition effect ofnitrogen compounds on CoMoP/ Al2O3catalysts with alkali or zeolite added in hydrodesulfurization of dibenzothiophene and 4,6-dimethyldibenzothiophene[J]. Applied Catalysis A: General,2005,295(2):193-200.
[3]CHAN K,JUNGJ L,JUN S B,et al.Poisoning effect of nitrogen compounds on the performance of CoMoS/ Al2O3catalyst in the hydrodesulfurization of dibenzothiophene, 4-methyldibenzothiophene, and 4,6-dimethyldibenzothiophene[J].Applied Catalysis B: Environmental,2001,35(1):59-68.
[4]LAREDO S G C,DE LOS REYES H J A,LUIS CANO D J,et al.Inhibition effects of nitrogen compounds on the hydrodesulfurization of dibenzothiophene[J]. Applied Catalysis,2001,207(1-2):103-112.
[5]SHIRAISHI Y,TACHIBANA K,HIRAI T,et al.A novel desulfurization process for fuel oils based on the formation and subsequent precipitation of S-alkylsulfonium salts 5 Denitrogenation reactivity of basic and neutral nitrogen compounds[J].Industrial Engineering Chemistry Research,2001,40(22):4919-4924.
[6]KOL TAIT,MACAUDA M,GUEVARA A. Comparative inhibiting effect of polycondensed aromatics and nitrogen compounds on the hydrodesulfurization of alkyldibenzothiophenes[J]. Applied Catalysis A: General,2002,232(2):253-261.
[7]EGOROVA M,PRINS R.Mutual influence of the HDS of dibenzothiophene and HDN of 2-methylpyridine[J].J Catal,2004,221(1):11-19.
[8]LAREDO G C,AL TAMIRANO E,DE LOS REYES J A. Self-inhibition observed during indole and o-ethylaniline hydrogenation in the presence of dibenzothiophene[J].Applied Catalysis A:General, 2003,242(2):311-320.
[9]RANA M S,NAVARRO R,L EGLISE J.Competitive effects of nitrogen and sulfur content on activity of hydrotreating CoMo/Al2O3catalysts:A batch reactor study[J].Catalysis Today,2004,98(1-2):67-74.
[10]LI D,NISHIJ IMA A,MORRIS D E,et al.Activity and structure ofhydrotreating Ni,Mo,and Ni-Mo sulfide catalysts supported onγ-Al2O3-USY zeolite[J]. Journal of Catalysis,1999,188(1):111-124.
[11]相春娥,柴永明,邢金仙,等.喹啉、吲哚对二苯并噻吩在NiMoS/γ-Al2O3上加氢脱硫反应的影响[J].石油学报(石油加工),2008,24(2):151-157.(XIANG Chune,CHAI Yongming,XINGJinxian,et al.Effects of quinoline and indole on the hydrodesulfurization of dibenzothiophene over NiMiS/γ-Al2O3catalyst[J].Acta Petrolei Sinica(Petroleum Processing Section),2008, 24(2):151-157.)
[12]RICHARD F,BOITA T,PÉROT G. Reaction mechanism of 4,6-dimethyldibenzothio-phene desulfurization over sulfided NiMoP/Al2O3-zeolite catalysts[J]. Applied Catalysis A:General,2007,320(1):69-79.
[13]VAN LOOIJ F,VAN DER L P,STORK W H J,et al. Key parameters in deep hydrodesulfurization of diesel fuel[J].Applied Catalysis A:General,1998,170(1): 1-12.
[14]LAREDO G C,AL TAMIRANO E,DE LOS R J A. Inhibition effects of nitrogen compounds on the hydrodesulfurization of dibenzothiophene:Part 2[J]. Applied Catalysis A:General,2003,243(2):207-214.
[15]LAREDO G C,MONTESINOS A,DE LOS R J A. Inhibition effects observed between dibenzothiophene and carbazole during the hydrotreating process[J].Applied Catalysis A:General,2004,265(2):171-183.
[16]SILVA-RODRIGO R, HERNÁNDEZ-LÓPEZ F, MARTIEZ-JUAREZ K,et al.Synthesis,characterization and catalystic properties of NiMo/Al2O3-MCM-41 catalyst for dibenzothiophene hydrodesulfurization[J]. Catalysis Today,2008,130(1):309-319.
[17]UDAY T T,MA X L,SONG C S.Influence of niteogen compounds on deep hydrodesulfurization over Al2O3-and MCM-41-supported Co-Mo sulfide catalysts [J].Catalysis Today,2003,86(1-4):265-275.
[18]SUMBOGO M S D,YANG H J,CHOI K H,et al. Influences of nitrogen species on the hydrodesulfurization reactivity of a gas oil over sulfide catalysts of variable activity[J].Applied Catalysis A:General,2003,252 (2):331-346.
[19]YANG S H, SATERFIELD C N. Catalytic hydrodenitrigenation of quinoline in a trickle-bed reaction effect of hydrogen sulfide[J].Ind Eng Chem Proc Dev, 1984,23(1):20-25.

