AZ31镁合金表面钼酸盐(Na2MoO4)转化膜的研究
郭志丹,夏兰廷,杨 娜
(太原科技大学材料科学与工程学院,山西 太原 030024)
镁合金是工程应用中最轻的金属结构材料,具有比重小,比强度、比刚度高,阻尼性、切削加工性、铸造性能好等优点,在汽车、机械、航空、航天领域以及便携式电子仪表、计算机等领域得到日益广泛的应用。但镁自身的电极电位很负,标准电极电位只有-2.37V[1],化学活性高,耐蚀性很差,成为制约其应用的一个主要因素,镁合金的腐蚀与防护问题日益突出。常用的表面处理方法有化学转化、阳极氧化、微弧氧化和化学镀等[2,3]。其中化学转化成本低,工艺操作性强,成熟的工艺有铬酸盐转化等,转化膜层耐蚀性能较好,但是由于Cr离子毒性很大,应用受到限制。钼酸盐是一种低毒低污染物质,其转化膜可以有效地保护基底金属,并为后续的涂装保护提供良好基底。目前关于镁合金钼酸盐转化膜的报道较少,本文在AZ31镁合金上制备钼酸盐转化膜,对其微观形貌、膜成分、成膜机理及耐蚀性能进行研究。
1 试验条件方案
试验材料为轧制的AZ31镁合金,试样尺寸为10mm×10mm×10mm,试样经粗磨细磨至表面无痕,腐蚀介质使用3.5%NaCl溶液,浸泡时间为48 h后测其腐蚀率。清除试样表面产物用100g三氧化铬(CrO3)+10g 铬酸银(AgCrO4)加蒸馏水配制成1000ml溶液,温度:95℃,时间:1 min[4]。试验用检测设备为笔型pH计pHB-1型、Keyence Digital Microscope金相显微镜、HITACHIS-3000N SEM扫描电镜、OXFORD INCA ENERG 250EDS X射线能谱仪。AZ31 镁合金化学成分为:ω(Al)=2.89%,ω(Zn)=0.9%,ω(Mn)=0.25%,ω(Fe)=0.03%,ω(Ni)=0.01%,ω(Cu)=0.01%,镁余量。试验工艺流程为:制备试样→预磨→水洗→碱除油→水洗→酸洗→水洗→氟活化→水洗→化学转化→称重→浸泡→清除腐蚀产物→蒸馏水洗→称重。为了选取较佳的转化液配比,经过先期试验后,现采用两种试验方案,其一,Na2MoO4浓度不变,改变NaF浓度以获得较佳的NaF配比;其二,Na2MoO4浓度改变,NaF固定,获得较佳的 Na2MoO4浓度,转化液 pH 值在 3.5~4,转化温度为70℃~75℃,并与未经转变的AZ31镁合金进行腐蚀性能对比,试验方案见表1。

表1 AZ31镁合金表面转化方案
2 结果及分析
2.1 微观形貌及腐蚀率
AZ31镁合金的金相显微组织见图1,其表面经Na2MoO4-NaF溶液转化后的宏观、其形貌见图2,其中 a)为宏观形貌,b)为微观形貌。图3为AZ31镁合金及经转化的AZ31镁合金的腐蚀形貌,其中a)为未经转化的AZ31镁合金,b)为经转化后的3号试样。

图1 轧制态AZ31合金显微组织

图2 转化膜形貌

图3 AZ31镁合金腐蚀形貌
由图1可见,AZ31镁合金组织主要由α(Mg)相和少量的条点状β(Mg17Al12)相组成。由于组成不同,前者是以Mg为基溶有Al的固溶体。后者是Mg与Al组成的化合物相,二者的电位不同,存在电位差,在腐蚀介质中电位较负的α相首先被腐蚀。由图2a)看到,AZ31镁合金在钼酸盐溶液转化后表面形成了将合金与腐蚀介质隔离的一层棕色转化层,完全覆盖了基底,由图2b)可见,该转化层形貌为网状,白亮处裸露出金属基底,说明该转化层致密性连续性不是很好。其表面呈凹凸不平的状态,为后续进行涂料防护提供了较理想的粗化表面,增强了转化层与涂料的附着力。由图3可见经转化后的AZ31镁合金表面的腐蚀程度低于未经转化的AZ31镁合金,说明该转化膜起到了防护作用。AZ31镁合金试样及经不同配比的转化液获得的转化膜试样在3.5%NaCl溶液中浸泡48 h后测得的腐蚀率列于表2。
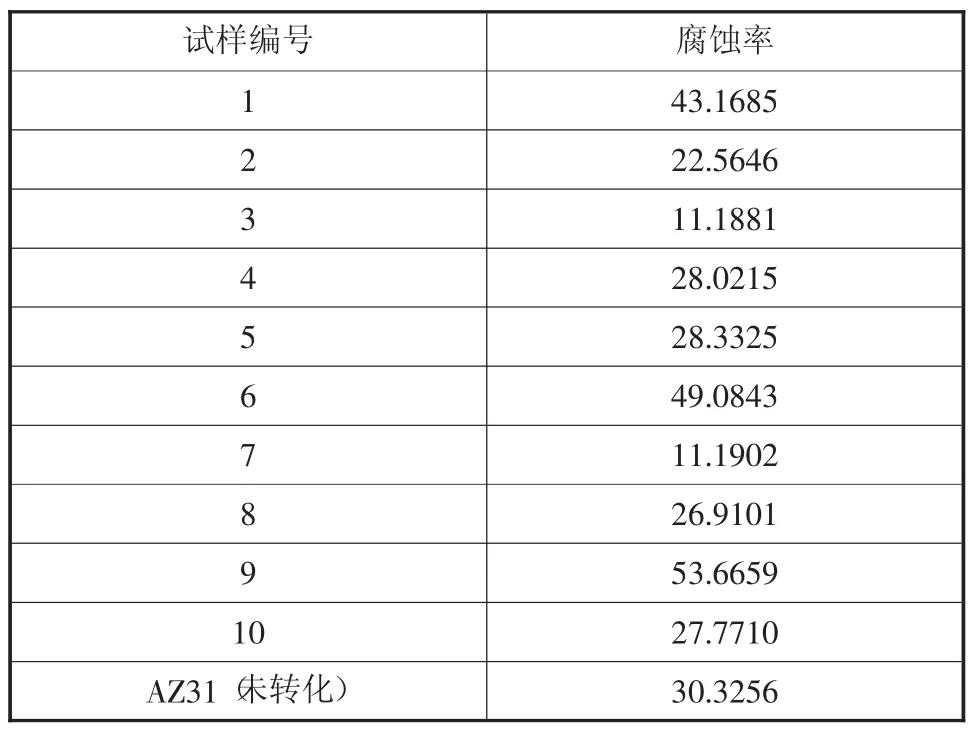
表2 AZ31镁合金及不同转化工艺腐蚀率(mm.a-1)
由表2可见,除1、6、9号试样外,AZ31镁合金的腐蚀率远大于AZ31合金表面经Na2MoO4—NaF转化后的腐蚀率。对比1~5号试样的腐蚀率可知,当Na2MoO4的浓度为20g/L,NaF的浓度在4g/L时即3号试样,经转化后的AZ31镁合金腐蚀率最小,对比6~10号试样,当NaF的浓度为4g/L不变时,Na2MoO4的浓度为20g/L时腐蚀速率最小,二组试验出现了很好的重复性。经转化后1号试样的腐蚀率大于未经转化的AZ31合金的腐蚀率,原因在于转化液中不含NaF,而导致活性较高的AZ31镁合金表面无法形成具有钝化作用的MgF2而难于形膜,此时单独存在的Na2MoO4加速了合金的腐蚀。6号试样的腐蚀率大于AZ31合金的腐蚀率原因则是由于Na2MoO4浓度较低,使其成膜的Na2MoO4含量不足所致,与不含NaF的1号试样和最大腐蚀率为53.76mm/a,Na2MoO4含量为 30g/L 的 9 号试样相比较,表明了Na2MoO4对转化膜腐蚀性能影响远大于NaF的影响并起到双重作用,当其浓度与NaF不匹配时,Na2MoO4有可能阻止破坏NaF在AZ31镁合金上形成MgF2膜,并导致Na2MoO4与NaF共同作用加速合金的腐蚀,因此该转化液对Al含量较低的化学电化学活性远高于AZ91D的AZ31镁合金进行化学转化时,其对转化液的配比要求严格,控制难度大,形成的转化膜保护作用也较差。
2.2 成膜性能分析
试验过程中,转化膜的成膜性能取决四个因素:Na2MoO4和NaF物质量的配比,转化液pH值,和转化液的转化温度。Na2MoO4和NaF物质量的配比,通过对比法已经确定。同样转化液pH值和转化液的转化温度亦通过对比确定。试验过程中,钼酸盐转化液pH值范围曾经在2~6间调整,转化温度在25℃~80℃间变动。试验中发现转化液pH值较大,接近中性时,由于镁合金呈碱性,获得的转化膜表面不均匀,局部基体裸露,转化膜不能很好地覆盖金属基体,甚至转化不到基体上。pH值在2~3时,溶液的酸性大,观察试样表面反应剧烈,导致析氢反应加剧,不利于转化膜的沉积、增厚和长大,使转化膜的均匀性、致密性减弱,甚至加剧镁合金基体的腐蚀,使成膜过程难以控制。综上所述pH定在3.5~4之间,反应速度适中,析氢速度减缓,成膜能力最好,转化膜完整地覆盖了金属基体,致密性、均匀性远优于其他pH值下的转化膜。转化液温度曾经控制在25℃,40℃~50℃,70℃~75℃。在25℃,40℃~50℃条件下,转化膜致密性、连续性较70℃~75℃条件下成膜能力差。当温度在80℃以上时,转化液pH在2~3,镁合金试样表面反应剧烈,难以成膜。
图4为3号试样转化膜的背散射及能谱检测点位置,图中深浅不同的位置表明不同的元素组成。由于元素的原子序数不同,其在背散射图上表现出不同的深浅颜色,对不同深浅位置进行能谱检测分析,确定其组成物相。化学转化后的AZ31镁合金表面转化膜的背散射检测点位置的能谱(EDS)检测值见表3。

图4 转化膜背散射图及检测位置点

表3 转化膜能谱检测结果(质量分数,%)
由表3可见,3个检测点中谱图2测点含Mg量最高,含F量最低,并且不含Mo及其他元素,表明该处仅由MgF2、Mg组成。谱图1中O含量达到8.21%,F含量是3个测点中最高的,镁含量最低,并含有 1.52%Al,表明该部位主要由 MgF2、MgO、及少量Al2O3组成,谱图2测点中未检测到Mo元素,可见经转化后的AZ31镁合金表面大部分未形成含Mo的转化膜,由谱图3测点可见,该点在3个测点中 Mg 含量最低,为 19.49%Mg,Al含量最高,达到4.38%Al以及较高的 F 含量(51.10%),表明转化膜在含Al较高的β相表面形成。同时该检测点O含量为3个检测点中最高的达到了8.56%,Al与O形成Al2O3膜,谱图3测点是所用检测点中唯一含Mo的,并且有高的O含量,是转化膜中形成了Mo的氧化物,由测点3元素的含量及分析可以得出,该点转化膜主要有MgF2、Al2O3及Mo的氧化物组成,而含Al较高的β(Mg17Al12)存在为形成含Mo转化膜提供了基底,由Mg-Al二元相图分析含Al仅为3%左右的AZ31镁合金作为变形镁合金其中Al大部分固溶于Mg,形成以α(Mg)为主的基体,使β(Mg17Al12)相的析出、形成很困难。由图1可见,β相数量很少,而有利于转化膜形成的基底很少,使该转化膜在含Al较低的Mg合金表面成膜困难,这也是AZ91D镁合金表面化学转化膜的成膜效果,成膜后的耐蚀性远优于 AZ31 镁合金的主要原因[5~7]。
在试验过程中,观察到镁合金试样上面有气泡析出,并且转化液的颜色由无色变为蓝色,表明了在镁合金基体上面发生了析氢反应。镁以Mg2+离子的形式溶于溶液,镁在阳极区发生如下溶解反应:

镁合金的β(Mg17Al12)相作为反应的阴极区,氢气在阴极析出:
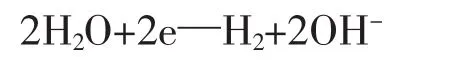
此反应使试样局部转化液的pH值上升,产生不溶性钼酸盐,并附着在阴极区表面形成钼酸盐转化膜,钼酸盐结晶最初在镁合金的β相上形成,随后沉积的钼酸盐转化膜作为阴极,使反应继续进行,膜的厚度不断增加直至结束。F-作为促进剂的同时也参与成膜,F-与一部分游离态的Mg2+生成极难溶的MgF2作用于机体表面:

难溶性MgF2沉积在基体表面为钼酸盐转化膜的形成和附着提供了有利条件。钼酸盐在酸性介质中具有弱氧化性[8],在镁合金表面发生还原反应,转化膜中各物质的形成反应如下:

其中MoO(OH)2在干燥过程中分解为MoO3。
3 结论
1)采用钼酸盐溶液对AZ31镁合金表面转化可形成表面较均匀、致密的转化膜,在Na2MO4浓度为20g/L,NaF浓度4g/L,pH值为3~4,温度为 70℃~75℃,获得的转化膜在3.5%NaCl溶液中的腐蚀率为11.1881mm·a-1,比未经转化的AZ31镁合金的30.3256mm·a-1的腐蚀率减少 63.11%,该转化膜可对AZ31镁合金提供有限程度的保护。
2)AZ31合金中含Al较高的β相是形成转化膜的基底。转化膜主要由MgF2、MoO2及Al2O3组成。
[1]孙承忠.金属的腐蚀与防护[M].北京:冶金工业出版社,1997.
[2]周婉秋,单大勇,曾荣昌,等.镁合金的腐蚀行为与表面防护方法 [J].材料保护,2002,35(7):1-3.
[3]罗小萍,夏兰廷,臧车勉.镁合金顼化转化处理研究现状[J].铸造设备研究,2007(2):44-47.
[4]中国工业防腐蚀技术学会,中国标准出版社第二编辑室.中国防腐蚀标准汇编 工程卷2005(上)[M].北京:中国标准出版社,2006.
[5]王辰浩.镁合金无铬化学转化及有机涂层防护研究[A].太原科技大学硕士论文太原[D].太原:太原科技大学,2008.
[6]宋光玲.镁合金腐蚀与防护[M].北京:化学工业出版社,2006.
[7]王辰浩,夏兰廷,臧东勉,等.A291D镁合金表面无铬化学转化膜的研究[J].铸造设备研究,2008(3):17-20.
[8]CHENG T P,LEE J T,TSAI W T.Passivation of titanium in molybdate-containning sulphuric acid solution[J].Electro-chimica Acta,1991,36(14):2069-2067.

