低聚羧甲基壳聚糖的抗氧化性能
孙 涛, 银旭红, 姚 倩, 周冬香, 邵则淮
(上海海洋大学 食品学院, 上海 201306)
低聚羧甲基壳聚糖的抗氧化性能
孙 涛, 银旭红, 姚 倩, 周冬香, 邵则淮
(上海海洋大学 食品学院, 上海 201306)
将低聚壳聚糖(chitosan oligosaccharide, COS)醚化得到O-羧甲基壳聚糖(O-carboxymethyl chitosan oligosaccharide,O-CMCOS)和N-羧甲基壳聚糖(N-carboxymethyl chitosan oligosaccharide,N-CMCOS), 其取代度(substituting degree, DS)均为0.54, 用红外光谱对其结构进行表征。同时, 考察了其结构对超氧阴离子的清除活性以及还原能力。结果表明, COS及其衍生物清除超氧阴离子的活性及还原能力的强弱顺序均为:O-CMCOS>COS>N-CMCOS。
低聚壳聚糖; 羧甲基壳聚糖; 取代度; 抗氧化; 还原能力
甲壳素是自然界存储量仅次于纤维素的第二大天然多糖, 广泛存在于甲壳动物外壳、某些植物及真菌类细胞壁中, 其脱乙酰基为壳聚糖。壳聚糖具有良好的生物相容性、可生物降解性等多种生物活性, 在食品、化工、环保和生物医学等领域的应用研究取得了重大进展[1~3]。羧甲基壳聚糖是壳聚糖经羧甲基化后的一类壳聚糖衍生物。根据羧甲基的取代位置不同, 可以分为O-羧甲基壳聚糖、N-羧甲基壳聚糖和N,O-羧甲基壳聚糖。羧甲基在多糖主链上取代的位置和程度都会直接影响到羧甲基壳聚糖的各种性能, 是壳聚糖在生产、研究和应用中的重要技术指标。有关羧甲基壳聚糖的取代位置、取代度及其功能之间关系的研究, 尚未见很多报道。
本实验以低聚壳聚糖(Chitosan oligosaccharide,COS)为原料, 制备了相同取代度的O-羧甲基壳聚糖(O-CMCOS)和N-羧甲基壳聚糖(N-CMCOS), 并研究了其结构对抗氧化能力的影响。
1 实验部分
1.1 材料与仪器
低聚壳聚糖(分子质量为5 ku), 购自浙江金壳生物化学有限公司; 鲁米诺, 硼氢化钠, 乙醛酸, 购自Sigma公司; 其余试剂均为分析纯, 购自上海化学试剂公司; 抗氧化测试所需溶液由二次蒸馏水配制。
作为减速器或变速器的传动部件[1],行星机构具有体积小、质量轻、结构紧凑、传动速比大、载荷分布均匀以及承载能力强等优点,广泛应用于航空、车辆及工程机械设备中.在所有行星机构中内外啮合单排行星机构是最基本的组成要素,其设计过程要满足严格的配齿条件,否则将因相互干涉而不能装配构成行星机构,最终导致设计任务失败.本文将基于齿轮传动理论,运用数学方法讨论内外啮合单排行星机构的配齿条件,为工程技术人员提供成熟的解决方案.
79-3型恒温磁力搅拌器, 上海司乐仪器有限公司; DELTA-320-S型pH计, 梅特勒-托利多仪器上海有限公司; DDS-307 电导率仪, 上海精密科学仪器有限公司; UV-2000型紫外可见分光光度计, 尤尼柯上海仪器有限公司; FFM-D型流动注射式化学发光仪, 西安瑞迈电子科技有限公司;EQUNOX55傅立叶红外-拉曼光谱仪, 德国BRUKER公司。
1.2 羧甲基壳聚糖的制备及表征
1.2.1 O-羧甲基壳聚糖的制备
红外光谱在 EQUNOX55傅立叶红外-拉曼光谱仪上进行, 采用 KBr压片法制样, 测定波数范围为500~4000 cm-1, 分辨率为0.8 cm-1。取代度通过电位滴定法测得[6]。
1.2.2 N-羧甲基壳聚糖的制备
对超氧阴离子的清除根据文献[7]测定并稍做改进。用pH为10.20的0.5 mol/L Na2CO3-NaHCO3缓冲溶液配制浓度为1.5×10-3mol/L的鲁米诺溶液, 用1×10-3mol/L的盐酸配制浓度为0.1 mol/L的邻苯三酚储备液, 使用前用去离子水稀释至1×10-4mol/L。以缓冲液作为溶剂, 配制成不同浓度的样品溶液。用流动注射化学发光分析仪依次测定从稀到浓的样品溶液, 读出峰面积。清除率=(A0-Ai)/A0×100%。式中A0为空白溶液峰面积;Ai为样品溶液峰面积。经SOD、过氧化氢酶及甘露醇检测, 该体系产生的自由基为超氧阴离子。
将5.0 g壳聚糖加入到50 mL42%NaOH溶液中,在室温下边搅拌边分别加入5.35、2.5和1.0 g氯乙酸, 反应28 h后, 用1∶1 HCl调节pH至7, 然后用无水乙醇沉淀并多次浸泡洗涤。最后60 ℃真空干燥,即得到白色的O-羧甲基壳聚糖[4]。
伴随着同一理性的自我分裂,工具理性的异化成为影响社会生活的引人瞩目的现象,当代西方思想家对其进行了深度的批判和反省,彰显了理性的批判性和超越性力量。
1.3 对超氧阴离子的清除
将4 g壳聚糖加入到含有0.2 g乙醛酸的150 mL的水溶液中, 搅拌反应2 h。用10%的NaOH调节pH至9, 然后加入10 mL10%的NaBH4, 继续搅拌2 h,然后调pH至中性, 然后用无水乙醇沉淀并多次浸泡洗涤, 最后60 ℃真空干燥, 即得到白色的N-羧甲基壳聚糖[5]。
1.4 还原能力的测定
还原能力根据文献[8]测定并稍做改进。取2.0 mL不同浓度的样品, 加入pH为6.60的0.2 mol/L磷酸缓冲液1%铁氰化钾溶液各2.5 mL, 混匀, 50 ℃水浴20 min后迅速冷却, 加入2.5 mL10%三氯乙酸溶液,混匀后在2000 r/min下离心10 min, 取上清液2.0 mL,加入2.5 mL去离子水和0.5 mL 0.1%的三氯化铁溶液, 静置10 min后在700 nm处测定吸光度。
2 结果与讨论
2.1 红外光谱及取代度

图1 COS, O-CMCOS和N-CMCOS的红外光谱Fig. 1 FTIR spectra of COS, O-CMCOS and N-CMCOS
2.2 对超氧阴离子的清除
图1是COS,O-CMCOS和N-CMCOS的红外光谱图。如图所示, 所有样品均在1 100 cm-1附近有较强的多糖特征吸收峰。其中1 030 cm-1和1 074 cm-1附近吸收峰分别是分子中伯羟基和仲羟基伸缩振动的结果。这两个吸收峰在O-CMCOS谱图中强度明显减弱, 由此说明 COS的伯羟基和仲羟基发生了羧甲基化反应。3 400 cm-1-OH吸收峰明显变窄, 这是由于C6位上-OH发生了醚化反应, -OH减少而引起的。在N-CMCOS的谱图中, 伯胺 N-H面内弯曲振动在1 612 cm-1处吸收峰均有减弱, 说明了在N位发生了羧甲基的取代反应[9]。经过电位滴定法测试,O-CMCOS和N-CMCOS的取代度均为 0.54, 这说明羧甲基取代O-CMCOS羟基和N-CMCOS氨基的程度相同。
“农区变景区、田园变公园、民房变客房”。当前,不少地方都把发展休闲农业和乡村旅游作为实施乡村振兴战略的主要抓手,观光农业园区、森林人家、康养基地、乡村民宿等新业态层出不穷。例如,北京农业嘉年华、江苏高淳国际慢城、陕西泾渭茯茶特色小镇等利用农村闲置土地和农民闲暇时间,不仅让闲置的土地“忙”起来,农民的钱包鼓起来,更让传统乡村文化“火”了起来。
第二,时刻关注林业资源的动态变化。木本植物消失、成长是影响林业资源整体变化的重要因素,在此基础上,林业资源还受到水资源、经济发展水平、农业建设进程、相关部门管理方案等因素的影响。对此,这就需要林业部分不定期对林业资源进行质量检查,深入到森林实处之内进行全方位的调研,从而全面把握林业资源的总体情况,为林业局林政资源管理方案的生成提供必要依据。

图2 COS、O-CMCOS和N-CMCOS对超氧阴离子的清除Fig. 2 Scavenging effects of COS, O-CMCOS and N-CMCOS on superoxide anion
2.3 还原能力的测定
还原能力和抗氧化活性之间有着密切的关系。抗氧化物质通过提供电子阻断 Fe2+向 Fe3+的转变,表现出一定的还原能力, 同样也可以通过提供电子和自由基反应, 表现出抗氧化活性。COS及其衍生物的还原能力如图3所示。随着浓度的增加, 各样品的吸光值随之增加, 还原能力逐渐增强。当质量浓度为2.0 g/L时, COS、O-CMCOS和N-CMCOS的吸光度分别是0.72、0.96和0.65。即COS及其衍生物的还原能力大小顺序为:O-CMCOS>COS>N-CMCOS。
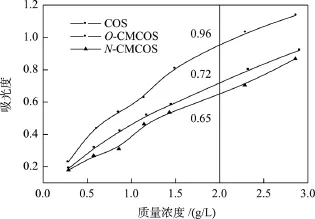
图3 COS、O-CMCOS和N-CMCOS的还原能力Fig. 3 Reducing power of COS, O-CMCOS and N-CMCOS
3 结论
本实验通过对COS进行醚化, 制备了取代度均为 0.54的O-CMCOS和N-CMCOS。抗氧化测试结果表明:COS及其衍生物对超氧阴离子的清除能力与还原能力的顺序大小均为:O-CMCOS>COS>N-CMCOS。壳聚糖以及衍生物抗氧化能力的大小与活性羟基和氨基密切相关。低聚壳聚糖由于主链上的β-(1,4)糖苷键发生断裂, 更多的活性羟基基团暴露出来, 因而具有良好的抗氧化能力。在COS分子链上引入羧甲基后, 由于-CH2COO-是推电子基团,它可以使活性羟基和氨基的电子云密度增大, 更有利于活性羟基和氨基与自由基反应, 故O-CMCOS的抗氧化活性与 COS相比有所增强。而对于N-CMCOS来说, 羧甲基的引入虽然使活性氨基和羟基的电子云密度增大, 但同时也减少了游离氨基的含量, 所以N-CMCOS的抗氧化活性相对最弱。这一结果也说明氨基在COS及其衍生物抗氧化活性中的重要性。
[1]Sweetie R K, Ramesh C, Arun S. Chitosan glucose complex- A novel food preservative[J]. Food Chem,2008, 106:521-528.
[2]Liu G Z, Zhu Y B, Du J Y,et al.Research advances of chitosan’s application in agriculture[J]. Chin Agric Sci Bul, 2007, 23:377-381.
[3]Wang X Y, Du Y M, Yang J H,et al. Preparation, characterization and antimicrobial activity of chitosan/layered silicate nanocomposites [J]. Polymer, 2006,47:6 738-6 744.
[4]Yu X F, Guan Y L, Yang D Z,et al. Antibacterial action of chitosan and carboxymethylated chitosan [J]. Journal of Applied Polymer Science, 2001, 79(7):1 324-1 335.
[5]陈浩凡, 潘仕荣, 王琴梅. 不同取代羧甲基壳聚糖的制备及其结构测定[J]. 华中科技大学学报(医学版),2003, 32(2):152-156.
[6]Muzzarelli R A A, Tanfani F, Emanuelli M,et al.N-(carboxymethylidene)chitosans andN-(carboxymethyl) chitosans:Novel chelating polyampholytes obtained from chitosan glyoxylate[J]. Carbohydrate Research, 1982, 107(2):199-214.
[7]孙涛, 周冬香, 毛芳,等. 流动注射化学发光法对超氧阴离子自由基和羟基自由基·OH的检测[J]. 食品工业科技, 2006, 27(11):182-187.
[8]Yen G C, Chen H Y. Antioxidant activity of various tea extracts in relation to their antimutagenicity[J]. Journal of Agriculture and Food Chemistry, 1995, 43(1):27-32.
[9]Kogan G, Skorik Y A, Zitnanova I,et al. Antioxidant and antimutagenic activity ofN-(2-carboxyethyl) chitosan[J]. Toxicology and Applied Pharmacology,2004, 201(3):303-310.
Antioxidant activity of carboxymethyl chitosan oligosaccharide
SUN Tao, YIN Xu-hong, YAO Qian, ZHOU Dong-xiang, SHAO Ze-huai
(College of Food Science, Shanghai Ocean University, Shanghai 201306, China)
Feb. ,28, 2009
chitosan oligosaccharide; carboxymethyl chitosan oligosaccharide; substituting degree; antioxidant activity; reducing power
O-carboxymethyl chitosan oligosaccharide (O-CMCOS) andN-carboxymethyl chitosan oligosaccharide(N-CMCOS) with the same substituting degree (0.54) of carboxymethyl group were prepared by the etherification of chitosan oligosaccharide (COS), with their structures characterized by FTIR spectra. The orders of COS,O-CMCOS andN-CMCOS scavenging effect on superoxide anion and reducing power wereO-CMCOS>COS>N-CMCOS.
TS202.3 文献标识码:A 文章编号:1000-3096(2010)02-0054-03
2009-02-28;
2009-06-29
上海市教育委员会科研项目(07zz134); 上海市重点学科建设专项基金项目(T1102)
孙涛(1970-), 女, 博士, 副教授, 研究方向:生物化学, 电话:021-61900363, E-mail:taosun@shou.edu.cn
康亦兼)

