p15INK4B基因对人胰腺癌细胞系BxPC3增殖的影响
张学彦 刘志强 景德怀 关景明 刘伟
·论著·
p15INK4B基因对人胰腺癌细胞系BxPC3增殖的影响
张学彦 刘志强 景德怀 关景明 刘伟
目的探讨p15INK4B(p15)基因转染对人胰腺癌细胞系BxPC3细胞增殖的影响。方法采用脂质体将pCDNA3.1(+)-p15质粒及阴性对照pCDNA3.1(+)-neo质粒转染BxPC3细胞,以亲本细胞作为对照组。应用RT-PCR检测细胞p15 mRNA表达;Western blotting检测细胞p15蛋白表达;MTT法检测细胞增殖;透射电镜观察细胞超微结构变化;流式细胞仪检测细胞周期和凋亡率。结果p15转染组细胞恢复p15 mRNA和蛋白表达。培养第2天生长被抑制,至第7天,生长抑制率达47.9%。G0/G1期细胞占(61.56±3.96)%,显著高于空质粒转染组的(47.44±6.35)%和对照组的(49.22±7.23)%(Plt;0.05)。出现明显的G1凋亡峰,细胞凋亡率为(5.27±1.04)%,显著高于空质粒转染组的(0.11±0.06)%和对照组的(0.09±0.07)%(Plt;0.05)。透射电镜观察到p15转染组发生细胞凋亡。结论体外p15基因转染可以抑制人胰腺癌细胞系BxPC3细胞增殖,并能诱导其凋亡。
胰腺肿瘤; 转染; 周期素依赖激酶抑制剂p15
p15INK4B(简称p15)是近年来发现的细胞周期蛋白依赖性激酶抑制因子(cyclin-dependent kinase inhibitors, CKI)家族中的一个新成员,在胰腺癌发生过程中经常失活[1]。为探讨恢复p15表达能否抑制人胰腺癌细胞的增殖,本研究将p15转染到人胰腺癌细胞系BxPC3中,观察其对胰腺癌细胞生长的影响。
材料和方法
一、材料
真核表达质粒pCMV5-p15由北京师范大学生命科学学院-教育部细胞增殖与调控重点实验室柳惠图教授惠赠,我实验室先期将其亚克隆至有真核筛选标志新霉素抗性基因(neo)的质粒pCDNA3.1(+)上,称为pCDNA3.1(+)-p15质粒[2]。BxPC3细胞株购自中国科学院上海细胞所。Trizol试剂盒是Gibco公司产品,Taq酶为上海生工公司产品,逆转录试剂盒、限制性内切酶、转染级质粒中提试剂盒是Promega公司产品。p15小鼠抗人单抗是Neo Markers公司产品,辣根酶标山羊抗小鼠IgG为北京中杉金桥公司产品。 actin beta(ACTB)抗体和Western blotting发光试剂是Santa Cruz公司产品。脂质体Lipofectamine2000购于Invitrogen公司。引物由上海生工公司合成。上海生工公司进行质粒测序。
二、p15质粒转染BxPC3
人胰腺癌BxPC3细胞系在37℃、5% CO2饱和湿度条件下,用含10%胎牛血清的DMEM高糖培养基培养传代,收集对数生长期细胞。
提取pCDNA3.1(+)-p15,转化感受态大肠杆菌DH5α,挑取单克隆,PCR扩增片段鉴定正确后用pCDNA3.1(+)载体的测序引物T7测序验证明确后扩增大肠杆菌,并抽提质粒。采用Lipofectamine2000脂质体将pCDNA3.1(+)-p15质粒转染BxPC3细胞,为p15转染组;用空质粒pCDNA3.1(+)-neo转染BxPC3细胞,为阴性对照组;未转染的BxPC3细胞为空白对照组。每组3个样本。
三、细胞p15 mRNA和蛋白的检测
p15 mRNA表达采用RT-PCR检测。采用Trizol提取细胞总RNA。逆转录cDNA反应体系20 μl,含随机引物0.5 μg、逆转录酶200 U、RNA 1.0 μg、dNTP 0.5 mmol/L、RNasin 20 U,37℃ 60 min,95℃ 5 min。
PCR反应体系25 μl,含Mg2+2.5 mmol/L、dNTP 0.5 mmol/L、cDNA 2 μl、TaqDNA合成酶2 U、上下游引物各0.4 μmol/L。p15 上游引物5′-CCAGAA-GCAATCCAGGCGCG-3′,下游引物5′-CGTTGG-CAGCCTTCATCG-3′,产物753 bp,退火58℃;内参β-actin上游引物5′-CCCAGCACAATGAAGATCAAG-ATCAT-3′,下游引物5′-ATCTGCTGGAAGGTGGAC-AGCGA-3′,产物100 bp,反应35个循环。产物经1.2%琼脂糖凝胶电泳,照相。
p15蛋白表达采用常规Western blotting检测,以表达p15蛋白的Hela细胞为阳性对照。
四、细胞增殖检测
采用MTT法。取对数生长期细胞,按3×103个细胞/孔接种96孔板,每孔加5 g/L MTT溶液20 μl,37℃孵育4 h,每孔加180 μl二甲基亚砜,振荡10 min, 测定A490值,每隔1天测定一次,连续测定7 d,绘制细胞生长曲线。
五、细胞凋亡检测
采用流式细胞仪检测。取各组1×106个细胞,加入70%冷乙醇4℃固定24 h,用50 mg/L RNase 37℃处理30 min,加100 mg/L碘化丙啶避光染色30 min,上流式细胞仪测定。
六、细胞超微结构观察
取各组1×106个细胞,1500 r/min离心10 min,加入3%戊二醛固定一周,送透射电镜检测。
七、统计学处理

结 果
一、BxPC3细胞p15 mRNA和蛋白的表达
亲本代BxPC3细胞不表达p15 mRNA和蛋白。p15转染组细胞表达p15mRNA,扩增出753 bp 的目的条带(图1);表达p15蛋白,存在分子质量为15 000的目的条带(图2)。空质粒转染阴性对照组和未转染空白对照组均不表达p15 mRNA和蛋白。
二、细胞增殖的变化
空质粒转染组和未转染组细胞增殖基本一致。而转染p15基因后BxPC3细胞增殖从第2天起开始被抑制,生长抑制率为17.4%,随时间延长抑制率逐渐升高,第7天时达47.9%(图3)。

1.Marker KL2000;2.BxPC3细胞;3.p15转染细胞

1.Marker;2.阳性对照Hela;3.p15转染组;4.空质粒转染组;5.BxPC组
图2各组细胞p15蛋白检测
三、细胞周期变化

图3 各组BxPC3细胞生长曲线
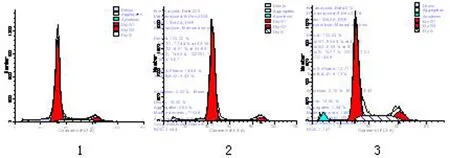
p15转染组的G0/G1期细胞占(61.56±3.96)%,显著高于空质粒转染组的(47.44±6.35)%和未转染组的(49.22±7.23)% (Plt;0.05);S期细胞占(21.75±1.99)%,显著低于空质粒转染组的(35.25±3.97)%和未转染组的(36.01±1.54)% (Plt;0.01)。p15转染组出现明显的G1凋亡峰,细胞凋亡率为(5.27±1.04)%,显著高于空质粒转染组的(0.11±0.06)%和未转染组的(0.09±0.07)%(图4,Plt;0.05)。
四、细胞超微结构的改变
空质粒转染组细胞生长状态较好,未见凋亡形态学改变,核浆比例大,圆形核仁多,细胞表面绒毛密集排列,双层核膜结构清晰,胞质内有丰富的游离核蛋白体。p15转染组可见部分细胞发生凋亡,细胞体积变小,表面绒毛消失,核固缩,染色质形成高密度斑块,胞质内出现大量脂肪滴颗粒,部分线粒体出现髓样变,游离核糖体减少(图5)。
1.BxPC3组;2.空质粒转染组;3. p15转染组

1.BxPC3组;2.空质粒转染组;3. p15转染组
讨 论
p15是近年来发现的一类CKI分子,定位于9号染色体9p21区,这一位点易发生缺失、突变和甲基化,从而导致恶性肿瘤发生。p15被认为是除了p53、Rb之外的CKI类重要抑癌基因[3]。p15的抑癌机制与细胞周期调控密切相关,它能直接作用于CyckinD1/CDK4复合物中的CyclinD1,从而影响CDK4激酶的活性,导致pRb磷酸化水平下降,使细胞被阻滞在G1期。其次,癌基因c-myc的产物Myc与Max结合形成一个转录因子,具有促进细胞转化、诱导肿瘤发生的作用,而p15高表达能引起c-Myc蛋白表达水平下降。第三,原癌基因c-fos参与形成转录因子AP-1,AP-1能激活生长类蛋白基因的转录,对细胞周期起正调作用[4],而p15高表达可引起c-fos蛋白表达水平的下降。此外,p15失活在恶变中所起的重要作用可能与其引起Cyckin-Rb通路失控和控制细胞增殖的作用丧失直接相关。
胰腺癌时Smad4失活,p15是Smad4的关键下游效应基因[5],Smad4和p15功能丧失就导致了TGF-β丧失诱导CDK抑制因子的作用[6]。Hitomi等[7]认为,p15是组蛋白去乙酰基(Histone deacetylase,HDAC)抑制物的重要分子靶点,而HDAC抑制物能将人肿瘤细胞阻滞于G1期,并能激活细胞周期依赖激酶抑制物p21WAF1。
p15基因在胰腺癌中有较高频率的失活,失活的主要机制包括纯合缺失及甲基化[1,8],p15基因有可能成为胰腺癌基因治疗的新目的基因。文献报道[2-4,9-11],p15基因转染食管癌、黑色素瘤细胞、肝癌、胆管癌及神经胶质瘤细胞均能抑制细胞生长,有关p15转染对胰腺癌细胞增殖是否有抑制作用尚无研究报道。本实验结果显示,BxPC3细胞在转染p15基因而恢复p15蛋白高表达后,其增殖明显受到抑制,细胞被阻滞在G1/S期,出现凋亡特征性的亚G1峰,提示p15转染对胰腺癌有明显的生长抑制作用,并能诱导细胞凋亡,为胰腺癌的基因治疗提供了一种新途径。p15转染的优点是其片段长度小,克隆和转染操作比较方便,可能是具有应用前景的基因治疗的较好的靶基因。
[1] Dong Ke,Li Bo,Qing Yang,et al.Aberrant Methylation in CpG Islands of pl5 and pl6 Tumor Suppressor Genes in Pancreatic Cancer Tissue.Chinese-German J Clinical Oncology,2005,4:214-217.
[2] 刘铁夫,张学彦,孙丽萍,等.p15 INK4B基因转染联合亚砷酸对人食管鳞癌的协同抑制作用.中华消化杂志,2006,26:610-613.
[3] 童迎凯,刘军,柳惠图.CKI p15INK4B高表达对人黑色素瘤细胞cyclinD1和c-myc表达的影响及生长特性的改变.中国生物化学与分子生物学报,2000,16:514-519.
[4] 张弘,柳惠图,石法武.P15INK4b/MTS2对人肝癌细胞增殖的影响及其机理的初步分析.科学通报,2000,45:521-525.
[5] Peng B,Fleming JB,Breslin T,et al.Suppression of tumorigenesis and induction of p15(ink4b) by Smad4/DPC4 in human pancreatic cancer cells. Clin Cancer Res,2002,8:3628-3638.
[6] De Bosscher K,Hill CS,Nicolás FJ.Molecular and functional consequences of Smad4 C-terminal missense mutations in colorectal tumour cells. Biochem J,2004,379:209-216.
[7] Hitomi T, Matsuzaki Y,Yokota T,et al.p15(INK4b) in HDAC inhibitor-induced growth arrest.FEBS Lett,2003,554:347-350.
[8] Muscarella P, Knobloch TJ, Ulrich AB,et al.Identification and sequencing of the Syrian Golden hamster (Mesocricetus auratus) p16(INK4a) and p15(INK4b) cDNAs and their homozygous gene deletion in cheek pouch and pancreatic tumor cells.Gene,2001,31:235-243.
[9] 覃扬,刘建余,李波,等.p16INK4A和p15INK4B对人肝癌细胞增殖和凋亡影响的研究.中华医学遗传学杂志,2004,21:132-137.
[10] 傅赞,赵翰林,王若宁,等.P15、p16对人胆管癌细胞增殖影响的实验研究.中华普通外科杂志,2003,18:153-155.
[11] Fuxe J,Akusjarvi G,Goike HM,et al.Adenovirus-mediated overexpression of p15INK4B inhibits human glioma cell growth, induces replicative senescence, and inhibits telomerase activity similarly to p16INK4A.Cell Growth Differ,2000,11:373-384.
2009-02-18)
(本文编辑:吕芳萍)
Inhibitoryeffectofp15INK4BgeneonproliferationofhumanpancreaticcancercelllineBxPC
ZHANGXue-yan,LIUZhi-qiang,JINGDe-huai,GUANJing-ming,LIUWei.
DepartmentofGastroenterology,SecondAffiliatedHospital,HarbinMedicalUniversity,Harbin150086,China
ZHANGXue-yan,Email:zxycxw@sina.com
ObjectiveTo investigate the effect of p15INK4B(p15) gene transfection on the proliferation of pancreatic cancer cell line BxPC3.MethodsIn p15 transfection group, pCDNA3.1(+) p15 was transfected into BxPC3 cell by the vector of Lipofectamine2000. In empty plasmid transfection group, pCDNA3.1(+) neo was transfected into BxPC3 cell with the same method as a blank control group. In non-transfection group, the BxPC3 cell was not transfected as a negative control group. The p15 mRNA expressions were assayed by RT-PCR, and p15 protein expressions were assayed by Western blot. The proliferation was determined by MTT assay, ultra-structure changes were measured by transmission electron microscope. Cell cycle and apoptosis were measured by flow cytometry.ResultsIn the pCDNA3.1(+) p15 transfection group, the expression of p15 mRNA and protein were resumed. Since the 2nd day of culture, the growth of pCDNA3.1(+) p15 transfection group was inhibited, till the 7th day, the inhibitory rate was 47.9%, G0/G1phase cell accounted for (61.56±3.96)% of all the cells, which was significantly higher than (47.44±6.35)% of the black control groups and (49.22±7.23)% of the negative control group(Plt;0.05). G1apoptosis peak occurred and the apoptosis rate was (5.27±1.04)% in pCDNA3.1(+) p15 transfection group, which was significantly higher than (0.11±0.06)% of the black control groups and (0.09±0.07)% of the negative control group (Plt;0.05). Apoptosis was also observed by transmission electron microscope in the pCDNA3.1(+)-p15 transfection group cells.ConclusionsAfter p15 gene transfection, BxPC3 cell proliferation could be significantly inhibited and apoptosis could be induced.
Pancreatic neoplasms; Transfection; Cyclin-dependent kinase inhibitor p15
10.3760/cma.j.issn.1674-1935.2009.06.007
黑龙江省科技计划攻关基金重点项目(GB05C401-09),黑龙江省教育厅科学技术研究项目(11521191),黑龙江省卫生厅科研项目(2007-304)
150086 哈尔滨,哈尔滨医科大学附属二院消化科
张学彦,Email:zxycxw@sina.com

