胃肠道间质瘤的临床病理及免疫组化分析
周伟平
(株洲市三医院,湖南 株洲 412003)お
摘 要:目的:探讨胃肠道间质瘤(GIST)的临床表现、临床病理特征和免疫组织化学特征。方法:对我院18例手术切除的GIST患者标本的临床表现、临床病理特征和免疫组织化学特征进行分析。结果:本组GIST最常发生于小肠,占55.6%(10/18);其次为胃,占27.8%(5/18);直肠,占11.1%(2/18);结肠,占5.6%(1/18)。肿瘤最小0.6cm×0.5cm×0.4cm,最大25cm×14cm×12cm。梭形细胞为主14例,上皮样细胞为主3例,混合细胞(兼有梭形和上皮样细胞特征)1例。本组GIST的CD34阳性率88.9%(16/18),CD117阳性率94.4%(17/18),SMA灶性阳性率16.7%(3/18),S-100均阴性,Desmin均阴性。18例GIST患者中,良性5例,交界性9例,恶性4例。结论:免疫组化联合使用,包括CD117和CD34在内的一组抗体是必要的,只有这样才可能提高GIST的诊断率。但在GIST良、恶性诊断上仍需结合肿瘤的大体、组织学形态及生物学行为等综合考虑。
关键词:胃肠道间质瘤;病理;免疫组化
中图分类号:R735文献标识码:A文章编号:1673-2197(2009)03-0090-03オ
GIST是消化道最常见的间叶源性肿瘤,是一种独立的疾病,在形态学上主要由梭形细胞和上皮样细胞组成,因其形态多变,光镜下很难与平滑肌(肉)瘤和神经鞘瘤相区别[1],随着免疫组化及分子生物学研究的突破,发现这类肿瘤具有多种免疫表形及分化,不一定具有平滑肌的免疫表型和电镜特点,目前认为其起源于胃肠道壁的卡哈尔细胞并表达CD117和/或CD34。本篇对18例GIST的临床表现、临床病理特征、免疫组织化学特征等进行分析,为GIST的诊断、鉴别诊断和治疗提供理论依据。
1 资料与方法
1.1 一般资料
18例标本来自我院病理科2001年11月—2007年11月期间手术切除的GIST患者,均符合目前公认的GIST组织学形态标准[2],并经免疫组化染色证实诊断;其中男10例,女8例;年龄15~83岁,平均54岁;临床表现主要为呕血、黑便、黏液便、腹痛、腹胀和腹部包块。
1.2 方法
全部标本经10%福尔马林固定,石蜡包埋切片,厚4mm连续切片,HE染色,光镜观察。采用S-P法检测CD117、CD34、结蛋白(Desmin)、平滑肌肌动蛋白(SMA)和S-100蛋白(S-100)。切片经二甲苯脱蜡、梯度酒精脱水后,3%H2O2冲洗;血清封闭非特异抗体;加一抗在室温下放置2h,冲洗;滴加试剂1,室温20min,冲洗;滴加试剂2,室温20min,冲洗;应用DAB溶液显色,蒸馏水冲洗、复染、脱水、封片。结果判断分阳性、阴性。肿瘤细胞阳性超过5%为阳性,否则为阴性,肿瘤细胞浆或膜呈棕黄色为阳性。所用免疫组化检测试剂均购自北京中山生物技术有限公司。
1.3 观察指标及疗效评定标准
1.3.1 GIST良恶性判断标准
采用Lewin等[3]和Emory等[4]的标准,将GIST的恶性指标划分为肯定恶性指标和潜在恶性指标,从而将GIST分为良性GIST(无任何恶性或潜在恶性指标);恶性GIST(具备1项恶性指标或2项潜在恶性指标);潜在恶性GIST(仅具备其中1项潜在恶性指标)。
1.3.2 恶性指标
肯定性恶性指标:①肿瘤出现远、近脏器的转移;②肿瘤浸润邻近器官。潜在恶性指标:①肿瘤直径:胃间质瘤>5.5cm,肠间质瘤>4cm;②核分裂象:胃间质瘤>5个/50HPF,肠间质瘤≥1个/50HPF;③肿瘤出现坏死;④核异形性明显;⑤细胞丰富密度大;⑥上皮样细胞呈巢状或腺泡状排列。
1.3.3 免疫组化结果判断及GIST分型免疫组化结果
阳性表达为肿瘤细胞胞浆呈棕黄色,阳性细胞>5%,即判为阳性。肿瘤细胞不表达或阳性细胞<5%判为阴性。GIST分型以免疫组化结果为主,若SMA部分阳性,即为GIST伴肿瘤平滑肌分化,S-100部分阳性为GIST伴神经分化;如果SMA和S-100均为阳性为双向分化,SMA和S-100均为阴性则为肿瘤未分化,为纯间质瘤。
1.4 统计学方法
使用SPSS 13.0统计软件进行统计分析,P<0.05表示差异有统计学意义。
2 结果
2.1 肿瘤分布和生长方式
本组GIST最常发生于小肠占55.6%(10/18),其次为胃占27.8%(5/18),直肠占11.1%(2/18),结肠占5.6%(1/18)。通常为肌壁间肿块,可向腔内生长,粘膜面光滑,亦可继发溃疡,或向外、向浆膜下生长,甚至肿物主体在壁外,只有细蒂与肠壁相连。
2.2 病理检查
大体:肿瘤最小0.6cm×0.5cm×0.4cm,最大25cm×14cm×12cm,大多数为境界清楚的结节状或分叶状肿物,呈圆形、卵圆形或哑铃形,结节状或分叶状,部分可见菲薄的纤维性包膜,切面灰白质韧,部分肿瘤呈鱼肉状伴出血、坏死及囊性变。
2.3 组织学特征
梭形细胞为主14例,上皮样细胞为主3例,混合细胞(兼有梭形和上皮样细胞特征)1例。2.4 免疫组化检查
本组GIST的CD34阳性率88.9%(16/18),CD117阳性率94.4%(17/18),SMA灶性阳性率16.7%(3/18),S-100均阴性,Desmin均阴性。
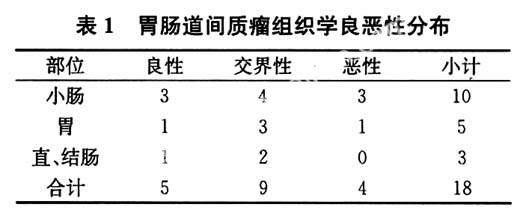
2.5 胃肠道间质瘤组织学良恶性分布
表1所示。
2.6 瘤细胞HE染色体及免疫组化图片
见图1、图2、图3、图4。


3 讨论
1983年Mazur等[5]等发现缺乏平滑肌细胞超微结构特征和免疫组化特征的一组非上皮源性胃肠道间质性肿瘤,命名为GIST。GIST是一种形态表现十分复杂的肿瘤,可发生于任何年龄段,但多见于中老年人群,男女发病率无明显倾向,光镜下其表现形式较多样。梭形细胞和(或)上皮样细胞可呈栅栏、编织状、弥漫片状、巢状等排列,瘤细胞也可呈明显的多形性,肿瘤小时通常无症状。X线照片、CT、MRI、胃肠镜或B超检查可能发现溃疡、肿块等,但定性诊断阳性率不高,仅凭HE染色形态学诊断该肿瘤也存在一定的困难。免疫组化分析简单易行,成为其诊断的辅助手段,且便于临床推广。
近年随研究的深入,GIST被定义为原发于消化道,表达c-kit蛋白(CD117),富于细胞的梭形、上皮样、偶或多形性的间叶肿瘤[6]。应注意勿与胃肠道间叶源性肿瘤(GIMT)相混淆。GIST的病理特点:①肿瘤细胞形态有两种:一种为梭形,核呈杆状,两端尖或钝圆,胞质较丰富,胞浆略嗜酸性或嗜碱性,一种为上皮样细胞呈圆形或多角形,核圆,胞浆丰富淡染,常见空泡形成。梭形细胞排列呈交叉束状、漩涡状、车辐状,上皮样细胞呈弥漫片状、巢索状排列;②70%的GIST是梭形细胞形态,20%~30%的GIST可见有上皮样细胞形态;③良性和交界性GIST瘤体直径较小,核分裂象均小于5个/50 HPF;④恶性GIST瘤体直径大,瘤细胞丰富至密集,核异型明显,核分裂象≥5/50 HPF。熟悉GIST的病理形态学特点,对诊断有重要意义。CD117是原癌基因c-kit的产物,是一种跨膜的Ⅲ型酪氨酸激酶的生长因子受体,属于免疫球蛋白的超基因家庭成员,CD117抗体对诊断GIST具有较好的敏感性和特异性。CD34是一种糖基化糖蛋白,是骨髓、造血前体细胞的抗原。Miettinen等[7]应用CD34、CD31、SMA、Desmin、S-100等检测109例GIST来分析其免疫组织化学特征,结果表明绝大部分GIST表达CD34,13%~25%灶性表达SMA,Desmin几乎无表达;典型平滑肌瘤及神经鞘瘤不表达CD34,分别SMA及S-100阳性;良恶性GIST免疫表型无显著差异。近年来研究发现CD34和CD117在GIST组织中广泛表达,阳性率分别为80%~100%和70%~80%;从本次研究结果中可以看出在GIST中CD117阳性表达率为94.4%,且其阳性表达不受组织学类型,良恶性及部位不同的影响。在本次GIST中CD34阳性表达率88.9%,但恶性GIST的表达低于良性,可能与CD34丢失有关,这一现象与隆突性皮肤纤维肉瘤发生纤维肉瘤性变后不表达CD34或灶性表达结果相同,说明GIST可出现部分平滑肌分化。同时还提示CD117是比CD34更敏感的指标。
综上所诉,对消化道梭形细胞为主的肿瘤、上皮样细胞为主或两者细胞并存的肿瘤,应首先考虑GIST的可能。免疫组化联合使用,包括CD117和CD34在内的一组抗体是必要的,只有这样才可能提高GIST的诊断率。但在GIST良、恶性诊断上仍需结合肿瘤的大体、组织学形态及生物学行为等综合考虑。
参考文献:
[1] LOGRONO R,JONES DV, FARUQI S, et al. Recent advances in cell biology, diagnosisand therapy of gastrointestinal stromal tumor (GIST)[J]. Cancer BiolTher, 2004, 3(3): 251-258.
[2] 赵海路,纪小龙.消化道间叶性肿瘤的新认识[J]. 新消化病学杂志,1996(4):100.
[3] LEWIN KJ, RIDDELL R H, WEINSTEIN WH, et al. Gastrointestinal pathologyand its clinical implications [M]. New York: Igaku- shoin,1992.
[4] EMORY TS, SOBIN LH, LUKES L, et al. Prognosis of gastrointestinalsmooth- muscle(stromal)tumors: dependence on anatomic site[J]. Am JSurg Pathol, 1999, 23: 82-87.
[5] MAZUR MT,CLARK HB. Gastric stromal tumors. Reappraisal of histogenesis[J]. Am J Surg Pathol, 1983, 7: 507.
[6] 朱雄增,侯英勇.对胃肠道间质瘤的再认识[J].中华病理学杂志,2004,33 (1):3.
[7] MIETTINEN M,VIROLAINEN M,SARLOMO-RIKALA. Gastrointestinal stromal tumors:Value of CD34 antigen in their indentification and separation from true leiomyomas and schwannomas [J]. Am J SurgPathol,1995,19:207.
(责任编辑:陈涌涛)

