多孔聚磷酸钙生物陶瓷的研究与应用
徐晓虹 李 坤 吴建锋 沈薇薇
摘要本文阐述了聚磷酸钙的国内外研究现状,初步揭示了聚磷酸钙生物陶瓷(CPP)的生物相容性和降解特性。现有的研究表明,聚磷酸钙的聚合度和晶型不同,降解速率也不同,为生物陶瓷可控降解提供了新的途径。聚磷酸钙属直链状无机聚合物,具有不完全结晶性,聚磷酸钙材料在生物相容性、降解性和力学性方面的综合优势,使其在骨修复材料领域格外受到青睐。
关键词聚磷酸钙,支架材料,骨修复材料,降解,研究与应用
1前 言
每年由于各种创伤、感染、肿瘤或先天性疾病等原因而造成骨折、骨缺损的患者全世界达几百万人。医学临床上用自体骨及异体骨移植来修复骨缺损,虽解决了生物相容性问题,但会增加患者的痛苦或增加感染的机会,而且移植所需的人体骨也不易获取。因此,研制理想的骨修复材料是医学和生物材料科学领域中的重要课题。其中钙磷系生物材料具有和脊椎动物相似的矿物成分和结构,又不存在免疫排斥反应,很早就被人们用于骨组织的修复。
钙磷系生物陶瓷作为骨修复材料是时下研究的热点。其中,羟基磷灰石(HAP)和β-磷酸三钙(β-TCP)等材料已经被用作骨修复的材料,但是它们的脆性和降解特性极大地限制了它们作为骨修复材料的临床应用。以聚乳酸(PLA)为代表的生物可降解高分子材料,尽管在降解性方面比传统的无机骨修复材料有较大优势,但是其力学特性限制了其作为承力骨修复材料的应用。因此寻找同时具有生物活性、可控的生物降解性和适当的力学性能的新型骨修复材料已经引起广泛的关注。聚磷酸钙(CPP)就是近年来国内外少数实验室正在研制的一种新型磷酸钙生物陶瓷骨修复材料。CPP是从磷酸钙陶瓷的基础上新近发展起来的一种多孔、生物相容性好和可降解的材料,可以提供必要的生物力学强度,降解释放出来的钙、磷离子能帮助细胞生长,通过控制材料的聚合度和晶型能改变材料的降解速率。
2多孔聚磷酸钙的国内外研究现状
2.1 多孔聚磷酸钙的结构
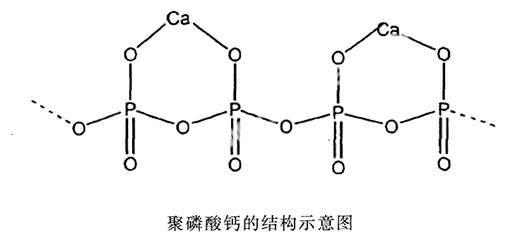
CPP由磷酸二氢钙通过分子间缩聚反应生成,密度为2.85g/cm3[1]。CPP的Ca/P摩尔比理论值为0.5,β-TCP的Ca/P摩尔比理论值为1.5,HAP的Ca/P摩尔比理论值为1.67。Pilliar RM等[1]的研究表明,随着Ca/P值的降低,磷酸钙原子结构能够成为直链聚合物形式。这种聚合物不同于一般的有机高分子聚合物,它的支链结构不是由简单的共价键连接而成,而是通过PO43-离子进行连接。随着Ca/P比的降低,可形成三维的笼状结构(超磷酸盐,Ultraphosphate)、环状结构(偏磷酸盐,Netaphosphate)以及链状结构(聚磷酸盐,Polyphosphate)。Anna Dion等[2]利用核磁共振(NMR)和拉曼光谱法对CPP的结构进行了研究,证实了CPP的直链结构。CPP的聚合物主链以-P-O-P-为主,其分子式为[Ca(PO3)2]n,其结构如图1所示。
2.2 聚磷酸钙聚合度的表征方法
聚磷酸钙是无机聚合物,其聚合度的表征不同于一般的有机聚合物。有机聚合物可以根据粘度变化来判断其大致范围,也可以通过凝胶色谱来进行表征。对CPP而言,由于本身为粉体,又属于磷酸盐,很难找到合适的溶剂,一般采用31P固相核磁共振来分析,通过不同化学环境中P元素的峰的积分面积对CPP的化学结构进行分析,然后计算出其聚合度。
2.3 多孔聚磷酸钙的国内外研究现状
目前已经报道的聚磷酸钙制备方法主要有:重力烧结法、固态自由成形法、低温等压法、单轴压缩法、聚合物泡沫法、高温拉丝法等。聚磷酸钙作为新型的生物材料主要用作支架材料、增强材料、骨修复材料,以下分别阐述。
2.3.1 聚磷酸钙支架材料
Pilliar RM[1]等人通过重力烧结法制备出β型多孔CPP支架材料。他们用粒径为150~250μm和106~150μm的CPP粉体作为原料,在965℃和970℃下烧结得到β型多孔支架材料,孔隙率在35~45%之间,孔径在70~100μm之间,用106~150μm的粉体制备的支架材料的抗压强度极高,最高抗压强度可达24.1MPa。在0.1mol的三羟甲基氨基甲烷(Tirs)缓冲液(pH=7.4)中对材料进行模拟降解,发现材料的抗压强度和失重在降解1天时变化最大,到30天时材料的抗压强度只有初始值的1/3。细粉支架的降解与介质的pH也有一定关系,酸性介质降解更快,而粗粉支架则几乎不受影响。动物实验结果表明[3],多孔CPP支架材料具有良好的相容性,能够迅速促使骨组织生产,经过12周和1年间形成的新骨量相当于相应部位天然骨的体积。CPP在体内的降解速率与制备支架所用粉体尺寸成反比,前6周降解速率较快,其后趋缓。
El Sayegh TY[4]等用重力烧结法制备了多孔CPP支架材料,他们用粒径为75~106μm的CPP粉体作为原料,在585℃和600℃下烧结分别得到无定型的CPP多孔支架材料和β型多孔支架材料,并在CPP材料上和钛基上培养成纤维细胞。结果表明,在细胞贴附、铺展方面,钛基是CPP材料的2~3倍,在细胞外基质方面,二者数量相似;两种CPP材料上的细胞贴附、铺展以及细胞外基质没有明显区别。因此,他们认为,CPP材料的降解速率和结晶状况对纤维细胞和CPP的相互作用没有影响。
Waldman SD[5]等也用重力烧结法制备了多孔CPP支架材料,并在支架材料上进行软骨细胞的培养。经过8周实验,发现在CPP上生长有连续的软骨组织,并且软骨组织与CPP表面已结合,体外培养生成的软骨组织形成了与天然软骨组织相似的厚度层。体外培养的软骨细胞合成了与天然软骨细胞相似的蛋白聚糖和Ⅱ型胶原,两种软骨细胞合成的蛋白聚糖相似,然而,前者合成的胶原偏少,这使得培养得到的软骨组织的力学性能仅有天然软骨组织力学性能的3%。
唐昌伟等[6]采用重力烧结法制备出聚合度为26的多孔CPP支架材料,其孔隙率约为50%,抗压强度为5.5~7.0MPa,并对CPP的晶型转变、体外降解及细胞相容性进行了初步研究。结果表明,CPP在0~1000℃之间会发生三次晶型转变,降解速率随晶型不同而不同,具体表现为:γ-CPP>β-CPP>α-CPP,多孔CPP支架材料能够支持成骨细胞的粘附、生长、增殖,并保持一定的活性和功能,成骨细胞在β-CPP多孔支架材料上表现出最强的增殖能力。邱凯等[7]以硬脂酸作成孔剂,制备了掺锶多孔CPP支架材料。他们创新性地提出了简便CPP聚合度的计算模型,并且研究了CPP的聚合度以及晶型对其降解的影响。结果发现,材料的晶型和聚合度对降解速率的影响显著,CPP的聚合度越小,支架材料的孔隙率越大;热处理的CPP颗粒粒径越小,降解速率就越快;低温烧结得到的CPP比高温烧结得到的CPP降解快。动物实验显示,掺锶量为1%的CPP样本中新骨生成快于CPP样本,掺锶CPP多孔结构中形成了大量的骨小梁,并有较多的血管长入。
Porter NL等[8]用固态自由成形(SFF)法制备了多孔CPP支架材料。他们用粒径小于25μm的粉体作为原料,在585℃和600℃下烧结分别得到无定型的CPP多孔支架材料和β型多孔支架材料,其孔隙率分别约为28%和23%,其抗弯强度分别为19.6MPa和31.59MPa。在0.1mol的Tirs缓冲液中,对材料进行模拟降解,发现两种支架材料的力学强度都随着降解时间的增加而降低,然而,无定型支架材料在降解1天后抗弯强度损失超过了50%,降解5天后损失超过95%,而β型支架材料降解1天后抗弯强度损失了25%,降解10天后损失60%。通过对降解液中磷含量进行检测,发现1天后无定形材料降解液中的磷含量是β型支架材料的4倍,仅仅5天后无定形支架材料的降解液中磷含量就达到24.2%,10天后β型多孔支架材料的降解液中磷含量仅为2.7%。对降解后的样品进行形貌分析,发现无定型支架材料的表面出现一沉淀层,内部出现大的孔洞,而β型支架材料的形貌没有明显变化,仅有部分颗粒表面发生了溶解。研究发现,超过60%的孔径尺寸小于30μm,将不利于新骨长入其中,一些学者认为孔径在200~400μm时最有利于新骨生长。
Filiaggi MJ等[9]用低温等压法和单轴压缩法制备了多孔CPP支架,避免了高温烧结,使支架材料的多孔结构更易控制。当支架材料的孔隙率为20%时,材料抗张强度仅有6MPa,因此不能作为承力的骨修复材料。他们后来在CPP材料中加入抗菌剂万古霉素,制备了一种抗感染的骨修复材料[2]。
Baksh D等[10]用聚氨酯泡沫技术制备了三维大孔连通的CPP支架材料,其孔径为0.3~1mm,并对材料进行了体外骨髓细胞培养和体内植入实验。研究发现,2周后,在体外培养和体内植入的实验样品中都有骨长入。在体外实验中,CPP和骨的界面上有明显的结合带,而在体内实验中,CPP和骨的界面上有非矿化纤维组织,并且骨已经长入多孔CPP的微孔中。CPP支架的某些表面颗粒形态在体内实验中已经变成圆形,而在体外实验中无任何变化,说明体内的一些CPP颗粒已经溶解。这一切初步表明,三维CPP可以作为骨组织工程的支架材料。
2.3.2 聚磷酸钙纤维增强材料
石宗利等[11,12]制备了无定型的CPP纤维,发现CPP纤维有优异的生物相容性、力学性能和可调控的表面降解性。他们用CPP纤维增强TCP和左旋聚乳酸(PLLA),取得了良好的效果[13,14,15],但并未对结晶后的生物陶瓷和聚合度进行相关的研究。
常青等[16]对CPP纤维的降解情况进行的研究表明,当pH值一定时,纤维质量随时间的变化表现为直线,即降解速率方程与时间成一次方关系。赵琳等[12]将CPP纤维束植入大鼠肢体对称部位的皮下、肌肉和肌键进行体内降解实验。X光片及组织切片表明,CPP纤维在肌肉内约16周完全降解,在肌键、皮下约20周完全降解,降解产物无局部沉积现象。
2.3.3 聚磷酸钙骨修复材料
Yang等[17]制备了聚己酸内酯和CPP的互穿相复合材料,其选用的CPP孔隙率为35%。研究发现,酶能促进聚己酸内酯的水解,在聚己酸内酯上引入离子基团,能有效增加两相材料的界面粘结强度,从而使复合材料的抗弯强度是CPP单一材料抗弯强度的7倍。由SEM发现,聚己酸内酯已经渗透到多孔CPP的所有孔隙中。研究结果进一步扩展了其在承力骨修复方面的应用潜力。
Yang SM等[18,19]制备了壳聚糖基复合材料,并在狗体内进行了实验,发现在狗体内有良好的生物相容性和骨传导性。
张志斌等[20]采用自行设计的悬浮液热分散复合法制备了大孔聚磷酸钙/壳聚糖(CPP/CS)复合材料棒材,将复合悬液滴入凝固液中,经浸泡-漂洗-干燥的工艺制备了CPP/CS微孔复合材料颗粒。大孔复合材料棒材的孔径为50~300μm,孔隙率为71.13%,微孔复合材料颗粒的孔径为10~100μm,孔隙率为40.76%。研究发现:大孔复合材料棒材的细胞相容性比微孔复合材料颗粒好,复合材料中随着CPP含量的增加,细胞相容性增加,当复合材料中CPP和CS的质量比为7/3时,复合材料的细胞相容性较好,此时的强度最高。
3CPP生物陶瓷的降解特性
CPP生物陶瓷属可降解和吸收的生物陶瓷。CPP属于无机聚合物,结晶性不完整,其降解性不同于一般的无机物和有机物。研究表明[21],随着聚合度的增加,材料的抗压强度增大,降解速率变小;不同晶型的材料具有不同的降解速率,降解速率为非晶CPP>γ-CPP>β-CPP>α-CPP,非晶CPP在第17 天完全降解,γ-CPP在第25 天完全降解,β-CPP和α-CPP降解缓慢,在第30 天时才分别降解了大约12%和5%。
常青等[16]通过实验证明,CPP纤维在中性介质中仅发生缓慢降解,在酸性介质中将会使降解加速,在碱性介质中降解速度最高。直链聚磷酸盐在水中缓慢水解而发生化学降解,其反应如下:
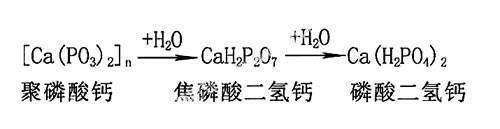
Pilliar RM等[1]把聚磷酸钙生物陶瓷的降解分为两个阶段:(1)在降解前期,无定型或结晶度小的区域发生快速降解,此区域内的力学强度丧失得非常快,此过程大概持续1天左右;(2)第二阶段是材料的高结晶区域发生降解,降解速率减缓,力学强度缓慢降低,到30天时材料抗压强度损失了2/3。姚康德[22]报道多孔聚磷酸钙支架在体内降解速率比体外的缓冲液(pH=7.4)快一个数量级,这是由于无机材料在体内的降解与细胞活性有关。总之,无定型材料降解最快,α型的降解最慢;气孔率越大,其降解越快。CPP生物陶瓷的降解速率与材料颗粒大小、晶型、聚合度、气孔率、孔径大小等因素有关。
4CPP生物陶瓷的应用
常青等[19]将CPP纤维用作可降解复合材料的增强纤维,用CPP和淀粉/聚乙烯醇薄膜制成了可降解复合材料。Lagow等将多孔聚磷酸钙生物陶瓷用于颚骨的替代,Nelson等将多孔聚磷酸钙生物陶瓷用于狗体上颚骨的修复,4个月后,通过扫描电镜观察,长入多孔聚磷酸钙中的骨组织比植入对侧位置的自体骨明显得多[1]。
在临床上,CPP生物陶瓷主要用于治疗脸部颌部的骨缺损,填补牙周的空洞以及与有机或无机物复合制成人造肌腱及复合骨板,还可作为药物的载体。聚磷酸钙粉末可用于不规则形状缺损的填充,比如牙周缺损,或者填入牙移植的植入部位起空间扩张作用,为移植提供空间[23]。
5结论与展望
聚磷酸钙作为一种刚刚发展的钙磷系生物材料,已引起国内外学者的关注,并得到研究和发展。CPP在0~1000℃之间会发生三次晶型转变,降解速率随晶型不同而不同,具体表现为:γ-CPP>β-CPP>α-CPP,其中β型存在的温度范围较宽,而且学者研究得最多。CPP生物陶瓷的降解分为两个阶段:(1)在降解前期,无定型或结晶度小的区域发生快速降解;(2)第二阶段是材料的高结晶区域发生降解,降解速率减缓,力学强度缓慢降低。经研究,CPP作为支架材料,适合软骨细胞、成骨细胞的生长,能够促进骨组织的生长,承担支架的作用,但仍需进一步研究细胞生长速率与材料的降解速率相匹配的问题。无定型CPP纤维增强TCP和PLLA,取得了良好的效果,展现了CPP纤维的增强作用,可开展研制复合生物材料。CPP作为单一材料,其强度可满足非承重骨的修复,Yang等[17]制备了聚己酸内酯和CPP的互穿相复合材料,使复合材料的抗弯强度为CPP单一材料抗弯强度的7倍,这在承力骨修复方面的研究方面开辟了方向。无论其用途如何,但作为生物材料,如何使细胞生长速率与材料的降解速率相匹配一直是有待解决的问题,通过刺激细胞生长或调控CPP降解速率有望解决这一问题。
CPP具有的链状结构和无机物特点,使其结晶具有不完整性,聚合度可因热处理制度不同而发生变化,这一切使其降解特性不同于一般的高分子化合物和无机物。其降解性通过聚合度和晶型调整可以达到可控。CPP的Ca/P摩尔比理论值为0.5,降解产生的钙、磷均能为细胞生长提供帮助。随着人类生活水平的提高,人类的健康日渐受到重视,生物产业发展迅猛。近10年来,全球生物医用材料和制品的市场一直保持15%以上的年增长率, 2002年全球仅生物相容性材料和终端产品市场的市场容量已从2000年230亿美元增长至500亿美元。生物材料和生物技术正在成长为本世纪世界经济的一个支柱性产业。
参考文献
1 RM.Pilliar,M.J.Filiaggi,J.D.Wells,et al.Porous Calcium Polyphosphate Scaffolds for Bone Substitute Applications——in Vitro Characterization[J].Biomaterials,2001,22:963~972
2 Anna Dion,Bob Berno,Gordon Hall,et al.The Effect of Processing on the Structural Characteristics of Vancomycin-loaded Amorphous Calcium Phosphate Matrice[J].Biomaterials,2005,26:4486~4494
3 Grynpas MD,Pilliar RM,Kandel RA,et al.Porous Calcium Polyphosphate Scaffolds for Bone Substitute Applications in Vivo Studies[J].Biomaterials,2002,23:2063~2070
4 El Sayegh Tarek Y,Pilliar RM,McCulloch ChristopherA. G.Attachment,Spreading,and Matrix Formation by Human Gingival Fibroblasts on Porous-structured Titanium Alloy and Calcium Polyphosphate Substrates[J].Journal of Biomedical Materials Research,2002,61:482~492
5 Waldman Stephen D,Grynpas Marc D, Pilliar Robert M, et al.Characterization of Cartilagenous Tissue Formed on Calcium Polyphosphate Substrates in Vitro[J]. Journal of Biomedical Materials Research,2002,62:323~330
6 唐昌伟.生物医用高分子材料[R].四川大学硕士学位论文,2005
7 邱 凯. 生物材料与组织工程[R].四川大学博士论文,2005
8 Porter N.L,Pilliar R.M.,Grynpas M.D.Fabrication of Porous Calcium Polyphosphate Implants by Solid Freeform Fabrication:A Study of Processing Parameters and in Vitro Degradation Characteristics[J].Journal of Biomedical Materials Research,2001,56:504~515
9 Filiaggi M.,Hall G..A Compaction Route for Low Temperature Processing of Porous CalciumPolyphosphate Matrices[J].Key Engineering Materials, 2002,218:43~46
10 Baksh D.,Davies J.E.,Kim S.Three-dimensional Matrices of Calcium Polyphosphates Support Bone Growth in Vitro and in Vivo[J].J Mater SciMater Med, 1998, 9:743~748
11 石宗利,戴 刚,李重庵等.一种新型骨组织工程支架材料——CPP纤维的制备与性能[J].兰州大学学报(自然科学版),2001,2:47~51
12 赵琳,孙正义.聚磷酸钙纤维体内降解及组织相容性实验[J].中国修复重建外科杂志,2002,5:300~302
13 徐立新,石宗利,史学婷等.CPP/α-TCP复合骨水泥复合材料研究[J].兰州大学学报(自然科学版),2004,3:22~25
14 石宗利,张媛,戴刚等.CPP/PLLA单向纤维骨内固定复合 材料制备和性能[J].机械工程学报,2004,11:53~57
15 王彦平,石宗利.CPP/PLLA软骨组织工程支架复合材料制备及其性能表征[J].兰州大学学报(自然科学版),2005,4:85~88
16 常 青,石宗利,李重庵.聚磷酸钙可降解纤维研究[J]. 环境科学,1997,2:52~53,57~58
17 Liu Yang, Jian Wang,Jason Hong,J.Paul Santerre,et al,Synthesis and Characterization of ANovel Polymer-ceramic System for Biodegradable Composite Applications[J].J.Biomed Mater Ices, 2003,66:622~632
18 Yang S.M.,Kim S.Y,Lee S.J,Ku Y,et al.TissueResponse of Calcium Polyphosphate in Beagle Dog[J]. Key Engineering Materials,2002,218:657~660
19 Yang S.M.,Kim S.Y,Lee S.J.,Lee YK.,et al.Tissueof Calcium Polyphosphate in Beagle Dog Part II:12 Month Result[J].Key Engineering Materials,2004,254:245~248
20 张志斌,黎达光,苏智青等.骨修复用聚磷酸钙/壳聚糖复合材料的合成及其细胞相容性[J].复合材料学报,2007,6:105~109
21 邱 凯,陈元维,张 琦等.骨组织工程用聚磷酸钙的结构和 性能的研究[J].生物医学工程学杂志,2006,6:1271~1274
22 姚康德,尹玉姬.组织工程相关生物材料[M].北京:化学工业出版社,2003,8:83~83
23 邱 凯,陈 馨,万昌秀.骨组织工程支架材料聚磷酸钙生物陶瓷研究进展[J].生物医学工程学杂志,2005,3:614~617
The Study and Application of Porous Calcium Polyphosphate Bioceramic
Xu XiaohongLi KunWu JianfengShen Weiwei
(School of Materials Science and Engineering, Wuhan University of TechnologyWuhanHubei430070)
Abstract: The recent research and application of calcium polyphosphate at home and abroad were discussed in this paper.It primarily revealed the biocompatibility and degradability of calcium polyphosphate bioceramic.The present research showed that different polymerization degree and crystalline structure result in the different biodegradation ratio,which points out the new approch for controllable biodegradation of bioceramic.Calcium polyphosphate is a long chain linear inorganic condensed phosphate with most crystalline structure.It is popular with the future bone repair because of its fine biocompatibility and degradability and mechanic property .
Keywords: calcium polyphosphate,scaffold,bone repair,degradation,study and application

