脐带间充质干细胞外泌体对心肌梗死小鼠心肌损伤的保护作用

【摘要】目的 探讨脐带间充质干细胞(UCMSCs)来源的外泌体(Exos)对心肌梗死(MI)小鼠心功能、心肌细胞凋亡蛋白及心肌组织损伤的影响。方法 将UCMSCs培养至第3~9代,分离UCMSCs中的Exos,应用蛋白质免疫印迹法(WB)鉴定其表面标志物CD63、CD81蛋白,应用实时荧光定量聚合酶链式反应(RT-PCR)检测miR-152-3p的相对表达量。取C57BL/6雄性小鼠15只,以随机数字表法分为sham组(5只)、MI组(5只)、MI+UCMSCs-Exos组(5只),采用冠状动脉左前降支结扎术构建MI模型小鼠,其中MI+UCMSCs-Exos组小鼠造模成功后将50 μL Exos均分为4份,注射至小鼠梗死区域周围4点,并于术后第2、5、7、9、12天行尾静脉注射50 μLExos,sham组与MI组小鼠于同时间点以等量的磷酸盐缓冲溶液(PBS)处理。3组小鼠术后均观察14 d。比较术后14 d 3组小鼠的心功能、血清miR-152-3p表达、心脏质量(HW)/胫骨长度(TL)、心肌组织病理形态学及心肌细胞中B淋巴细胞瘤-2(Bcl-2)蛋白、Bcl-2相关X蛋白(Bax)表达水平。结果 UCMSCs-Exos中的CD63、CD81蛋白表达量及miR-152-3p的相对表达量均高于UCMSCs;术后14 d,与sham组比,MI组与MI+UCMSCs-Exos组小鼠血清miR-152-3p、左室射血分数(LVEF)、左心室缩短分数(LVFS)水平均下降,HW/TL水平均升高,与MI组比,MI+UCMSCs-Exos组小鼠血清miR-152-3p、LVEF、LVFS水平均升高,HW/TL水平下降;术后14 d,与sham组比,MI组与MI+UCMSCs-Exos组小鼠心肌细胞受损、细胞排列紊乱、心肌纤维增生、细胞间隙增大、炎症细胞浸润,与MI组比,MI+UCMSCs-Exos组小鼠心肌细胞受损减轻、细胞排列稍紊乱、心肌纤维增生较少、细胞间隙的变化较小、炎症细胞浸润较少;术后14 d,与sham组比,MI组与MI+UCMSCs-Exos组小鼠心肌细胞中Bcl-2蛋白表达水平下降,Bax蛋白表达水平升高,与MI组比,MI+UCMSCs-Exos组小鼠心肌细胞中Bcl-2蛋白表达水平升高,Bax蛋白表达水平下降(均P<0.05)。结论 UCMSCs来源的Exos可改善MI小鼠的心功能,抑制心肌细胞凋亡,减轻心脏组织病理改变,且Exos在MI中发挥保护作用可能与高表达miR-152-3p有关。
【关键词】心肌梗死 ; 脐带间充质干细胞 ; 外泌体
【中图分类号】R541 【文献标识码】A 【文章编号】2096-3718.2024.23.0026.04
DOI:10.3969/j.issn.2096-3718.2024.23.009
心肌梗死(myocardial infarct,MI)是临床上较严重的一种心肌缺血性疾病,主要是由于心肌细胞凋亡和心肌重塑对心脏功能造成了不可逆的损伤。现阶段,临床上主要采取介入手术和溶栓治疗MI,但其对坏死心肌组织的治疗效果不甚理想[1]。脐带间充质干细胞(UCMSCs)是新生儿脐带组织中具有自我更新能力和多向分化潜能的多功能干细胞,在研究中被证实可以有效改善MI模型动物的心功能,且其外泌体(Exos)中的微小RNA(miRNA)可抑制MI后心肌细胞凋亡,减轻心肌缺血再灌注损伤[2]。研究表明,UCMSCs来源的Exos中表达量较大的miRNA之一为miR-152-3p,其在缺氧诱导的人脐静脉内皮细胞中高表达,可调节内皮细胞的通透性,并提高细胞存活率[3]。基于此,本研究旨在探讨UCMSCs来源的Exos对MI小鼠心肌损伤的保护作用及其作用机制,现报道如下。
1 材料与方法
1.1 实验动物、细胞、主要试剂及仪器
1.1.1 实验动物 C57BL/6雄性小鼠[湖北省实验动物研究中心,实验动物生产许可证号:SYXK(鄂)2024-0013],雄性小鼠6~8周龄,平均(7.35±0.64)周;体质量18~22 g,平均(20.46±1.48)g。饲养于广州医科大学附属第二人民医院动物实验室中,无特定病原体环境,温度20~26 °C,湿度40%~70%,所有小鼠均可自由获取水和食物,适应性饲养7 d,无不良反应后纳入实验。本研究经华南理工大学附属第六医院(佛山市南海区人民医院)动物医学伦理委员会批准。
1.1.2 实验细胞 UCMSCs(武汉普诺赛生命科技有限公司)。
1.1.3 主要试剂与仪器 miR-152-3p与U6引物(广州锐博生物科技公司)。胎牛血清、TRIzol试剂[赛默飞世尔科技(中国)有限公司];One Step PrimeScript miRNA cDNA逆转录试剂盒(TaKaRa);SYBR GreenPCR试剂(MedChemExpress);CD63、CD81、B淋巴细胞瘤-2(Bcl-2)、Bcl-2相关X蛋白(Bax)一抗与羊抗兔免疫球蛋白G[辣根过氧化物酶(HRP)标记]二抗(Abcam);放射免疫沉淀测定(RIPA)裂解液、二辛可宁酸(BCA)试剂盒及增强化学发光(ECL)试剂盒(上海碧云天生物公司)。分光光度计[赛默飞世尔科技(中国)有限公司,型号:NanoDrop 2000];超声成像系统(加拿大VisualSonics,型号:Vevo 2000);倒置显微镜(Olympus,型号:CKX31)。
1.2 研究方法
1.2.1 UCMSCs培养 UCMSCs用含有10%胎牛血清的DMEM培养基置于5% CO2、37 °C的加湿培养箱中培养,选取培养至第3~9代中生长良好的细胞用于后续实验。
1.2.2 Exos分离与鉴定 UCMSCs用磷酸盐缓冲溶液(PBS)洗涤,随后在不含Exos的DMEM培养基上培养48 h,收集条件培养基,离心(1 500 r/min,30 min)后取上清液,使用分离试剂收集上清液中的Exos。分别应用RIPA裂解液提取细胞、Exos总蛋白,以BCA法定量检测其蛋白浓度。采用蛋白质免疫印迹法(WB)鉴定Exos表面标志物(CD63和CD81),蛋白样品经聚丙烯酰胺凝胶电泳分离后,转移至聚偏二氟乙烯(PVDF)膜上,加入CD63(1∶1 000)和CD81(1∶1 000)一抗,于4 °C下孵育过夜。洗膜后加入羊抗兔免疫球蛋白G(HRP标记)二抗(1∶2 000),于37 ℃下孵育1 h,以ECL法显影。以β-肌动蛋白(β-actin)为内参,应用ImageJ软件计算目的蛋白的相对灰度值。
1.2.3 实时荧光定量聚合酶链式反应(RT-PCR)检测Exos中miR-152-3p的表达 分别提取UCMSCs与Exos总RNA,应用分光光度计测定其浓度和纯度,反转录为cDNA,以cDNA为模板进行RT-PCR扩增。反应体系:cDNA模板5 µL,正向引物与反向引物各0.5 µL、SYBR GreenPCR 10µL、加水补足至20 µL。反应条件:95 °C预变性2 min,95 °C变性15 s、60 °C退火30 s、72 °C延伸15 s。应用2-ΔΔCT法计算miR-152-3p的相对表达量。进行3次独立实验,取其平均值。
1.2.4 动物分组与造模 选取C57BL/6小鼠15只,以随机数字表法分为sham组(5只)、MI组(5只)、MI+UCMSCs-Exos组(5只)。sham组小鼠仅打开胸腔,不进行冠状动脉结扎处理,MI组与MI+UCMSCs-Exos组小鼠均进行造模处理。小鼠麻醉后,常规备皮并消毒,在心脏搏动最明显处,作一长约2.5 cm的切口,钝性分离皮肤与皮下肌肉层,暴露肋骨,剪断第三、四根肋骨及肋间肌,打开胸腔,剪开心包膜,在左心耳下方2~3 mm处由右向左穿过心肌,结扎冠状动脉,观察左心室壁变得苍白,关闭胸腔并缝合。心电图检测出现ST段上抬或T波倒置提示造模成功。MI建模成功后,取1.2.2中已鉴定的50 μL Exos,将其均分为4份,注射至MI+UCMSCs-Exos组小鼠梗死区域周围4点处,sham组与MI组小鼠注射等量PBS。于术后第2、5、7、9、12天时,MI+UCMSCs-Exos组小鼠行尾静脉注射50 μL Exos治疗,sham组与MI组小鼠注射等量的PBS。术后14 d,对3组小鼠实施安乐死,分离其心脏组织。
1.2.5 WB法检测心肌细胞凋亡蛋白 取各组小鼠适量心脏组织,应用RIPA裂解液提取细胞总蛋白,以BCA法定量检测蛋白浓度。应用WB法检测心肌细胞Bcl-2、Bax蛋白的表达水平,取每组小鼠25 μg蛋白样品,10%聚丙烯酰胺凝胶电泳进行分离,转移至PVDF膜上,5%脱脂牛奶封闭2 h。加入Bcl-2(1∶2 000)和Bax(1∶1 000)一抗后孵育,经洗膜、二抗孵育、显影处理后,应用ImageJ软件计算目的蛋白的相对灰度值。
1.2.6 苏木精 - 伊红(HE)染色 将各组小鼠心脏组织用4%多聚甲醛固定,石蜡包埋后进行切片,厚度5 μm,切片脱蜡至水化,行常规HE染色,经脱水、透明、中性树脂封片处理,在显微镜下观察心脏组织的形态变化。
1.3 观察指标 ⑴UCMSCs分泌的Exos的鉴定及其miR-152-3p的表达量。应用WB法检测CD63、CD81蛋白表达量;应用RT-PCR法检测miR-152-3p的相对表达量。⑵心功能。术后14 d,抽取小鼠腹主动脉血1 mL,离心(2 000 r/min,20 min),取上层血清,应用RT-PCR法检测血清中miR-152-3p的相对表达量;应用经胸超声心动图测定小鼠左室射血分数(LVEF)、左室缩短分数(LVFS);分离心脏组织后,测定心脏质量(HW),测量小鼠胫骨长度(TL),并计算HW/TL。⑶HE染色。术后14 d,比较3组小鼠心肌组织病理形态学。⑷凋亡蛋白表达。术后14 d,应用WB法测定3组小鼠心肌细胞凋亡Bcl-2、Bax蛋白表达水平。
1.4 统计学方法 应用GraphPad Prism 8.0软件进行统计学分析,计量资料经S-W检验符合正态分布,以( x ±s)表示,两组间比较采用独立样本t检验,多组间比较采用单因素方差分析,多组间两两比较采用SNK-q检验。P<0.05为差异有统计学意义。
2 结果
2.1 UCMSCs来源的Exos的鉴定及其miR-152-3p的表达量 UCMSCs-Exos中CD63、CD81蛋白的表达量分别为(3.46±0.37)、(2.98±0.31),miR-152-3p的相对表达量为(6.72±0.78),均高于UCMSCs的(1.00±0.09)、(1.00±0.09)、(1.00±0.09),差异均有统计学意义(t=11.190、10.620、12.840,均P<0.05),见图1。
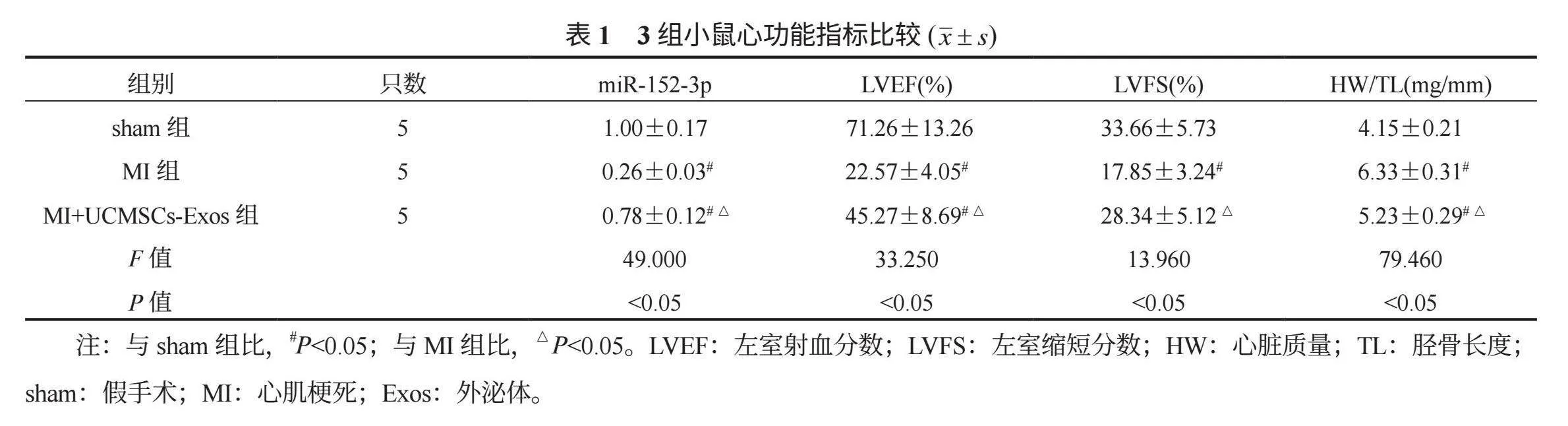
2.2 3组小鼠心功能比较 术后14 d,与sham组比,MI组与MI+UCMSCs-Exos组小鼠血清miR-152-3p、LVEF、LVFS水平均下降,MI+UCMSCs-Exos 组高于MI组;HW/TL水平均升高,MI+UCMSCs-Exos 组低于MI组,差异均有统计学意义(均P<0.05),见表1。
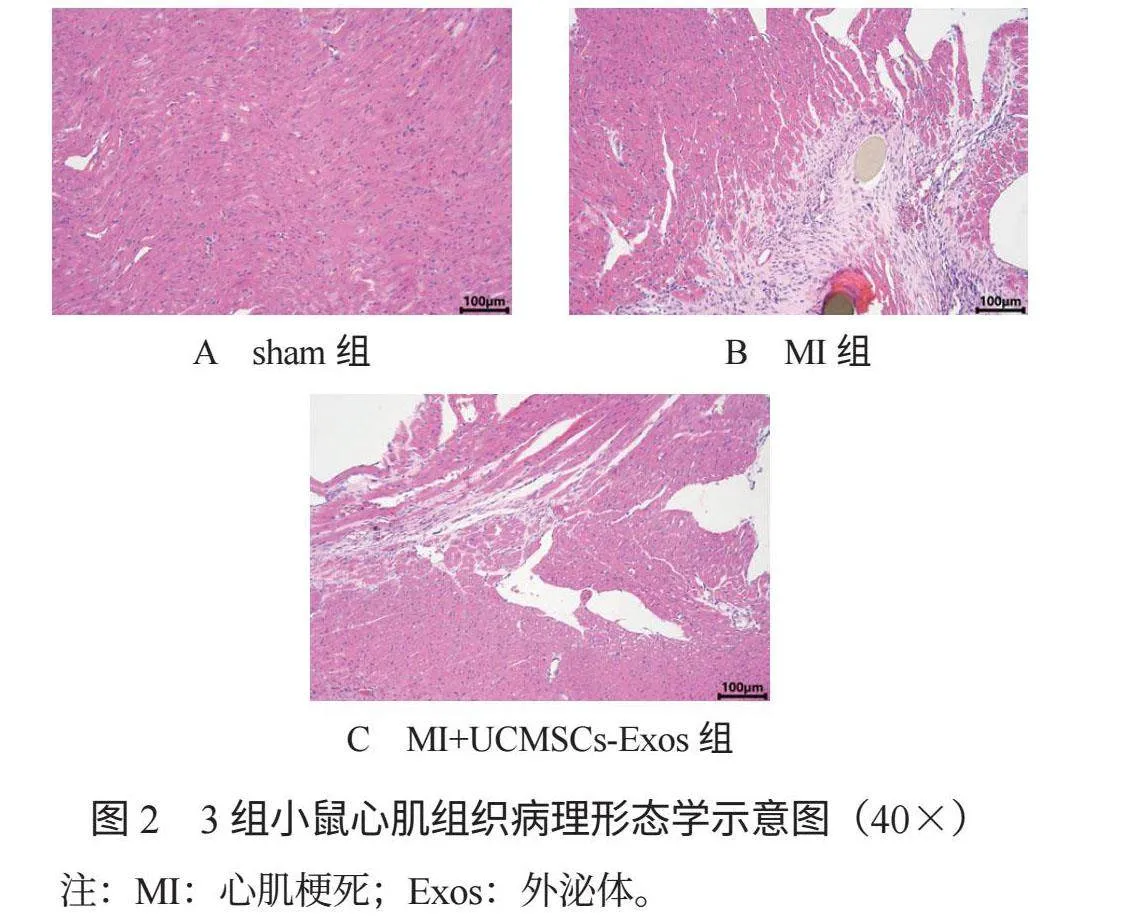
2.3 3组小鼠心肌组织病理形态学比较 术后14 d,与sham组比,MI组与MI+UCMSCs-Exos组小鼠心肌细胞受损、细胞排列紊乱、心肌纤维增生、细胞间隙增大、炎症细胞浸润;与MI组比,MI+UCMSCs-Exos组小鼠心肌细胞受损减轻、细胞排列稍紊乱、心肌纤维增生较少、细胞间隙的变化相对较小、炎症细胞浸润较少,见图2。
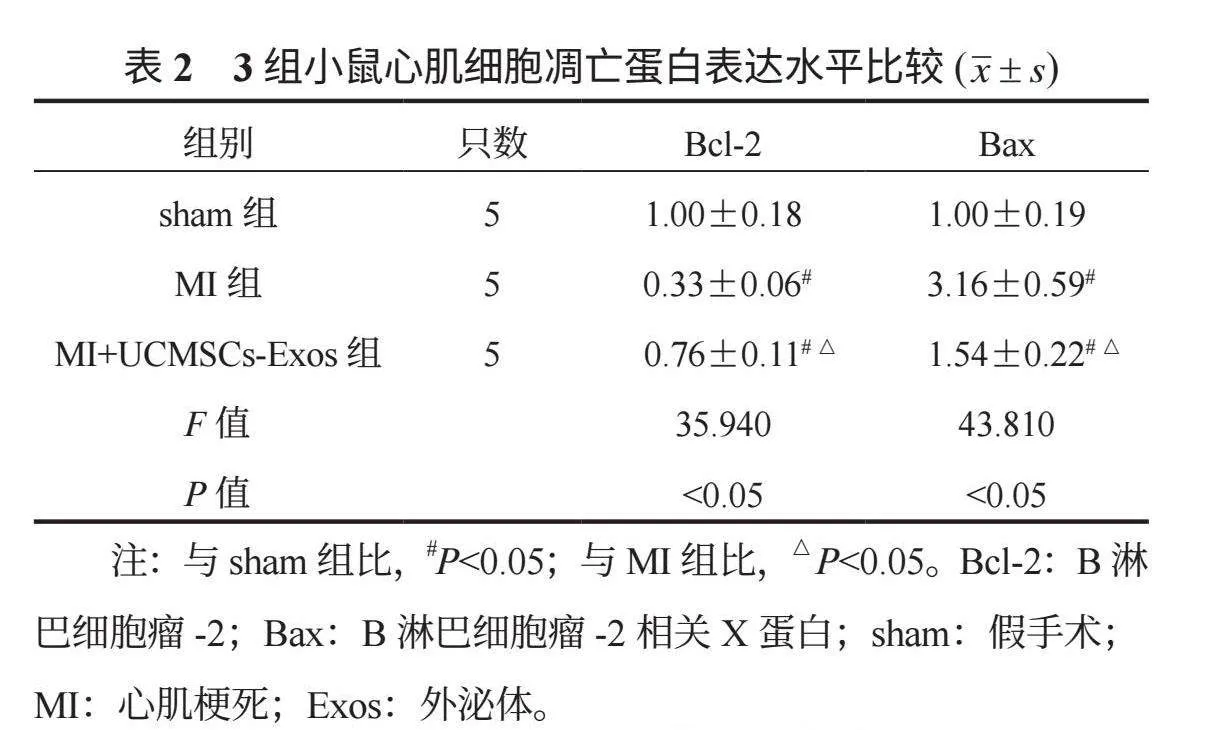
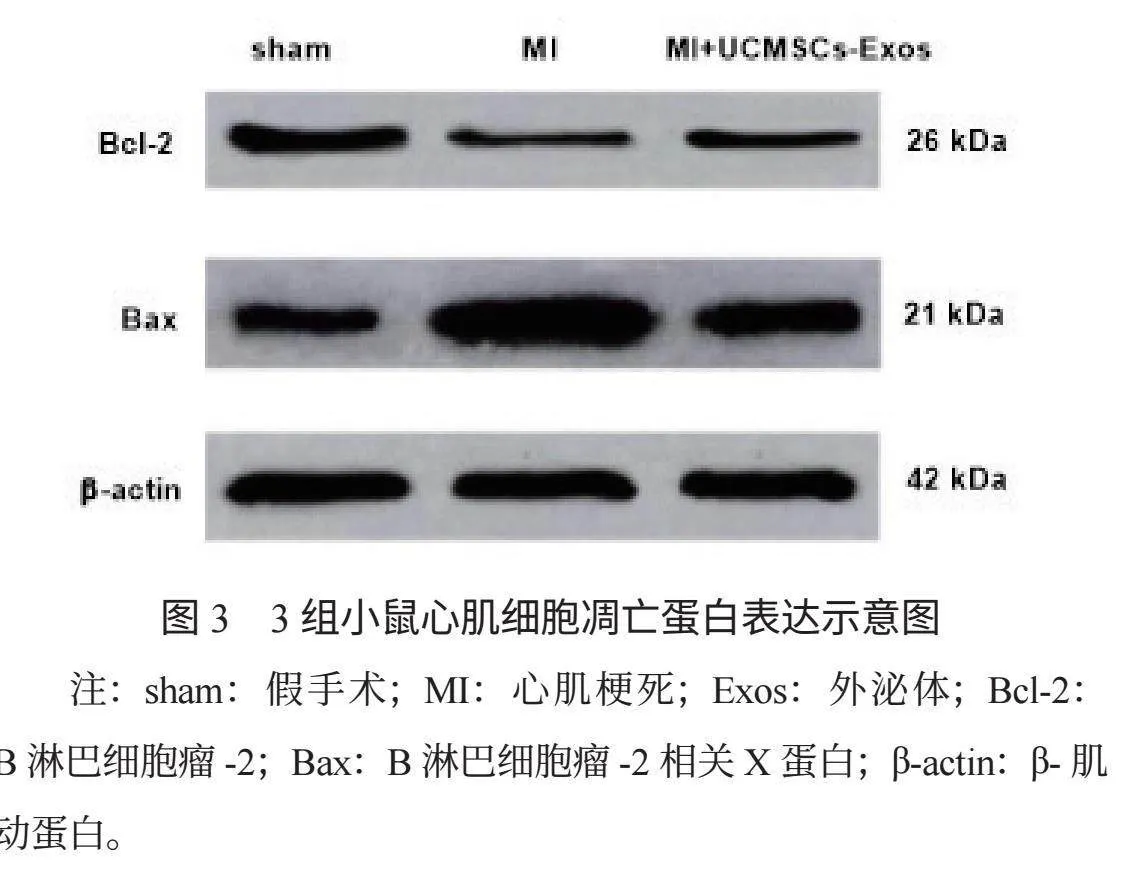
2.4 3组小鼠心肌细胞凋亡蛋白表达水平比较 术后14 d,与sham组比,MI组与MI+UCMSCs-Exos组小鼠心肌细胞中Bcl-2蛋白表达水平下降, MI+UCMSCs-Exos 组高于MI组,Bax蛋白表达水平升高, MI+UCMSCs-Exos 组低于MI组,差异均有统计学意义(均P<0.05),见表2、图3。
3 讨论
MI是临床上常见的心血管疾病,由MI引起的氧化应激和炎症反应会导致心肌细胞坏死,最终导致心室重构、心功能受损,影响患者生命安全,且近年来,其发病率呈升高趋势,加重社会的经济负担[4]。药物治疗、介入手术等传统治疗方法可有效降低MI患者的死亡率,但因心室重构无法逆转,部分患者治疗后仍会引起心力衰竭,因此,仍需探索新的治疗方法以提高MI的治疗效果。
Exos是一类由细胞分泌到胞外的微小囊泡,直径在30~50 nm之间,其内含有多种活性成分,如蛋白质、miRNA,可参与调节细胞增殖、凋亡、自噬、基因表达等多种生物学过程,目前在神经系统疾病、心血管疾病等多种疾病的治疗中受到广泛关注[5]。Exos可由多种不同细胞分泌而来,其来源不同,在MI中发挥心脏保护的作用机制不同,其中充质干细胞来源的Exos可通过调控下游靶基因的表达影响心肌细胞增殖,从而抑制细胞凋亡,减轻心肌损伤[6]。miRNA是Exos中的关键组分,可通过旁分泌作用调节相邻靶细胞,其中miR-152-3p是由前体miR-152产生的成熟miRNA,可抑制缺氧诱导的大鼠心肌细胞凋亡,缩小心肌梗死区域,有助于促进心肌组织修复[7]。CD63、CD81是UCMSCs分泌的Exos的特异性表面标志物,其表达水平较高表明UCMSCs分泌的Exos含量较高。本研究结果显示,UCMSCs-Exos组CD63、CD81蛋白表达量及miR-152-3p的相对表达量均高于UCMSCs组,这提示从UCMSCs中成功分离出Exos,且UCMSCs分泌的Exos中的miR-152-3p呈高表达。
LVEF可反映左心室收缩功能,LVFS可反映左心室收缩过程的运动速率,两者水平下降表明左心室收缩功能减弱;HW/TL是反映心脏肥大程度的重要指标,其比值越大表明心脏肥大越严重。本研究结果显示,术后14 d,与MI组比,MI+UCMSCs-Exos组小鼠血清miR-152-3p、LVEF、LVFS水平均升高,HW/TL水平下降,这提示UCMSCs分泌的Exos可发挥治疗作用,改善MI小鼠心功能。分析其原因为,UCMSCs分泌的Exos能够调节血管内皮细胞的增殖,促进新生血管,有助于抑制心肌纤维化;同时,Exos高表达miR-152-3p,可抑制促凋亡基因的表达,并激活抗凋亡基因,阻断凋亡信号的传导,从而抑制心肌细胞的凋亡,有助于改善心功能[8]。本研究中,术后14 d,与MI组比,MI+UCMSCs-Exos组小鼠心肌细胞受损减轻、细胞排列稍紊乱、心肌纤维增生较少、细胞间隙的变化相对较小、炎症细胞浸润较少,这提示MI小鼠经UCMSCs分泌的Exos治疗后,可减轻炎症反应,抑制心肌纤维化进程,有效减轻心肌细胞损伤。分析其原因为,UCMSCs分泌的Exos与纤维化疾病的发生、发展有关,其在心肌细胞中表达水平上调,可抑制心肌纤维化蛋白的表达,进而延缓心肌纤维化进程,减轻心肌细胞损伤;同时,Exos中可提高超氧化物歧化酶和过氧化氢酶的活性,降低氧化应激反应,从而减轻氧化损伤,并抑制白细胞介素-6、肿瘤坏死因子-α等多种促炎因子的表达,进一步减轻心肌细胞损伤[9]。本研究中,术后14 d,与MI组比,MI+UCMSCs-Exos组小鼠心肌细胞中Bcl-2蛋白表达水平升高,Bax蛋白表达水平下降,这提示UCMSCs分泌的Exos可抑制MI小鼠心肌细胞凋亡。分析其原因可能为,UCMSCs分泌的Exos可调节下游基因的表达,影响血管平滑肌细胞的增殖,还可抑制硫氧还蛋白结合蛋白的活性,调节氧化应激反应,减轻氧化损伤,从而降低促凋亡蛋白Bax的活性,有助于抑制血管内皮细胞的凋亡[10]。
综上,UCMSCs来源的Exos可在MI小鼠中发挥保护作用,可抑制心肌细胞凋亡,并减轻心脏组织病理改变,且Exos高表达miR-152-3p,能够参与调控细胞凋亡过程,有助于改善其心功能。但本研究仍存在一定局限性,未明确Exos对心肌损伤的作用机制,以及与miR-152-3p的关系,后续有待进一步研究。
参考文献
侯永波, 余骏马, 朱海娟. 外泌体在心肌梗死治疗中的研究新进展[J]. 天津医药, 2023, 51(9): 1016-1020.
胡珍艳, 尕永梅, 麦迪乃姆·努尔麦麦提. 间充质干细胞来源的外泌体中miR-143-3p抑制自噬并逆转心肌缺血再灌注损伤的机制研究[J]. 实用临床医药杂志, 2022, 26(17): 46-52.
ZHAO Z, WU C, HE X, et al. miR-152-3p aggravates vascular endothelial cell dysfunction by targeting DEAD-box helicase 6(DDX6) under hypoxia[J]. Bioengineered, 2021, 12(1): 4899-4910.
张蘋, 郭莹, 高亚杰, 等. 低氧预处理人脐带间充质干细胞促进其源性外泌体对心肌梗死后心肌损伤的修复[J]. 中国组织工程研究, 2019, 23(17): 2630-2636.
郝媛媛, 马爱群, 吴冠吉, 等. 间充质干细胞来源外泌体通过microRNA-210发挥对H2O2诱导的心肌损伤的保护作用[J]. 临床和实验医学杂志, 2020, 19(24): 2577-2581.
刘纽,田振军,甄志平.外泌体miRNAs在缺血性心脏保护及其运动干预中作用研究进展[J]. 生理科学进展, 2023, 54(5): 375-382.
梁丽英, 陈晶. 外泌体miRNA治疗心肌梗死的研究进展[J]. 海南医学, 2022, 33(24): 3252-3255.
孙铃, 朱文武, 张健, 等. miR-133a-3p修饰的间充质干细胞外泌体促进心肌梗死后大鼠心肌修复[J]. 中华心血管病杂志, 2024, 52(1): 72-78.
王鑫洋, 陶辉, 丁季飞, 等. miR-152调控糖尿病心肌病心肌成纤维细胞增殖的作用[J]. 中国药理学通报, 2020, 36(1): 92-96.
吴清权, 张勇, 钟书辉, 等. miR-152-3p调控硫氧还蛋白结合蛋白表达对过氧化氢诱导的内皮祖细胞凋亡的影响[J]. 中国动脉硬化杂志, 2022, 30(12): 1033-1039.

