老年居民代谢组分对心律失常影响的病例对照研究
摘 要 目的:了解老年居民代谢组分与心律失常之间的关系,为心律失常的防治提供依据。方法:采用随机数字表法在朱泾社区2023年体检的老年居民中抽取550例心电图提示心律失常的患者为心律失常组,其中男性257例,女性293例,平均年龄(72.45±7.51)岁。按照年龄、性别、现住地匹配550例正常心电图的居民为对照组,收集并整理体检相关资料,如腰围、体重指数(BMI)、收缩压(SBP)、舒张压(DBP)、空腹血糖(FBG)、三酰甘油(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)、血尿酸(UA)、血肌酐(Cr)、血尿素(BUN)等。采用多因素logistic回归分析心律失常的危险因素。结果:对照组与心律失常组的腰围、BMI、SBP、TC、TG、LDL-C、HDL-C、UA、Cr、BUN水平的差异均有统计学意义(均P<0.05),多因素Logistic回归分析显示高血糖、高血压、低HDL-C、高尿酸血症(HUA)的OR值分别为1.679、1.513、2.142、1.591,均P<0.05。结论:高血糖、高血压、低HDL-C、HUA是老年居民心律失常的独立危险因素。
关键词 心律失常;代谢组分;老年人
中图分类号:R541.7 文献标志码:A 文章编号:1006-1533(2024)16-0056-04
引用本文 苏朝霞, 李俊, 谢丽锋, 等. 老年居民代谢组分对心律失常影响的病例对照研究[J]. 上海医药, 2024, 45(16): 56-59.
基金项目:金山区医药卫生科技创新资金项目(2022-WS-52)
Case-control study on the effect of metabolic components on arrhythmia in the elderly residents
SU Zhaoxia, LI Jun, XIE Lifeng, YANG Danhong, LU Ying, LU Yehua, LI Yan
(General Practice Department of Zhujing Community Health Service Center of Jinshan District, Shanghai 201599, China)
ABSTRACT Objective: To investigate the relationship between metabolic components and arrhythmia in the elderly residents, and to provide evidence for the prevention and treatment of arrhythmia. Methods: A total of 550 elderly residents with arrhythmia indicated by electrocardiogram in the physical examination in 2023 in Zhujing Community were selected as the arrhythmia group by random number table method, and among them 257 were males and 293 females, and the average age was(72.45±7.51) years. Hundred and fifty residents with normal electrocardiogram were selected as the control group according to age, gender and current residence. Physical examination related data such as waist circumferenc366109e81528a01abe188028e4c505d8e724b0382fcec1a442a90d3595e3fe28e, body mass index(BMI), systolic blood pressure(SBP), diastolic blood pressure(DBP), fasting blood glucose(FBG), triglyceride(TG), total cholesterol(TC), low density lipoprotein cholesterol(LDL-C), high density lipoprotein cholesterol(HDL-C), blood uric acid(UA), creatinine(Cr), and blood urea nitrogen(BUN) were collected and analyzed. Multivariate logistic regression was used to analyze the risk factors of arrhythmia. Results: There were significant differences in waist circumference, BMI, SBP, TC, TG, LDL-C, HDL-C, UA, Cr and BUN between the control group and the arrhythmia group(P<0.05). Multivariate logistic regression analysis showed that hyperglycemia, hypertension, low HDL-C and OR values of hypertension were 1.679, 1.513, 2.142, and 1.591(P<0.05). Conclusion: hyperglycemia, hypertension, low HDL-C and hyperuricemia are independent risk factors for arrhythmia in the elderly residents.
KEY WORDS cardiac arrhythmia; metabolic component; elderly people
心律失常为心脏活动的起源和(或)传导障碍导致心脏搏动的频率和(或)节律异常一组心血管病,它可单独发病,亦可与其他心血管疾病伴发,可突然发作而致猝死,亦可持续累及心脏而衰竭[1]。相关研究显示心律失常的发生与多种代谢因素相关[2-4],本研究旨在探讨老年人群中代谢组分与心律失常的关系,从而开展针对性的预防和治疗。
1 对象与方法
1.1 对象
采用随机数字表法从上海朱泾社区卫生服务中心2023年60岁以上体检居民中随机抽取550例心电图提示心律失常的患者为心律失常组,并按照年龄、性别、现住地匹配550例正常心电图的居民为对照组。两组的年龄、性别差异无统计学意义(P>0.05)。
1.2 方法
所有体检工作人员经过统一的培训。记录所有调查对象性别、年龄、血压、身高、腰围、体重。测血压时嘱受检者休息5 min,取坐位采用水银血压计测量血压2次取平均值。用电子身高体重仪测量脱鞋受检者的身高和体重,身高精确到0.1 cm,体重精确到0.1 kg。腹围测量时绕腹部平骼峙测量,腹围卷尺平行于地,于受检者正常呼吸末读数,读数时视线与地面平行,皮尺紧贴皮肤。体质指数(body mass index,BMI)=体重(kg)/身高(m)2。所有体检居民空腹采集外周静脉血5 ml,采集前3 d清淡饮食,采集前12 h禁食。采用采用罗氏生化仪(COBAS C702)分别测定空腹血糖(fasting plasma glucose,FBG)、三酰甘油(triglyceride,TG)、总胆固醇(total cholesterol,TC)、低密度脂蛋白胆固醇(low density lipoprotein,LDL-C)、高密度脂蛋白胆固醇(HDL-C)、血尿酸(uric acid,UA)、血肌酐(Creatinine,Cr)、血尿素(blood urea nitrogen,BUN)、谷丙转氨酶(alanine aminotransferase,ALT)、谷草转氨酶(aspartate aminotransferase,AST)等。
1.3 诊断标准及相关定义
1.3.1 心律失常诊断标准
按照明尼苏达编码(Minnesota code,MC),主要心律失常包括:Ⅰ~Ⅲ房室传导阻滞(6-1、6-2、6-3)、完全性不完全性左束支、右束支、室内阻滞(7-1、7-2、7-4)、左前分支阻滞(7-7)、房性早搏(8-1-1)、室性早搏(8-1-2)、室上性早搏(8-1-3)、房颤(8-3)[5]。
1.3.2 异常代谢组分相关定义
采用《中国2型糖尿病防治指南》关于代谢综合征的相关定义[6-7],(1)高血糖:FBG≥6.1 mmol/L和(或)餐后2h血糖(2 h plasma glucose,2 h PG)≥7.8 mmol/ L和或已诊断为 2 型糖尿病并治疗者。(2)腹型肥胖:男性腰围>90 cm,女性腰围>85 cm。(3)高血压:SBP/DBP≥130/85 mmHg和(或)已确诊为高血压并治疗者。(4)高TG血症:空腹TG≥1.70 mmol/L;低HDL-C血症:HDL-C<1.04 mmol/L。(5)高尿酸血症( hyperuricemia, HUA):无论性别血UA>3KAy7sYnVPBe3yTmUq9h5GwQRBwP7WlGTZxZL+AAxYw=420 mmol/L。
1.4 统计学分析

2 结果
2.1 研究对象的一般情况
心律失常组中,Ⅰ~Ⅲ房室传导阻滞71例,占12.9%;完全性不完全性左束支、右束支、室内阻滞182例,占33.1%;左前分支阻滞19例,占3.5%;房性早搏131例,占23.8%;室性早搏45例,占8.2%;室上性早搏22例,占4%;房颤46例,占8.4%;2种及以上心律失常并存34例,占6.1%。
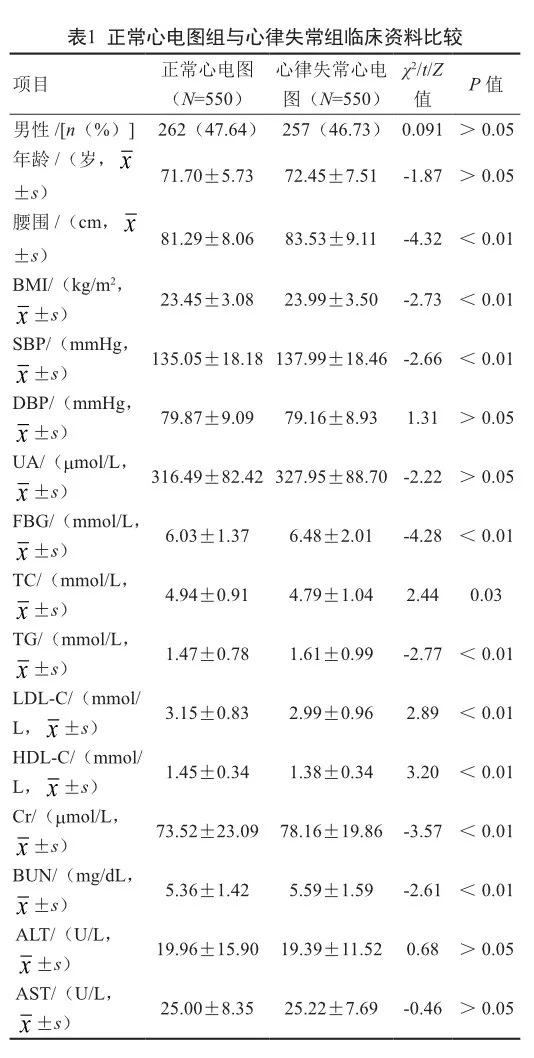
2.2 两组临床资料比较
对照组与心律失常组的腰围、BMI、SBP、UA、TC、TG、LDL-C、HDL-C、Cr、BUN水平的差异均有统计学意义(P<0.05),DBP、ALT、AST水平的差异均无统计学意义(均P>0.05)。见表1。
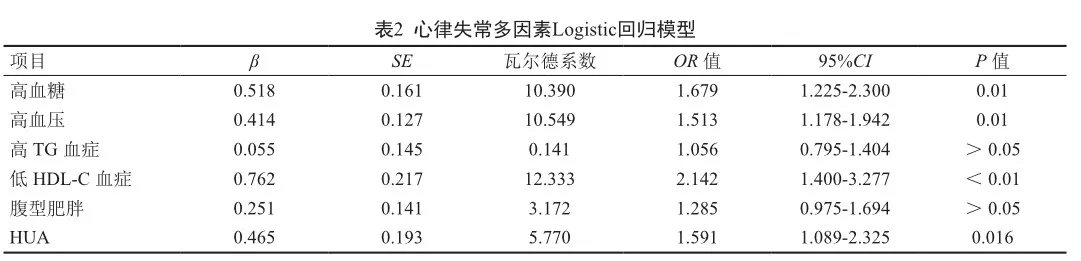
2.3 心律失常危险因素的多因素logistic回归分析
将单因素logistic回归分析分析中有统计学意义的因素进行多因素Logistic回归分析结果显示,高血糖、高血压、低HDL-C、HUA是心律失常的独立危险因素。见表2。
3 讨论
本研究结果显示,高血糖和高血压是心律失常的独立危险因素。一项大规模人群研究结果显示,在急性失代偿性糖尿病患者中有10.1%出现心律失常,并且心律失常组具有更高的死亡率[2]。糖尿病作为心律失常发生的重要危险因素之一的机制复杂,可能与炎症反应、氧化应激、自主神经功能异常、线粒体功能异常、心电重构、血糖水平及血糖波动等有关,而上述几方面也会相互影响,共同导致糖尿病相关心律失常的发生[8-10]。高血压是冠状动脉疾病、心力衰竭、脑出血等的常见危险因素,并且与多种房性和室性心律失常的发生和发展有关[11]。高血压导致室性心律失常的机制复杂,其中左心室肥厚被认为是高血压患者发生室性心律失常的最重要原因[12]。随着病程迁延,长期的高血压水平会导致患者左心室肥厚,进而导致心脏后负荷和心内压增加,促进心肌细胞肥大和心脏成纤维细胞胶原沉积,导致组织结构变形和心肌僵硬度增加,从而诱发室性心律失常[3]。
本研究多因素Logistic回归分析结果显示,低HDL-C是心律失常的独立危险因素,血HDL-C能将周围组织如动脉壁内的胆固醇转运至肝脏进行分解代谢,减少胆固醇在血管壁的沉积,而被视为与LDL-C相反的、能够拮抗动脉粥样硬化的保护性因素。此外,高密度脂蛋白还具有抗低密度脂蛋白氧化、促进损伤的内皮细胞修复、稳定前列环素活性等有益作用[ 1 3 ],因此,LDL-C降低导致胆固醇的转运降低,促使冠状动脉粥样硬化,引起心肌缺血,间接导致心律失常的发生率增高。
我国一项纳入8 937例居民的横断面研究结果显示,HUA老年居民房颤的发生率明显高于UA正常组[4]。多项研究显示血UA升高与心律失常存在关联。Yamada等[14]研究结果显示,HUA是室性心动过速的独立危险因素。Mantovani等[15]发现HUA组心脏传导阻滞的发生率是正常UA组的两倍。本研究结果提示HUA老年居民发生心律失常的风险是UA正常组的1.591倍,关于其机制目前暂不明确,可能与UA升高导致的炎症机制、细胞损伤、肾素血管紧张素系统激活等相关[14,16-17]。
综上所述,高血糖、高血压、低HDL-C、HUA是老年居民心律失常的独立危险因素,应在临床诊疗中引起足够的重视,早发现、早干预,以预防心律失常的发生。但本研究样本量较少,且为单中心研究,研究结果可能存在一定的偏倚。
参考文献
[1] 中华医学会心电生理和起搏分会, 中国医师协会心律学专业委员会. 室性心律失常中国专家共识基层版[J]. 中华心律失常学杂志, 2022, (2): 106-126.
[2] Patel U, Desai R, Munshi R, et al. Burden of arrhythmias and associated in-hospital mortality in acute decompensated diabetes mellitus[J]. Proc(Bayl Univ Med Cent), 2021, 34(5): 545-549.
[3] Romanov A, Minin S, Nikitin N, et al. The relationship between global cardiac and regional left atrial sympathetic innervation and epicardial fat in patients with atrial fibrillation[J]. Ann Nucl Med, 2021, 35(10): 1079-1088.
[4] Chen Y, Xia Y, Han X, et al. Association between serum uric acid and atrial fibrillation: a cross-sectional community-based study in China[J]. BMJ Open, 2017, 7(12): e19037.
[5] 姚建辉, 陈丽, 周京敏. 心电图明尼苏达编码在心血管病研究中的应用进展[J]. 内科理论与实践, 2017, 12(1): 73-76.
[6] 中华医学会糖尿病学分会. 中国2型糖尿病防治指南(2020年版)(上)[J]. 中国实用内科杂志, 2021, 41(8): 668-695.
[7] 中华医学会糖尿病学分会. 中国2型糖尿病防治指南(2017年版)[J]. 中国实用内科杂志, 2018, 38: 292-344.
[8] Liu F, Deng Y, Zhao Y, et al. Time series RNA-seq analysis identifies MAPK10 as a critical gene in diabetes mellitusinduced atrial fibrillation in mice[J]. J Mol Cell Cardiol, 2022, 168: 70-82.
[9] Lu S, Liao Z, Lu X, et al. Hyperglycemia acutely increases cytosolic reactive oxygen species via O-linked GlcN acylation and CaMKII activation in mouse ventricular myocytes[J]. Circ Res, 2020, 126(10): e80-e96.
[10] Rawshani A, McGuire DK, Omerovic E, et al. Cardiac arrhythmias and conduction abnormalities in patients with type 2 diabetes[J]. Sci Rep, 2023, 13(1): 1192.
[11] Nadarajah R, Patel PA, Tayebjee MH. Is hypertensive left ventricular hypertrophy a cause of sustained ventricular arrhythmias in humans?[J]. J Hum Hypertens, 2021, 35(6): 492-498.
[12] 童瑶, 李芳卉, 李文韬, 等. 高血压与心律失常相关性研究的进展[J]. 心血管康复医学杂志, 2022, 31(4): 485-489.
[13] 卜军, 陈章炜, 崔晓通, 等. 中国成人代谢异常与心血管疾病防治[J]. 上海医学, 2020, 43(3): 129-164.
[14] Yamada S, Suzuki H, Kamioka M, et al. Uric acid increases the incidence of ventricular arrhythmia in patients with left ventricular hypertrophy[J]. Fukushima J Med Sci, 2012, 58(2): 101-106.
[15] Mantovani A, Rigolon R, Pichiri I, et al. Relation of 055b051d4b7fab382b7d075a0515ed84ef65111121ab6dc8c116e3a8c7a29deaelevated serum uric acid levels to first-degree heart block and other cardiac conduction defects in hospitalized patients with type 2 diabetes[J]. J Diabetes Complications, 2017, 31(12): 1691-1697.
[16] Duncan DJ, Yang Z, Hopkins PM, et al. TNF-alpha and IL-1beta increase Ca2+ leak from the sarcoplasmic reticulum and susceptibility to arrhythmia in rat ventricular myocytes[J]. Cell Calcium, 2010, 47(4): 378-386.
[17] Yu MA, Sánchez-Lozada LG, Johnson RJ, et al. Oxidative stress with an activation of the renin-angiotensin system in human vascular endothelial cells as a novel mechanism of uric acid-induced endothelial dysfunction[J]. J Hypertens, 2010, 28(6): 1234-1242.

