注射器用于化学实验的改进
张纹 王曹兴 郑雨欣 林文珍


摘要: 利用注射器良好的气密性,采用胶头玻璃滴管作为气体干燥器,对氯气的制备及性质实验、铜与稀硝酸反应和氮氧化合物的性质与转化等实验进行探究与改进。改进实验实现了氯气、一氧化氮和二氧化氮等有毒气体的小剂量制备,能有效避免空气对铜与稀硝酸反应产物的干扰,提高氯气、氮氧化合物性质实验的效果。
关键词: 注射器; 实驗改进; 氮氧化合物; 氯气
文章编号: 1005-6629(2024)05-0075-04
中图分类号: G633.8
文献标识码: B
1 问题的提出
氯气的性质实验、铜与稀硝酸反应、氮氧化合物的性质与转化是中学化学课堂教学重点,是高中化学必修课程的核心内容之一。在《普通高中化学课程标准(2017年版2020年修订)》中“常见的无机物及其应用”主题下,明确给出设计实验及探究活动的学习建议[1]。但由于干燥的氯气、氮氧化合物制备与转化的实验装置比较复杂,废气污染大,限制了实验探究活动的开展。以人教版高中化学必修教材(2019版)中的相关内容为例进行如下分析。
1.1 氯气的性质实验
化学必修1中“氯及其化合物”在第一节介绍氯气的相关性质,在第二节给出制备氯气的具体方法[2]。教师在第1课时教学中讲解氯气性质时,需要提前在实验室制备好氯气,再在课堂教学中演示氯气的性质实验。由于氯气的制取与性质检验两个实验需在不同空间、不同步展开,不仅为教师备课带来诸多不便,也不利于学生对氯气性质和危害性的全面了解。目前大量研究集中在氯气制备装置的微型化改进[3~6],但受限于实验装置需要定制或改装以及干燥氯气的方法欠妥,不利于教师开展课堂演示。
1.2 铜与稀硝酸反应及氮氧化合物性质与转化实验
化学必修2在介绍二氧化氮、一氧化氮的性质实验时,并未指明二氧化氮、一氧化氮的来源[7],加之氮氧化合物的危害,导致教师在讲解这部分内容时通常采用播放视频或直接口述。此外,教材在介绍铜与硝酸反应时,给出的实验装置无法排除氧气对实验现象的干扰,导致铜与稀硝酸反应时直接放出二氧化氮,不利于学生正确理解铜与浓硝酸、铜与稀硝酸两个反应的区别。
基于上述分析,本文选取生活中易得的简易装置和材料,对氯气的制备及性质实验、铜与稀硝酸反应、氮氧化合物性质与转化实验进行改进和探索,以期为教师教学提供参考。
2 实验设计
2.1 氯气的性质实验
2.1.1 实验原理
84消毒液和洁厕灵溶液反应的主要化学方程式为:
2HCl+NaClONaCl+Cl2↑+H2O
由于该反应速率较快,为控制氯气的制备量,防止试管内压力过高,把洁厕灵溶液和84消毒液分别置于试管和注射器(50mL)中,通过控制注射器中84消毒液的注入量来控制氯气的生成量。
2.1.2 实验药品及仪器
NaOH溶液、84消毒液、洁厕灵、无水氯化钙、蒸馏水、pH试纸、50mL注射器(3支)、胶头玻璃滴管、试管、橡胶塞、脱脂棉
2.1.3 实验步骤
步骤一:氯气的制备
如图1A所示,组装好气体发生装置,将大试管固定于铁架台上。拉动注射器1活塞并松手,观察活塞位置是否复原,以此验证装置气密性是否良好。拔掉橡胶塞向试管中加入洁厕灵溶液,塞紧橡胶塞,之后将注射器2拔下(注意不要拔出针头,仅分离针头和注射器,保证针头始终扎穿橡胶塞以便更换注射器),吸取一定量的84消毒液后将注射器重新插入针头(见图1B)。缓慢推动注射器的活塞,将84消毒液注入试管,此时可引导学生观察84消毒液和洁厕灵溶液反应的现象,当观察到黄绿色气体即将充满试管后停止滴入84消毒液,并取下注射器2,在橡胶塞针头上重新接入一支洁净的注射器3(见图1C)用于平衡气压。随后拉动注射器1。随着反应进行可观察到试管中黄绿色的氯气进入注射器1,收集完毕后,取下注射器1并插入橡胶塞将针头密封(见图2A)。为保证实验过程中氯气的充足,可重复上述操作制备氯气。拔下注射器1后,为防止试管中氯气泄漏,可用橡皮泥将针孔封口(见图1D)。
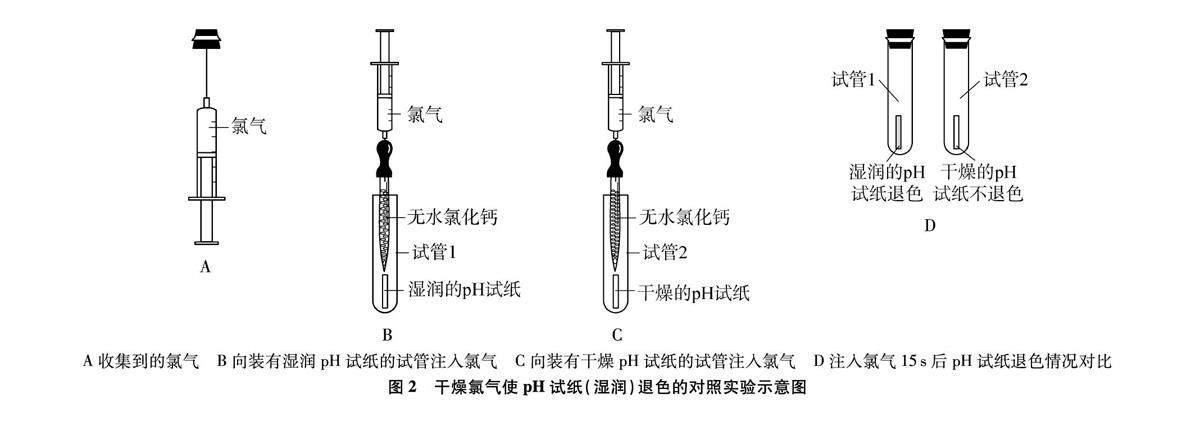
步骤二:干燥氯气使pH试纸(湿润)退色实验
实验前准备好两支干燥试管(试管1放入用蒸馏水润湿的pH试纸,试管2放入干燥的pH试纸)以及装满无水氯化钙的胶头滴管1支(滴管胶头上预先插入针头)。将先前收集满氯气的注射器密封针头拔下,换上插入装满无水氯化钙的胶头滴管的针头(为防止氯气泄漏,连结过程确保注射器竖直),然后将胶头滴管伸入试管1底部,缓慢推动活塞注入适量氯气(见图2B),之后取出胶头滴管迅速用橡胶塞塞紧试管密封。重复操作,将剩余的氯气注入试管2(见图2C)后密封。此时可引导学生观察并记录实验现象,约15秒后试管1中润湿的pH试纸退色,而试管2中干燥的pH试纸
几乎没有变化(见图2D),表明干燥的氯气没有漂白性,湿润的氯气才具有漂白性。进而讲解次氯酸的性质,并过渡到氯水的组成及其性质的讲解。
步骤三:氯水的制备及性质实验
将先前收集满氯气的注射器(见图2A)密封橡胶塞拔下吸入适量蒸馏水后再次密封,振荡注射器使氯气充分溶解,并引导学生观察注射器内气体以及溶液颜色的变化。学生可以观察到黄绿色气体消失,无色蒸馏水变成淡绿色水溶液这一过程,为学生理解新制氯水的组成提供强有力的实验支撑。随后,教师可进一步开展氯水性质实验。
步骤四:尾气处理
实验结束后,对于实验过程中试管、注射器内剩余的氯气,可通过注入或吸入适量氢氧化钠溶液除去。
2.1.4 实验注意事项
步骤一中要确保插入橡胶塞的针头未被堵塞。为保证收集的氯气纯度更高,需要将抽取的第一针管气体(多为试管中残留的空气)舍弃掉。为便于观察氯气的颜色最好使用无色透明的玻璃注射器和胶头滴管。步骤二中为获取充分干燥的氯气,可将装入胶头滴管的无水氯化钙用棉花分段隔开延长气体与氯化钙的接触时间。为了防止空气中水蒸气的干扰,需提前将放置pH试纸的试管进行烘干处理,并向试管中加入适量无水氯化钙用橡胶塞密封放置,實验前再将无水氯化钙取出,快速完成氯气的注入与密封,这样可以保持干燥的pH试纸长时间不退色。
2.2 铜与稀硝酸反应及氮氧化合物性质与转化实验
2.2.1 实验原理
铜与稀硝酸反应,利用注射器良好的密闭性,可以有效排除空气中氧气的干扰,在注射器筒内制备得到较纯净的一氧化氮,并以此开展氮氧化合物性质与转化探究实验。
铜与稀硝酸反应的主要化学方程式为:
3Cu+8HNO3(稀)3Cu(NO3)2+2NO↑+4H2O
一氧化氮与氧气反应为:
2NO+O22NO2
二氧化氮与四氧化二氮转化的可逆反应为:
2NO2N2O4
二氧化氮与水反应为:
3NO2+H2O2HNO3+NO
2.2.2 实验药品及仪器
稀硝酸(体积比1∶3)、铜片、NaOH溶液、50mL注射器(1支)、100mL烧杯(2只)、橡胶塞
2.2.3 实验步骤
步骤一:铜与稀硝酸反应
将注射器活塞拔下,向注射器筒中放入一片铜片后重新塞入活塞并推入底部,随后吸入20mL稀硝酸并排尽注射器中的空气,最后将针头插入橡胶塞密封(见图3A)。为达到最佳密封效果可将注射器倒放在500mL大烧杯内静止放置。本文对稀硝酸浓度进行探索后发现体积比为1∶3的稀硝酸与铜反应速率最快且无二氧化氮生成。反应过程中,可明显观察到铜片周围产生大量气泡,约20分钟后即可观察到注射器中收集到约10mL的无色一氧化氮,溶液颜色由无色变为蓝色(见图3B)。
步骤二:一氧化氮的收集
步骤一反应20分钟后,将反应后的溶液注入氢氧化钠溶液中,随后用橡胶塞密封注射器,这样便收集到了约10mL的一氧化氮(见图3C)。
步骤三:一氧化氮与氧气反应的演示实验
将图3C中的注射器密封橡胶塞拔下,随后拉动活塞吸入约3倍体积空气,并引导学生观察气体颜色的变化。当空气进入注射器瞬间,无色一氧化氮与空气迅速反应转变为红棕色的二氧化氮(见图3D)。吸入空气操作完成后,再次用橡胶塞密封。
步骤四:压强对二氧化氮与四氧化二氮可逆转化的影响演示实验
将图3D中的注射器,水平放置拿在手中,面向学生。随后迅速推动活塞挤压二氧化氮,可观察到气体红棕色瞬间加深,稍后颜色变浅。
步骤五:二氧化氮与水反应的演示实验
将图3D中的注射器橡胶塞拔下,吸入约10mL蒸馏水后用橡胶塞密封并充分振荡,引导学生观察现象。为验证二氧化氮与水反应有一氧化氮生成,将注射器橡胶塞拔下吸入一定量空气,可看到部分无色气体转变为红棕色气体。通过控制空气的吸入量,可将一氧化氮完全转化。
步骤六:尾气及废液处理
对于步骤四、五中注射器内的二氧化氮或硝酸溶液可通过吸入氢氧化钠溶液处理。
2.2.4 实验注意事项
步骤一中,应将铜片裁剪为较注射器筒身直径稍小的片状,方便铜片能平铺在注射器筒身内。由于铜与稀硝酸反应速率较慢,为节约课堂教学等待的时间,教师可在课前准备好反应一段时间后的装置进行展示。
3 总结
3.1 氯气的性质实验
氯气制取的实验装置简易,材料易得,尤其适合少量氯气的制备。此外,首次提出用胶头滴管代替传统干燥管获得干燥氯气,且密闭效果好,非常适合小剂量干燥。
3.2 铜与稀硝酸反应及氮氧化合物性质与转化实验
利用注射器密封隔绝空气,有效避免空气对观察一氧化氮生成的干扰,为教师获取一针筒的一氧化氮或二氧化氮提供可行方案。整个演示过程在密闭的注射器内完成,达到废气零排放,有利于开展学生分组实验。
3.3 注射器用于改进实验的利弊
由于注射器良好的气密性和操作上的便利性,在实验改进方面具有其独特的优势(例如在封闭教室环境中进行有害气体性质实验、反应装置微型化、定量加入反应溶液等)常在实验改进中看到注射器的身影。然而,针头的使用也具有一定的危险性,限制了其在课堂教学中的使用。常见的方法是用注射器配合橡胶管利用止水夹进行密封,这样可以避免针头的使用。但在材料的准备上却带来了困难,一般很难在市面上购买到和注射器配套的橡胶管。本实验改进中采用仅换注射器不换针头的方法是可取的,另外通过提前将针头扎穿或扎入橡胶塞来减少教学过程中裸露针头和扎针操作,可以有效提升注射器使用的工作效率和安全性。
参考文献:
[1]中华人民共和国教育部制定. 普通高中化学课程标准(2017年版2020年修订)[S]. 北京: 人民教育出版社, 2020.
[2]王晶主编. 普通高中教科书·化学必修第一册(第一版)[M]. 北京: 人民教育出版社, 2019: 41~44.
[3]李兴, 齐俊林. 次氯酸漂白作用实验的新设计[J]. 化学教学, 2018, (5): 62~80.
[4]袁君亚. 次氯酸漂白作用实验的新设计[J]. 化学教学, 2020, (5): 65~72.
[5]陈佳音, 冯高峰, 司二伟, 阎润鸿. 固液加热制取气体及其性质实验装置的改进[J]. 化学教学, 2023, (9): 74~76.
[6]马娟娟, 吴有萍, 余新红. 基于绿色化学理念的微型实验设计——以氯水制备为例[J]. 中国现代教育装备, 2022, (10): 46~47.
[7]王晶主编. 普通高中教科书·化学必修第二册(第一版)[M]. 北京: 人民教育出版社, 2019: 11~15.

