微创玻璃体切割术治疗增生性糖尿病视网膜病变的效果及术后玻璃体再出血的影响因素分析
朱文魁,徐培珊
(平煤神马集团总医院 眼科,河南 平顶山 467000)
增生性糖尿病视网膜病变(proliferative diabetic retinopathy,PDR)是糖尿病(diabetes,DM)最常见的微血管并发症,以玻璃体出血、新生血管膜生成、视网膜脱离为主要临床表现[1]。近几年随着经济的飞速发展以及不良生活、饮食习惯的流行,我国DM患病率逐年攀升,由DM引发的视网膜并发症发生率亦随之增长。据统计,在全球DM患者中,罹患PDR的患者为22.27%,其中威胁视力的糖尿病视网膜病变(diabetic retinopathy,DR)占6.17%[2]。深圳地区DM患者PDR患病率为18.58%,DR患病率为2.43%,与全球PDR、DR患病率趋势[3]一致。PDR如若不及时治疗可使患者视力下降,引起继发性视网膜脱落、广泛玻璃体积血等,损害视网膜血管内皮细胞功能,最终导致患者视力丧失,甚至失明[4]。玻璃体切割术(pars plana vit-rectomy,PPV)是治疗PDR的重要手段,能有效分离玻璃体视网膜之间的粘连、解除视网膜牵拉,提高患者视力,在临床应用上具有较大优势[5]。但PDR患者PPV术后玻璃体再出血(postoperative vitreous hemorrhage,PVH)十分常见,很大程度影响了其在PDR治疗中的应用。随着微创外科学的发展,PPV技术不断完善、成熟,微创玻璃体切割术(minimally invasive vitrectomy,MIV)逐渐成为玻璃体视网膜手术的趋势。目前临床已有较多MIV治疗PDR的报道,但结论各异,且有关PDR患者MIV术后PVH发生的危险因素并不明确。基于此,本研究选取286例PDR患者,观察MIV治疗PDR的临床效果,并分析其MIV后PVH发生的危险因素,以期为临床提供参考。
1 资料与方法
1.1 一般资料
纳入2019年1月至2022年6月平煤神马集团总医院诊治的286例PDR患者。纳入标准:符合DM诊断[6];经直间接检眼镜、眼底照相、裂隙灯附加前置镜等检查,符合PDR诊断要求[7];年龄18~<80岁;接受MIV治疗;术后配合随访;签署知情同意书。排除标准:DM合并妊娠;非DM本身导致的视网膜病变;双眼病变;既往眼内手术、外伤、皮质类固醇激使用史;角膜炎症、葡萄膜炎、青光眼等;病例资料不完整。286例患者中男172例,女114例;年龄23~80(55.49±5.18)岁;DM病程3个月~15 a,平均(8.31±2.10)a;眼别左眼149例,右眼137例;PDR分期Ⅳ期98例,Ⅴ期94例,Ⅵ期94例;合并高血压64例,心脑血管疾病(冠心病、脑梗死)27例;伴牵拉性视网膜脱离者36例36眼,伴黄斑水肿者6例6眼。本研究经医院医学伦理委员会审批。
1.2 方法
所有患者均接受MIV治疗,术前使用左氧氟沙星滴眼液、普拉洛芬滴眼液,每日4次。充分散瞳后,使用盐酸奥布卡因(沈阳药大药业有限责任公司,国药准字H21023206)表面麻醉,20 g·L-1利多卡因(广州市香雪制药股份有限公司,国药准字H20031189)与7.5 g·L-1布比卡因(上海禾丰制药有限公司,国药准字H31021919)等量混合球后阻滞,开睑,冲洗结膜囊。使用Alcon Constellation微创玻切机,23G微创刀(带套管)按照经睫状体平坦部三通道进行穿刺,切除前后混沌玻璃体、玻璃体后皮质,清除玻璃体内积血,显微镜下查找并充分剥离眼底增殖膜,电凝止血。若有视网膜裂孔,则补充全视网膜激光光凝,酌情选择玻璃体内填充物。利用膜分割技术去除机化膜,难以去除的部分可在解除牵拉张力的基础上分割孤立。术毕,拔出套管,用可吸收缝线缝合切口。所有手术均由同一组经验丰富的医生完成。术后嘱患者保持低头体位休息,所有患者术后常规行局部消炎抗感染治疗。
1.3 观察指标
(1)围手术期相关指标:手术时间、术中出血例数、电凝止血次数、玻璃体填充物(消毒空气或硅油)、是否联合白内障超声乳化摘出、术后玻璃体腔内是否注射抗血管内皮生长因子(vascular endothelial growth factor,VEGF)药物。(2)视力:于术前、术后3个月使用KR-8900型电脑角膜验光仪测定最佳校正视力(best corrected visual acuity,BCVA)。(3)眼压:使用佳能TX-F索非接触式眼压计测定术前、术后3个月的眼压,由同一人员连续测量3次,取平均值。(4)并发症发生率:主要包括PVH、切口区玻璃体嵌顿、增殖物内生、前房积血、并发性白内障。
1.4 统计学处理
2 结果
2.1 治疗效果
286例患者均顺利完成手术,手术时间、电凝止血次数分别为(66.36±12.74)min、(1.26±0.21)次,术中无出血情况,玻璃体内填充消毒空气、硅油、联合白内障超声乳化摘出及术毕玻璃体腔内注射抗VEGF药物占比分别为35.31%、64.69%、65.73%、31.12%;随访时间为(6.13±1.28)个月,患者术前、术后3个月的BCVA[(1.36±0.23) 、(0.90±0.15)]、眼压[(17.73±3.35)、(15.82±2.56)mmHg]比较,差异有统计学意义(t=40.944、10.894,P<0.05);患者术后并发症总发生率为13.99%(40/286),其中PVH 33例,前房积血2例,并发性白内障8例。
2.2 影响PDR患者MIV术后PVH发生的单因素分析
286例患者按术后是否发生PVH分为PVH组和非PVH组。与非PVH组相比,PVH组年龄、合并高血压、合并心脑血管疾病占比更高,DM病程更长(P<0.05)。与非PVH组相比,PVH组玻璃体内填充消毒空气、联合白内障超声乳化摘出占比更高,术毕玻璃体腔内注射抗VEGF药物占比更低(P<0.05)。见表1。

表1 影响PDR患者MIV术后PVH发生的临床资料单因素分析
2.3 影响PDR患者MIV术后PVH发生的多因素分析
以MIV术后是否发生PVH为因变量(否=0,是=1),以P<0.05的因素作为自变量并赋值(合并高血压=1,否=0;合并心脑血管疾病=1,否=0;玻璃体内填充消毒空气=1,否=0;联合白内障超声乳化摘出=1,否=0;术毕玻璃体腔内注射抗VEGF药物=0,否=1;年龄、DM病程原值输入)。多因素logistic回归分析显示,DM病程、合并高血压及玻璃体内填充消毒空气是PDR患者MIV术后PVH发生的危险因素,年龄、术毕玻璃体腔内注射抗VEGF药物是其保护因素(P<0.05)。见表2。
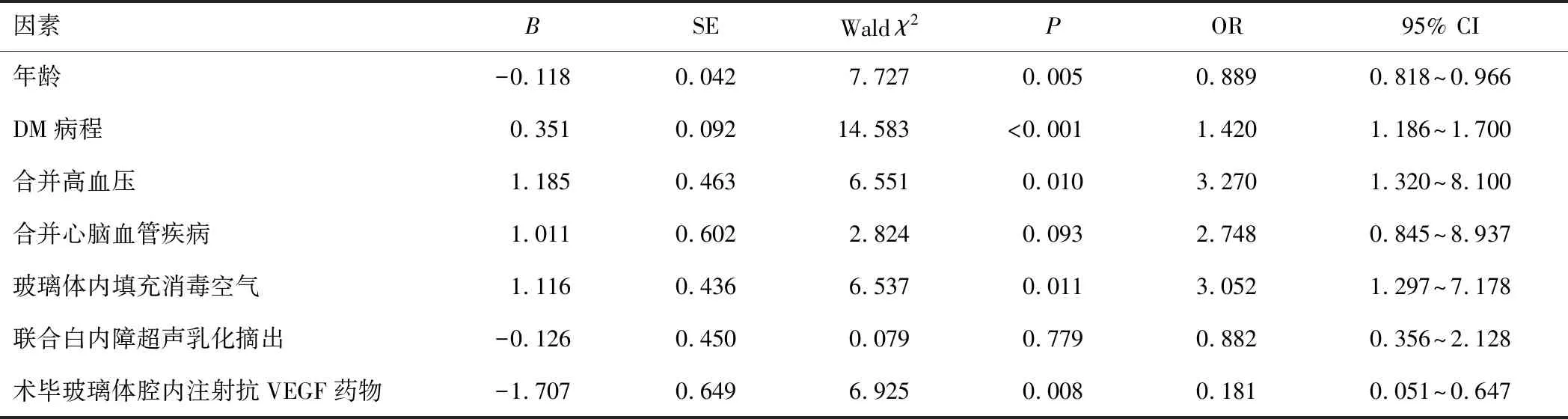
表2 影响PDR患者MIV术后PVH发生的多因素logistic回归分析
3 讨论
近几年,PDR作为发病率逐年攀升的DM常见并发症,引起了临床医生的广泛关注。关于PDR的发病机制,目前普遍认为是持续高血糖引发代谢紊乱,导致多种炎症相关因子及与其相关细胞因子相互作用[8-9]。PDR患者并发症较多,治疗上除了降糖、降压、抗炎等,还需行玻璃体视网膜手术,从而抑制病情进一步发展。
传统PPV术因其巩膜切口较大,术后并发症较多,且对手术要求较高,操作相对复杂,不同程度影响了手术效果,不利于患者术后恢复。现如今玻璃体视网膜手术已步入微创时代,MIV的出现不仅使手术切口小,而且术后疼痛轻、并发症少、恢复快,临床应用日益广泛[10]。本研究中,286例患者手术时间为(66.36±12.74)min,电凝止血次数为(1.26±0.21)次,术中无出血发生,患者术后3个月的BCVA、眼压均优于术前,术后总并发症发生率为13.99%,与王博等[11]的研究结果基本一致。这说明MIV不仅能提高患者视力,降低眼压,还能避免术中出血情况,安全有效,可作为PDR的理想治疗手段。考虑其原因可能是,本研究中应用23G经结膜免缝合系统,切割效率高,手术切口仅0.6 mm,术中无需切开结膜、缝合巩膜、结膜切口和止血操作,使操作步骤简化;此外,MIV术中眼表损伤程度小,可减轻因手术操作造成的炎症反应,从而促进患者术后早期视力的恢复,降低眼压,同时减少切口区玻璃体嵌顿、增殖物内生等并发症发生。但本研究未设置对照组,这亦是本研究的不足之处,建议今后开展前瞻性随机对照研究,根据手术方式或根据患者围手术期是否使用抗VEGF药物或根据PDR分期分组,以期得到更加科学、有价值的研究结果,进一步论证MIV的疗效。
PVH是影响患者术后视力改善的重要因素之一,纤维血管膜残端出血、视网膜切开及视网膜裂孔出血、术后剧烈呕吐或活动等均可能引起PVH,若处理不当可再次引起牵拉性视网膜脱离,导致手术失败[12]。本研究中PVH发生率为11.54%,与范小娥等[13]研究接近。本研究结果显示,DM病程、合并高血压及玻璃体内填充消毒空气是PDR患者MIV术后PVH发生的危险因素,年龄、术毕玻璃体腔内注射抗VEGF药物是其保护因素。本研究中,年龄每增长1岁,PDR患者MIV术后发生PVH的风险降低0.889倍,推测原因可能是,相比高龄患者,年轻PDR患者玻璃体与视网膜的粘连更为紧密,术中玻璃体后的脱离难度更大,易使得部分玻璃体后界膜及皮质残留并在纤维血管膜处黏附,导致新生血管随着玻璃体的收缩、牵拉而破裂,引起PVH[14]。此外,PDR患者年龄越小,机体对手术创伤的应激反应越大,形成活动性新生血管的风险越高,术后PVH的发生概率更高。目前,DM病程被一致认为是PDR的独立危险因素,病程越长,患者病情越严重,术后并发症发生的风险越高[15]。本研究也得出类似结论。研究发现,合并高血压对PVH发生有促进作用[16]。合并高血压影响MIV术后PVH发生的可能机制可从以下两个方面解释:高血压可损伤血管内皮,使血小板易于附着,形成血栓,造成组织缺氧、静脉扩张,导致新生血管破裂,引起PVH;PDR患者本身伴血管内皮功能、大血管弹性减退情况,合并高血压的患者在手术刺激下收缩压进一步升高,损伤血管内膜,使血管通透性增高,更易发生新生血管破裂[17]。关于玻璃体内填充物与PVH之间的联系目前尚存争议。本研究中,玻璃体内填充消毒空气者,较非玻璃体内填充消毒空气者MIV术后发生PVH的风险增加3.052倍,究其原因可能与消毒空气在眼内留存时间较短、对维持眼压、降低视网膜灌注压的作用较弱有关。术毕玻璃体腔内注射抗VEGF药物是预防赎回眼底病变的主要手段之一[18]。本研究发现,术毕玻璃体腔内注射抗VEGF药物者较术毕玻璃体腔内未注射抗VEGF药物者MIV术后发生PVH的风险降低0.181倍。考虑其原因可能是,术毕玻璃体腔内注射抗VEGF药物可促使新生血管收缩和残余积血的吸收,从而有效防止PVH发生。
4 结论
MIV不仅能提升患者视力,降低眼压,而且术后并发症少,可作为PDR患者治疗的优先选择方案。年龄、DM病程、合并高血压、玻璃体内填充消毒空气和术毕玻璃体腔内注射抗VEGF药物均为PDR患者MIV术后PVH发生的影响因素,临床应重点关注。但本研究属单中心研究,样本缺乏代表性,所得结论可能与临床实际存在一定偏差,建议今后增加样本量、扩大病例纳入范围进一步论证。

