非HIV感染免疫功能抑制状态者的预防性抗PCP治疗的研究进展
杜婷婷 彭丽
人类肺孢子菌肺炎(pneumocystis pneumonia, PCP)是一种由耶氏肺孢子菌(pneumocystis jirovecii, PJ)引起的机会性感染性疾病,多发生于免疫功能抑制状态者[1],其病原菌在自然界中普遍存在,通过呼吸道传播,也可在免疫功能正常的成年人肺部形成定植[2,3]。自20世纪80年代后,PCP作为获得性免疫缺陷综合征(AIDS)患者最常见的并发症在临床上引起了广泛关注和深入研究,PCP预防已成为HIV感染者的标准疗法之一,随之HIV感染人群中PCP的发病率出现大幅下降[4],但非HIV感染的免疫功能抑制状态者的PCP发病率却呈现上升趋势,这种现象可能与目前全球尚缺乏非HIV感染免疫功能抑制状态者预防抗PCP的规范指南存在一定相关性[5]。本文就PCP在非HIV感染免疫功能抑制状态者的发生发展和预防时机、方法、效果,以及不良反应等方面的研究进展进行综述。
一、PCP在非HIV感染者的发生
肺孢子菌肺炎几乎可发生于所有动物物种,但肺孢子菌具有不同的宿主特异性,比如:感染人的是耶氏肺孢子菌,感染大鼠的是卡氏肺孢子菌(pneumocystis carinii, PC)[1,6]。耶氏肺孢子菌在人类生存的环境中广泛存在,有学者采用血清学检测发现几乎100%的儿童在出生后两年内会感染PJ[7],健康的PJ携带者被认为是PJ经呼吸道传播的主要环节[8],而经胎盘途径是另一种人传人模式[9]。因此,PCP是发生于潜伏感染的重新激活还是获得新的感染目前暂无明确定论[10]。PCP通常发生在免疫抑制人群中,二战期间主要在欧洲孤儿院和急性淋巴细胞白血病儿童中发现[11],后来常发生于AIDS患者。随着AIDS患者广泛使用预防PCP药物及高效抗逆转录病毒治疗,PCP 在HIV感染人群中的发病率较前明显下降[4,12],而在器官移植、肿瘤、放化疗、长期使用大剂量激素或免疫抑制剂等无HIV感染的免疫功能抑制状态者的PCP发病率及死亡率却较前升高[5],并且已成为这类患者最常见的肺炎类型,有研究发现糖皮质激素的使用和细胞介导免疫的缺陷、化疗方案、基础疾病等均与PCP发生有关[13,14]。
二、非HIV感染PCP诊治面临的难题
PCP的临床表现与患者是否感染HIV无关,但有研究发现非HIV感染免疫功能抑制状态者与HIV感染者相比,疾病发展更快(病程更短),病情更重(呼吸衰竭发生率更高)[15],尽管孢子菌检测的载量低于非HIV感染者,但胸腔积液发生率、缺氧率、呼吸衰竭率和死亡率更高,并且影像学出现肺炎和接受治疗之间的时间窗更长,提示非HIV感染者发生PCP时更容易被延迟诊断[16]。诊断延误在一定程度上与目前尚无全球公认的肺孢子菌体外培养方法和技术,PCP的诊断仍依赖于临床症状、影像学检查及对下呼吸道标本进行特殊染色寻找病原菌等相关。PCP的影像学特点为双肺磨玻璃改变,在HIV感染者与未感染者之间没有显著区别[17]。诊断PCP的标准样本是支气管肺泡灌洗液,辅助排痰、口咽清洗液等也被用作诊断PCP的样本,样本的质量和类型以及医技人员对标本的检查能力对结果均有较大影响。未感染HIV的患者和曾经接受过PCP化学预防的患者发生PCP时PJ载菌量通常较低,显微镜诊断常出现假阴性。近年出现了以肺部标本为基础的聚合酶链反应、环介导等温扩增法、宏基因组下一代测序等方法,但这些技术的成本、敏感度、特异度、对采样技术的要求和对PJ定值的判断尚未完全统一,故这些技术还未被大规模推广使用[18,19]。
在AIDS患者中,PCP的死亡率为10%~30%,在非AIDS患者中,死亡率为40%~70%[20]。早期诊断和治疗对于非HIV感染PCP患者的生存至关重要,治疗的开始不能因诊断程序而推迟[16,21]。有研究报道非HIV感染PCP患者的预后较HIV阳性PCP患者预后差,淋巴细胞减少、治疗期间辅助使用类固醇、并发气胸、诊治延误与预后不良相关[16]。在此类人群中开展早诊早治,选择合适的人群进行恰当的预防性抗PCP治疗是降低非HIV感染PCP发病率、死亡率的关键措施。
三、PCP预防治疗的相关因素
1. 预防对象选择
PCP预防已成为标准HIV疗法的一部分,而非HIV感染的PCP患者由于其原发疾病较多,同一种疾病不同时期用药不同,使得除了AIDS外还需要对哪些疾病行PCP预防目前全球尚无明确定论。历史上,医疗中心移植受者PCP发生率≥3%~5%被认为是该中心所有移植患者预防抗PCP治疗的阈值[22]。10年前Green等人认为,为避免更多人群暴露于药物的不良反应,非HIV感染的免疫功能抑制状态者在整个免疫缺陷期间发生PCP的风险≥3.5%时,才有必要行PCP预防[23]。Dunbar等在一项多中心回顾性研究中发现,在HIV检测和治疗不受限制的地区,PCP主要发生在非HIV感染的免疫功能低下人群中,而这类人群中80%以上的患者从未接受过预防性治疗。为减少PCP发病率,迫切需要提高免疫功能低下患者和医务人员对抗菌药物预防指南的认识[24]。
目前,一些专业学术组织已制定和发布了一些相关经验及治疗建议。美国胸科学会在成人肺部和重症监护者的抗真菌治疗声明中建议,使用糖皮质激素超过20mg/d持续大于1个月者应预防性抗PCP治疗[25]。美国血液和骨髓移植协会发布的指南中,异体移植的受者和免疫抑制显著的自体移植受者均需行PCP预防[26],在澳大利亚皇家内科医学院编写的血液和实体恶性肿瘤的指南中,建议急性淋巴细胞白血病、异基因造血干细胞移植、接受长期大剂量皮质类固醇治疗(16~25mg泼尼松龙或每天≥4mg地塞米松,持续≥4周)、使用T细胞消耗药物、接受自体骨髓移植、接受某些高强度化疗方案的血液系统疾病患者,接受含有每天 16~25 mg 泼尼松龙或≥4 mg 地塞米松化疗方案持续≥4 周的实体瘤患者,以及因脑恶性肿瘤接受强化治疗的患者,应考虑 PCP 预防[27]。
2. 预防时机
针对存在不同基础疾病的情况,不同学术组织建议的预防时机有所不同,具体的预防建议(见表1)[28]。美国移植学会建议在器官移植后6~12 月进行一般预防[22]。在抗排斥治疗、剂量≥20 mg/天泼尼松龙或同等当量的皮质类固醇治疗超过 4 周或长期中性粒细胞减少症的情况下,应延长预防措施。建议对肺或小肠移植、慢性巨细胞病毒感染以及有 PCP发病史的患者进行终身预防[29]。一些专家还建议心脏和肝脏移植患者也应进行终身预防PCP[22,30]。欧洲肾脏协会建议在肾移植后第3~4 月每天使用 TMP-SMX 进行预防[31]。肾脏疾病改善全球指南建议在肾移植术后3~6月或6~12月期间预防性治疗[29]。

表1 非HIV感染者的肺孢子菌肺炎预防的适应证
然而,Goto等认为上述指南仅建议移植后1年以内的个体进行预防,没有对如何预防PCP爆发给出相应的建议,他们主张对肾脏移植患者进行终身预防以防止PCP爆发[32]。目前的指南建议在由于免疫抑制增加而导致PCP风险较高的时期进行额外的预防,这些风险因素包括:皮质类固醇的使用(>20mg泼尼松当量/天,持续2周或更长时间)、巨细胞病毒感染、需要额外免疫抑制治疗的排斥反应发作和淋巴细胞减少症(通常<500个/μL)[33,34]。
有关结缔组织疾病采用PCP预防的策略和建议,除了使用类固醇(>20 mg/天泼尼松当量×4周)需要预防PCP以外,对于哪些疾病或治疗需要 PCP 预防几乎没有取得一致意见,肉芽肿性多血管炎 (GPA) 诱导治疗阶段是广泛认可的唯一条件,对于系统性红斑狼疮、多发性肌炎/皮肌炎、结节性多动脉炎及ANCA相关性血管炎,则需要根据患者用药及自身情况进行预防,而类风湿性关节炎、巨细胞动脉炎和硬皮病,暂无研究支持需要PCP预防[35]。目前国内外尚缺乏关于结缔组织病患者或先天性免疫缺陷患者的PCP预防指南。
对于其他一些疾病的PCP预防存在不同的指导意见,对于预防的最佳持续时间没有普遍共识。对于原发性慢性呼吸系统疾病(如哮喘和慢性阻塞性肺疾病)及可能需要长期高剂量皮质类固醇治疗的隐源性机化性肺炎和间质性肺病(定义为使用泼尼松中位日剂量30 mg或等效药物,持续12周或更长时间),无明确证据证明需要对此类患者进行PCP预防,应考虑相关的合并症,如营养不良[23]。
3. 预防方法
目前,除非存在磺胺使用的明确禁忌证,复方磺胺甲噁唑(TMP-SMX)已被广泛推荐治疗 HIV 相关肺孢子菌机会性感染的一线疗法[36]。针对HIV感染者的PCP预防推荐的剂量是每天服用一粒双倍强度 (DS) 片剂(160 mg TMP 和 800 mg SMX)[37]。在Yang等人的一项前瞻性队列研究中,每日单倍强度的TMP-SMX方案比每周三次双倍剂量的TMP-SMX方案预防肾移植后6个月的PCP更有效[38]。Pereda等进行了系统综述,发现全身性自身免疫性风湿病(SARD)在接受糖皮质激素>20 mg/天期间每周三次使用单强度片剂或每天使用半强度(HS)片剂(40mgTMP和200mgSMX)均可有效预防PCP,但后者不良反应率更低,耐受性更好[39]。
在Utsunomiya等人的开放性随机对照试验中,接受强的松龙 0.6 mg/kg/天的成年风湿病患者,每天接受半强度剂量TMP-SMX的预防效果与单强度片剂的效果接近,但半剂量有更少的副作用和更低的停药率[40]。Yamashita回顾分析了非HIV感染免疫功能抑制状态需要行PCP预防但由于肾功能异常需行血液透析患者的资料,结果显示使用标准剂量(≥6片/周)与低剂量(< 6片/周)两种方案的预防效果无明显差异,但低剂量组因不良反应导致的停药率更低[41]。上述研究探讨了在某种或某些疾病中不同剂量TMP-SMX的预防效果,至于每种疾病的预防启动时间、最佳剂量和疗程等问题,还需更多高质量的随机对照试验研究对其进行探讨。
4. TMP-SMX预防PCP的不良反应与处理
使用TMP-SMX预防PCP时,药物不良反应相对常见,但程度总体较轻。常见的不良反应包括:胃肠道不适(恶心、呕吐)、皮疹、发热、头痛、贫血、白细胞减少、血小板减少、肝功能异常、高钾血症、血清肌酐升高、间质性肾炎。少见不良反应包括肝炎、无菌性脑膜炎、胰腺炎、低血糖和低钠血症。罕见不良反应可引起严重和危及生命的反应,如速发过敏反应、Stevens-Johnson综合征、中毒性表皮坏死松解症和骨髓抑制。由于TMP-SMX存在潜在的骨髓抑制,欧洲白血病感染协会建议在骨髓活体移植前期应避免使用TMP-SMX[28]。葡萄糖-6-磷酸脱氢酶(G6PD)缺乏症患者使用TMP-SMX可能导致溶血性贫血。Leoung建议对非危及生命的不良反应可使用抗组胺药或止吐药进行症状管理,或者在更换治疗方案前尝试逐步脱敏[42]。在Otani等人的回顾性研究中,当单强度剂量和半强度剂量对于PCP预防效果无差别时,可通过降低TMP-SMX的剂量来提高耐受性[43]。
当确实无法耐受TMP-SMX时,可尝试使用二线预防方案。二线药物包括:(1)氨苯砜:此药与磺胺甲噁唑类似,有磺胺类药物严重不良反应的患者应避免使用。(2)阿托伐醌:是一种广谱抗原虫药物,可安全地用于G6PD缺乏症患者。(3)喷他脒:作用机制尚不清楚,主要通过雾化形式预防。(4)克林霉素和伯氨喹:作用机制尚不清楚,目前较少用于预防。上述药物的常用方案及剂量(见表2)[27,44]。需要说明的是,目前所有二线药物的预防效果均低于TMP-SMX,同时也存在一定的不良反应,具体使用应根据患者自身情况和药物的可及性决定[44]。
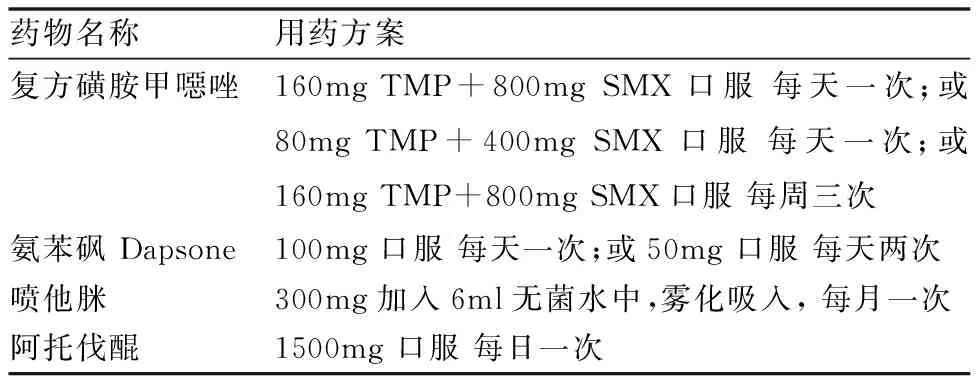
表2 目前常用于PCP预防的药物
5. 预防效果
在Park等人的一项关于复方磺胺甲噁唑对长期大剂量皮质醇激素暴露的风湿病患者的PCP预防效果的回顾性研究中,TMP-SMX的预防效果为93%[45],在Katsuyama等人开展的一项接受了生物制剂治疗的类风湿关节炎患者的回顾性研究中,预防组没有一例发生 PCP, 保护率为100%,非预防组中1.6%患者发生了PCP[46]。据报道,造血干细胞移植(HSCT)患者不进行PCP预防,PCP的发生率为5%~16%[47];若进行预防,PCP发生率则低于1%,其感染通常发生在移植过程后期或预防停止后,或在因并发症(如移植物抗宿主病)而增加的免疫抑制期间[48]。在Stern等人的Meta分析中,血液恶性肿瘤、干细胞移植和器官移植患者使用TMP-SMX预防可将发生PCP的风险降低85%[30]。在Lee等人的回顾性研究中,使用R-CHOP方案治疗的弥漫大B细胞淋巴瘤患者采用TMP-SMX预防后均没有发生PCP,而未预防组PCP发病率为8.1%[49]。在实体器官移植受体者接受PCP预防可将PCP发生率从5%~15%降至1%左右。在现代预防性时代,实体器官移植6~12个月后常规预防性治疗通常会中止,PCP往往是后期并发症,也常发生在器官排斥和CMV共感染期间[33]。因为预防性治疗常会出现药物的不良反应,如何权衡效益和不良反应,还需要更多的研究及根据患者实际情况做出调整。
四、总结与展望
肺孢子菌肺炎是一种免疫力低下人群常见的机会性感染。由于疾病、糖皮质激素使用、化疗方案更新等多种原因,非HIV感染免疫功能抑制状态者的PCP患病率较前升高,而非HIV感染的PCP危险因素和预防治疗还未形成统一的共识。由于免疫功能抑制状态者的基础疾病较多,针对不同疾病有不同的PCP预防时机、方案和效果。复方磺胺甲噁唑被多个学术团体推荐为一线预防药物,具有很好的预防效果,但也存在皮疹、白细胞减少等不良反应,多个研究均提示不良反应与药物剂量相关。是否使用氨苯砜、阿托伐醌等二线药物进行预防,需考虑保护效率、药物的可及性以及患者自身疾病状态等因素。因此,在全球范围内还需开展高质量的临床研究,对不同疾病导致的免疫功能抑制状态者预防PCP的用药对象、时机以及药物种类、剂量和疗程等重要因素进行探讨。

