左心瓣膜术后单纯性三尖瓣关闭不全的微创治疗方案及围术期结果
申 宏, 何潇一,2, 姜胜利,2
三尖瓣关闭不全是一种常见的心脏瓣膜病变,其患病率虽不及二尖瓣和主动脉瓣病变,但随着年龄的增长,其患病率也逐渐增加。据2019年美国社区的流行病学调查结果显示,中/重度三尖瓣关闭不全的患病率为0.55%。75岁以上年龄人群中三尖瓣患病率约占所有左侧瓣膜疾病的1/4,与主动脉瓣狭窄的患病率相似[1]。三尖瓣关闭不全主要表现为右心衰竭的症状和体征,如外周水肿、颈静脉压升高、运动耐力下降等[2],严重者逐渐发展为晚期心力衰竭并增加手术死亡率和降低远期生存率[3]。另外,三尖瓣关闭不全的患者常常合并房颤,而房颤可以进一步加重心脏扩大和瓣环扩张,从而加重三尖瓣反流的严重程度[4]。而左心瓣膜病变是三尖瓣关闭不全的独立影响因素[5],其发病率约为27%,且预后较差[6]。所以很多接受了左心瓣膜手术的患者仍需接受二次手术来处理三尖瓣病变。2021年欧洲心脏病学会/欧洲心胸外科学会瓣膜心脏病管理指南提出,伴有右心衰竭的三尖瓣关闭不全患者,利尿剂可以显著改善右心功能,同时控制心率的药物可能有助于减少三尖瓣反流并减缓合并房颤患者的瓣环扩张,但是药物治疗不应作为延缓手术或经导管治疗的手段[7]。因此,外科手术仍然是治疗三尖瓣关闭不全的主要方法。目前,手术方式主要包括成形和人工瓣膜置换,应用最多的成形方式是DeVega成形和人工瓣环成形。另外国内有研究报道采用新鲜自体心包条制成可调节式的心包软环进行三尖瓣成形,早中期临床效果良好[8],但再次心脏手术的风险明显提高[5,9-10]。尤其是对于需再次行经胸骨正中切开手术的患者,由于已经进行过一次手术,胸骨后组织粘连严重,分解粘连过程中往往出血较多,再次手术极易损伤胸骨后桥血管以及心脏重要结构,且还会面临术后胸骨愈合不良、骨髓炎、胸骨疼痛等问题,对患者预后影响较大。本团队采用胸腔镜微创三尖瓣手术治疗三尖瓣关闭不全,避开了前次手术入路,采用右侧腋前线第4肋间3 cm切口为手术入路,并经股动静脉插管建立体外循环。相较于传统正中开胸手术,该术式很好地解决了再次心脏手术的入路问题,极大地减少了对患者的创伤。现对2018年1月至2023年12月在解放军总医院第一医学中心心脏大血管外科接受全胸腔镜三尖瓣修复/置换手术治疗左心瓣膜术后单纯性重度三尖瓣关闭不全的134例患者的围术期临床资料以及治疗经验进行总结,报道如下。
1 资料与方法
1.1一般资料 回顾性分析2018年1月至2023年12月在解放军总医院第一医学中心心脏大血管外科接受全胸腔镜三尖瓣手术治疗134例的左心瓣膜术后单纯性重度三尖瓣关闭不全患者的临床资料。纳入标准:既往接受过至少一次正中开胸左心瓣膜手术,出现了单纯性重度三尖瓣关闭不全。排除标准:(1)同期合并接受其他心脏手术,如左心瓣膜手术、先天性心脏病矫治手术、冠状动脉搭桥手术、心脏大血管手术等。(2)存在严重外周动静脉病变无法经股动静脉插管建立体外循环。(3)严重肺动脉高压(肺动脉收缩压>60 mmHg)。(4)左心室射血分数(left ventricular ejection fraction,LVEF)<40%。72例(53.7%)患者行三尖瓣成形术(三尖瓣成形组),其中68例患者行人工瓣环成形,采用美国爱德华公司MC3成形环(26 mm 28例,28 mm 40例);4例患者行DeVega三尖瓣成形。62例(46.3%)患者行三尖瓣置换术(三尖瓣置换组),瓣膜尺寸为27 mm 2例,28 mm 2例,29 mm 58例。本研究获解放军总医院伦理委员会批准。
1.2手术方法
1.2.1 手术适应证和禁忌证 适应证:(1)经胸超声心动图检查提示三尖瓣重度反流,且其他非手术治疗效果不理想。(2)合并右心功能不全的症状和体征,如全身液体潴留(外周水肿、胸腔积液、腹腔积液或中心静脉压>14 mmHg)、呼吸困难、运动不耐受。禁忌证:(1)既往有右侧胸腔手术史且合并严重右侧胸腔粘连。(2)存在左心瓣膜功能严重障碍(LVEF<40%)。(3)严重肺动脉高压(肺动脉收缩压>60 mmHg)。
1.2.2 手术操作 患者常规取平卧位,右肩部垫高30°,放置体外除颤电极,采用双腔气管插管静吸复合麻醉。常规消毒铺单,待全身肝素化后,腹股沟处取2~3 cm切口暴露股动静脉,使用Seldinger技术进行股动静脉插管。股动脉插管采用15~18F管道,双层荷包缝合;股静脉插管采用21F或23F管道,单个荷包缝合。其中静脉插管末端置于下腔静脉心房连接处,约第5肋间水平,进行负压吸引。主操作孔位于腋前线第4肋间水平,切口长度约3.0 cm,并放置切口保护器,男性置于右侧乳头外侧,女性置于右乳下褶皱处。经切口保护器侧方置入二氧化碳管。腔镜孔位于第3肋间腋中线。进入胸腔前,患者单肺通气,右侧肺组织塌陷。在胸腔镜指引下,纵行切开心包,并用3~4根缝线悬吊心包,切开右心房,调整腔静脉插管前端于下腔静脉瓣下方,暴露并探查三尖瓣,在心脏不停跳下行三尖瓣成形术或置换术。术毕缝合右心房,采用经食道超声心动图评估三尖瓣形态功能良好后拔除体外循环插管,关闭手术切口。
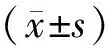
2 结果
2.1患者基线资料 134例患者中男40例,女94例,年龄(59.5±12.0)岁。体质量指数(body mass index,BMI)为(23.3±2.5)kg/m2。134例患者中既往均接受过至少一次正中开胸左心瓣膜单瓣或双瓣手术,距上次手术时间(15.8±8.1)年。经胸超声心动图检查,134例患者入院时三尖瓣关闭不全均为重度,右心房内径(right atrial diameter,RAD)56.0(54.0,60.0)mm,右心室舒张末期内径(right ventricular end-diastolic diameter,RVDD)47.5(42.3,52.0)mm,左心房内径(left atrial diameter,LAD)50.0(44.0,59.8)mm,左心室舒张末期内径(left ventricular end-diastolic diameter,LVDD)45(42.0,47.0)mm,LVEF 60.0(51.3,65.0)%,肺动脉压(pulmonary artery pressure,PAP)56.0(55.3,56.0)mmHg。纽约心脏病学会(New York Heart Association,NYHA)心功能分级为Ⅲ/Ⅳ级患者76例(56.7%)。术前有房颤者100例(74.6%),高血压病史24例(17.9%),糖尿病史18例(13.4%),冠心病史16例(11.9%),脑血管病史8例(6.0%),慢性肺疾病史2例(1.5%),肾功能不全病史6例(4.5%),外周动脉疾病史2例(1.5%)。
2.2两组术前一般资料比较 三尖瓣成形组PAP、术前房颤占比低于三尖瓣置换组,差异有统计学意义(P<0.05),两组患者年龄、性别、BMI、距上次手术时间、既往病史占比、NYHA心功能分级为Ⅲ/Ⅳ级占比、RAD、RVDD、LAD、LVDD、LVEF差异无统计学意义(P>0.05),见表1。
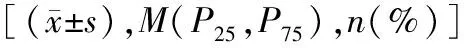
表1 两组术前一般资料比较
2.3患者手术情况 所有患者接受体外循环下不停跳全胸腔镜三尖瓣手术,无中转正中开胸。体外循环时间为92(77.0,112.0)min,平均手术时间为(183.8±56.1)min。手术结束前采用经食道超声心动图对三尖瓣反流情况进行复查评估,无严重反流及人工瓣膜功能障碍。其中2例(1.5%)患者体外循环撤机后出现右心功能不全,后予以体外膜肺氧合(extracorporeal membrane oxygenation,ECMO)支持。术中输注血制品54例(40.3%)。
2.4患者术后情况 术后带气管插管返回重症监护室(intensive care unit,ICU),待患者清醒后,查血气结果满意,自主呼吸恢复后拔除气管插管,术后患者呼吸机辅助通气时间为13.0(10.5,18.5)h。ICU停留时间为2.0(2.0,3.0)d,引流管拔除时间为2.0(1.0,3.0)d,术后胸腔引流量为475.0(205.0,1 048.0)mL。行ECMO循环支持患者术后1周内顺利撤机。16例患者出现术后早期并发症,包括室颤2例,胸腔积液4例,住院再手术2例,起搏器植入8例。无肺部感染、再次气管插管、肺水肿、肾功能不全、脑血管并发症、切口愈合不良等并发症发生。无术后早期死亡。2例患者因术后复查发现人工瓣功能障碍、三尖瓣狭窄再次行三尖瓣置换术,术后恢复良好,无其他并发症发生,正常出院。术后1周复查心脏超声结果显示,130例(97.0%)患者无或仅轻度三尖瓣反流;4例(3.0%)患者中度反流,经药物调整,术后1个月返院复查心脏超声结果明显改善;无重度反流。术后RAD(46.5±13.8)mm,RVDD(34.9±7.0)mm,LAD 47.0(38.3,53.0)mm,LVDD(43.0±5.5)mm,LVEF(64.3±7.2)%。
2.5两组术中及术后资料比较 三尖瓣成形组手术时间、术后机械通气时间、ICU停留时间短于三尖瓣置换组,术中输血浆量、术后引流量、术后RAD、术后RVDD、术后LAD、术后并发症发生率低于三尖瓣置换组,差异有统计学意义(P<0.05)。两组患者体外循环时间、术中输血率、引流管拔除时间、术后LVDD、术后LVEF、术后次日肌钙蛋白T(cardiac troponin T,cTnT)、术后次日肌酸激酶同工酶MB(creatine kinase isoenzyme MB,CKMB)、人工心脏辅助装置[包括ECMO和主动脉内球囊反搏(intra-aortic balloon pump,IABP)]使用率等差异无统计学意义(P>0.05),见表2。无一例患者死亡或自动出院。
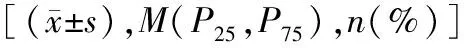
表2 两组术中及术后资料比较
3 讨论
3.1对于既往接受过正中开胸手术的患者,原手术入路胸骨后往往存在非常严重的组织粘连,为了解决此问题,术中需要耗费大量时间来松解粘连。另外,因为新生血管较多且走行复杂,在松解粘连过程中出血量会较初次正中开胸手术更大,可能需要大量的血制品输注,甚至止血药物和止血材料的使用也会较多,这也给患者带来了更大的经济负担。创伤大、出血多、术后切口愈合不良等并发症是传统正中开胸再次心脏手术难以逾越的问题,极大地增加了手术难度及手术风险。
3.2近年来,得益于新理念、新技术、新器械的不断发展,胸骨正中切口已经不再是唯一的入路,许多微创小切口极大地减少了心脏手术对机体的创伤[11]。同时经导管疗法也开始用于治疗三尖瓣关闭不全,但相关经验总结较少,需要高质量的RCT研究来确定其临床疗效[12-16]。随着腔镜器械的发展,胸腔镜技术在心脏外科中得到了很好的应用[17-19]。本研究团队开展全胸腔镜手术多年,手术的数量、种类、复杂性在不断增加[20],在全胸腔镜心脏瓣膜手术方面经验丰富。经过不断地积累总结经验,已将全胸腔镜技术应用于再次心脏手术,包括先天性心脏病、二尖瓣、三尖瓣手术。
3.3在本研究中,所有患者既往接受过至少一次正中开胸心脏手术。对于这些患者,本团队充分利用多年来在全胸腔镜心脏手术方面的优势和经验,选择经右侧腋前线第4肋间入路行全胸腔镜不停跳三尖瓣手术,外周股动静脉插管建立体外循环,使用单根下腔静脉插管,前端置于下腔静脉瓣下方进行负压吸引,通过与体外循环师密切配合并积极调整手术床体位及静脉插管位置,以保证手术视野无血。
3.4在实践中本团队证明了全胸腔镜入路再次心脏手术治疗左心瓣膜术后单纯性重度三尖瓣关闭不全优势明显。右侧腋前线第4肋间入路避开了需要处理前次正中开胸组织粘连严重的难题,既减少了手术创伤和术中出血量,也在一定程度上降低了手术难度。在胸腔镜高清高倍视野导航下,术者可以更加清晰地观察三尖瓣瓣叶瓣环形态病变程度,提高手术操作精度。全胸腔镜手术的心肌损伤及炎症反应水平显著低于正中开胸手术[21]。本研究结果显示,在再次单纯三尖瓣手术中,134例患者中72例行三尖瓣成形,三尖瓣成形率为53.7%。尽管有研究显示接受三尖瓣置换术和接受三尖瓣成形术的患者术后10年生存率无显著差异[22],但是本团队仍然将成形作为首要手术方式,因为它可以避免换瓣带来的抗凝风险、出血、卒中、血栓、生物瓣衰败等问题。既往有文献报道接受三尖瓣手术患者住院死亡率为13%~26%[23-25]。在本研究134例患者中,无术后早期死亡,术后早期无严重并发症,早期手术效果满意。因为左心瓣膜手术是三尖瓣关闭不全的独立危险因素[5],所以在初次行左心瓣膜手术时,如果存在轻中度三尖瓣关闭不全也应该同期进行三尖瓣成形,以减少患者因左心瓣膜术后三尖瓣关闭不全再次接受手术的风险。
3.5有研究显示,对于左心瓣膜术后重度三尖瓣关闭不全的患者,在左心功能失调和贫血发展之前早期行三尖瓣手术干预,可以改善三尖瓣手术临床结果[22]。本研究结果显示,三尖瓣成形组PAP、术前房颤占比低于三尖瓣置换组,差异有统计学意义(P<0.05),表明在瓣膜结构条件允许的情况下,心脏和全身情况更好的患者有更大的概率接受三尖瓣成形术。另外,术后资料显示,三尖瓣成形组的手术时间、术后机械通气时间、ICU停留时间短于三尖瓣置换组,术中输血浆量、术后引流量、术后并发症发生率低于三尖瓣置换组,差异有统计学意义(P<0.05),表明接受三尖瓣修复的患者术后恢复更快,围术期状况更好。值得注意的是,三尖瓣成形组术后三尖瓣中度及以上反流的占比低于三尖瓣置换组,表明全胸腔镜三尖瓣修复技术有较好的修复效果。所以本团队主张尽早对左心瓣膜术后三尖瓣关闭不全患者进行手术治疗。
综上所述,对于既往接受过正中开胸左心瓣膜术后单纯性重度三尖瓣关闭不全的患者行全胸腔镜三尖瓣手术治疗,安全可行。对于满足手术指征的患者,尽早手术可能有更高概率接受三尖瓣成形术和获得更好的围术期结果。

