基于多模式识别结合UPLC指纹图谱及多指标成分定量测定的薏苡仁质量评价研究
高 童,张晓丹,冯庭辉,尹 峰,方嘉豪,张朝军,蔡烈涛,金 燕,梁宗锁, *,黄文丽*
基于多模式识别结合UPLC指纹图谱及多指标成分定量测定的薏苡仁质量评价研究
高 童1,张晓丹2,冯庭辉2,尹 峰2,方嘉豪2,张朝军3,蔡烈涛3,金 燕4,梁宗锁1, 2*,黄文丽1*
1. 陕西中医药大学药学院,陕西 咸阳 712046 2. 浙江理工大学生命科学与医药学院,浙江 杭州 310018 3. 浙江康莱特药业有限公司,浙江 杭州 310018 4. 道地药材国家重点实验室,北京 100700
建立薏苡仁UPLC指纹图谱及多指标成分定量测定方法,并将薏苡仁UPLC指纹图谱、化学模式识别和多指标成分定量测定相结合,进而对不同产地薏苡仁药材进行综合质量评价。采用Waters C8色谱柱,以甲醇-纯水等度洗脱;体积流量0.2 mL/min;检测波长205 nm;柱温25 ℃;进样量0.3 µL,建立15个不同产地薏苡仁药材指纹图谱,并进行相似度评价和化学模式识别;同时对不同产地薏苡仁药材进行一般性检查、浸出物测定及多个指标性成分含量测定。15个不同产地薏苡仁药材UPLC指纹图谱共标定14个共有峰,通过对照品指认了其中7个成分,包括三亚油酸甘油酯、1,2-二亚油酸-3-棕榈酸甘油酯、1,2-二亚油酸-3-油酸甘油酯、1-棕榈酸-2-油酸-3-亚油酸甘油酯、1,2-二油酸-3-亚油酸甘油酯、1,2-二油酸-3-棕榈酸甘油酯和三油酸甘油酯,上述7个成分重复性、稳定性及加样回收率结果均较好。此外,UPLC指纹图谱相似度范围为0.972~1.000;15个产地薏苡仁药材聚为3类,云南、福建样品聚为一类,贵州兴仁药材聚为一类,贵州兴义、安龙药材聚为一类;主成分综合得分表明云南、福建产地样品较优,通过筛选得出色谱峰2、5(三亚油酸甘油酯)、8和11(1,2-二油酸-3-棕榈酸甘油酯)是引起不同产地薏苡仁质量差异的主要成分;不同产地薏苡仁药材均符合《中国药典》2020年版水分、灰分和浸出物的标准;同时,多成分定量测定结果表明,7个指标性成分之间存在显著差异。建立了15个不同产地薏苡仁药材UPLC指纹图谱及含量测定方法,并结合UPLC指纹图谱、化学模式识别和多指标成分含量测定进行进一步研究,可为薏苡仁药材质量的综合评价提供参考。
薏苡仁;UPLC指纹图谱;化学模式识别;三亚油酸甘油酯;1,2-二亚油酸-3-棕榈酸甘油酯;1,2-二亚油酸-3-油酸甘油酯;1-棕榈酸-2-油酸-3-亚油酸甘油酯;1,2-二油酸-3-亚油酸甘油酯;1,2-二油酸-3-棕榈酸甘油酯;三油酸甘油酯;质量评价
薏米L. var.(Roman.) Stapf为禾本科(Gramineae)薏苡属L.一年生草本植物,其干燥成熟种仁-薏苡仁是中医药史上常用中药材[1]。到目前为止,薏苡仁中已有70多种化学成分被发现并分离鉴定,主要包括脂肪酸及其脂类、糖类、多酚类等[2]。现代药理学研究表明,薏苡仁油脂是薏苡仁抗癌活性成分,可通过诱导癌细胞凋亡、抑制癌细胞转移和增殖,对非小细胞肺癌[3-5]、结肠癌[6]、胰腺癌[7]、喉癌[8]、胃癌[9]等发挥治疗作用。甘油三酯类成分是薏苡仁油的主要成分,占总油脂的86%~95%。目前,薏苡仁油脂部分共有22种三酰甘油类成分得到鉴定,含量较高的有三油酸甘油酯(triolein,OOO)、1,2-二亚油酸-3-油酸甘油酯(1,2-dilinoleoyl-3-oleoyl-glycerol,LLO)、1,2-二油酸-3-亚油酸甘油酯(1,2-dioleoyl-3-linoleoyl-glycerol,OOL)、三亚油酸甘油酯(trilinolein,LLL)、1-棕榈酸-2-油酸-3-亚油酸甘油酯(1-palmitoyl-2-oleoyl-3-linoleoyl-glycerol,POL)、1,2-二油酸-3-棕榈酸甘油酯(1,2-dioleoyl-3-palmitoyl-glycerol,OOP)、1,2-二亚油酸-3-棕榈酸甘油酯(1,2-dilinoleoyl-3-palmitoyl-glycerol,LLP)[10-11]。
文献调研发现,薏苡仁液相色谱指纹图谱和成分检测方法中,常以C18柱为固定相,乙腈-二氯甲烷为流动相进行洗脱[10, 12-15]。二氯甲烷是一种中等极性溶剂,常作为正相色谱流动相[16]。在反相色谱体系中使用二氯甲烷作为流动相时,需利用异丙醇在使用前后对溶剂体系进行过渡,以防止溶剂间产生不混溶现象而造成管路堵塞[16]。因此,为避免潜在实验风险,降低实验操作复杂性,寻找简单、高效且低风险的薏苡仁反相色谱检测方法,对薏苡仁的深入研究具有非常大的助力。
过去几十年,由于薏苡仁产量较低和大宗农作物的不断挤压,各省份薏苡仁种植逐渐减少。近些年,在中医药思想的不断影响下,薏苡仁开始被广泛重视。目前,市场上流通的薏苡仁药材主要分布在云南、贵州和福建等主要产区[17]。然而,因薏苡属品种较多,加之薏苡仁市场需求量不断增大,价格上涨,使得伪品、劣质品不断增多,严重影响薏苡仁产业的进一步发展[18]。《中国药典》2020年版[19]规定了薏苡仁甘油三油酸酯含量测定标准,指标较为单一,同时,结合薏苡仁指纹图谱、多种化学模式识别以及多指标含量测定的综合评价研究较为少见。因此,本研究建立了薏苡仁UPLC-TUV检测方法,并结合15个不同产地薏苡仁药材UPLC指纹图谱、多种化学模式识别和多指标成分含量测定,对薏苡仁药材质量进行综合评价。
1 仪器与材料
1.1 仪器
Waters Acquity UPLC H-Class超高效液相色谱仪(Waters公司);高速中药粉碎机(瑞安市百信制药机械有限公司);BT25S型十万分之一分析天平(德国Sartorius公司);TP-213型万分之一分析天平(美国Denver Instrument公司);KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司);AP-9925型真空泵(天津奥特赛恩斯仪器有限公司);HH-4PD型数显恒温水浴锅(金坛区西城新瑞仪器厂);XY-GZH-500远红外快速干燥箱(上海昕仪仪器仪表有限公司);SX2-2.5-12TP箱式电阻炉(济南精密科学仪器仪表有限公司);CR-Easy 15系列超纯水机(力康生物医疗科技控股有限公司)。
1.2 药物与试剂
三油酸甘油酯(批号111692-202208,质量分数≥98.7%,购自中国食品药品检定研究院);薏苡仁油标准品(薏苡仁油提取物中7种主要的甘油三酯类成分标定所得)(批号ZJ0003-202208,其中LLL:4.73%;LLO:17.85%;LLP:6.26%;OOL:19.32%;POL:12.76%;OOO:16.00%;OOP:9.16%,由浙江省食品药品检验研究院标定);色谱级甲醇(德国Merk公司);色谱级甲酸(上海麦克林生化科技有限公司);分析纯甲醇和乙醇(杭州高晶精细化工有限公司)。
1.3 药材
薏苡仁药材为课题组在2022年10月—2022年12月于贵州、云南、福建调研后收集得到,药材信息见表1。所有药材均经浙江理工大学梁宗锁教授鉴定为禾本科植物薏米L.var.(Roman.) Stapf的干燥成熟种仁。

表1 薏苡仁药材样品信息
2 方法与结果
2.1 不同产地薏苡仁药材UPLC指纹图谱研究
2.1.1 色谱条件 Waters Acquity UPLC H-Class超高效液相色谱仪;Waters C8色谱柱(100 mm×3 mm,2.7 µm);流动相为甲醇-水98.5∶1.5,等度洗脱;柱温25 ℃,体积流量0.2 mL/min,检测波长205 nm,进样量0.3 µL。
2.1.2 对照品溶液的制备 精密称取甘油三油酸酯对照品20 mg,加入甲醇溶解制成0.2 mg/mL对照品溶液Ⅰ,用于确定薏苡仁油对照品中7种指标性成分的相对保留时间;再取薏苡仁油对照品30 mg,加入甲醇溶解并制成1.2 mg/mL混合对照品溶液Ⅱ,用于进样后得到混合对照品色谱图及外标法定量。
2.1.3 供试品溶液制备 取薏苡仁药材粉末(过65目筛)500 mg,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,称定质量,超声处理(功率250 W,频率40 kHz)30 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,取续滤液即得。
2.1.4 精密度试验 精密称取适量薏苡仁样品(S6),在“2.1.3”项方法下制备供试品溶液,按“2.1.1”项色谱条件连续进样6次,计算得到各共有峰保留时间的RSD均小1.0%,峰面积的RSD均小于2.0%。
2.1.5 稳定性试验 精密称取同一薏苡仁样品(S6),按“2.1.3”项下方法制备供试品溶液,在“2.1.1”项色谱条件下,分别于0、2、4、8、12、24 h各进样1次,测得各共有峰保留时间的RSD均小1.0%,峰面积的RSD均小于3.0%。
2.1.6 重复性试验 精密称取薏苡仁样品(S6)6份,各0.5 g,在“2.1.3”项方法下制备供试品溶液,在“2.1.1”项色谱条件下分别进样,计算得到各共有峰保留时间的RSD均小于1.5%。
2.1.7 UPLC指纹图谱的研究及相似度评价 分别取不同产地薏苡仁样品,在“2.1.3”项方法下制备供试品溶液,于“2.1.1”项色谱条件下进行分析,得到不同产地薏苡仁药材UPLC色谱图,将色谱数据导入“中药色谱指纹图谱相似度评价系统2012版”,设置S1样品为参照图谱,采用中位数法,时间窗宽度设为0.1 min,通过多点校正、Mark峰匹配生成对照指纹图谱(R),其对照指纹图谱和叠加图谱见图1(S1~S15),共标定14个共有峰。通过与混合对照品(图2)比对,指认出7个成分,分别为LLL、LLP、LLO、POL、OOL、OOP、OOO。相似度评价结果见表2,15个产地样品与对照指纹图谱的相似度范围为0.972~1.000,表明不同产地薏苡仁药材化学成分相似。
2.2 化学模式识别
2.2.1 聚类分析(cluster analysis,CA):将15个不同产地薏苡仁14个共有峰峰面积作为变量,导入SPSS 26.0软件,以组间联接法和平方欧式距离法进行系统聚类分析,结果见图3。当欧式距离10时,不同产地薏苡仁药材聚为3类,第1类为贵州盘州市(S3)、贵州安龙县(S6)、贵州兴义市(S10)、贵州兴义市(S13)、贵州普安县(S11);第2类为贵州兴仁市样品(S2)、(S4)、(S7)、(S9)、(S14)、(S15);第3类为云南曲靖市(S1)、福建三明市(S5)、云南蒙自市(S8)、福建南平市(S12)。结果表明,不同产地薏苡仁样品内在化学组成存在一定的相似性,同时发现产地接近的薏苡仁样品亦存较大的差异性。

图1 15个产地薏苡仁药材UPLC叠加指纹(S1~S15)及对照图谱 (R)

图2 混合对照品溶液UPLC色谱图
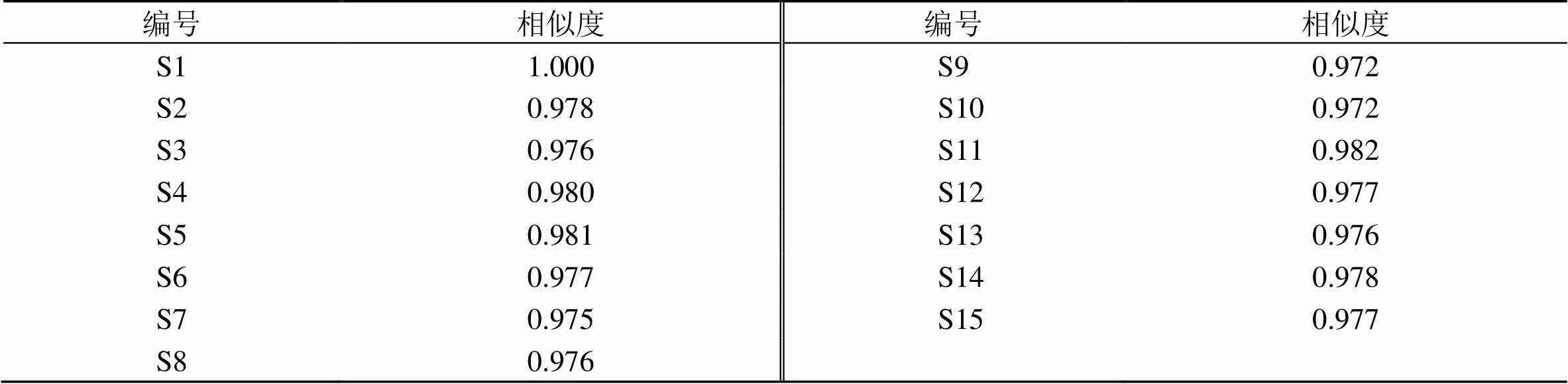
表2 15个产地薏苡仁药材UPLC指纹图谱相似度评价结果
2.2.2 主成分分析(principal component analysis,PCA) 将15个不同产地薏苡仁样品14个共有峰峰面积作为变量,导入SPSS 26.0软件,得到相关系数特征值和方差贡献率,见表3。选取特征值>1为标准,得到3个主成分,可用于反映薏苡仁指纹图谱85.307%的信息。通过SPSS 26.0软件计算得到主成分载荷矩阵,见表4,主成分1主要反映了色谱峰3、4、5(LLL)、6(LLP)、7(LLO)、8、9(POL)、10(OOL)、11(OOP)、12(OOO)的信息,主成分2主要反映了色谱峰1、13、14的信息,主成分3主要反映了色谱峰2的信息。
将14个共有峰数据标准化,结合主成分得分系数,以3个主成分对应的方差贡献率为权重系数,通过公式1=0.5701-0.4442+0.6453+0.8054+0.9225+0.9496+0.9737+0.8788+0.9879+0.98610+0.92411+0.97312+0.43413-0.22414;2=0.6561-0.0892-0.2963+0.2214-0.2705-0.2216-0.0647-0.0898-0.0639+0.03510+0.06211+0.13712+0.52113-0.08914;3=−0.0311+0.8482-0.2683-0.0294-0.1265+0.1206+0.0047+0.3558+0.1289+0.03910+0.20011+0.07212+0.15413+0.17514;=(64.561%×1+12.356%×2+8.391%×3)/85.307%,分别计算3个主成分得分1、2、3和综合得分(),结果见表5。15个不同产地薏苡仁药材综合得分为−9.61~11.04,表明不同产地薏苡仁药材整体质量差异较大,云南曲靖市(S1)综合得分最高,表明该地薏苡仁药材质量较好,其次为福建三明市(S5)、云南蒙自市(S8)、福建南平市(S12);贵州兴仁市薏苡仁药材综合得分排名在5~10,质量处于中等;贵州兴义市(S10)、贵州普安县(S11)、贵州安龙县(S6)、贵州盘州市(S3)、贵州兴义市(S13)综合得分排名分别为11~15,表明贵州省的兴义市、盘州市、普安县及安龙县薏苡仁药材质量均低于其他产地。

表3 薏苡仁药材样品主成分分析相关系数特征值和累积方差贡献率
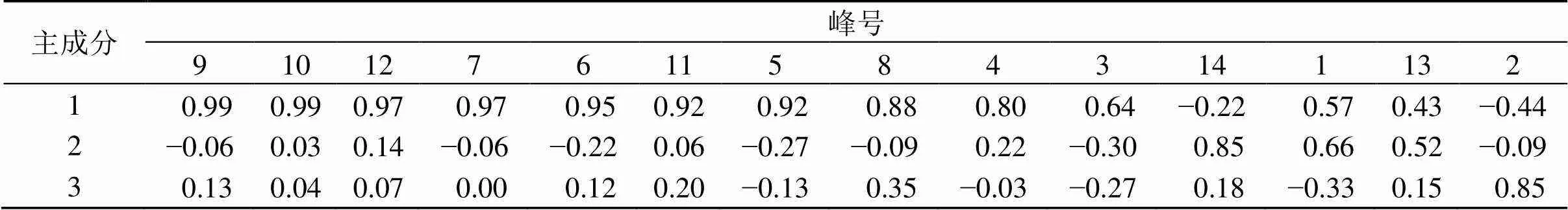
表4 薏苡仁药材样品主成分分析因子载荷矩阵
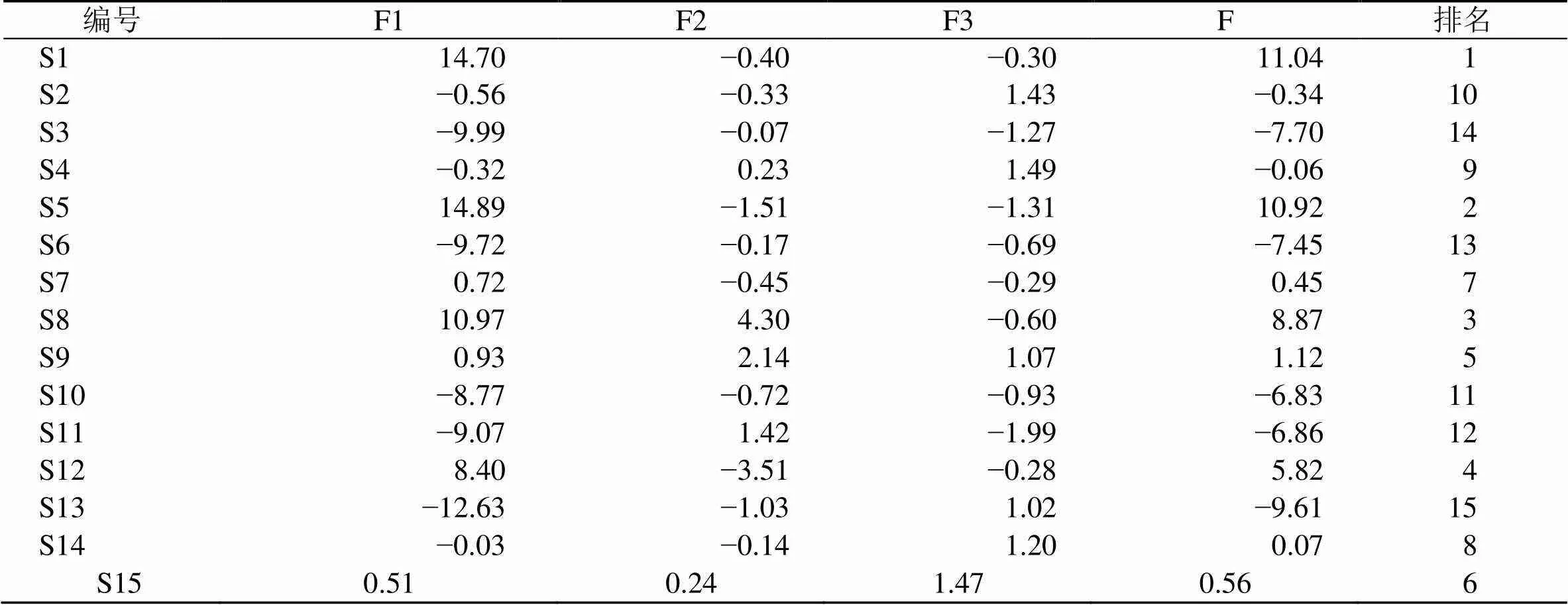
表5 薏苡仁药材样品主成分得分与综合得分排序
2.2.3 正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA) 以15个不同产地薏苡仁共有峰峰面积为变量,导入SIMCA 14.1软件归一化处理后,进行PCA,通过自动拟合得到2个主成分,2为0.914,2为0.764(>0.5),表明模型拟合较好,同时具有良好的预测能力,结果见图4-A。15个产地薏苡仁样品分为3类,云南、福建样品为一类,贵州兴仁市样品为一类,贵州其他县市样品为一类,与CA结果一致。
根据PCA和CA结果,将15个产地薏苡仁分成3组,云南、福建产地为一组,贵州产地分为2组,进行(图4-B),模型参数2为0.967,2为0.791。结合VIP>1,筛选出4个可以区分3个组别的差异指标,如图5所示,分别为色谱峰2、色谱峰5(LLL)、色谱峰8和色谱峰11(OOP)。

图5 15个不同产地薏苡仁药材样品VIP值图
2.3 一般性检查及浸出物测定
按照《中国药典》2020年版:烘干法(通则0832第二法),灰分测定方法(通则2302)及醇溶性浸出物测定法(通则2201)项下的热浸法[14],对15个不同产地薏苡仁药材进行测定,结果见表6。15种样品均符合药典标准,水分在8.91%~11.67%,灰分在1.77%~2.69%,醇溶性浸出物含量在10.80%~14.92%。
2.4 样品含量测定
2.4.1 线性关系考察 精密称取薏苡仁油对照品30 mg,加入甲醇溶解并制成1.2 mg/mL混合对照品溶液,取混合对照品溶液1.5 mL,3/4倍稀释5次,分别制得5个不同质量浓度点的工作曲线溶液。在“2.1.1”项色谱条件下进样测定,以对照品溶液质量为横坐标(),峰面积为纵坐标(),进行线性回归,结果见表7。

表6 15个不同产地薏苡仁药材质量评价结果
2.4.2 精密度试验 取薏苡仁供试品溶液,在“2.1.1”项色谱条件下连续进样6次,计算得到LLL、LLP、LLO、POL、OOL、OOP、OOO峰面积的RSD分别为0.60%、0.86%、0.26%、0.75%、0.47%、1.26%、0.95%。
2.4.3 稳定性试验 取同一薏苡仁供试品溶液,在“2.1.1”项色谱条件下,分别于0、2、4、8、12、24 h进样测定,测得LLL、LLP、LLO、POL、OOL、OOP、OOO峰面积的RSD分别为0.97%、1.03%、0.77%、1.58%、1.02%、2.69%、0.88%。
2.4.4 重复性试验 分别称取同一薏苡仁样品(S6)6份,按“2.1.3”项方法制备供试品溶液,在“2.1.1”项色谱条件下进样测定,计算得到LLL、LLP、LLO、POL、OOL、OOP、OOO含量的RSD分别为1.02%、0.63%、1.08%、1.37%、1.50%、2.35%、2.15%。
2.4.5 加样回收率试验 精密称定6份已知成分含量的薏苡仁样品(S6)粉末各0.2 g,分别加入适量对照品,在“2.1.3”项方法下制备供试品溶液,按照“2.1.1”项色谱条件进样,计算得到LLL、LLP、LLO、POL、OOL、OOP、OOO的平均加样回收率分别为96.49%、98.08%、98.28%、95.73%、95.81%、96.99%、93.03%,RSD分别为0.51%、1.66%、1.45%、1.06%、1.12%、0.83%。
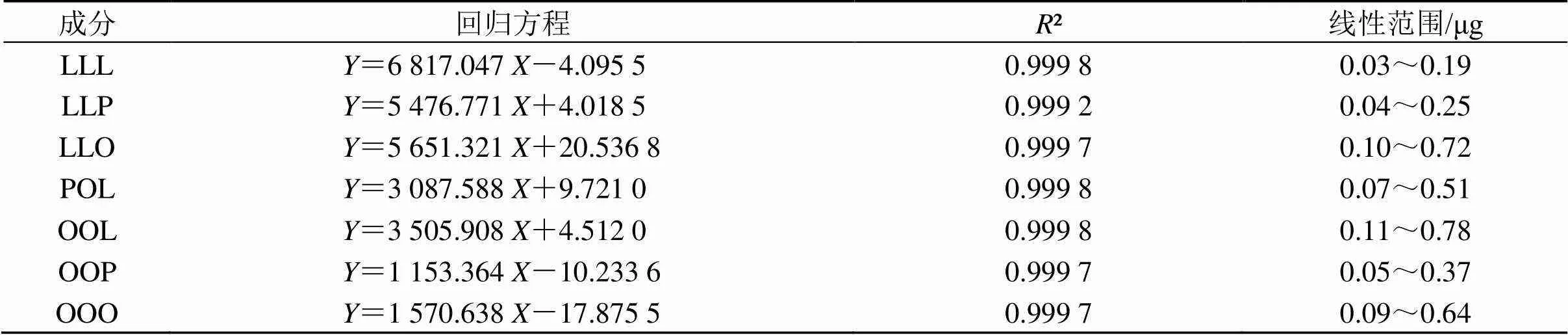
表7 薏苡仁药材中7个成分线性关系考察结果
2.4.6 含量测定 分别取15个不同产地薏苡仁药材样品粉末,在“2.1.3”项方法下制备供试品溶液,同时在“2.1.1”色谱条件进行测定,计算样品中LLL、LLP、LLO、POL、OOL、OOP、OOO及7种甘油三酯类成分总含量,结果见表8。15个不同产地薏苡仁药材样品中上述成分质量分数范围分别为2.734~4.831、3.670~5.158、9.522~13.374、7.175~9.796、11.296~15.468、5.381~7.322、8.863~12.965、49.041~68.094 mg/g。结果表明,不同产地薏苡仁药材甘油三酯类成分具有显著的差异性。15个不同产地薏苡仁药材中,OOL含量最高,其次为LLO、OOO、POL、OOP和LLP,而LLL含量最低。

表8 15个不同产地薏苡仁药材7种成分含量测定结果
3 讨论
实验前期,在大量文献调研下发现,有关薏苡仁甘油三酯类成分的检测多涉及二氯甲烷的使用[10, 12-15],而多数实验室的液相色谱为反相色谱,对于正相溶剂的使用需非常谨慎。因此,通过筛选大量薏苡仁油脂检测方法,本研究最终确定以《美国药典》薏苡仁粉测定方法为基础[20],该方法以Waters C8色谱柱为固定相,甲醇为流动相,利用HPLC-ELSD进行检测,在很大程度上避免了使用二氯甲烷带来的潜在风险。实验前期,在相同固定相(Waters C8色谱柱)下,对比了HPLC-ELSD和UPLC-TUV 2种检测方法,结果发现,HPLC-ELSD检测方法得到的色谱峰分离度较差,整体出峰时间较长,同时指纹图谱共有峰数量较少;而UPLC-TUV检测方法下各峰分离度显著较好,耗时更短,共有峰数量较多,同时各色谱峰具有良好的信噪比。众所周知,UPLC具有更快的速度、更好的灵敏度和分离度等,同时还能大大降低流动相的浪费[21];此外,相比蒸发光检测器,紫外检测器具有更好的普适性,这也进一步使得该方法更容易被复现。因实验条件限制,本研究未进一步对UPLC-ELSD检测方法进行验证,后续深入研究将对此进行验证。
综合以上结果,本实验选择UPLC-TUV检测方法进行后续研究。基于该检测方法,对色谱条件进行进一步优化,首先,对不同流动相比例:甲醇(100%);甲醇∶乙腈=95∶5;甲醇∶乙腈=98∶2;甲醇∶水=95∶5;甲醇∶水=98∶2;甲醇∶纯水=98.5∶1.5;甲醇∶水=99∶1进行了比较,结果表明,流动相为甲醇:水=98.5∶1.5时薏苡仁指纹图谱色谱峰具有较好的分离情况;进一步对不同体积流量(0.20、0.25、0.30 mL/min)、柱温(25、30 ℃)、进样量(0.2、0.3、0.5 µL)条件下指纹图谱色谱峰分离情况进行比较,结果显示,体积流量0.20 mL/min、柱温为25 ℃、进样量0.3 µL时色谱峰分离效果较佳。由于薏苡仁油存在饱和甘油三酯类成分紫外吸收较弱特性,综合不同甘油三酯类成分最大响应值和最低噪音[22]分别对203、205、210 nm指纹图谱进行比较,结果表明,在205 nm下,薏苡仁中各组分响应较好。
指纹图谱研究结果表明,云南、贵州和福建3个省份15个薏苡仁药材指纹图谱相似度均大于0.970,说明3个省份薏苡仁药材化学组成较为相似,推测可能与相近的气候条件有关。进一步结合化学模式识别进行薏苡仁综合质量评价,其中,CA和PCA结果表明,薏苡仁药材质量与产地位置有着较为显著的相关性,云南省、福建省薏苡仁药材质量较好;OPLS-DA分析中,通过VIP值筛出色谱峰2、5(LLL)、色谱峰8和11(OOP)是导致不同产地薏苡仁药材质量差异的重要化合物,后续研究可进一步对未知色谱峰2和色谱峰8进行分析和鉴定,从而确保薏苡仁质量评价的全面性和准确性。
一般性指标和浸出物测定结果表明,15个产地薏苡仁水分、灰分及浸出物均符合《中国药典》2020年版[19]要求,表明3产区薏苡仁种植质量良好。同时,多含量测定结果表明,7个指标性成分中,OOL含量最高,其次为OOO(均符合《中国药典》2020年版规定),而LLL含量最低,结合OPLS-DA的VIP筛选结果可以发现,药典指标甘油三油酸酯含量在不同产地药材中呈现较小差异,由此可以看出单一指标性成分对评估药材质量优劣具有一定的局限性。此外,云南和福建产地药材总油脂和7种指标性成分含量虽具有一定的相似性,但云南样品中OOO含量显著较高;而福建样品中LLL、OOL、LLP含量较高,结合两地气候特征,初步推测是云南显著的立体气候特点所致。在所有贵州药材中,发现7个指标性成分含量比例较为一致,但从总油脂含量来看,贵州兴仁市薏苡仁药材质量整体优于贵州其他县市,由此可以看出,近些年来,在国家政策、当地政府和相关研究所的推动和带领下,贵州兴仁市薏苡仁种植较为规范,药材质量较为稳定,而贵州其他县市薏苡仁目前可能仍存在种植不规范,质量参差不齐的现象。
综上,本研究建立的UPLC-TUV检测方法,能快速使薏苡仁甘油三酯类成分得到较好的分离,且仪器方法学考察良好,可用于薏苡仁药材质量的科学评价。在此方法基础上,本研究将薏苡仁UPLC指纹图谱与化学模式识别和多种指标性成分含量相结合,对不同产地薏苡仁药材进行综合评价,结果表明,相比薏苡仁研究中常见的单一指纹图谱和含量测定研究,该方法能更好地反映薏苡仁药材的整体质量特征,为今后薏苡仁药材的质量控制和栽培选育提供科学的依据。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国植物志编辑委员会. 中国植物志[M]. 北京: 中国科学出版社, 2006, 22: 648-649.
[2] 李晓凯, 顾坤, 梁慕文, 等. 薏苡仁化学成分及药理作用研究进展 [J]. 中草药, 2020, 51(21): 5645-5657.
[3] Lu X Y, Liu W, Wu J H,. A polysaccharide fraction of adlay seed (L.) induces apoptosis in human non-small cell lung cancer A549 cells [J]., 2013, 430(2): 846-851.
[4] 卢存存, 乔萌, 王子怡, 等. 康莱特注射液治疗非小细胞肺癌与肝癌论文的关键特征与安全性信息报告: 基于CONSORT-Harms的横断面调查[J]. 中草药, 2023, 54(20): 6791-6797.
[5] 江国强, 方芳. 厄洛替尼联合康莱特对肺癌A549 细胞增殖、侵袭及JAK2/STAT3信号通路的影响 [J]. 郑州大学学报: 医学版, 2019, 54(3): 418-422.
[6] Ni C L, Li B L, Ding Y Y,. Anti-cancer properties ofseed oil against HT-29 colon cells through regulation of the PI3K/AKT signaling pathway [J]., 2021, 10(11): 2833.
[7] Yang J, Liu Y, Lu S N,.seed oil regulates mitochondrial functional damage to induce apoptosis of human pancreatic cancer cells via the PTEN/PI3K/AKT signaling pathway [J]., 2022, 49(7): 5897-5909.
[8] 熊美华, 谌建平, 操润琴, 等. 薏苡仁油对喉癌细胞侵袭迁移能力的影响 [J]. 当代医学, 2018, 24(8): 15-18.
[9] 苏伟贤, 朱光辉, 肖焕擎, 等. 康莱特对胃癌细胞增殖及凋亡能力的影响 [J]. 临床和实验医学杂志, 2008, 7(4): 89-90.
[10] 向智敏, 祝明, 陈碧莲, 等. HPLC-MS分析薏苡仁油中的甘油三酯成分 [J]. 中国中药杂志, 2005, 30(18): 1436-1438.
[11] Hou J J, Cao C M, Xu Y W,. Exploring lipid markers of the quality of coix seeds with different geographical origins using supercritical fluid chromatography mass spectrometry and chemometrics [J]., 2018, 45: 1-7.
[12] 王燕雄, 李振雨, 童培珍, 等. 基于HPLC-ELSD指纹图谱和含量测定的薏苡仁药材质量评价研究 [J]. 亚太传统医药, 2020, 16(9): 64-67.
[13] 张婷, 罗云云, 杜伟锋, 等. 不同产地薏苡仁HPLC指纹图谱建立及甘油三油酸酯测定 [J]. 中成药, 2021, 43(4): 944-948.
[14] 崔媛, 王小明, 杨勇, 等. 薏苡仁油融合指纹图谱研究 [J]. 中草药, 2014, 45(12): 1698-1701.
[15] 马振中, 李晓琦, 黄萌萌, 等. 不同产地薏苡仁药材中甘油三酯和脂肪酸含量测定及其质量评价 [J]. 中草药, 2020, 51(1): 210-215.
[16] 于世林. 图解高效液相色谱技术与应用 [M]. 北京: 科学出版社, 2009: 150, 454.
[17] Diao X M. Production and genetic improvement of minor cereals in China [J]., 2017, 5(2): 103-114.
[18] 陈维, 叶开梅, 何大智, 等. 黔中山区薏苡产业发展现状、存在问题及对策 [J]. 中国种业, 2022(9): 34-36.

[20] United States Pharmacopeial Convention.[M]. USP 42-NF 37, 2018: 4861-4863.
[21] Nováková L, Matysová L, Solich P. Advantages of application of UPLC in pharmaceutical analysis [J]., 2006, 68(3): 908-918.
[22] 宁永成. 有机化合物结构鉴定与有机波谱学 [M]. 第2版. 北京: 科学出版社, 2000: 23.
Quality evaluation ofbased on multiple pattern recognition combined with UPLC fingerprint and determination of mult-index component content determination
GAO Tong1, ZHANG Xiaodan2, FENG Tinghui2, YIN Feng2, FANG Jiahao2, ZHANG Chaojun3, CAI Lietao3, JIN Yan4, LIANG Zongsuo1, 2, HUANG Wenli1
1. College of Pharmacy, Shaanxi University of Chinese Medicine, Xianyang 712046, China 2. College of Life Sciences and Medicine, Zhejiang Sci-Tech University, Hangzhou 310018, China 3. Zhejiang Kanglaite Pharmaceutical Co., Ltd., Hangzhou 310018, China 4. State Key Laboratory of Dao-di Herbs, Beijng 100700, China
To establish a method for the UPLC fingerprint and multi-indicator component content determination of Yiyiren(), and to combine the UPLC fingerprint of, chemical pattern recognition, and multi-indicator component content determination with the aim of evaluating the quality ofherbs from different origins.A Waters C8column was used with isocratic elution of methanol-pure water; the flow rate was 0.2 mL/min; the detection wavelength was 205 nm; the column temperature was 25 ℃; the injection volume was 0.3 µL; the fingerprints of 15herbs of different origins were established; the similarity evaluation and chemical pattern recognition were carried out; At the same time, the herbs of different origins ofwere subjected to general examination, determination of leachate and determination of the content of several index components.A total of 14 common peaks were identified in the UPLC fingerprints of 15 herbs of different origins of, and seven of them were identified by the control, including trilinolein (LLL), 1,2-dilinoleoyl-3-palmitoyl-glycerol (OOP), 1,2-dilinoleoyl-3-oleoyl-glycerol, 1-palmitoyl-2-oleoyl-3-linoleoyl-glycerol, 1,2-dioleoyl-3-linoleoyl-glycerol, 1,2-dioleoyl-3-palmitoyl-glycerol, and triolein, the results of reproducibility, stability and spiked recoveries of the above seven components were good. In addition, the similarity of UPLC fingerprints ranged from 0.972 to 1.000; the 15 originherbs were clustered into three categories, the samples from Yunnan and Fujian were clustered into one category, the herbs from Xingren of Guizhou were clustered into one category, and the herbs from Xingyi and Anlong of Guizhou were clustered into one category; the composite scores of the principal components indicated that the samples of Yunnan and Fujian origins were superior, and the chromatographic peaks 2, 5 (LLL), 8 and 11 (OOP) obtained by screening were the main components that caused the quality differences offrom different origins; the herbs offrom different origins complied with the standards of moisture, ash and leachate in the 2020 edition of the; meanwhile, the results of multi-component quantitative determination showed that there were significant differences between the seven index components.The study established the UPLC fingerprints of 15herbs from different origins and their content determination methods, and combined with UPLC fingerprints, chemical pattern recognition, and multi-indicator component content determination for further research, which can provide a reference for the comprehensive evaluation of the quality ofherbs.
; UPLC fingerprint; chemical pattern recognition; trilinolein; 1,2-dilinoleoyl-3-palmitoyl-glycerol; 1,2-dilinoleoyl-3-oleoyl-glycerol; 1-palmitoyl-2-oleoyl-3-linoleoyl-glycerol; 1,2-dioleoyl-3-linoleoyl-glycerol; 1,2-dioleoyl-3-palmitoyl-glycerol; triolein;quality evaluation
R286.2
A
0253 - 2670(2024)08 - 2755 - 09
10.7501/j.issn.0253-2670.2024.08.024
2023-11-05
中央本级重大增减支项目“名贵中药资源可持续利用能力建设项目”(2060302)
高 童,女,硕士,研究方向为中药资源与鉴定。E-mail: 1019490241@qq.com
通信作者:梁宗锁,男,教授,博士生导师,主要从事药用植物次生代谢研究。E-mail: liangzs@ms.iswc.ac.cn
黄文丽,女,副教授,主要从事中药化学药效物质基础研究。E-mail: heng_long531@163.com
[责任编辑 时圣明]

