冠状动脉钙化积分、血压变异性对维持性血液透析患者动静脉内瘘的影响#
刘龙云肖丽群胡君刘鸿颖胡远松
(1. 赣南医学院第三附属医院内科,江西 赣州 341000;2. 赣南医学院第一附属医院消毒供应中心,江西 赣州 341000)
慢性肾脏病属于全球主要的非传染性病变之一,通常具有起病隐匿、并发症发生率高等特征,对人类生命健康具有重大威胁。其中终末期肾脏病患者需要采取长期血液透析治疗,血液透析机制为通过将患者体内血液引流值体外,以透析其清除体内毒素以及代谢废物,维持电解质、酸碱平衡,进而挽救患者生命,延长患者生存期。
自体动静脉内瘘(AVF)为该类患者透析的主要血管通道,相较于外周静脉导管以及人工血管具有优势[1]。因此AVF 的使用寿命以及质量与血液透析患者的生存期以及透析效果息息相关。而患者在透析中其AVF 功能可出现障碍,主要包括近瘘口部位狭窄或血栓形成等,将直接影响患者干预效果,不利于患者预后[2]。研究显示[3],维持性血液透析(MHD)患者通常年龄较大,血管弹性较差,且透析中钙磷元素堆积于血管壁极易导致血管钙化,因此可增加患者血栓发生率。此外透析通路与患者血流动力学因素有关,因此血压变化可能导致患者AVF 功能障碍[4]。考虑MHD 患者血管钙化以及血压变化可能与AVF 功能存在关联。鉴于此,本研究分析70 例MHD 患者资料,分析冠状动脉钙化(CAC)积分以及BPV 水平与AVF功能的关系,旨在为临床提供决策依据。
1 资料与方法
1.1 研究对象
选取2023 年1 月~2023 年8 月收治的70 例于赣南医学院第三附属医院接受MHD 的患者为研究对象。纳入标准:(1)年龄≥18 岁;(2)患有慢性肾脏病且初次建立内瘘;(3)患者以自体AVF 为血管通路;(4)透析时间≥3 个月;(5)无冠状动脉CT 血管造影(CTA)禁忌症。(6)患者及家属签署知情同意书。排除标准:(1)合并恶性肿瘤者:(2)接受腹膜透析者;(3)合并其他重要脏器功能障碍者;(5)合并凝血功能障碍者;(6)合并免疫系统疾病者;(7)肾移植者。脱落标准:(1)患者依从性较差,无法配合研究;(2)研究期间患者采用其他方式治疗。本研究经本院伦理委员会批准通过。70 例患者在研究中无脱落,依据内瘘功能障碍标准分组,其中35 例发生AVF 功能障碍患者纳入观察组,35 例未发生AVF 功能障碍纳入对照组。内瘘功能障碍[5]:临床听诊内瘘杂音消失;患者透析过程中内瘘流量持续<200 mL·min-1;触摸内瘘处脉搏较弱或消失;超声检查显示吻合口或附件头静脉、贵要静脉狭窄。
1.2 方法
(1)一般资料收集:查阅患者病历,收集患者性别、年龄、身体质量指数(Body Mass Index,BMI)、原发病等资料,并统计患者透析龄。(2)血液指标检查:采用贝克曼DXC 全自动生化分析仪测定患者血磷、血红蛋白、血肌酐水平。(3)冠状动脉钙化(CAC)积分:患者接受CTA 检查,采用多层螺旋CT 扫描患者心脏,并采用横断位预想测量,选取其中质量较好图像。将CT 值130Hu 以上判断为具有钙化,测得钙化区域面积需在0.5 mm 以上,130 Hu~199 Hu 钙化灶定为CT 值1 分,200~299 Hu 为2 分,300~399 Hu为3 分,400 Hu 为4 分,各区域CT 分值与钙化面积的乘积即为各钙化灶积分,积分累加则为CAC 积分。(4)血压变异性(BPV):在患者接受血液透析过程中采用心电监护仪监测血压变化,分别于透析开始时、透析第1 h、2 h、3 h、4 h 各测定一次血压,收集12 次透析共60 次血压数据,依据血压变异性公式[6],计算BPV。
1.3 统计学方法
采用SPSS25.0 软件进行数据统计与分析,符合正态分布或近似正态分布计量资料采用均值±标准差(±SD)表示,比较采用t 检验;计数资料使用例(%)表示,组间比较使用χ2检验;MHD 患者AVF功能的影响因素采用多因素Logistic 回归分析,指标对AVF 功能障碍的预测价值采用受试者工作特征(ROC)曲线分析;以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者临床资料比较
观察组患者透析龄、血磷、血红蛋白、血肌酐、CAC 积分以及BPV 水平显著高于对照组(P<0.05)。见表1。
表1 两组患者临床资料比较[±SD,例(%)]
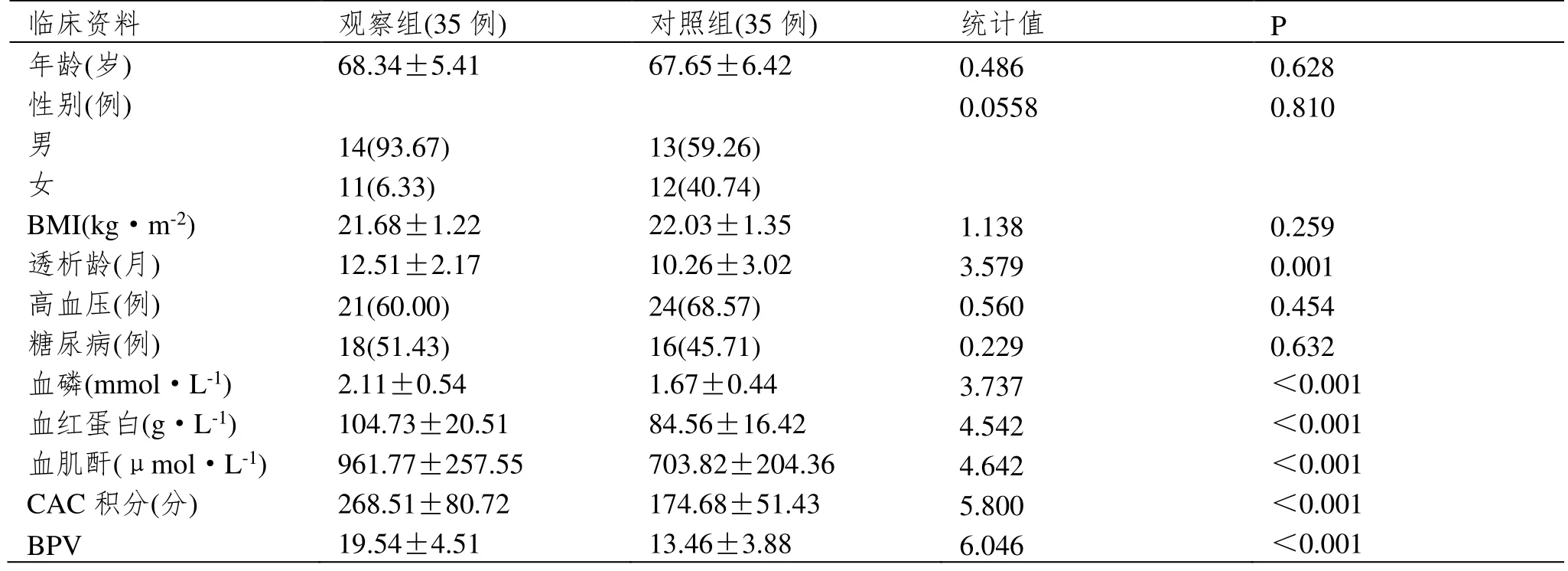
表1 两组患者临床资料比较[±SD,例(%)]
?
2.2 MHD 患者AVF 功能的多因素Logistic 回归分析
以患者AVF 功能情况(未发生功能障碍=0,功能障碍=1)为因变量,以透析龄、血磷、血红蛋白、血肌酐、CAC 积分以及BPV 为自变量行多元Logistic回归分析,结果显示透析龄、血磷、血红蛋白、血肌酐、CAC 积分以及BPV 均为AVF 功能的影响因素(P<0.05)。见表2。
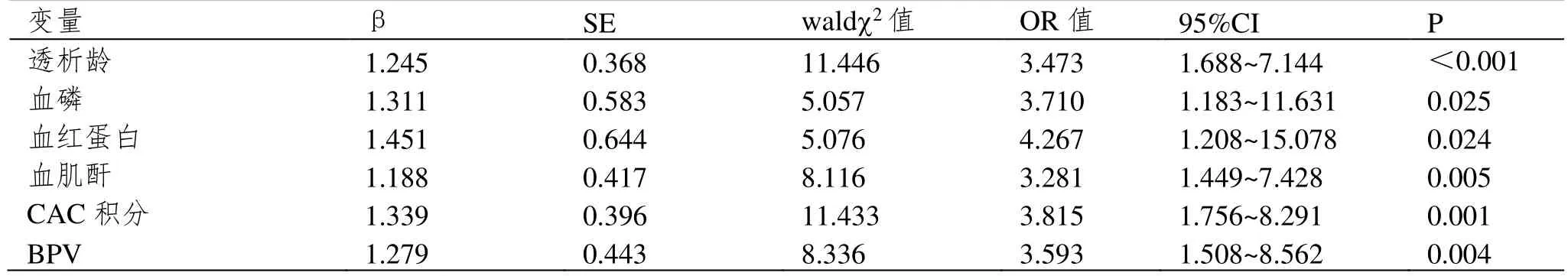
表2 MHD 患者AVF 功能的多因素Logistic 回归分析
2.3 CAC 积分、BPV 对MHD 患者AVF 功能障碍的预测价值
CAC 积分以及BPV 预测MHD 患者AVF 功能障碍的ROC 曲线下面积(AUC)为0.860、0.868,临界值为246.45 分、17.03,敏感度为94.29%、88.57%,特异度为71.43%、80.00%。见表3。
3 讨论
血液透析主要是通过将患者血液引流,并利用透析器交换患者血液以及透析液间物质,进而实现清除代谢物、维持电解质以及酸碱平衡等作用[7]。因此血液透析患者血管通透至关重要,而AVF 使目前透析效果最佳的血管通路。目前,随着临床医疗技术水平的快速发展,血液透析患者生存其也逐渐延长。
但相关研究显示[8],血液透析患者并发AVF 功能障碍发生率明显增加,而AVF 功能障碍也是透析失败的重要原因之一。血管钙化为MHD 患者常见并发症之一,主要由于处于终末期的肾脏病患者存在较严重的骨代谢失衡以及矿物质代谢失衡,因此MHD 患者常存在不同程度的血管、内膜钙化,而在接受透析后这一进程将加快[9]。研究显示[10],血管钙化可影响AVF 功能。此外,在陈迎归[11]研究中发现BPV 可对透析患血管通路功能产生影响。本研究着重从以上两方面进行研究得到确切结论。
本研究结果显示,观察组透析龄、血磷、血红蛋白、血肌酐、CAC 积分以及BPV 水平显著高于对照组;提示出现AVF 功能障碍的维持性透析患者存在上述多种指标的异常。因此进一步对上述差异指标进行多因素Logistic 回归分析显示,透析龄、血磷、血红蛋白、血肌酐、CAC 积分以及BPV 均为AVF 功能的影响因素。分析上述原因:透析龄较长的患者接受透析时间长,由于透析液中磷等成分长期摄入,导致患者血管壁极易沉积磷、钙等元素,因此患者血管壁易被堵塞,进而促进血管钙化形成;而血管钙化可导致血管僵硬,血管充盈减少,因此透析流量不足,进而导致血肌酐水平升高[12-13]。相关研究发现[14],较低的血红蛋白有利于AVF 发育,其机制可能在于在缺血缺氧状态下,一氧化氮合成升高,促进血管舒张;而当血红蛋白升高则代表血管舒张相对较弱,因此更易出现AVF 功能障碍。血管钙化由于患者血管壁堆积大量钙、磷元素,极易导致AVF 口近端堵塞或产生血栓,进而导致AVF 功能障碍。此外相关研究显示[15],较高的BPV 可导致透析中泵前压与泵孔血流速比值变异,进而反馈出剪切力对血管内皮可造成影响;血管内皮功能受损可导致患者炎症加重,动脉粥样硬化改变,而BPV 较大者可导致多种血管效应被激活,导致血管壁重构,进而导致动脉粥样硬化;而透析患者原本存在静脉内膜增生风险,在上述条件下风险增高,因此发生AVF 功能障碍风险也随之增高。本研究进一步对CAC 积分、BVP 对MHD 患者AVF功能障碍的预测效能发现,CAC 积分以及BPV 预测MHD 患者AVF 功能障碍AUC 为0.860、0.868,均具有良好预测效果。
综上所述,AVF 功能障碍的MHD 患者通畅具有透析龄较长,血磷、血红蛋白、血肌酐水平、CAC 积分以及BPV 较高等特征,其中CAC 积分以及BPV对MHD 患者AVF 功能障碍具有良好的预测效果。

