经皮血氧监测及远端灌注管在静脉-动脉体外膜肺氧合急性肢体缺血并发症中的应用价值
路 坤,朱森燚,陈真真,吴 强,汪华学
(蚌埠医科大学第一附属医院 重症医学科,安徽 蚌埠 233004)
静脉-动脉体外膜肺氧合(venoarterial extracorporeal membrane oxygenation,VA-ECMO)主要用于各种原因导致的难治性心源性休克病人[1]。随着经皮穿刺技术的进步及超声引导的使用,股动静脉经皮置管已成为VA-ECMO最常用的置管方式。但由于循环衰竭及股动脉插管的闭塞作用,病人存在下肢灌注不良甚至缺血的风险。有研究[2-4]显示,急性肢体缺血(acute limb ischemia,ALI)是VA-ECMO常见的血管并发症,且与死亡率增加相关。即使进行了积极的筋膜切开减压术,其仍然与高住院死亡率相关[5]。近年来研究[6-8]显示远端灌注管(distal perfusion catheter,DPC)的缺失是ALI的独立危险因素,预防性放置DPC可以减少ALI的发生,但并不能完全避免。但也有研究[9-10]认为预防性放置DPC并不能减少ALI的发生,反而可能会导致或加重相关并发症,建议DPC仅用于治疗ALI。ALI轻者可能遗留有肢体功能障碍,重者将会导致截肢,甚至死亡,因此,如何早期发现肢体灌注不足并及时干预,防止产生不可逆的肢体损伤是值得研究的重要内容。经皮血氧监测可以无创、快速、持续监测皮肤组织的经皮氧分压(transcutaneous oxygen pressure,PtcO2)和经皮二氧化碳分压(transcutaneous carbon dioxide pressure,PtcCO2)可以用来反映局部组织灌注水平[11]。但目前该技术在VA-ECMO肢体缺血并发症中的应用研究极少。因此,本研究通过对VA-ECMO病人实施下肢经皮血氧监测,发现PtcO2、PtcCO2在ALI方面的预测价值,以及进一步明确DPC在ALI中的应用价值,现作报道。
1 资料与方法
1.1 研究对象
选择2021年1月至2023年10月接受蚌埠医科大学第一附属医院重症医学科VA-ECMO治疗的50例病人作为研究对象。其中男31例,女19例,平均年龄(55.80±15.15)岁。原发疾病:急性心肌梗死19例,暴发性心肌炎13例,心脏术后低心排综合征9例;其他9例;ECMO运行时间(128.40±37.86)h。根据有无发生ALI,分为缺血组(n=15)和未缺血组(n=35)。ALI的诊断主要依靠临床表现和血清生化标志物(肌酸激酶、肌红蛋白)[12],具体包括动脉置管侧肢体较对侧肢体是否出现苍白、皮温发凉、花斑、肢体肿胀、关节活动度下降、足背动脉搏动减弱或消失、毛细血管再充盈时间明显延长(>4.5 s)等。本研究遵循赫尔辛基宣言和中国有关临床试验研究的法规,经蚌埠医科大学第一附属医院伦理委员会审查通过(伦科批字〔2022〕第153号),取得病人或近亲属知情同意并签署知情同意书。
1.2 纳入及排除标准
纳入标准:(1)年龄≥18岁;(2)接受股动静脉置管的VA-ECMO治疗;(3)早期置入DPC。排除标准:(1)置管时即出现严重血管并发症,如大出血、动脉夹层、动脉撕裂等;(2)其他ECMO模式及血管入路;(3)既往有下肢动脉闭塞症及缺血表现;(4)存在经皮血氧监测禁忌,如皮肤溃烂、过敏、瘢痕或重度水肿等;(5)临床资料缺失;(6)经皮血氧监测未完成,放弃治疗。
1.3 研究方法
1.3.1 VA-ECMO置管方式 所有病人在接受VA-ECMO治疗时,血管入路均选择股动静脉。在置管前常规进行超声检查,明确血管有变异、钙化、狭窄等病变,以及测量血管直径。根据血管条件选择合适的插管,静脉插管直径为20F或21F,动脉插管直径为15F、16F、17F,DPC使用直径为6F动脉鞘管。ECMO静脉引流管首选从右侧股静脉进入,动脉回输管从左侧股动脉置入,动静脉插管置于病人两侧肢体,但必要时动静脉插管也可置于病人一侧肢体。所有置管方式均在床旁超声引导直视下采用改良Seldinger法置入,置管顺序为静脉引流管、DPC、动脉回输管。在体外心肺复苏时,因需要尽快恢复组织灌注,可以先置入动脉回输管再及时置入DPC。DPC置入后予以肝素盐水封管,暂时不接入ECMO环路。
1.3.2 经皮血氧监测 VA-ECMO转机成功后,使用丹麦雷度公司经皮血氧监测仪(TCM4),选择动脉插管侧小腿内侧为探测器测定部位,局部加热平衡10~15 min,待读数逐步稳定后,记录基础PtcO2、PtcCO2,然后立即行氧负荷试验(oxygen challenge test,OCT),ECMO氧体积分数由50%增加至100%,记录增氧10 min后PtcO2、PtcCO2,10 min-OCT值=OCT后PtcO2-基础PtcO2。然后密切监测病人ALI临床表现,考虑到病人安全,需每小时至少观察1次病人下肢情况,并详细记录,最长观察时间为3 h,根据观察期间有无肢体缺血表现分为缺血组和未缺血组。记录病人有缺血表现时PtcO2、PtcCO2,未缺血组记录第3小时PtcO2、PtcCO2。当观察到有肢体缺血表现时,及时接入DPC增加下肢血供,未缺血组为预防晚期肢体缺血的发生,在第3小时将DPC接入至ECMO环路。在DPC开始供血1 h后,再次记录PtcO2、PtcCO2及肢体缺血情况。
1.4 观察指标
除记录PtcO2、PtcCO2外,同时记录病人性别、年龄、体质量指数、病因、基础疾病、ECMO持续时间、置管部位、插管型号、乳酸水平、APACHE Ⅱ评分、SOFA评分等基线资料,以及2组病人的撤机成功率及撤机后28 d存活率。
1.5 统计学方法
采用t检验、χ2检验及受试者工作特征曲线(ROC曲线)。
2 结果
2.1 一般资料
2组病人在年龄、性别、体质量指数、原发病、基础疾病、置管部位、ECMO持续时间、插管型号、乳酸水平、APACHE Ⅱ评分、SOFA评分、撤机成功率、28 d存活率方面差异均无统计学意义(P>0.05)(见表1)。

表1 研究对象的一般资料比较
2.2 OCT前后2组病人PtcO2、PtcCO2及10 min-OCT比较
2组病人在OCT前基础PtcO2、PtcCO2比较差异均无统计学意义(P>0.05);2组病人在OCT后PtcO2和10 min-OCT比较差异均有统计学意义(P<0.01),但PtcCO2比较差异无统计学意义(P>0.05);缺血组病人在OCT前后PtcO2、PtcCO2比较差异均无统计学意义(P>0.05);未缺血组病人在OCT前后PtcO2比较差异有统计学意义(P<0.01),PtcCO2比较差异无统计学意义(P>0.05)(见表2)。
表2 OCT前后2组病人PtcO2、PtcCO2及10 min-OCT比较
2.3 DPC接入前后2组病人PtcO2、PtcCO2比较
2组病人在DPC接入前PtcO2、PtcCO2比较差异均有统计学意义(P<0.01);2组病人在DPC接入后PtcO2、PtcCO2比较差异均无统计学意义(P>0.05);缺血组病人在DPC接入前后PtcO2、PtcCO2比较差异均有统计学意义(P<0.01);未缺血组病人在DPC接入前后PtcO2、PtcCO2比较差异均无统计学意义(P>0.05)(见表3)。
表3 DPC接入前后2组病人PtcO2、PtcCO2比较
2.4 不同指标对VA-ECMO病人ALI的预测价值
通过ROC曲线分析显示,10 min-OCT、 OCT后PtcO2、DPC接入前PtcO2和PtcCO2的ROC曲线下面积(AUC)分别为0.945(95%CI:0.934~1.000)、 0.904(95%CI:0.821~0.987) 、0.939(95%CI:0.870~1.000) 、0.874(95%CI:0.766~0.983)(见表4),均具有较好的预测价值,并对上述4个指标ROC曲线进行两两比较差异均无统计学意义(P>0.05)(见图1)。
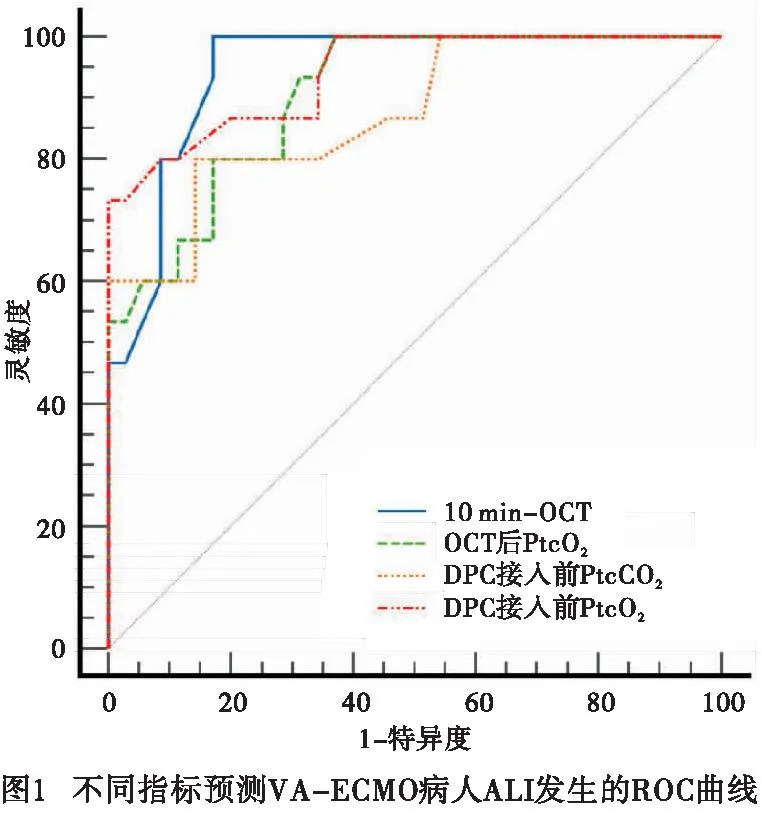
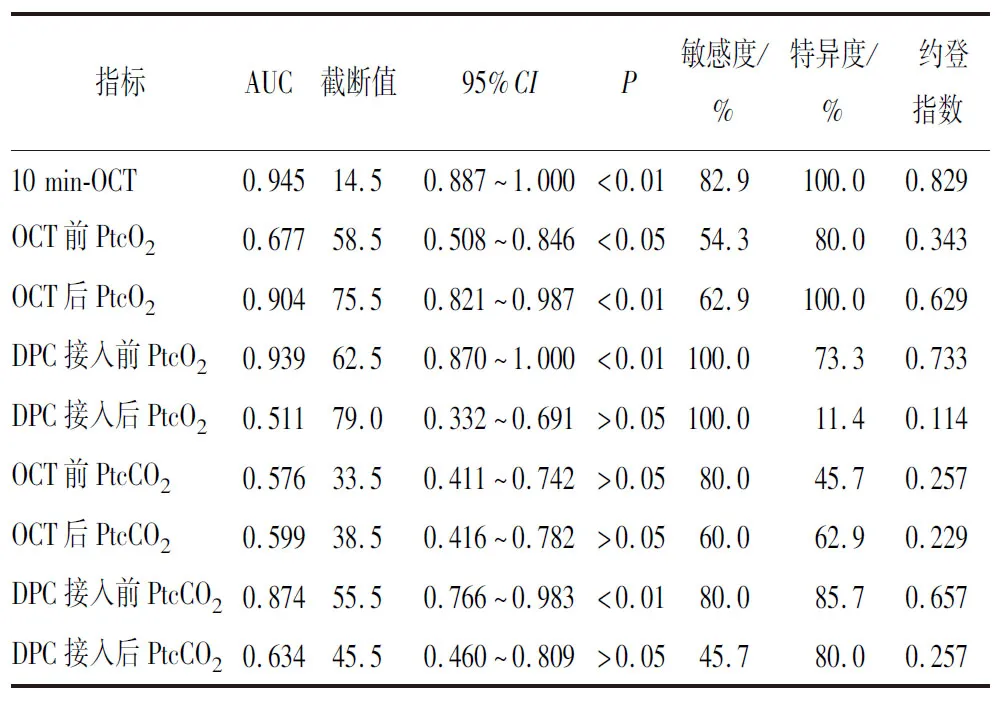
表4 不同指标对VA-ECMO病人ALI发生的预测价值
3 讨论
近年来VA-ECMO在临床中的应用越来越多[13],但相关血管并发症的发生率仍然较高[2,14]。BLAKESLEE-CARTER等[2]研究显示在所有类型的ECMO中,有23.6%(54/229)病人的血管并发症需要接受血管外科手术治疗,其中ALI是最常见的并发症,整体发生率为16.5%(38/229),但在外周VA-ECMO中ALI发生率高达22.8%(26/114),并与住院生存率降低相关。本研究中ALI的发生率为30.0%(15/50),较该研究结果略高。想要避免ALI并发症造成的严重不良后果,需要早期发现、诊断及干预。6P综合征是ALI的典型临床表现,主要包括疼痛、苍白、无脉、感觉异常、肢体发凉和运动障碍,临床上常采用卢瑟福分级系统从感觉、运动、血流多普勒信号三个方面对ALI进行分级[15]。但对于VA-ECMO病人,这些指标具有一定的局限性,不利于ALI早期诊断。如VA-ECMO的非搏动性血流可能会导致远端动脉搏动减弱或消失,难以进行脉搏检查,也影响血流多普勒检查的准确性;VA-ECMO病人早期常需较深的镇痛镇静,导致对疼痛、感觉及运动的检查受限;此类病人因严重的心源性休克及血管活性药物的使用,外周肢体往往变得更冷,导致皮温检查受限,且这些指标存在一定的滞后性和主观性影响。在这些情况下,需要一种更灵敏的工具来检测早期ALI,因此,在中国成人经股动脉 VA-ECMO 治疗期间下肢缺血防治专家共识中推荐流程化监测下肢血供,建议使用经皮血氧监测仪持续监测下肢灌注情况[16],但并未给出监测方案的具体步骤及判断ALI的具体标准。
PtcO2、PtcCO2监测在临床中的应用已有几十年,其原理是通过特殊电极对皮肤加热,皮肤毛细血管床血供增加,氧和二氧化碳进而从毛细血管中弥散出来,扩散到皮下组织、皮肤,被电极监测到。研究[17-18]表明PtcO2和PtcCO2的变化呈血流依赖性,可用于反映脓毒症休克时微循环障碍、监测液体复苏疗效及判断预后。潘飞艳等[19]回顾性研究发现经皮氧分压用于预测病人发生下肢缺血的截断值为67.5 mmHg,AUC为0.937,具有较高诊断效能,但该研究没有对ALI的诊断标准及PtcO2、PtcCO2监测数据采集时间点进行描述,导致其临床应用受限。本研究详细描述了经皮血氧监测方案同时进行了OCT,研究结果表明缺血组病人由于血流受限,在OCT前后PtcO2、PtcCO2比较差异无统计学意义,而未缺血组病人在OCT后PtcO2升高明显,间接说明未缺血组病人下肢存在足够的血流,导致2组病人在OCT后PtcO2、10 min-OCT比较差异有统计学意义。通过ROC曲线判别分析发现OCT后PtcO2、10 min-OCT、DPC接入前PtcO2和PtcCO2对ALI的发生具有重要预测价值,且预测效能接近,但由于DPC接入前PtcO2和PtcCO2指标的延迟性,早期OCT可以将ALI发现时间提前,有利于ALI的早期诊断。同时经皮血氧监测的无创性和持续性,可作为ALI临床症状和体征的补充,在一定程度上可以减少医护工作量。
研究[20]显示急性筋膜室综合征引起的缺血可在创伤后3 h内引起肌肉坏死。本研究对ALI的观察时间窗设为3 h,研究期间一旦发现病人存在肢体灌注不足的症状及体征,立即予以DPC接入环路,增加下肢血供。通过比较DPC接入前后PtcO2、PtcCO2的变化,可以发现缺血组病人PtcO2明显下降、PtcCO2明显增高。当开通DPC增加下肢血流后,PtcO2、PtcCO2可逐渐恢复正常,缺血的临床表现好转。研究中所有病人均未因ALI进行筋膜切开减压术或截肢手术,且2组病人ECMO撤机成功率及28 d存活率相似。说明DPC对VA-ECMO病人下肢血供恢复起到重要作用,可用于预防和治疗ALI。尽管仍有研究[9-10]表明DPC的预防放置会增加血流感染和出血,其被用于ALI的治疗而不是预防,但更多的研究[6-8,21-22]表明DPC是预防ALI的保护因素,近年DPC已作为ALI的标准预防手段写入国内外VA-ECMO指南[1,16]。结合本研究ALI的高发病率及DPC改善灌注的明确作用,同时考虑到ALI的严重后果及DPC后期放置的技术难度,建议在VA-ECMO置管期间常规放置DPC。
本研究不足之处:首先,研究时间较短,未对病人晚期ALI的发病原因进行统计分析;其次,由于仪器原因,未同时监测病人双侧下肢PtcO2、PtcCO2水平,以进一步发现双侧肢体的差异;再则,未同时采集病人动脉血行血气分析,探讨血气指标和PtcO2、PtcCO2比值对ALI的预测价值;最后,本研究为单中心研究,纳入样本量有限,需要进一步的研究来验证截断值的准确性。
综上所述,经皮血氧监测可以作为VA-ECMO病人并发ALI的有效监测手段,通过OCT可以更早地识别出ALI的发生。DPC可以明显改善VA-ECMO病人的下肢血供,建议在ECMO置管时常规放置。

