克癀胶囊治疗非酒精性脂肪性肝炎小鼠药效学研究*
李晓静 刘雅茹 李 冉 涂天智△ 胡义扬,3,4△
1.上海中医药大学附属曙光医院肝病研究所 (上海, 201203) 2.科兴生物制药股份有限公司 3.上海市中医临床重点实验室4.肝肾疾病病证教育部重点实验室
随着全球代谢综合征、糖尿病和肥胖的增加,非酒精性脂肪性肝病(NAFLD)的患病率也在急剧上升,据估计其全球患病率约为25%[1]。NAFLD的疾病谱包含非酒精性肝脂肪变性、非酒精性脂肪性肝炎(NASH)、肝硬化和肝细胞癌[2]。NASH是NAFLD 的严重类型,其特征是一种以肝脂肪变性、肝细胞损伤、炎症和纤维化为组织学特征的慢性肝病,而NASH合并纤维化患者可能会进展为肝硬化、门静脉高压或肝细胞癌[3]。虽然在疾病流行病学、发病机制和治疗靶点的了解方面取得了稳步进展,但在治疗领域进展缓慢。目前还没有美国食品药品监督管理局(FDA)获批的治疗NASH的特定药物,NASH治疗的药物研究仍是国际热点[4]。
克癀胶囊主要成分有三七、黄连、黄芩、黄柏、大黄、山银花、人工牛黄及麝香等十六味中药组成,有清热解毒、活血利湿、化瘀散结之功效,主要应用于急慢性肝炎的湿热内蕴、瘀血内阻证。临床研究显示克癀胶囊对急性肝炎和慢性肝炎具有良好的疗效[5]。前期运用高脂饮食诱导的NAFLD大鼠模型,发现克癀胶囊对NAFLD大鼠肝脏病变程度、血清TC及LDL-C水平具有改善作用[6]。为进一步明确克癀胶囊药效,本实验运用高脂饮食高糖饮水(HFHS)诱导的NASH小鼠,观察克癀胶囊治疗NASH的作用,以期为临床推广应用奠定基础。
1 材料与方法
1.1 实验动物 SPF级C57BL/6J雄性小鼠60只,体重21~25 g,购自上海吉辉实验动物有限公司,动物生产许可证编号:SCXK(沪)2012-0014,实验动物使用许可证编号:SYXK(沪)2021-0005。小鼠饲养于上海中医药大学实验动物中心,适应性饲养1周,观察无异常后开始实验。
1.2 实验药物与试剂 克癀胶囊(深圳市同安药业有限公司,批号191108),奥贝胆酸(阳性对照药,Med Chem Express公司,批号61353)。甘油三酯(TG)试剂盒(货号:F001-1-1),丙氨酸氨基转移酶(ALT)试剂盒(货号:C009-2-1),天冬氨酸氨基转移酶(AST)试剂盒(货号:C010-2-1),γ谷氨酰转移酶(GGT)试剂盒(货号:C017-2-1),HE染色试剂盒(货号:D006-1-3),油红O试剂盒(货号:D027-1-3),均购自南京建成生物工程研究所;血糖试纸购自罗氏诊断产品有限公司(货号:220811);血清胰岛素ELISA试剂盒购自Crystal chem 公司(货号:90080)。
1.3 主要仪器 酶标仪(TECAN公司),石蜡包埋机(Lecia公司),冷冻离心机(Sigma公司),荧光倒置显微镜(Olympus公司),7020全自动生化分析仪(HITACCHI公司)。
1.4 动物造模、分组及药物干预 60只SPF级C57BL/6J雄性小鼠,随机分为正常组(Ctrl组)10只和高脂高糖组50只。正常组予以对照饲料(Research diet 12450J),饮用双蒸水;高脂高糖组予以高脂饲料(Research diet 12492i),饮用浓度为42 g/L的糖水(糖水配比为55%果糖和45%蔗糖),造模12周。
12周末将高脂高糖组分为模型组(HFHS组),克癀胶囊低、中、高剂量组(KL、KM、KH组),奥贝胆酸组(OCA组),每组10只。造模第13周首日开始给药,克癀胶囊低、中、高剂量组小鼠分别灌胃0.5、1、2 g/kg克癀胶囊溶液,奥贝胆酸组小鼠灌胃10 mg/kg奥贝胆酸溶液,以上药物均以0.4%的羧甲基纤维素钠溶液配制,用药组小鼠予以相应药物,灌胃体积为0.1 ml/10 g,1次/d,连续6周干预。正常组和模型组小鼠分别给予等体积的0.4%羧甲基纤维钠溶液。
1.5 检测指标及方法
1.5.1 肝组织TG含量 称取小鼠肝组织(50±2 mg),使用无水乙醇丙酮提取肝组织中TG,运用TG检测试剂盒检测肝组织中TG含量,实验操作步骤参考试剂盒说明书。
1.5.2 血清ALT,AST和GGT活性检测 采用ALT、AST和GGT检测试剂盒检测。
1.5.3 血清TG、TC及HDL-C、LDL-C、FFA检测 将各组小鼠血清样本各取120 μl送至上海中医药大学附属曙光医院检验科协助检测,检测血清TG、TC、LDL-C、HDL-C、FFA水平。
1.5.4 胰岛素抵抗指数 实验结束当天,小鼠禁食12 h,换用正常水,处理小鼠时取3 μl血液滴于血糖试纸上,通过血糖仪测得小鼠的空腹血糖(FBG)。通过胰岛素ELISA试剂盒测定空腹胰岛素(INS)。HOMA-IR=(FBG 测量值*INS 测量值)/22.5。
1.5.4 肝组织HE染色 选取肝大叶,修剪肝组织为0.5 cm×0.5 cm×0.2 cm大小的2块方块,置于10%中性甲醛缓冲液固定72 h后,行脱水、包埋、切片、HE染色处理,并进行NAS评分分析(表1)。

表1 非酒精性脂肪性肝病NAS评分
1.5.5 肝组织油红O染色 选取肝大叶,修剪肝组织为0.5 cm×0.5 cm×0.2 cm大小的方块,置于OCT胶中,-80℃保存。将肝组织用冰冻切片机切成6~10 μm厚度。油红O染液中(加盖),密闭染色10~15 min。甘油明胶封固,显微镜下观察切片组织病理改变及拍照。

2 结果
2.1 克癀胶囊对小鼠一般状态及肉眼肝脏形态的影响 对每组小鼠的大体外观和肝脏外观进行拍照,并用肉眼观察组间差异。Ctrl组小鼠形体匀称,体宽3~4 cm。HFHS组小鼠体形圆润,肥胖,体宽5~5.5 cm;克癀胶囊治疗组小鼠体宽约4 cm,各剂量组间肉眼观察无明显差异(图1A)。Ctrl组小鼠肝脏呈暗红色,质地柔软。HFHS组小鼠肝脏体积较大、油腻,表面呈颗粒状,肉眼可见黄白色局灶性脂肪沉积。克癀胶囊治疗组小鼠肝脏呈暗红色,体积显著缩小,质地柔软(图1B)。动态检测各组小鼠的体重,与Ctrl组小鼠相比,从第2周开始,HFHS组小鼠体重显著升高(P<0.05)(图1C)。与Ctrl组小鼠相比,HFHS组小鼠每日卡路里摄入量和体重显著升高(P<0.01)。与HFHS组小鼠相比,各药组小鼠进食总热量及体重无差异(表2)。

图1 各组小鼠一般状态记录 (A)小鼠大体外观,(B)小鼠肝脏形态,(C)小鼠体重记录

表2 各组小鼠进食总热量及终末体重比较
2.2 克癀胶囊对小鼠肝脏指数的影响 与Ctrl组相比,HFHS组小鼠肝重显著增加(P<0.01)。用药治疗8周后,各组小鼠肝重、脾重及肝体比无显著差异(P>0.05)(表3)。

表3 各组小鼠肝脏指数比较
2.3 克癀胶囊对小鼠肝脏TG含量的影响 与Ctrl组小鼠相比,HFHS组小鼠肝脏TG含量显著升高(P<0.01),与HFHS组小鼠相比,KL,KM,KH组小鼠肝脏TG含量显著降低(P<0.05,且对肝脏TG含量的改善作用具有剂量依赖性趋势(表4)。

表4 各组小鼠肝组织TG含量比较
2.4 克癀胶囊对小鼠肝组织病理学影响 肝组织病理染色结果见图2。H&E染色结果(200 ×)显示,Ctrl组小鼠肝小叶结构清晰,肝索排列整齐;HFHS组小鼠肝细胞出现明显的弥漫性肿胀、脂肪变性,胞浆内大小不一的脂滴,部分汇管区、小叶内可见炎细胞浸润;克癀胶囊及OCA组小鼠肝索排列较整齐,胞浆内脂滴明显减少,脂肪变性和炎性细胞浸润均有所减轻,气球样变性较少见。同样,克癀胶囊各用药组小鼠的肝脂肪变性评分、小叶炎症评分、气球样变化评分均显著低于HFHS组小鼠(表5)。

表5 各组小鼠NAS评分比较
2.5 克癀胶囊对小鼠血清肝功能的影响 与Ctrl组小鼠相比,HFHS组小鼠血清ALT、AST活性均显著升高(P<0.01);与HFHS组小鼠相比,KL组和OCA组小鼠血清ALT和AST活性显著下降(P<0.05),KH组小鼠血清ALT活性显著下降(P<0.05)(表6)。

表6 各组小鼠血清肝功能比较
肝组织油红O染色结果(见图3)。Ctrl组小鼠肝组织仅有少量油滴均匀散在分布于肝细胞胞浆内;HFHS组小鼠肝细胞结构肿胀明显,肝细胞内呈弥漫性脂肪变性,肝细胞内见大量鲜红色脂滴;与HFHS组相比,克癀胶囊各剂量组及OCA组小鼠脂滴数量及大小均显著减少,散在分布于肝细胞胞浆内。
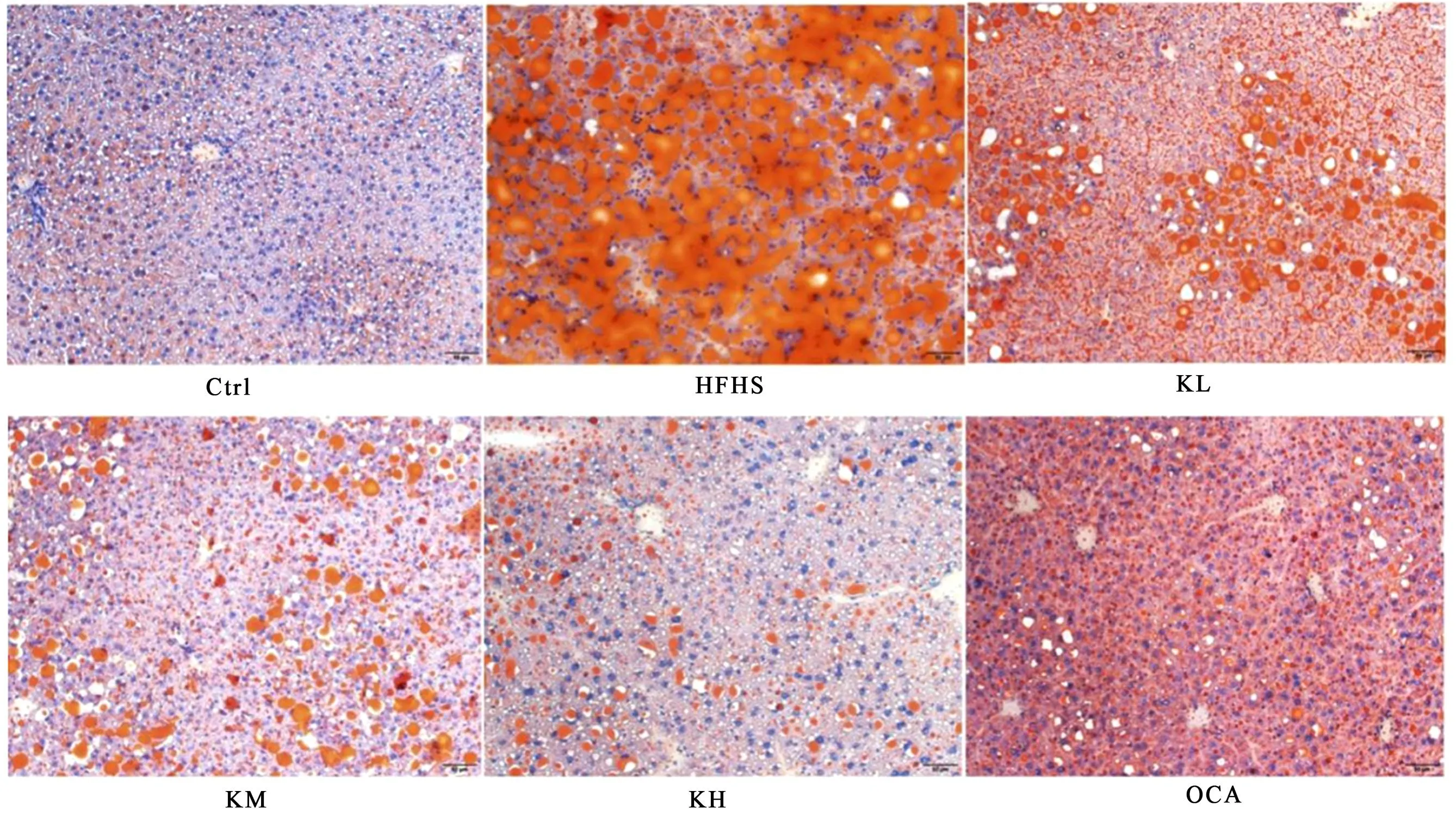
图3 各组小鼠肝组织油红O染色 染色观察(200×)
2.6 克癀胶囊对小鼠血清脂质含量的影响 与Ctrl组小鼠相比,HFHS组小鼠血清TC,HDL-C,LDL-C含量显著升高,FFA含量显著下降(P<0.01)。与HFHS组小鼠相比,KL组小鼠血清TC,HDL-C含量均显著下降,血清TG,FFA含量显著升高(P<0.05);KM组小鼠HDL-C含量显著下降(P<0.05)(表7)。

表7 各组小鼠血清脂质含量比较
2.7 克癀胶囊对小鼠糖代谢的影响 与Ctrl组小鼠相比,HFHS组小鼠FBG,FINS含量及HOMA指数均显著升高(P<0.01);与HFHS组小鼠相比,KM,KH组小鼠FBG水平显著下降(P<0.05)(表8)。

表8 各组小鼠胰岛素抵抗状态比较
3 讨论
NAFLD尤其是在中心性肥胖、Ⅱ型糖尿病、血脂异常和代谢综合征的患者中成为常见的慢性肝病之一。NAFLD人群普遍具有代谢综合征特征,并伴有相关的心血管疾病危险因素[7]。大多数肝脂肪变性患者的疾病是“非进行性”的,但也有一小部分患者发展为的NASH, 进而导致肝硬化甚至肝细胞癌[3]。因此寻求有效的防治NASH的药物十分重要。由于NASH是复杂的、系统性的疾病,这也提示针对单一靶点治疗的药物难以满足该疾病的治疗目标。中药复方具有多种成分、多个途径和多个靶点的作用特点,针对系统性疾病具有一定的优势和前景。目前没有FDA获批的治疗NASH的特定药物,但是在临床中,中医药广泛应用于NASH的防治[8]。中医认为NAFLD主要的病理基础为痰、湿、瘀、积[9]。NAFLD的证型分布也提示痰湿内阻证,湿热内蕴和痰瘀互结证是常见的证型[10]。因此灵活运用具有清热利湿、活血散瘀功效的中药方剂对NASH可有良好的改善作用。前期有动物实验提示具有清热利湿的经典名方三仁汤、活血化瘀功效的血府逐瘀汤等对NAFLD均有显著的改善作用[11,12]。克癀胶囊是一种已上市的中成药,主要适用于胁肋胀痛或刺痛,胁下痞块,口苦口粘,纳呆腹胀,面目黄染,小便短赤,舌质黯红或瘀斑、瘀点,舌苔黄腻,脉弦滑或涩等湿热毒邪内蕴、瘀血阻络证及急、慢性肝炎。克癀胶囊中三七为君药具有活血化瘀之功效,黄连、黄芩、黄柏等多味药物具有清热利湿之功效。选用克癀胶囊作为治疗NASH的中成药符合中医临床用药的原则。
本研究结果表明克癀胶囊对HFHS诱导的NASH小鼠模型有较好的改善作用。克癀胶囊在不影响NASH小鼠卡路里摄入总量的情况下,对于小鼠的体重增加有一定的抑制作用(P>0.05)。NASH是以肝脏脂质积累为主要特征的慢性肝脏疾病,改善肝脏脂质沉积是治疗NASH的首要任务。低、中、高剂量(分别相当于临床等效剂量的6.17、12.33、24.66倍)的克癀胶囊均可显著地降低NASH小鼠的肝脏TG含量(P<0.05),改善NASH小鼠肝脏病理变化、NAS评分(P<0.05),且具有剂量依赖性趋势。对于NASH小鼠的血清ALT、AST酶活性的影响,低剂量的克癀胶囊效果更为显著(P<0.05);中剂量克癀胶囊可显著改善血清HDL-C含量及FBG水平(P<0.05);而高剂量的克癀胶囊对降低小鼠血清ALT酶活性,血清TC、HDL-C、LDL-C含量及FBG水平效果更优(P<0.05)。这与之前高脂饮食诱导的NAFLD大鼠实验结果类似[6],提示针对临床NAFLD患者的异常指标,应调整最佳给药剂量。值得注意的是,在动物实验中观察到低剂量的克癀胶囊给药组小鼠血清中TG和FFA有升高情况,因此在后期临床试验中应密切关注患者的血脂情况。鉴于本次实验以克癀胶囊对NASH小鼠的药效学观察为主,该药的机制研究亟需进一步开展。
综上,克癀胶囊低、中、高剂量组(0.5 g/kg、1 g/kg、2 g/kg),分别相当于临床等效剂量的6.17、12.33、24.66倍,对高脂饮食高糖饮水诱导的小鼠NASH模型均具有不同程度的治疗作用,可为该药的临床推广应用提供实验依据。

