人参皂苷Rg3 脂质体制备工艺优化
赵秋凝,刘雪坤,武子敬,高 媛,李昭熙,刘成琳
(通化师范学院•吉林 通化•134002)
人参皂苷Rg3 属于人参稀有皂苷,主要存在于人参的炮制品红参和黑参中。人参皂苷Rg3 具有良好的抗肿瘤生物学活性[1]。国内研究发现人参皂苷Rg3能通过抑制长链非编码RNA -LINP1(lncRNA -LINP1)的表达,从而抑制胃癌细胞的增殖与迁移,并促进其凋亡,发挥抗癌作用,并且这种作用与Rg3 浓度成正比[2]。目前,市场上有关人参皂苷Rg3 的相关药品主要是参一胶囊。参一胶囊在提高癌症治疗效果的同时还具有补益作用,是癌症患者的常用药[3],具有效果好、副作用小的优点。
脂质体是由脂质双分子层所形成的封闭囊泡,囊泡内水相和双分子层内可以包裹不同类型的活性药物。与其他传统药物载体系统相比,脂质体基于纳米结构的特点,可改善药物渗透性和溶解性,提高难溶性药物口服生物利用度,通过包载活性药物来改善制剂体内外稳定性,提高疗效,减少毒副作用,改善患者顺应性[4-6]。脂质体经修饰后可以被动或主动靶向肿瘤部位,从而将药物有效递送至靶向部位[7]。通过对脂质体进行一定的结构修饰,如连接甘草次酸及其衍生物等靶头,可发挥配体-受体间的特异性结合作用,促进包载药物的脂质体主动靶向肝组织,提高生物利用度。这种利用配体-受体特异性结合的作用,可为主动靶向其他组织治疗相关疾病的药物递送研究提供参考[8]。因为人参皂苷Rg3 存在水溶性差,生物利用度低的缺点[9],所以利用脂质体材料具有两亲性的特点,可以考虑通过脂质体同时将脂溶性药物包覆,改善人参皂苷Rg3 的生物利用度[10]。本试验采用大豆卵磷脂和胆固醇为载体材料制备人参皂苷Rg3 脂质体,旨在提高人参皂苷Rg3 的生物利用度和其抗肿瘤的靶向性,为人参皂苷Rg3 剂型进行深入研究奠定基础。
1 材料与仪器
1.1 材料、仪器和试剂
1.1.1 材料
大豆卵磷脂(南京都莱生物科技有限公司);磷脂(天津博迪化工有限公司);人参皂苷Rg3(成都彼样生物科技有限公司)。
1.1.2 试剂
甲醇,乙腈,均为色谱纯(德国Merck 公司);磷酸(天津大茂化学试剂厂);水为娃哈哈纯净水。
1.1.3 仪器
赛默飞高效液相色谱仪(包括自动取样器、四元泵系统、紫外检测器、工作站);精密电子分析天平(天津天马恒基仪器有限公司)。
2 方法与结果
2.1 人参皂苷Rg3 脂质体供试品溶液的制备
采用薄膜分散法制备人参皂苷Rg3 脂质体,分别取Rg3 提取物、大豆卵磷脂和胆固醇,置烧杯中加15 mL 甲醇,超声溶解后,置梨形瓶中,旋蒸挥去溶剂,梨形瓶中形成均匀的薄膜后,加入适量pH=7.4 的PBS溶液,在一定温度的水浴中水化一段时间,取出冷却至室温,即得Rg3 脂质体。同法制备不加人参皂苷Rg3 原料药的空白脂质体。
2.2 包封率的测定
2.2.1 色谱条件
色谱柱:Ultimate Polar RP(250mm ×4.6mm,5μm);流动相:乙腈(A)-0.01%磷酸水(B)(50%;50%);柱温:30℃;检测波长:203nm;进样量:5 μL。
2.2.2 人参皂苷Rg3 对照品溶液的制备
精密称取10.01mg 对照品人参皂苷Rg3,加甲醇并转移到10mL 容量瓶中定容至刻度,即得人参总皂苷对照品溶液(1.001mg•mL-1)。
2.2.3 线性关系考察
精密吸取人参皂苷Rg3 脂质体对照品溶液2、5、10、15、20 μL,按“2.2.1”项下色谱条件,连续进样5次,记录不同进样量的对照品溶液峰面积,以进样浓度为横坐标,峰面积为纵坐标绘制标准曲线Y=59.784X-0.2659,R2=0.9997(n=5),人参皂苷Rg3 含量在0.2~2 μg 时线性关系最好,结果见图1。

图1 人参Rg3 对照品标准曲线图
2.2.4 供试品溶液的制备及包封率的测定
精密量取人参皂苷Rg3 脂质体1mL,置10mL 容量瓶中,加入适量甲醇溶解并稀释至刻度,摇匀,过0.45μL 微孔滤膜,测定脂质体中总的药物量(C总)。精密量取人参皂苷Rg3 脂质体2mL 溶液离心,取上清液0.2 mL 加入适量甲醇溶解并稀释至刻度,超声5 min 破乳,过0.45μL 微孔滤膜(C游离),计算包封率(EE)=C游离/C总×100%。
2.2.5 空白干扰试验
精密吸取对照品溶液、人参皂苷Rg3 脂质体、空白脂质体溶液各10 μL,按“2.2.1”项下色谱条件测定,结果载体对本品含量测定无干扰。详见图2。
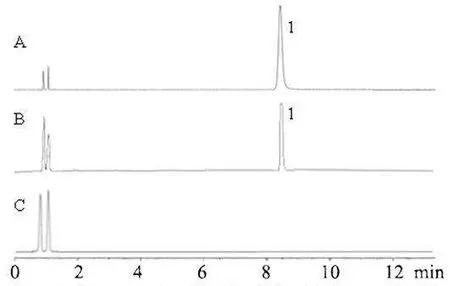
图2 人参皂苷Rg3 对照品(A)、人参皂苷Rg3 脂质体(B)、空白脂质体(C)HPLC 图谱
2.2.6 精密度试验考察
分别精密吸取同一供试品溶液10 μL,连续进样6 次,记录峰面积,计算RSD 值为0.89%,表明仪器精密度良好。
2.2.7 稳定性试验考察
分别精密吸取同一供试品溶液10 μL,分别在0、2、4、6、8、10 h 进样10 μL,记录峰面积,计算含量为0.141%,RSD 值为0.73%,表明供试品溶液稳定性良好。
2.2.8 重复性试验考察
取同一黑参样品,按“2.1”项下方法分别制备6 份,依次测定含量,记录峰面积,计算黑参中人参皂苷Rg3含量,RSD 值为0.88%,表明供试品溶液重复性良好。
2.2.9 回收率试验考察
精密称取6 份人参皂苷Rg3 脂质体1mL,分别置于10mL 容量瓶中,精密加入人参皂苷Rg3 对照品溶液,其余按脂质体制备和上述色谱条件依法测定,计算回收率,结果平均加样回收率为99.19%,RSD 值为1.32%,符合规定。
2.3 正交试验优化人参皂苷Rg3 脂质体
本实验以包封率为指标,脂质体选取人参皂苷Rg3 与大豆卵磷脂和胆固醇的质量比(A)、水化体积(B)作为考察因素。详见表1,试验设计及结果见表2,方差分析结果见表3。
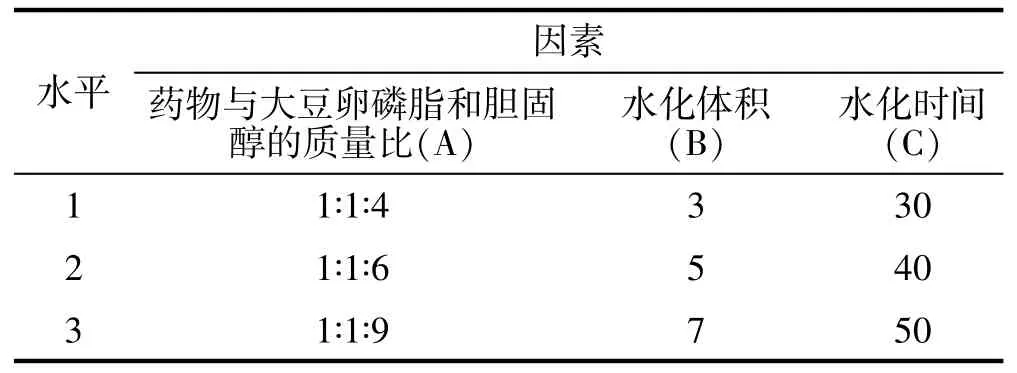
表1 因素水平表
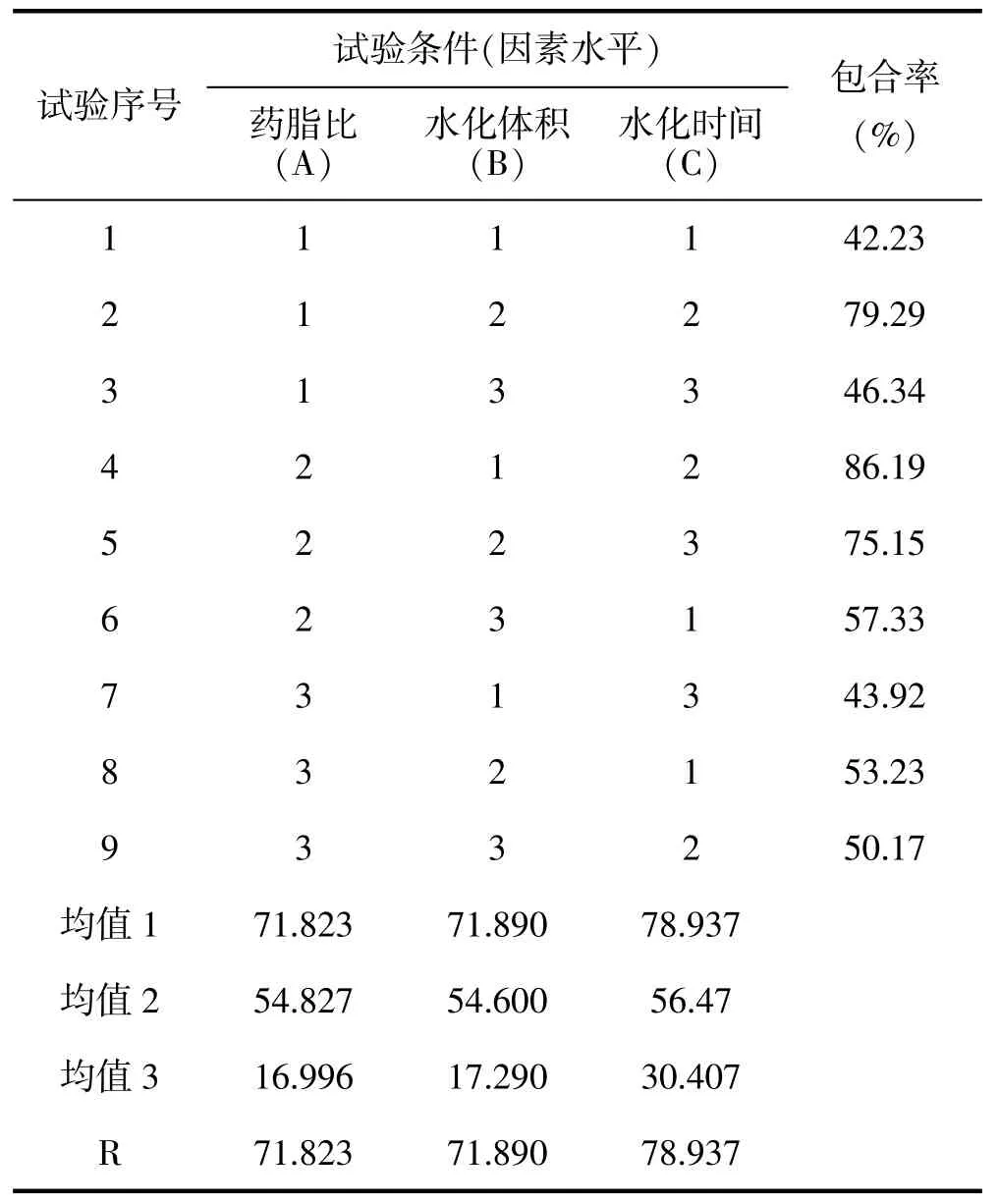
表2 正交试验结果

表3 方差分析表
通过表2、表3 分析可知,水化时间对工艺的影响具有显著性,确定最佳制备工艺为:药物与大豆卵磷脂与胆固醇的质量比为1∶1∶6,水化体积为3 mL,水化温度为40℃。
2.4 制备工艺验证
按上述得到的最佳制备工艺,精密称取2mg 人参皂苷Rg3,平行制备三批人参皂苷Rg3 脂质体,测定包封率分别为83.56%、85.11%、86.49%,平均包封率85.05%。表明该制备工艺合理、可行、重复性好,且包封率不低于80%,因此本实验所确定的薄膜水化法的工艺条件,适用于人参皂苷Rg3 脂质体的制备。
3 结论与讨论
本实验采用薄膜分散-超声法制备人参皂苷Rg3脂质体,以包封率为评价指标,考察药物与大豆卵磷脂与胆固醇的质量比、水化体积和水化温度对包封率的影响,最终确定人参皂苷Rg3 脂质体的最佳制备工艺。
脂质体的制备方法有薄膜分散法、注入法、逆向蒸发法等。通过查阅文献发现薄膜分散法和注入法都属于被动载药,应用较多效果较好,前期预试验对比二者发现,通过薄膜分散法得到的人参皂苷Rg3 脂质体包封率较高且粒径较为均匀,故本实验选择薄膜分散法制备人参皂苷Rg3 脂质体。
通过TCMSP 数据库发现人参皂苷Rg3 口服利用度OB 值仅为5.95%(其中OB 值≥30%时,口服利用度较好),因此人参皂苷Rg3 的口服剂型选择显得尤为重要。脂质体是一种人工膜,既具有亲水性,又具有亲脂性,因此能够更好的包裹人参皂苷Rg3,达到较好的口服利用度。

