电催化硝酸根还原制氨
于一夫,周瑾
1 天津大学分子+研究院,天津 300072
2 天津大学化工学院,天津 300072
氨作为一种潜在的无碳能源载体,具有高能量密度、易液化储运、安全性高和运输体系完备等优势,被认为是未来最有潜力的清洁燃料之一[1–3]。传统合成氨的哈伯-博施法以空气分离得到的氮气和化石燃料重整得到的氢气为原料在高温高压条件下反应,会造成大量的碳排放和能量消耗。因此绿色合成氨一直是人们追求的目标[4–6]。电合成具有反应条件温和、可选择性转化及利用可再生电能等优点[7],有望成为未来最具潜力的应用技术之一。此外,由于氮肥的过量使用和废水的不当排放,硝酸盐污染已成为对人类健康的严重威胁[8]。因此,利用硝酸盐污染物作为氮源,在温和条件下通过电催化技术合成氨是一种有效的途径[9,10]。
本实验以电催化硝酸根还原制氨反应为案例,基于大学无机化学以及物理化学中的电化学基础知识,使学生在掌握电化学基本原理的基础上,学习电化学测试与分析方法,加深对电催化的理解与认识,旨在培养储能专业人才。该实验可分为溶剂配制、电化学测试、产物定量三部分,计划分配4个学时。
1 实验目的
(1) 了解电催化硝酸根还原到氨的原理;
(2) 学习电催化基本概念,掌握电化学测试与分析方法;
(3) 掌握核磁定量分析方法及紫外-可见分光光度计使用方法;
(4) 提升绿色能源的化学意识。
2 实验原理
2.1 电催化硝酸根还原到氨
电催化作用是指在电场作用下,存在于电极表面或溶液相中的修饰物能促进在电极上发生的电子转移反应,而电极表面或溶液相中的修饰物本身并不发生变化的一类化学作用[11]。电催化剂对一个或一类反应有催化作用主要体现在:电极反应氧化还原超电势的降低或在某一给定电势下氧化还原电流的增加。因此,只要测定出电极反应体系的氧化还原电势、电流密度、法拉第效率等因素就能评价出催化剂对电极反应发生时催化活性的高低。
硝酸根还原到氨是一个多电子、多质子的转移过程,总反应可以总结为:
2.2 线性扫描伏安法
线性扫描伏安法是控制电极电势以恒定的速率变化,即连续线性变化(图1a),同时测量通过电极的响应电流(图1b)。以还原反应为例,电势从Ei开始向负方向扫描,开始时没有还原电流。随着电势负移,还原电流逐渐出现并增大。电势移向更负时,电流进一步增大,这时的电极反应主要受界面电荷传递动力学所控制。但当电势进一步负移到足够负时,达到扩散控制区电势后,电流则转而受到扩散控制,因而会随时间(也就是随电势的进一步负移)而衰减,使得I–E曲线上出现电流峰[12]。

图1 (a) 线性扫描伏安法的电势–时间曲线;(b) 电流–电势响应曲线
2.3 计时电流法
计时电流法属于恒电位法,是指向工作电极施加一个大的阶跃电位(从一个无法拉第反应发生的电位跃至发生电化学反应的电位,图2a)[12],记录电位阶跃下电极电流随时间的变化关系的方法。
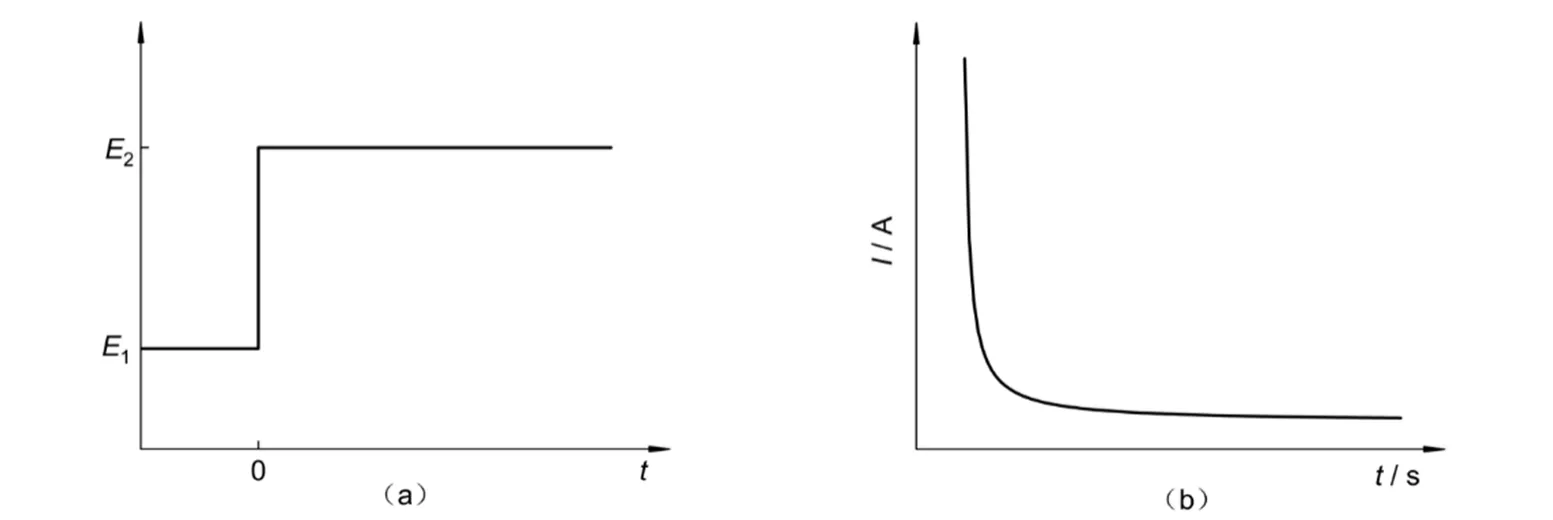
图2 (a) 计时电流法的电势–时间曲线;(b) 电流–时间响应曲线
3 实验仪器及试剂
3.1 实验仪器
电化学工作站(CHI 650D,上海辰华)、H型电解池(C007,武汉高仕睿联)、紫外-可见分光光度计(General T6,北京普析)、比色皿、泡沫镍基底、氧化汞电极、玻碳棒电极、分析天平、电磁搅拌器、磁子、250 mL容量瓶、移液枪、10 mL离心管、烧杯。
3.2 实验试剂
氢氧化钾、硝酸钾、水杨酸钠、酒石酸钾、氢氧化钠、亚硝基铁氰化钠二水化合物(硝普钠)、次氯酸钠、氯化铵、盐酸、氨基磺酸、马来酸、氘代二甲基亚砜(以上试剂均为分析纯,采购自阿拉丁、安耐吉等公司)。
4 实验步骤
4.1 电解液配制
在250 mL容量瓶中分别配制含有1 mol·L−1硝酸钾、0.1 mol·L−1氢氧化钾的混合溶液以及只含有0.1 mol·L−1氢氧化钾的溶液,超声后备用。
4.2 不同电位下电化学还原硝酸根性能测试
电化学测试在电化学工作站上进行,采用典型的H型电解槽,阴极使用泡沫镍作为工作电极(面积为1 × 1 cm2),阳极使用玻碳棒作为对电极,氧化汞电极作为参比电极,采用Nafion-117质子交换膜对H型电解池的阴、阳极室进行分离。首先向阳极室均加入25 mL步骤4.1配制的0.1 mol·L−1氢氧化钾溶液,将工作电极、参比电极以及对电极进行正确连接,装置示意图如图3所示。在反应前通入20 min氩气,之后使用电化学工作站进行线性扫描伏安测试得到稳定的伏安曲线(扫速:10 mV·s−1,扫描范围:−0.5 – 0.3Vvs. RHE)。随后,重新进行电化学测试,不同的是,此次向电解池的阴极室加入步骤4.1配制的1 mol·L−1硝酸钾、0.1 mol·L−1氢氧化钾的混合溶液,其余操作不变。并记录该条件下的线性扫描伏安曲线图。根据两次实验的伏安曲线差异(图4a),选取适当的电位进行计时电流法测试(图4b),并进行三次平行测试。
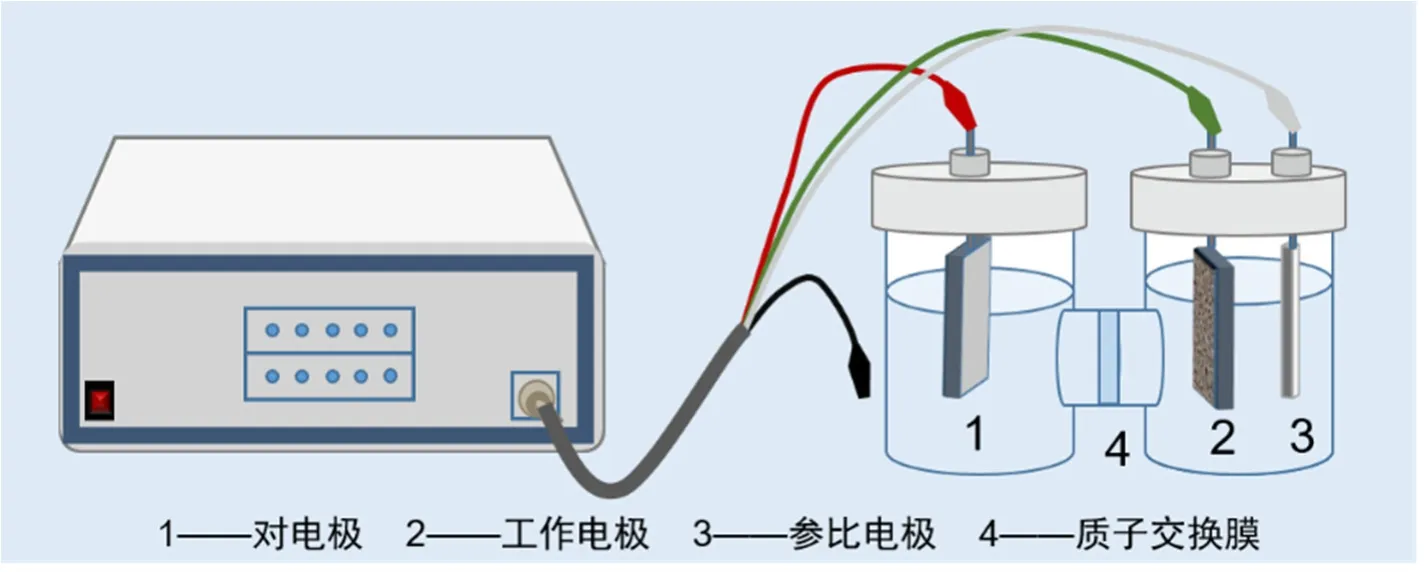
图3 电化学性能测试装置图
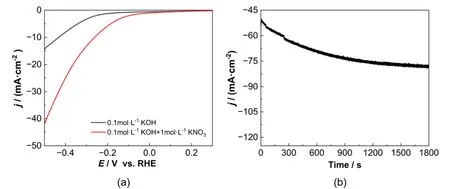
图4 (a) 线性扫描伏安法电流-电位曲线;(b) 计时电流法曲线
4.3 产物氨根浓度测定
4.3.1 显色法定量
采用紫外-可见分光光度法测定产物氨浓度。标准曲线绘制:将氯化铵晶体在105–110 °C下提前干燥2 h,配制一系列标准氯化铵溶液(0、0.02、0.04、0.06、0.08、0.1 mmol·L−1),按照以上步骤测试不同浓度氯化铵溶液的吸光度,绘制吸光度–浓度曲线,结果如图5所示(图5b插图为不同浓度氯化铵溶液显色后的样品)。
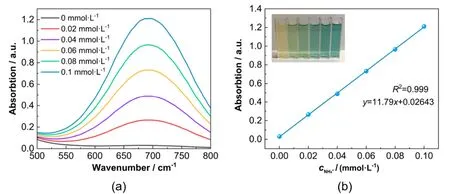
图5 (a) 氨的紫外-可见光谱图;(b) 不同浓度下的标准曲线
电化学反应结束后,从电解槽阴极室中取出一定量的电解液,稀释至5 mL至紫外-可见法检测离子浓度范围。然后在上述溶液中加入0.5 mL水杨酸钠溶液(含50 g·L−1水杨酸钠、50 g·L−1酒石酸钾和20 g·L−1NaOH)、0.05 mL硝普钠溶液(含10 g·L−1硝普钠)和0.05 mL次氯酸钠溶液(含40 mL·L−1质量分数13%的NaClO和30 g·L−1NaOH)。20 min后,用紫外-可见分光光度计测试吸收光谱,记录650 nm波长处的吸收强度。根据朗伯-比尔定律,计算出生成的产物氨浓度。
4.3.2 核磁法定量
采用核磁法测定氨浓度。标准曲线绘制:首先,配制一系列已知浓度(0、2、4、6、8、10 mmol·L−1)的氯化铵作为标准品,向其中分别加入一定量的马来酸作为内标物,并将各溶液的pH调至酸性(pH = 3)。随后测试不同浓度上述溶液的核磁共振光谱,以氨与马来酸的积分面积比为纵坐标,以氨的浓度为横坐标,绘制标准曲线,结果如图6所示。

图6 (a)标准溶液的1H NMR谱图;(b) 的标准曲线
电化学测试后,取0.5 mL反应液,加入50 μL氘代二甲基亚砜和50 μL上述一定量的马来酸进行混合,并将该混合溶液的pH调至酸性(pH = 3)。随后将该混合溶液转移至核磁管内,进行核磁共振氢谱测试。根据上述绘制的标准曲线来计算出氨产物浓度。
核磁定量测试参数:1H NMR,600 MHz,测定温度为25 °C,扫描次数32;内标基准峰:6.2 (6.1–6.3);样品基准峰:~6.8、6.9、7.0。
4.4 反应物硝酸根浓度测定
采用紫外-可见分光光度计法检测和定量硝酸根离子浓度。电化学测试后,从电解槽中取出一定量的电解液,稀释至5 mL至紫外-可见法检测离子浓度范围。然后,在上述溶液中加入0.1 mL 1 mol·L−1的盐酸和0.01 mL 0.8% (质量分数)的氨基磺酸溶液。随后用紫外-可见分光光度计测试吸收光谱,记录220 nm和275 nm波长处的吸收强度。最终吸光度值由以下公式(2)计算
标准曲线绘制:将硝酸钾在105–110 °C下提前干燥2 h,配制一系列标准硝酸钾溶液 (0、0.1、0.2、0.4、0.8、1.6、2 mg·L−1),按照以上步骤测试不同浓度硝酸钾溶液的吸光强度,绘制吸光强度–浓度曲线,结果如图7所示。
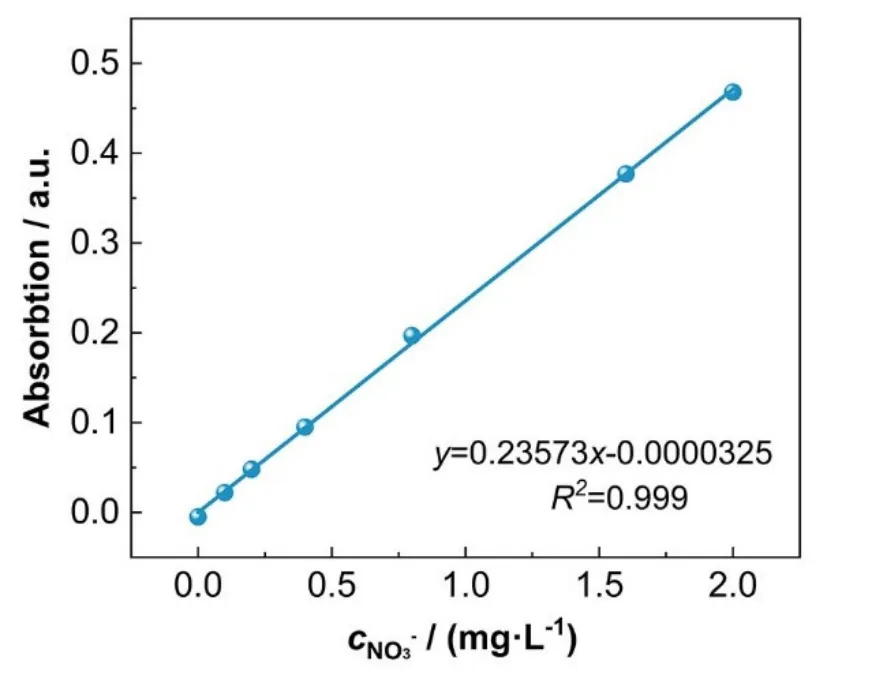
图7 标准NO3−溶液的标准曲线
5 结果与讨论
表1为依据显色法、核磁法得到的反应后的离子浓度,之后根据式(3)–(6)计算产率、转化率、选择性、法拉第效率等结果,结果见表2。

表1 反应后离子浓度

表2 反应结果
氨的产率由式(3)计算:
转化率由式(4)计算:
氨的选择性由式(5)计算:
氨的法拉第效率由式(6)计算:
其中cNH3表示电解后溶液中氨的浓度;V为阴极室中电解液体积;MNH3为氨的摩尔质量;t为电解时间,S为工作电极的几何面积;ΔcNO3–为电解前后的浓度差;c0为初始浓度;F为法拉第常数96485 C·mol−1);Q为通过电极的总电荷。
6 结语
本实验内容丰富、学科涵盖面广,涉及了无机化学、仪器分析、物理化学和电化学等多个二级学科领域。同时,在实验教学中引入电催化技术,使得教学内容新颖,选择的反应在室温下进行、操作安全,非常适合教学使用。科教融合是培养创新性人才的有效途径,我们将前沿科学研究成果转化为教学实验,在培养学生分析思考、创新创造能力的同时,拓宽学生的科研视野、激发学生的科研热情。此外,通过介绍绿色电合成技术,深化学生的绿色发展理念和社会责任感。

