N-(苯基)噻唑酰胺类衍生物的合成及杀菌活性
张 勇, 时锦超, 胡 勇, 廖 灿, 王美美, 朱 祥,3, 余林花*, 李俊凯*
(1.长江大学 农学院,湖北 荆州 434025; 2. 长江大学 农药研究所,湖北 荆州 434025; 3. 贵州大学 绿色农药与农业生物工程国家重点实验室培育基地/教育部重点实验室,贵州 贵阳 550025)
近年来,由于气候变化加剧,作物真菌病害在我国的发生越来越严重。真菌病害因具有很强的暴发性和传染性,易使农作物大面积减产,造成严重的经济损失[1-6]。目前,使用化学杀菌剂对作物真菌病害进行防治,仍然是最为经济、有效的手段。然而,由于传统杀菌剂的长期使用,在保障粮食产量和品质的同时,化学农药的残留、抗性和再猖獗等问题也日益突出。因此,设计以天然产物结构为先导,进行结构修饰改造或将活性结构单元引入天然产物结构中,是开发高效、低毒新型杀菌剂最有效的方式之一。
噻唑(图1, Thiazole)是同时含有氮、硫原子的五元芳香杂环,易与金属离子配位,也可同其它有机分子形成氢键,因此具有生物活性广泛的特点。Thiasporine A(图1)作为一种含有噻唑杂环的天然产物,于2015年[7]首次由MACMILLAN课题组从海洋放线菌ActinomycetosporachloraSNC-032的代谢产物中分离得到。含噻唑结构的化合物具有抗菌、杀虫和抗肿瘤等生物活性,在农用活性中已被开发为除草剂、杀虫剂等,如目前已经上市的杀菌剂噻唑菌胺(图1, Ethaboxam)与杀虫剂噻虫嗪(图1, Thiamethoxam)。本课题在前期的研究中[8]通过对Thiasporine A的杀菌、除草和杀虫等活性进行筛选发现,该类结构具有较好的杀真菌活性;由初步构效关系发现,无取代的苯基噻唑结构具有更好的杀菌活性,可作为杀菌先导结构进行优化。与此同时,酰胺结构(图1, Amide)作为具有多种优良生物活性的结构片段,广泛存在于农药和医药中,尤其在农用杀菌剂领域中广泛存在,如杀菌剂氟酰胺(图1, Flutolanil)、呋吡菌胺(图1, Furametpyr)和啶酰菌胺(图1, Boscalid)。

图1 含噻唑环/酰胺化学结构的天然产物和农药Figure 1 Natural products and pesticides containing thiazole ring/amide chemical structure
基于以上结果,本研究以Thiasporine A中的杀菌活性结构苯基噻唑为先导,设计合成了一系列含酰胺结构的苯基噻唑类衍生物(图2~3),并测定了化合物对6种植物病原真菌的离体杀菌活性,以期得到具有较高杀菌活性的化合物。通过探讨N-(苯基)噻唑酰胺类衍生物的构效关系,旨在为今后苯基噻唑类衍生物的杀真菌活性研究提供理论依据。
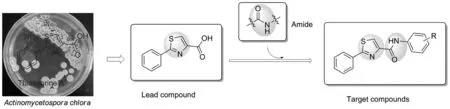
图2 目标化合物的设计思路Figure 2 Design idea of the target compounds

图3 目标化合物(6a~6l)的合成路线Figure 3 Synthesis route of target compounds(6a~6l)
1 实验部分
1.1 仪器与试剂
WRR型熔点仪(上海精密科学仪器有限公司); Q Exactive型高分辨质谱仪(德国,赛默飞公司); Bruker AV 400型核磁共振仪(内标为TMS,溶剂为CDCl3和DMSO-d6); Digital water bath SB-1000型旋转蒸发仪(日本EYELA公司)。
所有化学药品均为市售国产试剂,除特别注明外,未经进一步处理,直接使用。苯甲腈,上海麦克林生化科技有限公司; 3-溴丙酮酸乙酯,质量分数为80%,上海毕得医药科技股份有限公司; 不同取代苯胺,质量分数为99%,上海麦克林生化科技有限公司。薄层和柱层析用硅胶均为青岛海洋化工厂产品。
1.2 供试真菌
水稻纹枯病菌Rhizoctoniasolani、白芨白绢病菌Sclerotiumrolfii、水稻稻瘟病菌Magnaportheoryzae、柑橘黑点病菌Phomacitricarpa、油菜菌核病菌Sclerotiniasclerotiorum和烟草赤星病菌Alternariaalternata均由长江大学农学院植物病理实验室提供。
1.3 化合物的合成
(1) 化合物2的合成
参照文献[7]方法,将MgCl2·6H2O(21.7 g, 110.0 mmol)和苯甲腈(10.0 g, 100.0 mmol)分别加入250 mL的N,N-二甲基甲酰胺(DMF)溶液中。室温搅拌15 min后,将NaHS·H2O(12.0 g, 210.0 mmol)加入反应液,持续室温搅拌16 h。监测反应完成后,反应液用水(70 mL)和饱和食盐水(10 mL)稀释,并用乙酸乙酯(4×50 mL)萃取。合并的有机相用饱和食盐水(3×50 mL)洗涤并用无水硫酸钠干燥,得到粗产物化合物2。
(2) 化合物3的合成
参照文献[9]方法,将硫代苯甲酰胺(15.0 g, 110.0 mmol), 250 mL无水乙醇加入到1000 mL圆底烧瓶,搅拌至完全溶解,室温下用恒压滴定管缓慢滴加80% 3-溴丙酮酸乙酯(29.5 g, 120.0 mmol),室温下反应0.5 h后,加热回流2 h,监测至反应结束。向反应液中加入饱和NaHCO3调节pH=8~9,减压蒸馏后加CH2Cl2溶解,加入饱和食盐水进行交叉萃取,用无水硫酸钠干燥,脱溶剂得到化合物2的粗产品。随后通过柱层析纯化(洗脱剂:石油醚 ∶乙酸乙酯=4 ∶1,V∶V),得到化合物3。
(3) 化合物4的合成
将化合物2和溶解在水中的NaOH(4.8 g, 120.0 mmol)依次加入圆底烧瓶中,加热回流反应5 h,监测至反应结束。向反应液中加入稀盐酸调节pH=4~5,搅拌0.5 h后,加水析出白色固体,抽滤得到滤饼,即化合物3的纯品(4)[6]。
(4) 目标化合物6a~6l的合成
参照文献[10-11]方法,将6.0 mmol化合物3加入含有50 mL CH2Cl2的圆底烧瓶中,用恒压滴定管缓慢滴加二氯亚砜,随后滴加2滴DMF,待体系稳定后升温反应2 h。监测至反应结束后,将反应液旋干并加入20 mL CH2Cl2溶解。冰浴条件下加入不同取代苯胺(6.6 mmol),同时加入三乙胺(6.6 mmol)作为缚酸剂,在室温下反应6 h。反应结束后,向反应液中加入稀盐酸调pH=5~6,加入饱和食盐水和反应液进行交叉萃取,合并有机层,干燥,减压浓缩得粗品,经柱层析(洗脱剂:乙酸乙酯 ∶石油醚=5 ∶1,V∶V)纯化,得到目标化合物6a~6l。
N-(2-乙基苯基)-2-苯基噻唑-4-酰胺(6a):棕色固体,产率56.1%, m.p.124~126 ℃;1H NMR(400 MHz, CDCl3)δ: 9.49(s, 1H), 8.23(m, 2H), 7.99(dd,J=6.8 Hz,J=3.2 Hz, 2H), 7.50(m, 3H), 7.29(m, 2H), 7.14(t,J=8.0 Hz, 1H), 2.80(q,J=7.6 Hz, 2H), 1.38(t,J=7.6 Hz, 3H);13C NMR(101 MHz, CDCl3)δ: 168.15, 158.82, 151.13, 135.21, 133.72, 132.70, 130.80, 129.17, 128.75, 126.92, 126.55, 124.93, 123.32, 121.83, 24.68, 13.98; HR-MS(ESI)m/z: calcd for C18H16N2OS{[M+H]+}309.1056, found 309.1051。
N-(4-乙基苯基)-2-苯基噻唑-4-酰胺(6b):棕红色液体,产率91.2%;1H NMR(400 MHz, CDCl3)δ: 9.26(s, 1H), 8.17(d,J=12.6 Hz, 1H), 8.00(dd,J=6.8 Hz, 2.8 Hz, 2H), 7.66(d,J=8.4 Hz, 2H), 7.48(m, 3H), 7.22(d,J=8.4 Hz, 2H), 2.66(q,J=7.6 Hz, 2H), 1.25(t,J=7.6 Hz, 3H);13C NMR(101 MHz, CDCl3)δ: 168.21, 158.76, 150.95, 140.50, 135.27, 132.68, 130.76, 129.02, 128.39, 126.96, 126.68, 123.47, 119.91, 28.34, 15.63; HR-MS(ESI)m/z: calcd for C18H16N2OS{[M+H]+}309.1056, found 309.1051。
N-(2-异丙基苯基)-2-苯基噻唑-4-酰胺(6c):棕黄色固体,产率58.1%, m.p.119~121 ℃;1H NMR(400 MHz, CDCl3)δ: 9.50(s, 1H), 8.21(s, 1H), 8.14(d,J=8.0 Hz, 1H), 7.99(dd,J=6.4 Hz, 2.8 Hz, 2H), 7.51(m, 3H), 7.34(d,J=7.6 Hz, 1H), 7.29(d,J=7.6 Hz, 1H), 7.20(t,J=7.2 Hz, 1H), 3.24(dt,J=13.6 Hz, 6.8 Hz, 1H), 1.38(d,J=6.8 Hz, 6H);13C NMR(101 MHz, CDCl3)δ: 168.16, 158.97, 151.13, 138.85, 134.34, 132.71, 130.79, 129.17, 126.55, 125.63, 125.38, 123.34, 122.81, 28.35, 22.79; HR-MS(ESI)m/z: calcd for C19H18N2OS{[M+H]+}323.1213, found 323.1210。
N-(4-异丙基苯胺)-2-苯基噻唑-4-酰胺(6d):棕红色液体,产率67.3%;1H NMR(400 MHz, CDCl3)δ: 9.26(s, 1H), 8.18(d,J=13.2 Hz, 1H), 8.00(dd,J=6.8 Hz, 2.8 Hz, 2H), 7.67(d,J=8.4 Hz, 2H), 7.50(m, 3H), 7.26(s, 1H), 7.24(s, 1H), 2.92(dt,J=13.6 Hz, 6.8 Hz, 1H), 1.27(d,J=6.8Hz, 6H);13C NMR(101 MHz, CDCl3)δ: 168.24, 158.78, 150.97, 145.17, 132.70, 130.73, 129.04, 126.98, 126.71, 123.50, 119.94, 33.64, 24.03; HR-MS(ESI)m/z: calcd for C19H18N2OS{[M+H]+}323.1213, found 323.1207。
N-(4-叔丁基苯基)-2-苯基噻唑-4-酰胺(6e):黄色液体,产率51.9%;1H NMR(400 MHz, CDCl3)δ: 9.26(s, 1H), 8.19(s, 1H), 8.00(dd,J=6.8 Hz, 3.2 Hz, 2H), 7.67(d,J=8.8 Hz, 2H), 7.50(m, 3H), 7.41(d,J=8.8 Hz, 2H), 1.32(d,J=16.8 Hz, 9H);13C NMR(101 MHz, CDCl3)δ: 168.25, 158.80, 150.96, 147.43, 135.02, 132.70, 130.79, 129.13, 128.33, 126.71, 125.91, 123.53, 119.62, 34.42, 31.37; HR-MS(ESI)m/z: calcd for C20H20N2OS{[M+H]+}337.1369, found 337.1359。
N-(3-氯苯基)-2-苯基噻唑-4-酰胺(6f):白色固体,产率55.6%, m.p.102~103 ℃;1H NMR(400 MHz, CDCl3)δ: 9.32(s, 1H), 8.21(s, 1H), 8.00(m, 2H), 7.86(t,J=2.0 Hz, 1H), 7.62(dd,J=8.0 Hz, 1.2 Hz, 1H), 7.51(m, 3H), 7.31(t,J=8.0 Hz, 1H), 7.14(ddd,J=8.0 Hz, 2.0 Hz, 0.8 Hz, 1H);13C NMR(101 MHz, CDCl3)δ: 168.48, 158.86, 150.41, 138.81, 134.75, 132.53, 130.92, 130.08, 129.16, 126.71, 124.46, 124.04, 119.84, 117.76; HR-MS(ESI)m/z: calcd for C16H11ClN2OS{[M+H]+}315.0353, found 315.0350。
N-(4-氯苯胺)-2-苯基噻唑-4-酰胺(6g):白色固体,产率68.8%, m.p.113~115 ℃;1H NMR(400 MHz, CDCl3)δ: 9.31(s, 1H), 8.21(s, 1H), 8.00(dd,J=6.8, 3.2 Hz, 2H), 7.72(d,J=8.8 Hz, 2H), 7.51(m, 3H), 7.36(d,J=8.8 Hz, 2H);13C NMR(101 MHz, CDCl3)δ: 168.46, 158.84, 150.51, 136.26, 132.56, 130.91, 129.40, 129.14, 126.71, 123.91, 121.02; HR-MS(ESI)m/z: calcd for C16H11ClN2OS{[M+H]+}315.0353, found 315.0349。
N-(3-溴基苯基)-2-苯基噻唑-4-酰胺(6h):白色固体,产率57.0%, m.p.109~111 ℃;1H NMR(400 MHz, CDCl3)δ: 9.31(s, 1H), 8.21(s, 1H), 8.00(d,J=6.6 Hz, 3H), 7.69(m, 1H), 7.51(m, 3H), 7.29(m, 2H);13C NMR(101 MHz, CDCl3)δ: 168.50, 158.85, 150.40, 138.95, 132.53, 130.93, 130.39, 129.17, 127.39, 126.72, 124.05, 122.69, 118.25; HR-MS(ESI)m/z: calcd for C16H11BrN2OS{[M+H]+}358.9848, found 358.9846。
N-(4-溴基苯基)-2-苯基噻唑-4-酰胺(6i):白色固体,产率56.3%, m.p.116~117 ℃;1H NMR(400 MHz, CDCl3)δ: 9.30(s, 1H), 8.20(s, 1H), 7.99(dd,J=6.7 Hz, 2.9 Hz, 2H), 7.67(d,J=8.8 Hz, 2H), 7.50(dd,J=6.2 Hz, 2.8 Hz, 5H);13C NMR(101 MHz, CDCl3)δ: 168.46, 158.84, 150.50, 136.76, 132.55, 132.06, 130.91, 129.16, 126.71, 123.94, 121.34, 117.01, 112.25; HR-MS(ESI)m/z: calcd for C16H11BrN2OS{[M+H]+}358.9848, found 358.9846。
N-(3-氟苯基)-2-苯基噻唑-4-酰胺(6j):白色固体,产率59.6%, m.p.113~114 ℃;1H NMR(400 MHz, CDCl3)δ: 9.35(s, 1H), 8.22(s, 1H), 8.00(m, 2H), 7.72(dt,J=10.8 Hz, 2.2 Hz, 1H), 7.51(m, 3H), 7.35(ddd,J=14.4 Hz, 12.0 Hz, 7.6 Hz, 2H), 6.86(tdd,J=8.4 Hz, 2.4 Hz, 1.2 Hz, 1H);13C NMR(101 MHz, CDCl3)δ: 168.47, 158.88, 150.45, 139.23, 132.55, 130.92, 130.15, 129.17, 126.72, 124.03, 115.10, 111.25, 111.04, 107.40, 107.14; HR-MS(ESI)m/z: calcd for C16H11FN2OS{[M+H]+}299.0649, found 299.0645。
N-(4-硝基苯基)-2-苯基噻唑-4-酰胺(6k):黄色固体,产率67.5%, m.p.129~131 ℃;1H NMR(400 MHz, CDCl3)δ: 8.40(dd,J=7.6 Hz, 2.0 Hz, 2H), 8.06(dd,J=7.6 Hz, 2.0 Hz, 2H), 7.52(m, 7H);13C NMR(101 MHz, CDCl3)δ: 188.12, 173.80, 132.86, 131.92, 130.71, 130.36, 129.27, 128.69, 128.33, 127.48; HR-MS(ESI)m/z: calcd for C16H11N3O2S{[M+H]+}324.0448, found 324.0448。
N-(2-甲氧苯基)-2-苯基噻唑-4-酰胺(6l):白色固体,产率93.6%, m.p.110~111 ℃;1H NMR(400 MHz, CDCl3)δ: 9.96(s, 1H), 8.56(d,J=6.4 Hz, 1H), 8.19(s, 1H), 8.02(dd,J=6.4 Hz, 3.2 Hz, 2H), 7.50(m, 3H), 7.08(m, 2H), 6.95(d,J=8.0 Hz, 1H), 3.99(s, 3H);13C NMR(101 MHz, CDCl3)δ: 168.03, 158.82, 148.47, 130.69, 129.10, 127.55, 126.65, 123.99, 123.34, 121.13, 119.85, 110.09, 55.98; HR-MS(ESI)m/z: calcd for C17H14N2O2S{[M+H]+}311.0849, found 311.0838。
1.4 生物活性测定
采用菌丝生长速率法[12-15]测定化合物6a~6l对6种植物病原真菌的离体杀菌活性,药剂初筛浓度为0.200 mmol/L。操作方法为:将目标化合物溶解于0.5 mL 二甲基亚砜(DMSO)。用含有0.1%(质量分数)的吐温80水溶液定容至50 mL,并加入到灭菌后的PDA培养基中,制成含药培养基。在含药培养基上接入菌饼,每个药剂重复3次,以申嗪霉素为对照药剂,以0.5 mL DMSO处理组为溶剂对照。将接种后的培养基置于生化培养箱中培养,培养温度为28 ℃。待空白对照菌落长至接近2/3培养皿直径时,以十字交叉法测定各处理菌落的直径,并计算供试化合物对病原菌的生长抑制率。选择在初筛浓度下对病原菌抑制率大于60%的化合物,测定EC50值。同样采用菌丝生长速率法,操作方法同上,测定各浓度下目标化合物对供试植物病原菌的抑制率。采用软件DPS计算EC50值和95%置信限。
2 结果与讨论
2.1 化合物的合成分析
本研究通过五步反应得到目标化合物6a~6l。以苯甲腈为原料,通过成环,水解反应分别得到化合物2~4;进一步将化合物4与二氯亚砜反应得到相应的酰氯,此过程应保证在无水条件下进行;待反应结束后应迅速以二氯甲烷为溶剂,三乙胺为缚酸剂进行酰胺反应,此过程要求将酰氯缓慢滴加至苯胺溶液中。该反应在低温条件下对反应有利,高于室温时副产物增多。化合物结构均经1H NMR,13C MNR和HR-MS(MSI)得到确证。
2.2 目标化合物的杀菌活性
离体杀菌活性测定结果如表1所示,结果表明,目标化合物对6种供试真菌均有一定的杀菌活性。在0.2 mmol/L浓度下,化合物6b、6c、6d、6e、6k和6l对水稻纹枯病菌的抑制率为57.0%~84.0%,其中6b和6k与对照药剂申嗪霉素抑菌效果相当;化合物6a、6c和6l对水稻稻瘟病菌的抑制率分别为75.8%、 88.8%和91.6%,均略低于申嗪霉素。根据预实验结果测定了杀菌活性较高化合物的EC50值。从表2数据可以看出,化合物6b对水稻纹枯病菌杀菌活性较强,EC50值为0.041 mmol/L,但杀菌活性低于对照药剂申嗪霉素;化合物6c和6l对水稻稻瘟病病菌杀菌活性最强,EC50值分别为0.015 mmol/L和0.020 mmol/L,其毒力高于对照药剂申嗪霉素。初步构效关系分析结果表明,目标化合物对供试病菌的抑制活性与连接酰胺的苯环上取代基(R)的性质有关。当取代基R为烷基(供电子基团)时,对位取代的总体活性要优于邻位取代的活性;当取代基R为卤素原子时,其对水稻纹枯的抑制率较优,而总体活性则是对位取代更优于邻位和间位;对于取代基R为其它基团时,则有不同的抑制效果,如6k(R为吸电子基团)对水稻纹枯病菌具有良好抑制作用。

表1 目标化合物对6种植物病原真菌的抑制作用aTable 1 Inhibitory effects of target compounds on 6 plant pathogenic fungi

表2 部分目标化合物对供试病原菌的EC50值Table 2 EC50 values of partial target compounds against test phytopathogens
本研究以Thiasporine A中的杀菌活性结构苯基噻唑为先导,将酰胺活性亚结构单元引入到苯基噻唑分子骨架,设计合成了12个N-(苯基)噻唑酰胺类衍生物(6a~6l)。杀菌活性结果表明:在0.200 mmol/L时,大部分化合物对水稻纹枯病菌表现出较好的杀菌活性,其中6b和6k抑制作用与对照药剂申嗪霉素相当;化合物6c和6l对水稻稻瘟病菌表现出良好的杀菌活性,其EC50值均低于对照药剂申嗪霉素,抑制作用高于对照药剂,说明将酰胺活性亚结构单元引入到苯基噻唑分子骨架上对生物活性有一定的改善作用,而其结构的改造有待进一步研究。

