医用放射性同位素制备的现状与展望
刘 鹏,杜克泽,马福秋,吉明波,王跃霖,桂云阳,李蕴财
(1.哈尔滨工程大学 烟台研究(生)院,烟台 265500;2.哈尔滨工程大学 核科学与技术学院,哈尔滨 150006)
放射性药物由放射性同位素标记的化合物或生物制剂制成,但目前国内用于制备放射性药物的同位素多依赖进口,这是导致目前国内核医学普及水平较低的重要因素。由于放射性药物的靶向能力,放射性药物治疗较传统的放射性治疗更精准[1]。随着较多的放射性药物批准上市,更多有前景的放射性同位素被发现,如利用177Lu生产的药物Lutetium-177-DOTATATE治疗神经内分泌肿瘤[2]、177Lu-PSMA-617治疗前列腺癌[3]、利用131I制备的放射性药物131I-mIBG治疗复发/难治性神经母细胞瘤[4]、利用125I粒子治疗前列腺癌[5]、通过[225Ac]Ac-PSMA-I&T治疗前列腺癌[6]、利用 (211At)-labeled PSMA1治疗前列腺癌[7]等。
目前常用的医用放射性同位素有99mTc[11]、125I[12]、131I[4]、14C[13]、68Ga[14]、177Lu[3]、18F[15]、90Y[16]、89Sr[17]等,这些核素主要有反应堆制备和加速器制备两个来源。反应堆生产的医用放射性同位素有177Lu、131I、125I、113Sn、99Mo、32P、14C、3H、89Sr、133Xe、186Re、153Sm等。加速器能加速质子、氘核、α粒子等带电粒子,这些带电粒子轰击不同的靶核,引起不同核反应,可以生成多种医用放射性同位素。常用加速器生产的医用放射性同位素有18F、68Ga、11C、15O、201Tl、13N、123I、111In等。
世界上生产放射性同位素的研究反应堆有数十座,大部分反应堆在20世纪60~70年代建造,所以大部分用于生产医用同位素的研究堆都面临着退役或需要维护翻新,2021年国家八部委联合发布的《医用同位素中长期发展规划(2021—2035年)》(《规划》)中提到,目前国内可用于放射性同位素生产的研究堆有中国先进研究堆(CARR)、游泳池反应堆(SPR)、高通量工程实验堆(HFETR)、岷江实验堆(MJTR)、中国绵阳研究堆(CMRR)5座。我国目前的研究堆大多服务于国家科研任务,无法进行稳定的医用同位素生产,产量不足以满足国内市场需求,所以目前国内大多医用同位素均依赖进口[10]。
加速器生产医用同位素在英国起步较早、发展较快,1955年英国便建造了第一台用于医用放射性同位素生产的加速器。目前用于生产医用放射性同位素的加速器主要以质子回旋加速器为主,国际原子能机构(IAEA)数据显示,全球用于医用同位素生产的回旋加速器约有1 500多台,其中大部分加速器的粒子能量集中在20 MeV以下,主要用于生产短寿命同位素生产,用于正电子发射计算机断层扫描(PET),仅有小部分粒子能量30~100 MeV的加速器可以生产较长半衰期的同位素。加速器制备核素在国内起步较晚,发展也比较缓慢[8]。中国共有160多台能量在20 MeV以下的PET小型医用回旋加速器,能量大于20 MeV的回旋加速器不足10台,并且主要依赖进口[9]。
目前全球医用同位素生产与供应体系相对完善且稳定,但随着用于生产医用同位素的研究堆老化,将面临退役关闭。新技术的发展将为该行业的发展提供更稳定、更安全的核素供应。本研究通过对医用放射性同位素的生产方式进行总结和分析,希望给研究者提供一定的参考信息。
1 反应堆
研究反应堆在放射性医用同位素的生产中发挥着重要的作用,全球生产放射性同位素的反应堆有数十座[18]。反应堆具有中子注量率高,可大量生产多种放射性同位素的优点[19]。虽然部分反应堆存在老化或不符合当前的安全性与法规要求的问题,但目前全球大部分医用放射性同位素的制备仍以反应堆为主[10]。
1.1 反应堆制备99Mo
目前,99Mo主要通过反应堆制备[20],99Mo的供应主要来自全球少数几个反应堆,自2009年以来,由于反应堆的老化,曾发生多次99Mo供应中断的问题[21]。针对医用99Mo同位素的生产开发了不同的工艺以满足99Mo的供应。当前利用核反应堆主要通过核裂变和中子活化两种途径生产99Mo,这两种途径又细分为实验堆裂变法、98Mo中子活化法以及溶液堆裂变法三种方式[22],图1为目前堆照生产99Mo的主要类型。
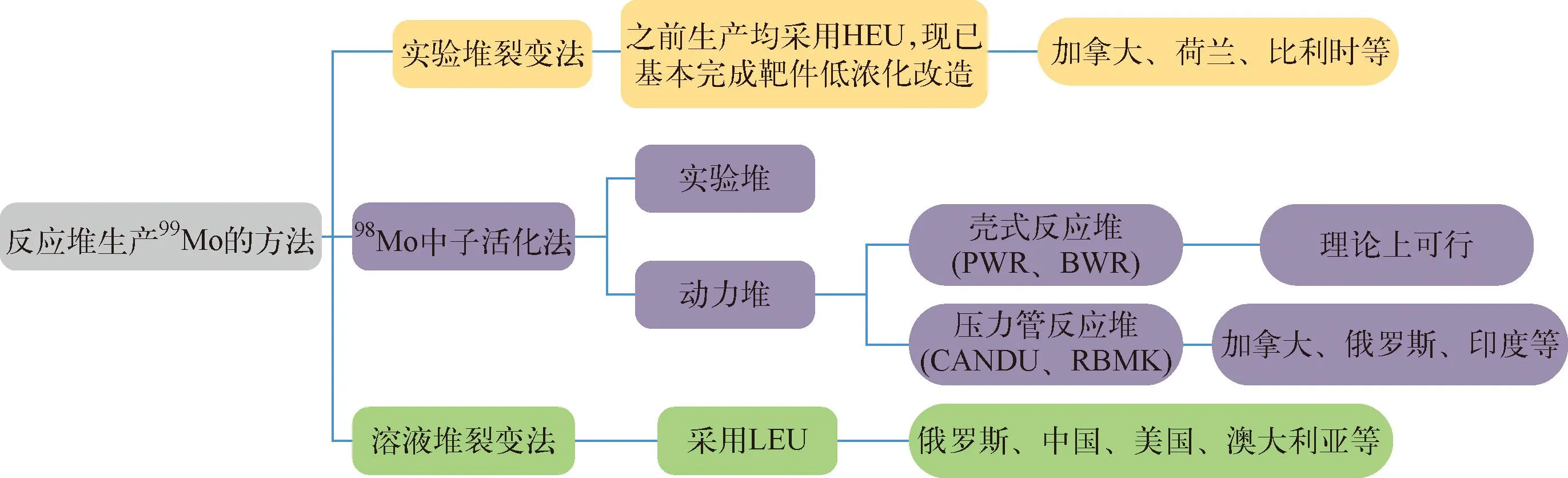
注:PWR-Pressurized-Water Reactor:压水堆;BWR-Boiling Water Reactor:沸水堆;CANDU-Canadian Deuterium Uranium (Reactor):加拿大重水反应堆;RBMK-Reaktor Bolshoy Moshchnosti Kanalnyy:俄罗斯石墨水冷堆。图1 反应堆生产99Mo的方式[27]Fig.1 The way of producing 99Mo by reactor[27]
其中实验堆裂变法最为成熟,目前现存生产99Mo实验堆大多为该类型,之前生产99Mo均采用高浓铀靶件(HEU),但是HEU靶存在核扩散风险,且放射性废物水平高,乏燃料后处理困难,235U利用率低,仅为千分之几,加之当前大部分实验堆面临退役,建设新堆存在审批困难、成本高和周期长等问题。近年来随着核不扩散影响,各国研究重点均转向低浓铀靶件(LEU)。LEU靶件减少了对铀资源的浪费,放射性废物水平较低,全球主要99Mo生产商已基本完成靶件低浓化改造,但现存实验堆大部分面临退役[23-26]。
98Mo中子活化法由于不使用HEU,产生的高放废物相对少,避免了核扩散风险,但由于钼靶活化制备99Mo的产额较低,且与大量未发生核反应的98Mo载体无法分离,得到的99Mo属于有载体产品,比活度较低,不利于大规模应用。溶液堆裂变法具有安全性好、生产周期短、235U利用率高、产生的放射性废物少、有较好的经济性,并且该方法目前已较为成熟,在俄罗斯、中国、美国、澳大利亚等多个国家已有初步的研究或应用,该方法可作为现阶段缓解99Mo供应紧张的重要方法[9,27]。
1.2 反应堆制备125I
125I在医学上主要用于低能辐射治疗和诊断,可用于前列腺癌治疗(臂疗法)。在臂部治疗中,使用颗粒、针、线等形式的封闭辐射源[28-29]。
目前,125I主要由反应堆热中子辐射124Xe产生的125Xe衰变得到,其核反应为:
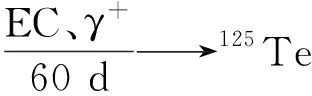
在反应堆辐照124Xe过程中,存在两个次级核反应分别为:
这两个次级核反应会产生126I,对125I的生产造成影响。126I半衰期为13.11 d且具有较高的能量,这些次级核反应会减少125I的产量,影响125I的纯度。为了减少126I含量,提高125I产量,通常在反应堆内进行短时间照射高富集度的124Xe靶材料[30],其优点示于图2。
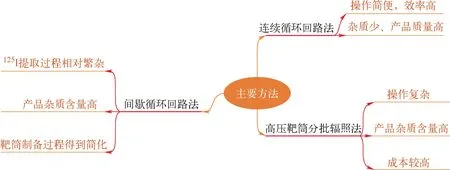
图2 利用124Xe气体在反应堆中辐照生产125I的方法及优点Fig.2 Method and advantages of 125I production using 124Xe gas irradiated in a reactor
目前利用124Xe气体在反应堆中辐照生产125I主要有高压靶筒分批辐照法(批生产法)、间歇循环回路法和连续循环回路法三种方法[31]。
高压靶筒分批辐照法的生产主要包括高压气体靶件制备、辐照、衰变、分离提取四个过程。生产流程为:首先将天然(或富集)的124Xe压缩到锆合金或铝合金制成的靶筒内制成高压靶件;放入反应堆孔道内辐照一定时间取出,随后放置约一个月;使124Xe与126I衰变为125I,最后使用氢氧化钠溶液浸取并分离纯化得到Na125I[32]。
间歇循环回路系统主要有反应堆活性区辐照部分和堆外非活性区两部分,生产流程为:先向反应堆活性区的辐照瓶内冲入124Xe,辐照一定时间后,将气体转移到非活性区的衰变瓶中,衰变结束后,利用液氮或干冰使125I吸附在衰变瓶内壁上,将124Xe通过管路回到辐照瓶中继续辐照,每次生产可进行单次或多次循环,完成后取下衰变瓶,用碱液浸取并分离纯化得到Na125I[33]。
连续循环回路法即在反应堆旁设计建造一个密闭回路系统,利用压力差、热量差或外力等不同的驱动原理使气体沿着回路系统循环进入活性区与非活性区,同时气体循环通过碘吸附装置或其他可以实现125I与124Xe分离装置,经过一定时间的循环后取下该装置,对该装置进行淋洗处理得到产品[34]。
其中高压靶筒分批辐照法由于在辐照期间生成的125I吸收中子产生126I,导致产品中杂质含量较高(产品中126I占比为1%~10%),同时高压靶筒在每次生产时都需要重新制作,增加了操作的复杂程度和生产成本。为了克服批生产法的不足,提出了间歇循环回路法,该方法前期靶筒制备过程得到简化,但并未很好的解决126I杂质的问题,同时在后续的125I产品提取过程相对繁杂。为了提高125I的品质,研究者们继而提出了杂质少、产品质量高、操作步骤得到简化的连续循环回路法[30,35]。
1951年Bergstrfm利用堆辐照诱导制备了125I[36],随着反应堆生产工艺的发展,到1961年美国ORNL宣布可以随时供应125I,1968年Kiss等用一种稳定的氙固体化合物(XeF2)代替气体作为靶材料生产125I,可以大幅提高125I的产率[37]。
中国核动力院刘宜树等[38]在1999年报道了利用天然氙气作为靶材料制作高压气体氙靶生产125I的工艺,该高压气体氙靶采用液氮冷冻、冷焊密封技术制备,向4个100 mL的靶容器中装入总质量为50 g富集的124Xe,在中子注量率为2.5×1014n/(cm2·s)的高通量反应堆中辐照4~5 d,出堆冷却50~60 d后,采用铜基铂(PCC)选择性吸附碘,吸附效率大于99.9%,水洗碘的脱附率低于0.1%,利用30 mL 0.1 mol/L的氢氧化钠溶液淋洗,采用该方法单个靶件可得到125I活度167~219 GBq,放化纯度大于98.5%,126I杂质小于1.0%。
1.3 反应堆制备131I
131I是医学诊断中使用最广泛的核素之一,碘具有靶向性,131I半衰期为8.05 d,其衰变链示于图3,可以用于治疗甲状腺等疾病[39]。现今通常采用碲靶或铀靶生产131I,核反应分别为130Te(n,γ)131Te与235U(n,f)131I[31]。目前大部分的131I通过在研究堆中对TeO2进行中子辐照获得[40]。采用热中子诱导235U生产131I的过程中累计产额约为3%,但该方法产生的放射性废物较多、成本较高,且产生的131I提取效率较低[41]。采用碲靶制备131I的方法是将单质碲或碲的化合物为原料,碲靶在反应堆中发生核反应生产131Te,131Te经过β-衰变生成131I,但是碲靶的制备成本较高[31]。分离131I的方法主要有湿法蒸馏和干法蒸馏,其中干法蒸馏效率高、时间短、产生的废物少、杂质少,应用最为广泛。
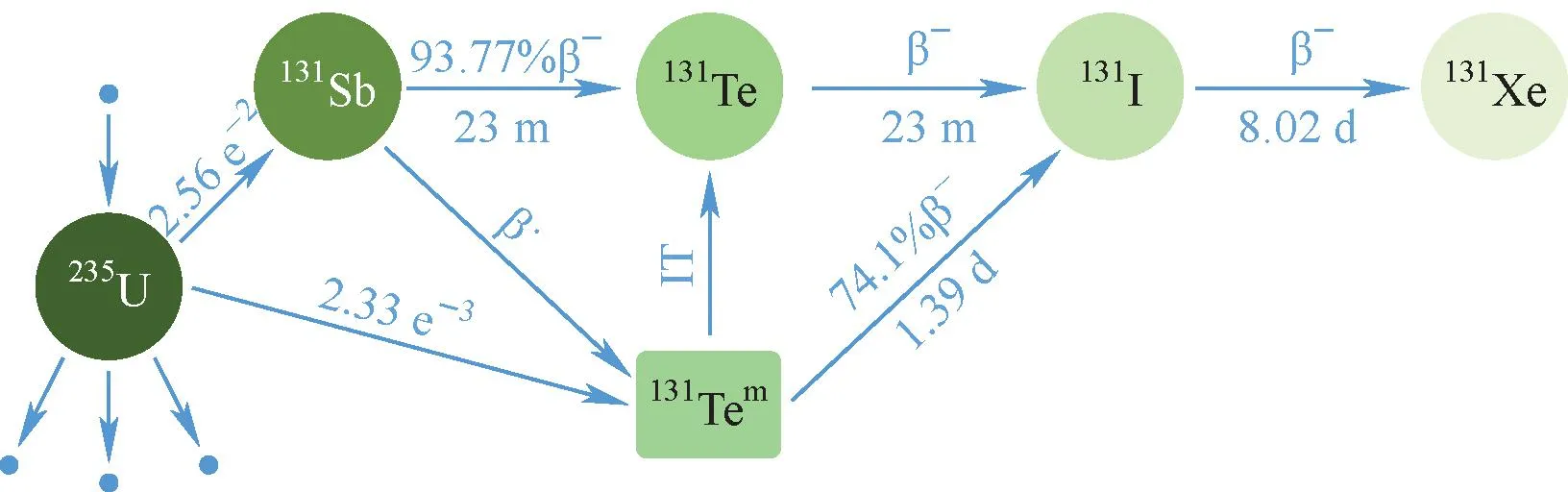
图3 衰变为131I的过程[41]Fig.3 Decay-transmutation chain of 131I[41]
现阶段生产131I方法较多,如 Khalafi等[42]采用了两种不同的方法对德黑兰研究堆(TRR)的131I的生产工艺进行了优化研究,通过计算和实验结果表明,每100 g天然铀(UO2)在3.5×1013n/(cm2·s)热中子通量下辐照100 h可生产约为5 Ci的医用131I,此外可以在其他生产线上照射生产如99Mo和133Xe等医用同位素。中国科学院上海应用物理研究所的邹阳等[43]进行了熔盐堆生产131I的生产特性研究,结果表明,采用HF-H2鼓泡法从熔盐中提取131I,每年可从熔盐中回收3.49×108GBq。
1.4 反应堆制备177Lu
177Lu可用于神经内分泌肿瘤和前列腺肿瘤的靶向治疗[44]。目前已有反应堆生产177Lu的方法为富集镥(176Lu)靶热中子活化法(直接法)和富集钇(176Yb)靶热中子活化法(间接法)[45]。
直接法是采用反应堆制备177Lu最简单的方法,该方法所需的设备易于安装和维护,产生的废料少,所需靶件的处理也较为简单,成本低。但为了提高177Lu的产量和比活性,需要使用富集的176Lu靶,通过该方法获得的产物比活性与理论值不符,在产物中只有25%的原子是177Lu,采用该方法获得的比活性约为理论值的70%。
间接法制备的核素纯度高于直接法,并且该方法的产物排除了长寿命放射性杂质的影响(如产生的177mLu<10-5%)。但是采用该方法从176Yb靶中分离产生的177Lu困难,相比于直接法会产生大量的放射性废物,由于需要制备176Yb靶、分离产物并且176Yb靶需要回收和重复利用,所以通过该方法制备高纯度的177Lu成本较高。
Chakraborty等[45]证明了176Lu(n,γ)177Lu核反应在中通量研究堆中大规模生产177Lu的可行性(图4),采用该方法生产的177Lu可以用于医疗领域,并且具有一定的经济性。我国对于无载体177Lu的生产能力不足,177Lu过于依赖进口,随着国家的重视,中国工程物理研究院与核动力设计研究院等单位加大了对177Lu工艺的研发。
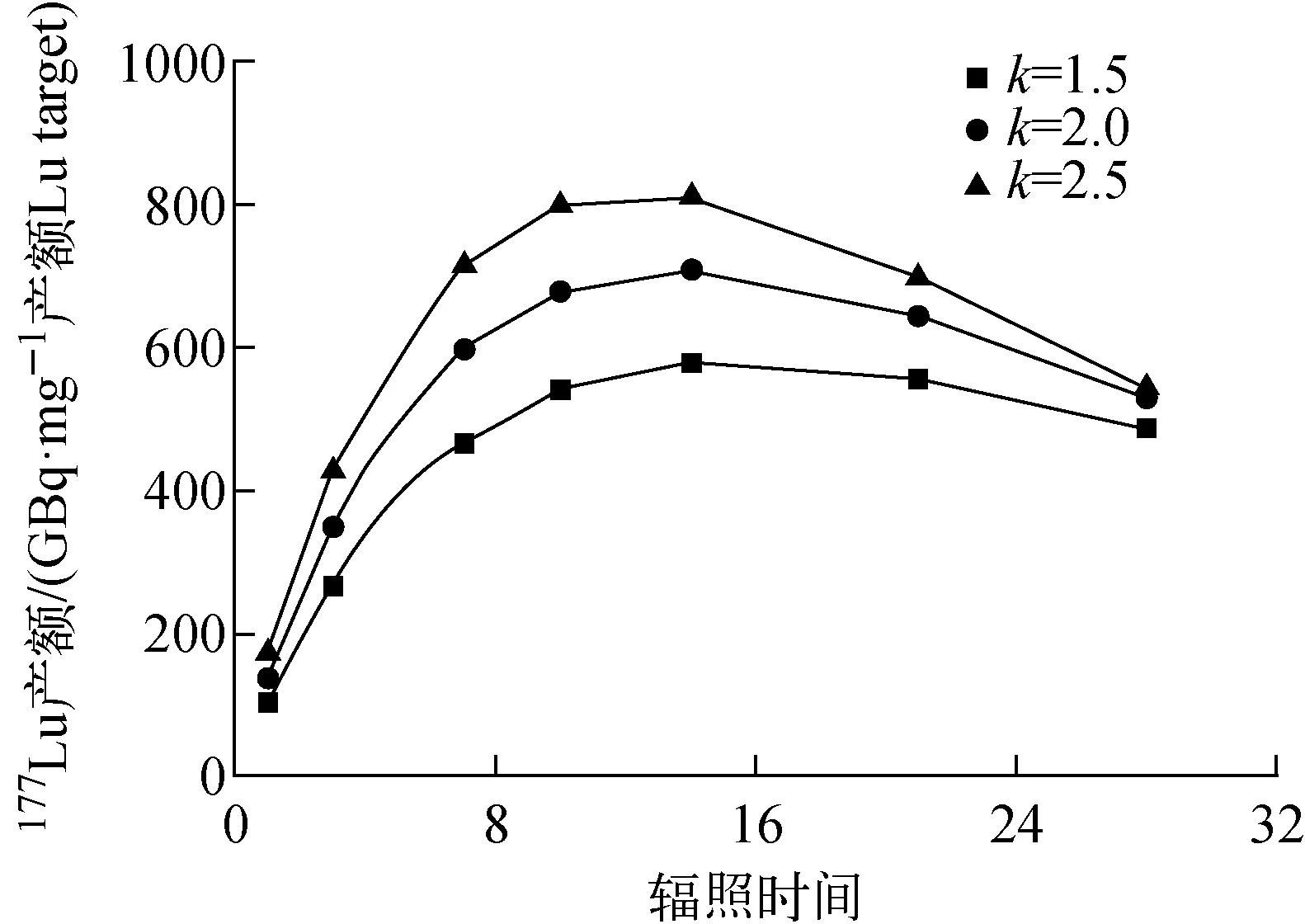
图4 177Lu的比活度随辐照时间的变化[45](当富集176Lu(82%)靶热中子通量为1.2×1014 n/(cm2·s),理论计算值k分别为1.5、2.0和2.5时)Fig.4 Variation of specific activity of 177Lu[45](theoretically calculated using k=1.5, 2.0 and 2.5,with duration of irradiation when enriched (82 % in 176Lu) target is irradiated at a thermal neutron flux of 1.2×1014 n/(cm2·s))
微型中子源反应堆(MNSRs)是最安全、最经济的研究反应堆之一,具有用于中子研究的潜力,Golabian等[46]对伊朗伊斯法罕MNSRs采用直接法生产177Lu的可行性进行了分析(图5)。在热中子通量为5×1011n/(cm2·s)的条件下,辐照4 min,通过MCNPX2.6进行模拟分析,177Lu最大产量可达723.5 mCi/g。
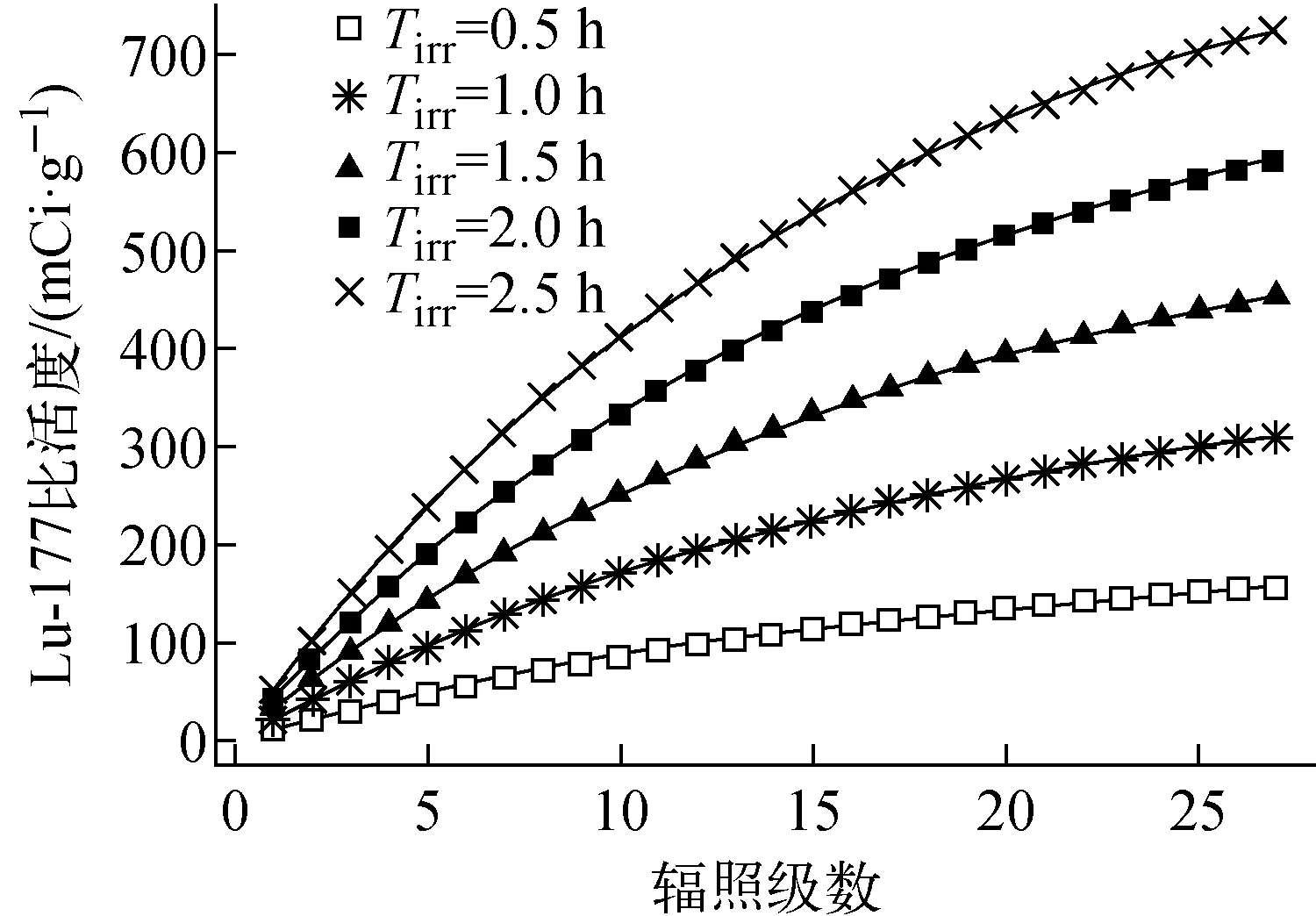
图5 不同辐照时间的177Lu比活度[46](在伊斯法罕微堆采用多级辐照获得,中子通量为1012 n/(cm2·s))Fig.5 177Lu specific radiation[46](obtained using multi-stage irradiation methods in the Isfahan MNSR reactor with neutron flux of 1012 n/(cm2·s) for different irradiation times)
1.5 反应堆制备89Sr
89Sr半衰期为50.53 d,衰变时主要放出β射线,该核素主要用于恶性肿瘤晚期发生骨转移患者的镇痛,可以提高患者的生活质量。89Sr的生产分为中子辐照法和铀裂变产物提取两种方法。
中子辐照法根据生产有无载体89Sr分为两种方式,其中有载体89Sr利用88SrCO3为原料,通过88Sr(n,γ)89Sr核反应得到89Sr;无载体89Sr利用89Y2O3为原料,通过89Y(n,p)89Sr核反应得到89Sr[47]。
铀裂变产物法是利用均匀性水溶液反应堆,以UO(NO)或UO2SO4为原料,在反应堆运行过程中235U首先裂变为89Br、90Br等短半衰期核素,由于这些核素半衰期较短,在短时间内再次衰变为为89Kr,最终89Kr衰变为89Sr[47]。
目前开发了较多的新方法,如Saha等[48]研究了利用89Y(n,p)89Sr在快速增殖反应堆生产89Sr的可行性,实验研究发现,1 g钇颗粒可产生89Sr的活性为19 mCi。中科院上海应用物理研究所的蔡翔舟等[49]对2 MW熔盐反应堆(MSR)中89Sr的生产能力进行了评估(图6),89Sr的年产量可以达到约9 000 Ci,其中杂质小于2 ppm,可达到医用要求。
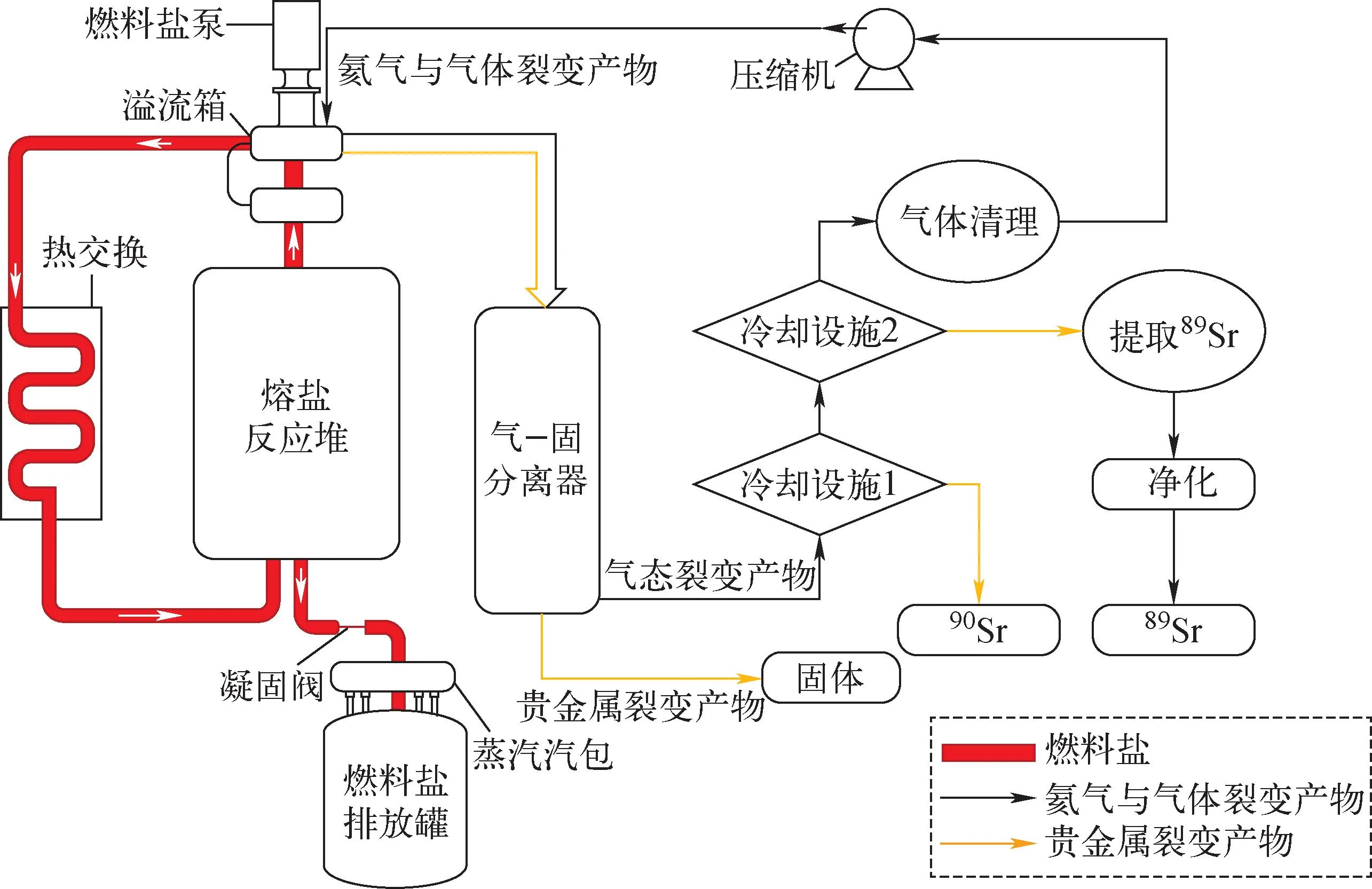
图6 89Sr在2 MW熔盐反应堆生产原理图[49]Fig.6 89Sr roduction schematic diagram of the 2 MW MSR[49]
Vereshchagin等[50]给出了采用溶液燃料反应堆生产89Sr的技术方案。该方法采用硫酸铀酰溶液作为原料,经过核反应与一系列的衰变最终生成89Sr。采用该方法获得89Sr具有生产率高、方法简单、产生放射性废物少等特点。采用功率为20 kW的微型溶液反应堆预计每年的89Sr产量为(1.5~1.8)×103GBq,相比60 MW的BOR-60反应堆产量(约4×103GBq/年)低的并不多。该方法在生产89Sr的过程中分离出的副产物如133Xe和135Xe也可用于医疗。
Saha等[48]采用快增殖实验堆通过89Y(n,p)89Sr反应生产89Sr,在反应堆中的一个组件中添加钇颗粒,经过处理后将89Sr洗脱出来,1 g钇颗粒产生的89Sr活性为19 mCi。
采用反应堆制备医用同位素具有较高的产量,但是也存在反应堆的建造维护成本高,生产医用同位素的原料(靶材)难以获得等因素限制,无法得到大规模的应用与普及。
2 加速器
加速器生产的同位素相较于利用反应堆生产同位素,具有比活度高、半衰期短等特点[8]。加速器具有可加速的粒子种类多、能量范围广、平均束流强度高等技术特征,是医用放射性同位素制备的主要设备之一[51]。
2.1 加速器生产18F
利用回旋加速器生产18F主要是利用回旋加速器产生的6~18 MeV的质子轰击[18O]H2O靶,18F主要是由该过程中18O(p,n)18F反应产生[52]。
北京大学肿瘤医院的王风等[53]利用蒙特卡罗方法研究了回旋加速器质子辐照靶室模型(图7)在医用回旋加速器生产18F时的照射条件和轰击参数的应用,优化了生产条件并给出了最佳的轰击参数,结果表明,18F的产量随束流强度增大而增大,但随着轰击时间延长增长趋势变缓。最佳条件为质子能量20 MeV,推荐Havar膜厚度60 μm,靶水厚度3 mm,轰击时间60 min。
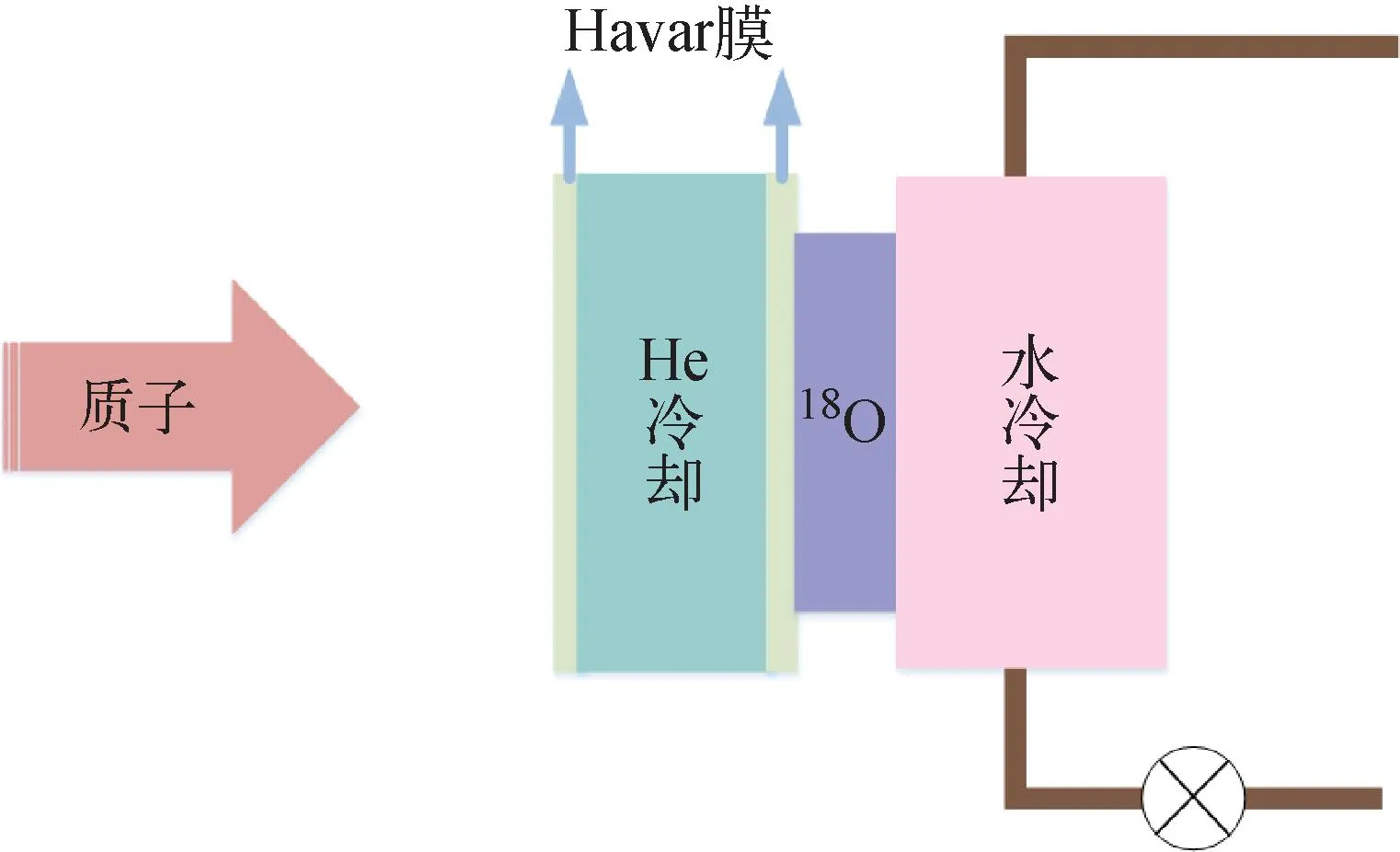
图7 靶照射装置示意图[53]Fig.7 Sketch of target irradiation device[53]
Roberts等[54]在美国威斯康辛州利用Siemens/CTI 11 MeV质子回旋加速器上研制了一种具有提高亲电性[18F]F2产率的Al基体靶,当波束电流达到45 μA时,饱和产率为(3.10±0.40) GBq/μA,该靶比之前使用的Ni靶具有更高的产率,并且在一系列的实验中表现可靠。
Hess等[55]报道了一种改进的铝靶系统,通过18O(p,n)18F反应采用两步辐照方案生产单质氟,第一步用质子照射高度富集的气态18O形成18F,18F沉积在目标的内部表面。第二步,在低温回收18O目标气体后,引入元素“冷”氟和氪的混合物,并进行短质子照射,从而在气态氟和沉积的放射性氟之间进行同位素交换,回收步骤参数表明,以20 μA的束流照射15~20 min,足以使氟载体与沉积在靶壁上的18F放射性物质发生同位素交换,采用该方法生产18F产量高达34 GBq,比活性为350~600 GBq/mmol。
2.2 加速器生产68Ga
68Ga在神经内分泌肿瘤显像、前列腺癌诊疗中都具有一定的优势,是核医学领域的研究热点之一。68Ga半衰期(68 min)的限制,不适于反应堆生产,在利用锗-镓发生器68Ga的过程中,存在68Ge的残留干扰,而且存在产率随时间延长而下降的问题,对其批量生产存在一定程度的限制[56]。
Nelson等[57]将100 mg富集68Zn(68Zn含99.3%)颗粒压在银盘上,在回旋加速器中采用12.5 MeV质子束能量和10~30 μA电流轰击20~75 min。经过实验验证,通过该方法获得与锗-镓发生器制备的68Ga质量类似,但该方法可以避免68Ge的残留干扰且具有成本较低、靶材制备快、效益更高等优点。
Tieu等[58]介绍了在低能医用回旋加速器上制备68Ga的简便方法(图8)。使用医用回旋加速器在电流强度为34 μA,束流能量为14.5和12.0 MeV的条件下轰击富集氯化锌靶,然后采用辛醇树脂对辐照锌靶进行提纯。在轰击8.5 min后可获得(6.30±0.42) GBq的68Ga,并且产生的杂质很低(66Ga<0.005%,67Ga<0.09%)。

图8 68Ga生产流程[58]Fig.8 68Ga production process[58]
2.3 加速器生产225Ac
在治疗癌症方面,α-发射体与目前广泛使用的β-发射体相比优势更大,因为α-发射体在组织中具有更大的线传能密度(LET)和有限的射程,是当前各国科研团队研究的热点,目前225Ac是最有前途的同位素,其半衰期为9.9 d,且适用于抗体靶向药物治疗,在其衰变链中将发射4个α粒子,对癌细胞进行有效的杀伤[59]。
中能质子束辐照232Th通过多个途径生成225Ac(图9)[59-60]:1) 主要通过232Th(p,p7n)225Th,然后225Th通过β+衰变生成225Ac;2) 通过232Th(p,2p6n)225Th反应直接生成225Ac;3) 通过核反应232Th(p,p4n)229Pa→225Ac和232Th(p,3p5n)225Ra→225Ac。
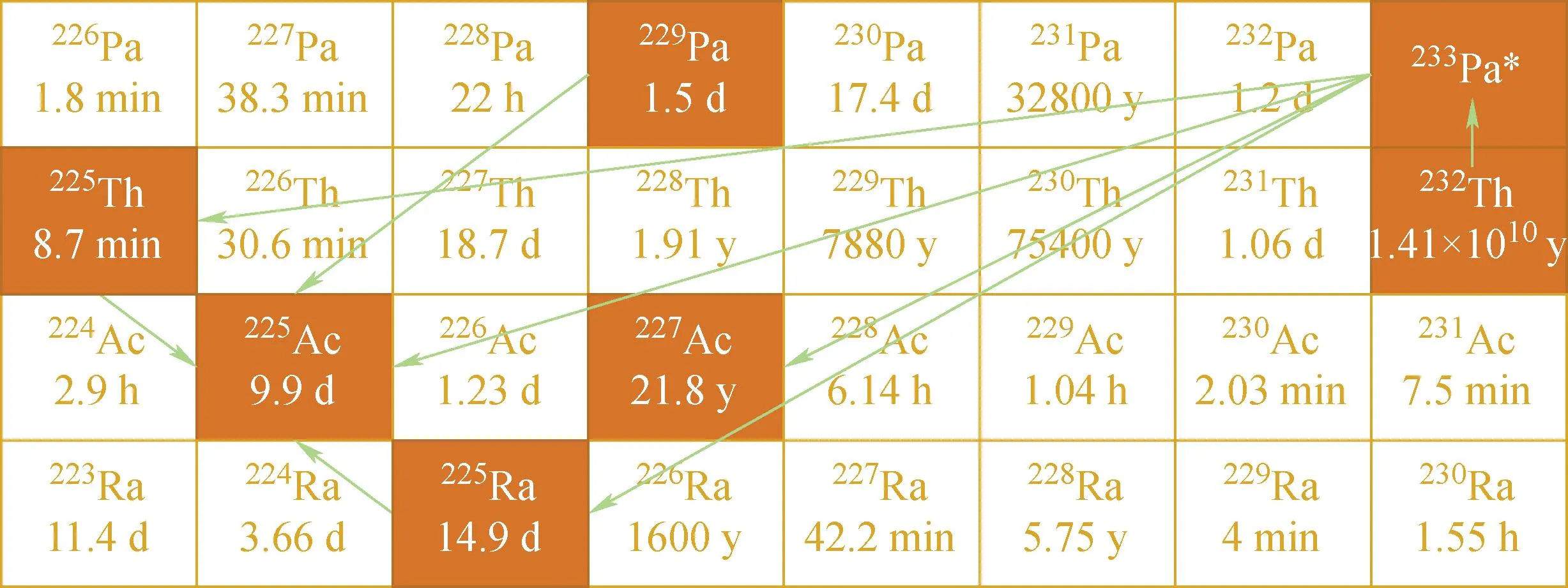
图9 中能质子辐照Th产生225Ac的主要途径[60]Fig.9 Principal nuclear channels resulting in 225Ac generation via irradiation of thorium with medium energy protons[60]
Nagatsu等[61]用螯合树脂从镭源中提取226Ra。采用离子交换法得到载钡的226Ra,采用电镀法制备镭靶。使用15.6 MeV的质子在20 μA的条件下轰击5 h,使其达到最大活化。使用功能树脂与硝酸对225Ac纯化与回收226Ra。将中间产物静置2~3周可使副产物衰变以获得更高纯度的225Ac。在轰击结束时该团队获得了2.4 MBq的225Ac,轰击4 d后获得了1.7 MBq的225Ac,由于额外的冷却过程和纯化步骤使得225Ac的放射性核素纯度大于99%。
中国原子能科学研究院的王雷等[59]在100 MeV回旋加速器上开展了放射性医用同位素的生产实验。使用Fluka程序模拟计算了质子束流辐照不同厚度的ThO2粉末靶产生的224-228Ac等几种产额较高的同位素活度,研究了不同厚度的ThO2靶材锕同位素产额变化规律,设计了一套225Ac生产装置并进行了生产实验,通过对实验后提取的225Ac测量计算得到辐照结束时产生的225Ac活度为2.29×107Bq,产额为2.39×105Bq/(μA·h)。
目前多数医用放射性核素都是利用核反应堆和回旋加速器生产[62]。一些有潜力的医用放射性核素的生产还存在着一些困难,如:225Ac、67Cu、47Sc、166Ho、195mPt等[63]。目前部分研究者对利用线性电子加速器生产医用同位素的优缺点进行了研究,线性电子加速器生产医用同位素的方法主要是电子入射到转换器上断裂并产生韧致辐射光子,从而利用光核反应来生产目标同位素。如Aliev等[63]验证了利用光核法生产医用同位素176Tm的可能性,该团队使用55 MeV的韧致辐射光子照射天然镱靶制备了176Tm,测得176Tm产率为(7.8±1.1)×103Bq·μA·h-1·cm2·g-1。加速器生产医用同位素也可以获得较高的产值,相对反应堆的建造维护成本更低,并且加速器的建设条件比反应堆更宽松,利于广泛建设使用。
3 其他方法
3.1 放射性核素发生器
由于大多医用放射性同位素寿命较短,同时有些地区离反应堆较远,也不具备加速器,这时可以利用放射性核素发生器提供寿命较短的医用放射性同位素,该设备可以定期从长寿命母体核素中分离出短寿命子体核素,并且母、子体通常不是同位素,通过选择合适的化学分离方法(如:离子交换法、色谱法、萃取或升华等)使母体留在发生器,而子体被分离出来。目前最常见的核素发生器有188W-188Re、99Mo-99mTc、68Ge-68Ga发生器等,该设备可以多次、安全方便地提供无载体、高比活度的短半衰期核素,目前已有较为广泛地应用[64]。
3.2 激光脉冲法
随着激光技术的发展,利用激光加速电子实现光核反应生产同位素被认为有巨大的发展前景,生产方式示于图10。激光脉冲在相对密集的等离子体中传播,当激光脉冲的速度耗尽,它就会将电子加速到几十到几百兆电子伏的能量,被加速的电子离开等离子体,被送到转换器或靶件产生韧致辐射,进而发生光核反应生产医用同位素[65-69]。Lobok等[69]通过Geant4模拟,在激光脉冲传播的RST体制下,使用伽马源或电子源,该团队证明了激光脉冲生产医用同位素的可能性。在RST体制下利用激光脉冲产生的伽马辐照生产的医用同位素可以达到医疗需求,与电子辐照相比在辐照较厚靶材的时候,该方法具有一定的优势。研究表明,10 Hz、30 fs、4 J的激光脉冲非常适合生产111In、123I、103Pd、62Cu、64Cu几种核素。
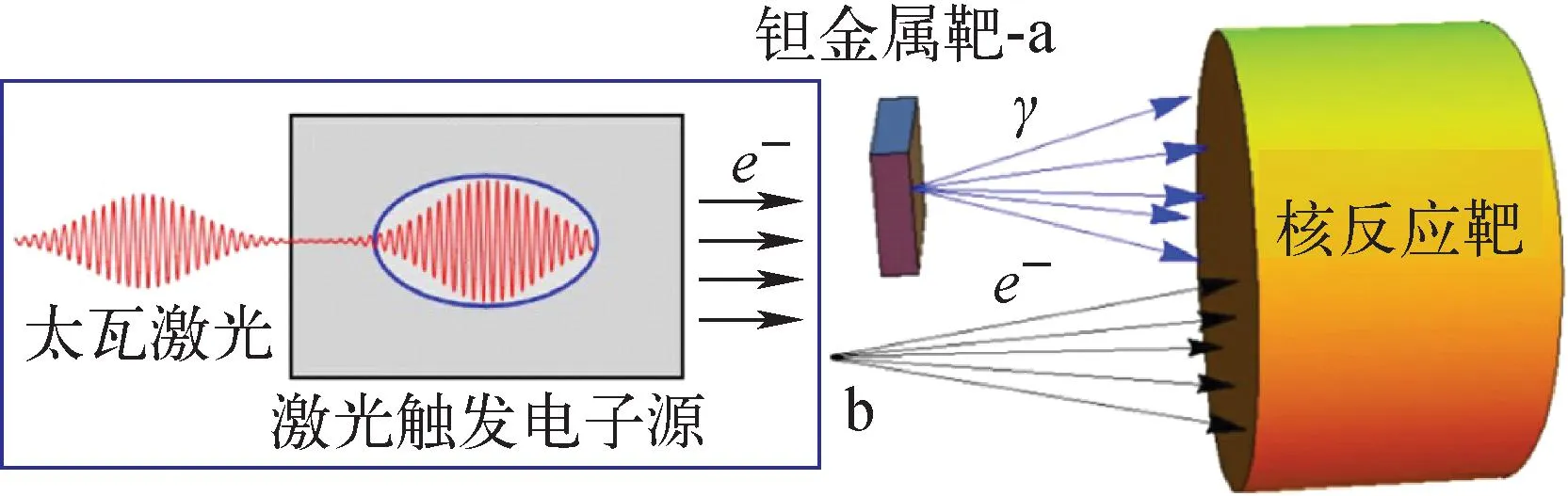
a——采用附加的激光转换器靶从激光加速电子束产生γ射线照射目标;b——采用激光加速电子直接照射目标所触发的光核反应的激光目标布局图10 激光脉冲法生产方式[69]Fig.10 Laser-pulse method production Laser-target layout for photonuclear reactions triggered by using (a) additional converter target producing gamma rays from laser-accelerated electron beam to irradiate nuclear target and (b) direct irradiation of nuclear target by laser-accelerated electrons[69]
3.3 激光共振电离法
激光共振电离法需要使用激光共振电离离子源,在工作时激光共振电离离子源使用可调谐激光将原子从基态激发到激发态,再将其激发到自电离态,在引出区静电场的作用下引出并形成离子束,对于不同的核素有不同的原子能级,因此需要根据不同的研究对象选择合适的激光波长,提高电离效率,随后采用质量分离器选择性的提取离子束[70-71]。
激光共振电离法可以用于生产非传统的医用放射性同位素,使用激光共振电离可以提高放射性同位素的质量和产量,由于目前生产方式的限制,许多较有前景的放射性同位素生产具有一定的困难(如149Tb、161Tb、152Tb)这些同位素的生产过程易受到污染,目前还未受到证实),激光共振电离可以提高同位素的纯度,使生产的同位素达到医用要求。该方法可以处理来自加速器、反应堆等核设施的辐照物质,实现放射性同位素的净化与提取。该方法基于激光的多步激发和电离过程,理想情况下,只有一种元素被电离,由于激光电离过程具有较高的效率,离子束的产生和提取效率也得到了较大的提高,再结合电磁质量分离,该方法具有较高效率且同位素的纯度也得到了很大程度的提高[71-73]。Gadelshin等[71]利用CERN-MEDICIS采用两步电离激光共振电离工艺对铽进行了制备和表征。该设施是基于电磁质量分离从预辐照目标材料中提取所需的放射性核素[74]。
这些其他方法给医用同位素的生产提供了新的思路,如核素发生器已经有较多的应用,有较好的前景,与传统方法相比具有一定的优势且可以制备一些具有很好研究前景的同位素与非常规的医用同位素。
4 结论与展望
本文根据目前的发展情况介绍了目前医用同位素的制备方法,对目前应用较为广泛的几种同位素的制备情况进行了综述。目前已经有大量的放射性同位素已经被证实在诊断和治疗疾病方面具有一定的潜力,但是如今主流的两种生产医用放射性同位素的方法具有一定的局限。由于目前存在的问题,世界各国研究团队也尝试通过其他方法来生产医用放射性同位素,其中一些方法已经得到了验证。
结合2021年国家八部委联合发布的《医用同位素中长期发展规划(2021—2035年)》(以下简称《规划》)对国内放射性医用同位素存在的现状进行总结并展望未来。
1) 2018年全球核医药市场达到50亿美元,预计2030年将达到260亿美元,复合增长率为14%,不过这其中很大一部分占比为欧美等发达国家消费[75]。
2) 目前全球平均每万人开展核医学检查的人数约64人,其中美国695人,欧盟国家240人,日本111人,我国为19人,仅为全球平均水平的30%左右,更远低于世界发达国家水平[76]。
3) 2019年中国放射性药物市场规模为35.93亿元,较2018年的29.7亿元同比增长21%。虽然国内目前市场规模总值相对发达国家较低,但是国内发展速度较快且国内市场巨大,所以放射性药物在国内还具有相当大的发展空间[77]。
近年来随着国内核医学的发展及新堆的建立,以及加速器的快速发展,国内的众多科研机构推进了对医用同位素的研制与生产进程,加快或实现了(如131I、99Mo、89Sr、14C、177Lu、18F、201Tl、67Ga、211At、111In、89Zr等重要医用同位素)医用同位素国产化[31,52]。如2015年,中国工程物理研究院利用CMRR堆完成国内131I供应,打破了我国医用同位素完全依赖进口的困境,2018年依托CMRR建立了堆照176Lu制备177Lu生产工艺,依托CMRR堆建成了高浓铀靶裂变制备99Mo的生产平台,设计99Mo年产量在10 000 Ci;开展了无载体89SrCl2溶液的研究工作,并建立了离子树脂柱分离Sr/Y工艺流程,开展了氮化铝靶件辐照生产14C的前期研究工作;2018年核动力院构建了有载体89SrCl2溶液生产装置,并完成了辐照验证实验,具备了30~50 Ci/年的89Sr生产能力;报道了AIN靶件辐照生产14C的工艺[31]。中国原子能科学研究院、原子高科股份有限公司等单位,利用Cyclone 30回旋加速器开展了67Ga、201Tl、18F等放射性同位素的研制,建立了相应的工艺路线[52];四川大学依托CS-30回旋加速器也已先后研发出111In、89Zr、211At等医用放射性同位素[78]。
尽管目前国内放射性医用同位素的发展相较于西方发达国家还较为落后,但是国家已经开始关注该行业的发展,2021年《规划》中给出了重点任务与总体要求,设立了建立稳定自主的医用同位素供应保障体系,满足人民日益增长的健康需求。为了实现建成健康国家的目标,《规划》又设立了2025目标与2035目标,将其分为两步走。重点任务中主要分为:1) 加大技术研发,促进创新发展;2) 提升能力水平,实现自主供应;3) 加快产业步伐,推动高效发展。为了保证目标的完成《规划》中建立了完善的保障措施:1) 优化产业政策;2) 健全监管体系;3) 加强人才培养。
未来关于医用同位素生产的技术在国内会得到快速发展,以放射性医用同位素为基础的产业也将迎来发展新时机。

